Рекомбинантная ДНК - Recombinant DNA
| Часть серия на |
| Генная инженерия |
|---|
 |
| Генетически модифицированные организмы |
| История и регулирование |
| Процесс |
| Приложения |
| Споры |
Рекомбинантная ДНК (рДНК) молекулы ДНК молекулы, образованные лабораторными методами генетическая рекомбинация (Такие как молекулярное клонирование ) объединяет генетический материал из нескольких источников, создавая последовательности что иначе не было бы найдено в геном.
Рекомбинантная ДНК - это общее название фрагмента ДНК, который был создан путем объединения как минимум двух фрагментов из двух разных источников. Рекомбинантная ДНК возможна, потому что молекулы ДНК всех организмов имеют одинаковую химическую структуру и отличаются только нуклеотид последовательность внутри этой идентичной общей структуры. Рекомбинантные молекулы ДНК иногда называют химерная ДНК, потому что они могут быть сделаны из материала двух разных видов, например, из мифических химера. Технология R-DNA использует палиндромные последовательности и приводит к производству липкие и тупые концы.
Последовательности ДНК, используемые для создания рекомбинантных молекул ДНК, могут происходить из любых разновидность. Например, ДНК растений может быть соединена с ДНК бактерий, или ДНК человека может быть соединена с ДНК грибов. Кроме того, последовательности ДНК, которые не встречаются в природе, могут быть созданы химический синтез ДНК и включены в рекомбинантные молекулы. Используя технологию рекомбинантной ДНК и синтетическую ДНК, можно создать буквально любую последовательность ДНК и ввести ее в любой из очень широкого круга живых организмов.
Белки, которые могут быть результатом экспрессии рекомбинантной ДНК в живых клетках, называются рекомбинантные белки. Когда рекомбинантная ДНК, кодирующая белок, вводится в организм-хозяин, рекомбинантный белок не обязательно продуцируется.[1] Экспрессия чужеродных белков требует использования специализированных экспрессионных векторов и часто требует значительной реструктуризации с помощью чужеродных кодирующих последовательностей.[2]
Рекомбинантная ДНК отличается от генетической рекомбинации тем, что первая является результатом искусственных методов в пробирке, а вторая - нормальным биологическим процессом, который приводит к повторному смешиванию существующих последовательностей ДНК практически во всех организмах.
Создание ДНК

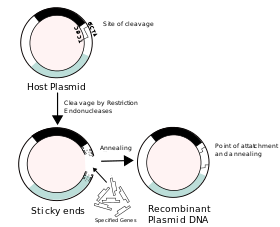
Молекулярное клонирование - это лабораторный процесс, используемый для создания рекомбинантной ДНК.[3][4][5][6] Это один из двух наиболее широко используемых методов наряду с полимеразной цепной реакции (ПЦР), используемый для управления репликацией любой конкретной последовательности ДНК, выбранной экспериментатором. Между методами есть два принципиальных различия. Во-первых, молекулярное клонирование включает репликацию ДНК внутри живой клетки, в то время как ПЦР реплицирует ДНК в пробирке, свободной от живых клеток. Другое отличие состоит в том, что клонирование включает вырезание и вставку последовательностей ДНК, а ПЦР амплифицируется путем копирования существующей последовательности.
Для образования рекомбинантной ДНК требуется клонирование вектор, молекула ДНК, которая реплицируется в живой клетке. Векторы обычно получают из плазмиды или же вирусы, и представляют собой относительно небольшие сегменты ДНК, которые содержат необходимые генетические сигналы для репликации, а также дополнительные элементы для удобства вставки чужеродной ДНК, идентификации клеток, содержащих рекомбинантную ДНК, и, при необходимости, экспрессии чужеродной ДНК. Выбор вектора для молекулярного клонирования зависит от выбора организма-хозяина, размера клонируемой ДНК и от того, должна ли и как экспрессироваться чужеродная ДНК.[7] Сегменты ДНК могут быть объединены с использованием различных методов, таких как клонирование рестрикционного фермента / лигазы или Сборка Гибсона.
В стандартных протоколах клонирования клонирование любого фрагмента ДНК по существу включает семь этапов: (1) Выбор организма-хозяина и вектора клонирования, (2) Получение векторной ДНК, (3) Подготовка ДНК для клонирования, (4) Создание рекомбинантная ДНК, (5) введение рекомбинантной ДНК в организм-хозяин, (6) отбор организмов, содержащих рекомбинантную ДНК, и (7) скрининг клонов с желаемыми вставками ДНК и биологическими свойствами.[6]Эти шаги подробно описаны в соответствующей статье (молекулярное клонирование ).
Экспрессия ДНК
После трансплантации в организм-хозяин чужеродная ДНК, содержащаяся в конструкции рекомбинантной ДНК, может или не может быть выразил. То есть ДНК может просто реплицироваться без экспрессии, или она может быть записано и переведено и продуцируется рекомбинантный белок. Вообще говоря, экспрессия чужеродного гена требует реструктуризации гена для включения последовательностей, необходимых для производства мРНК молекула, которая может быть использована хозяином переводной аппарат (например. промоутер, сигнал инициации трансляции, и терминатор транскрипции ).[8] В организм-хозяин могут быть внесены специфические изменения для улучшения экспрессии эктопического гена. Кроме того, могут потребоваться изменения и в кодирующих последовательностях, чтобы оптимизировать трансляцию, сделать белок растворимым, направить рекомбинантный белок в нужное клеточное или внеклеточное местоположение и стабилизировать белок от деградации.[9][10]
Свойства организмов, содержащих рекомбинантную ДНК
В большинстве случаев организмы, содержащие рекомбинантную ДНК, имеют нормальный фенотипы. То есть их внешний вид, поведение и метаболизм обычно не изменяются, и единственный способ продемонстрировать присутствие рекомбинантных последовательностей - это исследовать саму ДНК, обычно с использованием теста полимеразной цепной реакции (ПЦР).[11] Существуют значительные исключения, которые обсуждаются ниже.
Если последовательности рДНК кодируют ген, который экспрессируется, то присутствие РНК и / или белковых продуктов рекомбинантного гена может быть обнаружено, обычно с использованием ОТ-ПЦР или же западная гибридизация методы.[11] Грубые фенотипические изменения не являются нормой, если только рекомбинантный ген не был выбран и модифицирован так, чтобы вызвать биологическую активность в организме хозяина.[12] Дополнительные фенотипы, которые встречаются, включают токсичность для организма-хозяина, индуцированную продуктом рекомбинантного гена, особенно если он чрезмерно выраженный или экспрессируется в неподходящих клетках или тканях.
В некоторых случаях рекомбинантная ДНК может оказывать вредное воздействие, даже если она не экспрессируется. Один из механизмов, с помощью которого это происходит: инсерционная инактивация, в котором рДНК вставляется в ген клетки-хозяина. В некоторых случаях исследователи используют это явление для "нокаутировать «гены для определения их биологической функции и важности.[13] Другой механизм, с помощью которого вставка рДНК в хромосомную ДНК может влиять на экспрессию генов, - это неправильная активация ранее невыраженных генов клетки-хозяина. Это может произойти, например, когда фрагмент рекомбинантной ДНК, содержащий активный промотор, оказывается рядом с ранее молчащим геном клетки-хозяина или когда ген клетки-хозяина, который функционирует для ограничения экспрессии гена, подвергается инсерционной инактивации рекомбинантной ДНК.
Применение ДНК
Рекомбинантная ДНК широко используется в биотехнология, лекарство и исследование. Сегодня рекомбинантные белки и другие продукты, полученные в результате использования технологии ДНК, можно найти практически в каждой западной аптеке, у врача или ветеринара, в медицинской испытательной лаборатории и лаборатории биологических исследований. Кроме того, организмы, которыми манипулировали с помощью технологии рекомбинантной ДНК, а также продукты, полученные из этих организмов, нашли свое применение во многих фермах, супермаркеты, шкафы домашней медицины и даже зоомагазины, например те, которые продают GloFish и другие генетически модифицированные животные.
Чаще всего рекомбинантная ДНК применяется в фундаментальных исследованиях, в которых технология важна для большинства текущих работ в биологических и биомедицинских науках.[11] Рекомбинантная ДНК используется для идентификации, картирования и определения последовательности генов, а также для определения их функции. Зонды рДНК используются для анализа экспрессии генов в отдельных клетках и в тканях целых организмов. Рекомбинантные белки широко используются в качестве реагентов в лабораторных экспериментах и для создания зондов антител для изучения синтеза белка в клетках и организмах.[4]
Многие дополнительные практические применения рекомбинантной ДНК находят в промышленности, производстве продуктов питания, медицине и ветеринарии, сельском хозяйстве и биоинженерии.[4] Ниже приведены некоторые конкретные примеры.
- Рекомбинантный химозин
- Нашел в сычужный фермент, химозин - это фермент, необходимый для производства сыра. Это была первая пищевая добавка, созданная с помощью генной инженерии, которая используется в коммерческих целях. Традиционно переработчики получали химозин из сычужного фермента, препарата, полученного из четвертого желудка телят, вскармливаемых молоком. Ученые создали непатогенный штамм (К-12) Кишечная палочка бактерии для крупномасштабного лабораторного производства фермента. Этот рекомбинантный фермент, полученный микробиологически, идентичный по структуре ферменту, полученному из теленка, стоит меньше и производится в больших количествах. Сегодня около 60% твердого сыра в США производится с использованием химозина, полученного с помощью генной инженерии. В 1990 году FDA предоставило химозин "общепризнанно безопасным "(GRAS) статус основан на данных, показывающих, что фермент безопасен.[14]
- Рекомбинантный человек инсулин
- Практически полностью заменил инсулин, полученный из животных источников (например, свиней и крупного рогатого скота) для лечения инсулинозависимых сахарный диабет. Широко используется множество различных препаратов рекомбинантного инсулина.[15] Рекомбинантный инсулин синтезируется путем вставки гена человеческого инсулина в Кишечная палочка, или дрожжи (Saccharomyces cerevisiae)[16] который затем производит инсулин для использования человеком.[17]
- Рекомбинантный человек гормон роста (HGH, соматотропин)
- Вводится пациентам, у которых гипофиз вырабатывает недостаточное количество для поддержания нормального роста и развития. Прежде чем рекомбинантный гормон роста стал доступным, гормон роста для терапевтического использования был получен из гипофиза трупов. Эта небезопасная практика привела к развитию у некоторых пациентов Болезнь Крейтцфельдта-Якоба. Рекомбинантный гормон роста устранил эту проблему и теперь используется в терапевтических целях.[18] Его также неправильно использовали спортсмены и другие люди в качестве препарата, повышающего спортивные результаты.[19] Запись в DrugBank
- Рекомбинантное свертывание крови фактор VIII
- Белок свертывания крови, который вводят пациентам с формами гемофилии с нарушением свертываемости крови, которые не могут продуцировать фактор VIII в количествах, достаточных для поддержания нормальной свертываемости крови.[20] До разработки рекомбинантного фактора VIII белок получали путем обработки больших количеств крови человека от нескольких доноров, что несло в себе очень высокий риск передачи инфекционные заболевания, передающиеся через кровь, например ВИЧ и гепатит В. Запись в DrugBank
- Рекомбинантный вакцина против гепатита В
- Гепатит Б Инфекция контролируется с помощью рекомбинантной вакцины против гепатита В, которая содержит форму поверхностного антигена вируса гепатита В, который продуцируется в дрожжевых клетках. Разработка рекомбинантной субъединичной вакцины была важной и необходимой разработкой, поскольку вирус гепатита В, в отличие от других распространенных вирусов, таких как вирус полиомиелита, нельзя выращивать in vitro. Информация о вакцинах от Фонда гепатита В
- Диагностика заражения ВИЧ
- Каждый из трех широко используемых методов диагностика ВИЧ-инфекции был разработан с использованием рекомбинантной ДНК. Тест на антитела (ELISA или же вестерн-блот ) использует рекомбинантный белок ВИЧ для проверки наличия антитела что организм производит в ответ на ВИЧ-инфекцию. ДНК-тест выявляет наличие генетического материала ВИЧ, используя полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР). Разработка теста RT-PCR стала возможной благодаря молекулярному клонированию и анализу последовательности геномов ВИЧ. Страница тестирования на ВИЧ из Центров по контролю за заболеваниями США (CDC)
- Золотой рис
- Рекомбинантный сорт риса, который был разработан для экспрессии ферментов, ответственных за β-каротин биосинтез.[12] Этот сорт риса имеет большие перспективы для снижения заболеваемости дефицит витамина А в населении мира.[21] Золотой рис в настоящее время не используется, ожидая решения регулирующих органов и интеллектуальной собственности.[22] вопросы.
- Устойчивые к гербицидам культуры
- Были выведены коммерческие сорта важных сельскохозяйственных культур (включая сою, кукурузу / кукурузу, сорго, канолу, люцерну и хлопок), которые включают рекомбинантный ген, который приводит к устойчивости к гербициду. глифосат (торговое наименование Округлять) и упрощает борьбу с сорняками путем внесения глифосата.[23] Эти культуры широко используются в коммерческих целях в нескольких странах.
- Устойчивые к насекомым культуры
- Bacillus thuringeiensis это бактерия, которая естественным образом производит белок (Bt токсин ) с инсектицидными свойствами.[21] Бактерия применялась к посевам в качестве стратегии борьбы с насекомыми в течение многих лет, и эта практика широко применяется в сельском хозяйстве и садоводстве. Недавно были разработаны растения, которые экспрессируют рекомбинантную форму бактериального белка, которая может эффективно контролировать некоторых насекомых-хищников. Экологические проблемы, связанные с использованием этих трансгенный посевы полностью не рассеяны.[24]
История
Идея рекомбинантной ДНК была впервые предложена Питером Лоббаном, аспирантом проф. Дейл Кайзер на кафедре биохимии Медицинской школы Стэнфордского университета.[25] Первые публикации, описывающие успешное получение и внутриклеточную репликацию рекомбинантной ДНК, появились в 1972 и 1973 гг. Стэнфорд и UCSF.[26][27][28][29] В 1980 г. Пол Берг, профессор кафедры биохимии в Стэнфорде и автор одной из первых статей [26] был удостоен Нобелевской премии по химии за свою работу по нуклеиновым кислотам «с особым вниманием к рекомбинантной ДНК». Вернер Арбер, Гамильтон Смит, и Дэниел Натанс разделила 1978 Нобелевская премия по физиологии и медицине для открытия эндонуклеазы рестрикции которые усовершенствовали методы технологии рДНК.
Стэндфордский Университет подал заявку на патент США на рекомбинантную ДНК в 1974 году, указав изобретателей как Герберт В. Бойер (профессор Калифорнийский университет в Сан-Франциско ) и Стэнли Н. Коэн (профессор Стэндфордский Университет ); этот патент был получен в 1980 году.[30] Первым лицензированным препаратом, созданным с использованием технологии рекомбинантной ДНК, был человеческий инсулин, разработанный Genentech и лицензировано Эли Лилли и компания.[31]
Полемика
Ученые, связанные с первоначальной разработкой методов рекомбинантной ДНК, признали, что у организмов, содержащих рекомбинантную ДНК, существует возможность иметь нежелательные или опасные свойства. В 1975 году Асиломарская конференция по рекомбинантной ДНК эти опасения были обсуждены, и был введен добровольный мораторий на исследования рекомбинантной ДНК для экспериментов, которые считались особенно рискованными. Этот мораторий широко соблюдался до тех пор, пока Национальные институты здравоохранения (США) не разработали и не выпустили официальные инструкции по работе с рДНК. Сегодня рекомбинантные молекулы ДНК и рекомбинантные белки обычно не считаются опасными. Однако остаются опасения по поводу некоторых организмов, экспрессирующих рекомбинантную ДНК, особенно когда они покидают лабораторию и попадают в окружающую среду или в пищевую цепь. Эти опасения обсуждаются в статьях на генетически модифицированные организмы и генетически модифицированные пищевые споры. Кроме того, существуют опасения по поводу побочных продуктов в биофармацевтическом производстве, когда рекомбинантная ДНК приводит к образованию определенных белковых продуктов. Основной побочный продукт, называемый белок клетки-хозяина, происходит от системы экспрессии хозяина и представляет угрозу для здоровья пациента и окружающей среды в целом.[32][33]
Смотрите также
- Asilomar конференция по рекомбинантной ДНК
- Генная инженерия
- Генетически модифицированный организм
- Рекомбинантный вирус
- Векторная ДНК
- Биомолекулярная инженерия
- Технология рекомбинантной ДНК
- Белок клетки-хозяина
Рекомендации
- ^ Rosano, Germán L .; Чеккарелли, Эдуардо А. (17 апреля 2014 г.). «Экспрессия рекомбинантного белка в Escherichia coli: достижения и проблемы». Границы микробиологии. 5: 172. Дои:10.3389 / fmicb.2014.00172. ISSN 1664-302X. ЧВК 4029002. PMID 24860555.
- ^ «Промоторы, используемые для регулирования экспрессии генов». www.cambia.org. Получено 16 февраля 2018.
- ^ Кэмпбелл, Нил А. и Рис, Джейн Б. (2002). Биология (6-е изд.). Сан-Франциско: Эддисон Уэсли. С. 375–401. ISBN 978-0-201-75054-6.
- ^ а б c Питер Уолтер; Альбертс, Брюс; Джонсон, Александр С .; Льюис, Джулиан; Рафф, Мартин С .; Робертс, Кит (2008). Молекулярная биология клетки (5-е издание, расширенная версия). Нью-Йорк: Наука Гарланд. ISBN 978-0-8153-4111-6.. Четвертое издание доступно в Интернете на книжной полке NCBI: связь
- ^ Берг, Джереми Марк; Тимочко, Джон Л .; Страйер, Люберт (2010). Биохимия, 7-е изд. (Биохимия (Берг)). W.H. Фриман и компания. ISBN 978-1-4292-2936-4. Пятое издание доступно онлайн на книжной полке NCBI: связь
- ^ а б Уотсон, Джеймс Д. (2007). Рекомбинантная ДНК: гены и геномы: краткий курс. Сан-Франциско: W.H. Фримен. ISBN 978-0-7167-2866-5.
- ^ Рассел, Дэвид В .; Сэмбрук, Джозеф (2001). Молекулярное клонирование: лабораторное руководство. Колд-Спринг-Харбор, штат Нью-Йорк: Лаборатория Колд-Спринг-Харбор. ISBN 978-0-87969-576-7.
- ^ Hannig, G .; Макридес, С. (1998). «Стратегии оптимизации экспрессии гетерологичных белков в Escherichia coli». Тенденции в биотехнологии. 16 (2): 54–60. Дои:10.1016 / S0167-7799 (97) 01155-4. PMID 9487731.
- ^ Брондык, В. Х. (2009). «Глава 11 Выбор подходящего метода экспрессии рекомбинантного белка». Руководство по очистке белков, 2-е издание. Методы в энзимологии. 463. С. 131–147. Дои:10.1016 / S0076-6879 (09) 63011-1. ISBN 9780123745361. PMID 19892171.
- ^ Ортега, Клаудиа; Прието, Даниэль; Абреу, Сесилия; Оппеццо, Пабло Хавьер; Корреа, Агустин (2018). «Набор векторов с несколькими отсеками и несколькими хозяевами для экспрессии и очистки рекомбинантного белка». Границы микробиологии. 9: 1384. Дои:10.3389 / fmicb.2018.01384. ISSN 1664-302X. ЧВК 6030378. PMID 29997597.
- ^ а б c Браун, Терри (2006). Клонирование генов и анализ ДНК: введение. Кембридж, Массачусетс: Blackwell Pub. ISBN 978-1-4051-1121-8.
- ^ а б Ye, X .; Аль-Бабили, С .; Klöti, A .; Zhang, J .; Lucca, P .; Beyer, P .; Потрикус, И. (2000). «Разработка пути биосинтеза провитамина А (бета-каротин) в (не содержащий каротиноидов) эндосперм риса». Наука. 287 (5451): 303–305. Bibcode:2000Sci ... 287..303Y. Дои:10.1126 / science.287.5451.303. PMID 10634784.
- ^ Koller, B.H .; Smithies, О. (1992). «Изменение генов у животных путем нацеливания на гены». Ежегодный обзор иммунологии. 10: 705–730. Дои:10.1146 / annurev.iy.10.040192.003421. PMID 1591000.
- ^ Донна У. Фогт и Микки Пэриш. (1999) Пищевая биотехнология в США: наука, регулирование и проблемы
- ^ Gualandi-Signorini, A .; Георгий, Г. (2001). «Препараты инсулина - обзор». Европейский обзор медицинских и фармакологических наук. 5 (3): 73–83. PMID 12004916.
- ^ # Инсулин аспарт
- ^ DrugBank: Обычный инсулин (DB00030)
- ^ Von Fange, T .; McDiarmid, T .; MacKler, L .; Золотор, А. (2008). «Клинические исследования: Может ли рекомбинантный гормон роста эффективно лечить идиопатический низкий рост?». Журнал семейной практики. 57 (9): 611–612. PMID 18786336.
- ^ Fernandez, M .; Хози, Р. (2009). «Наркотики ловят и неспортивных людей». Журнал семейной практики. 58 (1): 16–23. PMID 19141266.
- ^ Манко-Джонсон, М. Дж. (2010). «Достижения в уходе и лечении детей с гемофилией». Достижения в педиатрии. 57 (1): 287–294. Дои:10.1016 / j.yapd.2010.08.007. PMID 21056743.
- ^ а б Пейн, Дж. А .; Шиптон, К. А .; Chaggar, S .; Howells, R.M .; Кеннеди, М. Дж .; Vernon, G .; Wright, S. Y .; Hinchliffe, E .; Adams, J. L .; Сильверстоун, A. L .; Дрейк, Р. (2005). «Повышение питательной ценности золотого риса за счет увеличения содержания провитамина А». Природа Биотехнологии. 23 (4): 482–487. Дои:10.1038 / nbt1082. PMID 15793573. S2CID 632005.
- ^ Deccan Herald, «Иностранная группа поддерживает« золотой рис »в Индии», 18 марта 2015 г. http://www.deccanherald.com/content/466247/foreign-group-roots-golden-rice.html
- ^ Funke, T .; Han, H .; Healy-Fried, M .; Фишер, М .; Шенбрунн, Э. (2006). «Молекулярная основа устойчивости к гербицидам культур Roundup Ready». Труды Национальной академии наук. 103 (35): 13010–13015. Bibcode:2006ПНАС..10313010Ф. Дои:10.1073 / pnas.0603638103. ЧВК 1559744. PMID 16916934.
- ^ Мендельсон, М .; Kough, J .; Vaituzis, Z .; Мэтьюз, К. (2003). "Безопасны ли Bt-культуры?". Природа Биотехнологии. 21 (9): 1003–1009. Дои:10.1038 / nbt0903-1003. PMID 12949561. S2CID 16392889.
- ^ Лир, Дж. (1978). Рекомбинантная ДНК: невыразимая история. Нью-Йорк: Crown Publishers. п. 43.
- ^ а б Джексон, Д .; Саймонс, Р.; Берг, П. (1972). «Биохимический метод встраивания новой генетической информации в ДНК обезьяньего вируса 40: кольцевые молекулы ДНК SV40, содержащие гены лямбда-фага и оперон галактозы Escherichia coli». Труды Национальной академии наук Соединенных Штатов Америки. 69 (10): 2904–2909. Bibcode:1972PNAS ... 69.2904J. Дои:10.1073 / пнас.69.10.2904. ЧВК 389671. PMID 4342968.
- ^ Mertz, J. E .; Дэвис, Р. У. (1972). «Расщепление ДНК эндонуклеазой рестрикции R 1 приводит к образованию липких концов». Труды Национальной академии наук Соединенных Штатов Америки. 69 (11): 3370–4. Bibcode:1972ПНАС ... 69.3370М. Дои:10.1073 / pnas.69.11.3370. ЧВК 389773. PMID 4343968.
- ^ Лоббан, П .; Кайзер, А. (1973). «Ферментативное соединение молекул ДНК от конца к концу». Журнал молекулярной биологии. 78 (3): 453–471. Дои:10.1016/0022-2836(73)90468-3. PMID 4754844.
- ^ Cohen, S .; Чанг, А .; Boyer, H .; Хеллинг, Р. (1973). «Конструирование биологически функциональных бактериальных плазмид in vitro». Труды Национальной академии наук Соединенных Штатов Америки. 70 (11): 3240–3244. Bibcode:1973PNAS ... 70.3240C. Дои:10.1073 / пнас.70.11.3240. ЧВК 427208. PMID 4594039.
- ^ Хьюз, С. (2001). «Создание долларов из ДНК. Первый крупный патент в области биотехнологии и коммерциализации молекулярной биологии, 1974-1980 гг.» (PDF). Исида; Международный обзор, посвященный истории науки и ее культурному влиянию. 92 (3): 541–575. Дои:10.1086/385281. HDL:10161/8125. PMID 11810894.
- ^ Джонсон, И. С. (1983). «Человеческий инсулин из технологии рекомбинантной ДНК». Наука. 219 (4585): 632–637. Bibcode:1983Sci ... 219..632J. Дои:10.1126 / science.6337396. PMID 6337396.
- ^ Ван, Син; Хантер, Алан К .; Мозье, Нед М. (15.06.2009). «Белки клетки-хозяина в разработке биопрепаратов: идентификация, количественное определение и оценка риска». Биотехнологии и биоинженерия. 103 (3): 446–458. Дои:10.1002 / бит. 22304. ISSN 0006-3592. PMID 19388135. S2CID 22707536.
- ^ Bracewell, Daniel G .; Фрэнсис, Ричард; Smales, К. Марк (2015-07-14). «Будущее идентификации белков клетки-хозяина (HCP) во время разработки процесса и производства связано с управлением, основанным на оценке риска». Биотехнологии и биоинженерия. 112 (9): 1727–1737. Дои:10.1002 / бит. 25628. ISSN 0006-3592. ЧВК 4973824. PMID 25998019.
дальнейшее чтение
- Восьмой день творения: создатели революции в биологии. Книги Touchstone, ISBN 0-671-22540-5. 2-е издание: Cold Spring Harbor Laboratory Press, 1996 г., мягкая обложка: ISBN 0-87969-478-5.
- Миклас, Дэвид. 2003 г. Наука о ДНК: первый курс. Пресса Колд Спринг Харбор: ISBN 978-0-87969-636-8.
- Расмуссен, Николас, Джин-Жокеи: Наука о жизни и рост биотехнологического предприятия, Johns Hopkins University Press, (Балтимор), 2014 г.. ISBN 978-1-42141-340-2.
- Розенфельд, Израиль. 2010 г. ДНК: графический путеводитель по молекуле, потрясшей мир. Издательство Колумбийского университета: ISBN 978-0-231-14271-7.
- Шульц, Марк и Зандер Кэннон. 2009 г. Материал жизни: графическое руководство по генетике и ДНК. Хилл и Ван: ISBN 0-8090-8947-5.
- Ватсон, Джеймс. 2004 г. ДНК: секрет жизни. Случайный дом: ISBN 978-0-09-945184-6.
внешняя ссылка
| Библиотечные ресурсы о Рекомбинантные белки |
- Информационный бюллетень по рекомбинантной ДНК (из Университета Нью-Гэмпшира)
- Плазмиды в дрожжах (Информационный бюллетень Государственного университета Сан-Диего)
- Анимация, иллюстрирующая создание рекомбинантной ДНК и продукцию чужеродного белка рекомбинантными бактериями
- Исследование рекомбинантной ДНК в UCSF и коммерческое применение в Genentech Отредактированная стенограмма интервью 1994 года с Гербертом В. Бойером, проект «Живая история». Устная история.
- Руководство по принципам и методам очистки рекомбинантных белков
