Талимоген лахерпарепвец - Talimogene laherparepvec - Wikipedia
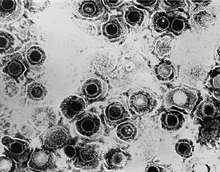 Просвечивающая электронная микрофотография немодифицированного вируса простого герпеса | |
| Генная терапия | |
|---|---|
| Целевой ген | GM-CSF |
| Вектор | Вирус простого герпеса 1 |
| Клинические данные | |
| Торговые наименования | Т-Век, Имлиджик, Онковекс |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a616006 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Инъекция |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| Количество CAS | |
| DrugBank | |
| ChemSpider |
|
| UNII | |
| КЕГГ | |
Талимоген лахерпарепвец[а] это биофармацевтический лекарство для лечения меланома что нельзя прооперировать; он вводится непосредственно в подмножество поражений, что вызывает системный иммунный ответ против рака пациента.[3] Заключительный четырехлетний анализ основного исследования фазы 3, по результатам которого TVEC был одобрен FDA, показал уровень отклика 31,5% при 16,9%. CR ставка. Также наблюдалось существенное и статистически значимое улучшение выживаемости у пациентов с более ранним метастатическим заболеванием (стадии IIIb-IVM1a) и у пациентов, которые ранее не получали системного лечения меланомы. В группе более ранней стадии риск смерти снизился примерно на 50%, причем каждый четвертый пациент, похоже, соответствовал медицинскому определению излечения или был близок к нему.[4] Использование талимогена лахерпарепвек в реальном мире показало, что частота ответа достигает 88,5%, а частота полного ответа достигает 61,5%.[5]
Около половины людей, получавших талимоген лахерпарепвек в ходе клинических испытаний, испытывали усталость и озноб; около 40% страдали лихорадкой, около 35% - тошнотой и около 30% имели симптомы гриппа, а также боль в месте инъекции. Реакции были от легкой до умеренной по степени тяжести; 2% людей имели тяжелые реакции, обычно целлюлит.[6]
Талимоген лахерпарепвек - это генно-инженерный вирус герпеса ( вирус онколитического герпеса ). Были удалены два гена - один, который отключает защиту отдельной клетки, другой, который помогает вирусу уклоняться от иммунной системы, - и ген человеческого GM-CSF был добавлен. Лекарство действует путем репликации в раковых клетках, заставляя их лопаться; он также был разработан для стимуляции иммунного ответа против рака пациента, что было продемонстрировано множеством данных, включая регрессию опухолей, в которые не вводили талимоген лахерпарепвек.[7][3]
Препарат был создан и первоначально разработан компанией BioVex, Inc. и продолжен Amgen, которая приобрела BioVex в 2011 году.[8] Это был первый онколитическая иммунотерапия одобрен во всем мире; он был одобрен в США в октябре 2015 года и одобрен в Европе в декабре 2015 года.[9][7][10]
Медицинское использование
Талимоген лахерпарепвек доставляется путем инъекции непосредственно в опухоли, тем самым создавая системный противоопухолевый иммунный ответ.[11]
В США талимоген лахерпарепвек одобрен FDA для лечения пациентов с меланомой стадии IIIb-IVM1c, которым хирургическое вмешательство нецелесообразно, и с опухолями, которые можно вводить напрямую; одобренная EMA популяция в Европе относится к стадиям IIIb-IVM1a.[11][6]
Доказано, что талимоген лахерпарепвек значительно увеличивает выживаемость пациентов с меланомой стадии IIIb-IVM1a и пациентов, которые ранее не получали системную терапию меланомы.[12]
Побочные эффекты
Около половины людей, получавших талимоген лахерпарепвек в ходе клинических испытаний, испытывали усталость и озноб; около 40% страдали лихорадкой, около 35% - тошнотой и около 30% имели симптомы гриппа, а также боль в месте инъекции. Реакции были от легкой до умеренной по степени тяжести; 2% людей имели тяжелые реакции, обычно целлюлит.[6]
Более 10% людей имели отек, головная боль, кашель, рвота, диарея, запор, мышечная боль или боль в суставах. От 1% до 10% в очаге поражения развились герпес, боль или инфекция, анемия, иммуно-опосредованные события (например, васкулит, пневмония, обострение псориаза, гломерулонефрит и витилиго[13] ), обезвоживание, спутанность сознания, беспокойство, депрессия, головокружение, бессонница, боль в ушах, быстрое сердцебиение, глубокие венозные тромбы, высокое кровяное давление, приливы, одышка при тренировке, боль в горле, симптомы простуда, боль в животе, боль в спине, боль в паху, потеря веса или выделения из места инъекции.[6]
Фармакология
Талимоген лахерпарепвек поглощается нормальными клетками и раковыми клетками, такими как клетки дикого типа. Вирус простого герпеса, очищается таким же образом.[6]
Механизм
Талимоген лахерпарепвек непосредственно разрушает раковые клетки, которые он заражает, вызывая системный иммунный ответ против рака пациента.[7][3]
Вирус проникает как в раковые, так и в здоровые клетки, но он не может продуктивно размножаться в здоровых тканях, потому что ему не хватает Белок инфицированных клеток 34,5 (ICP34.5). Когда клетки заражены вирусом, они отключаются и умирают, но ICP34.5 блокирует это. реакция на стресс, позволяя вирусу захватить клетки перевод машины, чтобы копировать себя. Вирус герпеса, у которого отсутствует ген, кодирующий ICP34.5, не может реплицироваться в нормальной ткани. Однако во многих раковых клетках стрессовая реакция уже нарушена, поэтому вирус, лишенный ICP34.5, все еще может реплицироваться в опухолях. После многократной репликации вируса клетка набухает и, наконец, лопается, убивая клетку и высвобождая копии вируса, которые затем могут инфицировать соседние клетки.[3][14]
Хотя талимоген laherparepvec использует механизм трансляции клетки для репликации, он также использует его, чтобы заставить клетку создавать GM-CSF. GM-CSF секретируется или высвобождается, когда раковые клетки лопаются, привлекая дендритные клетки к участку, который собирает опухолевые антигены, обрабатывает их, а затем представляет их на своей поверхности для цитотоксические (киллеры) Т-клетки что, в свою очередь, вызывает иммунный ответ.[7][3]
Сочинение
Talimogen laherparepvec - это биофармацевтический препарат, средство, медикамент; это вирус онколитического герпеса это было создано генная инженерия напряжение вирус простого герпеса 1 (HSV-1), полученный от человека, инфицированного вирусом, а не лабораторного штамма.[7] Обе копии вирусного гена, кодирующего ICP34.5 были удалены и заменены геном, кодирующим человеческий GM-CSF, и ген, кодирующий ICP47 был удален.[7][3][15] У дикого вируса герпеса ICP47 подавляет иммунный ответ на вирус; он был удален, потому что препарат был разработан с целью активировать иммунную систему.[3]
История
Первым онколитическим вирусом, одобренным регулирующим органом, был генетически модифицированный аденовирус под названием H101 компании Shanghai Sunway Biotech. В 2005 году он получил одобрение от государственного управления по контролю за продуктами и лекарствами Китая (SFDA) для лечения рака головы и шеи.[16] Талимоген лахерпарепвек - это первая в мире одобренная онколитическая иммунотерапия, т. Е. Он также был разработан для обеспечения системного противоопухолевого действия за счет индукции противоопухолевого иммунного ответа.
Talimogen laherparepvec был создан и первоначально разработан компанией BioVex, Inc. под брендом OncoVEX.GM-CSF. Развитие продолжили Amgen, которая приобрела BioVex в 2011 году.[8][7] BioVex была основана в 1999 году на основе исследования Роберта Коффина в Университетский колледж Лондона,[17] и переехал в Уоберн, Массачусетс в 2005 году, оставив около половины сотрудников в Великобритании.[18]
В клиническое испытание фазы II в меланоме был опубликован в 2009 году[19] и фаза III испытания вышла в 2013 году.[20]
Талимоген лахерпарепвек был одобрен Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США лечить меланома в октябре 2015 года. Это было первое одобрение онколитический вирус и первое одобрение генной терапии на Западе.[9] Он был одобрен Европейское агентство по лекарствам в декабре того же года.[6][7]
Общество и культура
Экономика
По оценкам Amgen, талимоген лахерпарепвек будет стоить 65 000 долларов США на пациента на момент утверждения.[21]
Исследование
По состоянию на 2016 год талимоген лахерпарепвек изучался на ранних стадиях клинических испытаний в панкреатический рак, саркома мягких тканей, и плоскоклеточный рак головы и шеи; он также был протестирован в сочетании с ингибиторы контрольных точек ипилимумаб и пембролизумаб.[7]
Смотрите также
Примечания
- ^ /тəˈлɪмədʒяплəˌчасɜːrпəˈрɛпvɛk/ tə-LIM-ə-jeen lə-HUR-pə-REP-век (T-Vec, торговое название Imlygic, ранее назывался OncoVexGM-CSF)[2]
Рекомендации
- ^ «Талимоген лахерпарепвек (имлигик) во время беременности». Drugs.com. 25 декабря 2019 г.. Получено 2 апреля 2020.
- ^ «Талимоген лахерпарепвец». AdisInsight. Получено 16 октября 2016.
- ^ а б c d е ж грамм Фукухара Х, Ино Й, Тодо Т (октябрь 2016 г.). «Онколитическая вирусная терапия: новая эра лечения рака на заре». Наука о раке. 107 (10): 1373–1379. Дои:10.1111 / cas.13027. ЧВК 5084676. PMID 27486853.
- ^ Андтбака Р.Х., Колличио Ф., Харрингтон К.Дж., Миддлтон М.Р., Дауни Г., Эрлинг К., Кауфман Х.Л. (июнь 2019 г.). «Заключительный анализ OPTiM: рандомизированное испытание фазы III талимогена лахерпарепвек по сравнению с фактором, стимулирующим колонию гранулоцитов-макрофагов, при неоперабельной меланоме III-IV стадии». Журнал иммунотерапии рака. 7 (1): 145. Дои:10.1186 / s40425-019-0623-z. ЧВК 6554874. PMID 31171039.
- ^ Franke V, Berger DM, Klop WM, van der Hiel B, van de Wiel BA, Ter Meulen S, Wouters MW, van Houdt WJ, van Akkooi AC (август 2019 г.). «Высокая частота ответа на T-VEC при ранней метастатической меланоме (стадия IIIB / C-IVM1a)». Международный журнал рака. 145 (4): 974–978. Дои:10.1002 / ijc.32172. PMID 30694555.
- ^ а б c d е ж "Imlygic". Европейское агентство по лекарствам. Получено 16 октября 2016. Видеть Приложение 1: Обзор характеристик продукта; последнее обновление 7 сентября 2016 г.
- ^ а б c d е ж грамм час я Билсланд А.Е., Спилиопулу П., Эванс Т.Р. (2016). "Виротерапия: наконец-то генная терапия рака?". F1000 Исследования. 5: 2105. Дои:10.12688 / f1000research.8211.1. ЧВК 5007754. PMID 27635234.
- ^ а б «Amgen покупает BioVex, производителя противораковых препаратов». Новости Bloomberg через The New York Times. 24 января 2011 г.
- ^ а б «FDA одобряет инъекционную иммунотерапию меланомы Amgen». Рейтер. 27 октября 2015 г.
- ^ «Имлыгик (талимоген лахерпарепвек)». НАС. Управление по контролю за продуктами и лекарствами (FDA). 1 марта 2018. Архивировано 23 апреля 2019 года.. Получено 1 апреля 2020.CS1 maint: неподходящий URL (связь)
- ^ а б "Imlygic label" (PDF). FDA. Октябрь 2015 г.. Получено 16 октября 2016. Для обновлений этикеток см. Индексная страница FDA для BLA 125518
- ^ Конри Р.М., Уэстбрук Б., Макки С., Норвуд Т.Г. (3 апреля 2018 г.). «Талимоген лахерпарепвек: первая в своем классе онколитическая виротерапия». Hum Vaccin Immunother. 14 (4): 839–846. Дои:10.1080/21645515.2017.1412896. ЧВК 5893211. PMID 29420123.
- ^ Харрингтон К.Дж., Михиелин О., Мальвехи Дж., Пеццани Грютер И., Гроув Л., Фраучигер А.Л., Даммер Р. (август 2017 г.). «Практическое руководство по обращению с талимогеном лахерпарепвек и его применению в Европе». ОнкоЦели и терапия. 10: 3867–3880. Дои:10.2147 / OTT.S133699. ЧВК 5546812. PMID 28814886. 101514322.
- ^ Агарвалла ПК, Аги МК (2012). «Разработка и подготовка онколитического вируса простого герпеса». Онколитические вирусы. Методы молекулярной биологии. 797. С. 1–19. Дои:10.1007/978-1-61779-340-0_1. ISBN 978-1-61779-339-4. PMID 21948465.
- ^ Лю Б.Л., Робинсон М., Хан З.К., Бранстон Р.Х., Инглиш К., Рей П. и др. (Февраль 2003 г.). «ICP34.5 удаленный вирус простого герпеса с усиленными онколитическими, иммуностимулирующими и противоопухолевыми свойствами». Генная терапия. 10 (4): 292–303. Дои:10.1038 / sj.gt.3301885. PMID 12595888.
- ^ Гарбер К. (март 2006 г.). «Китай одобрил первую в мире онколитическую вирусную терапию для лечения рака». Журнал Национального института рака. 98 (5): 298–300. Дои:10.1093 / jnci / djj111. PMID 16507823.
- ^ Тиммерман Л. (30 марта 2009 г.). «BioVex привлекает 40 миллионов долларов на вирус, борющийся с раком». Xconomy.
- ^ Тиммерман Л. (1 июня 2008 г.). «Вирусное лечение BioVex уменьшает опухоли меланомы в испытаниях». Xconomy.
- ^ Сензер Н.Н., Кауфман Х.Л., Аматруда Т., Немунайтис М., Рид Т., Дэниэлс Г. и др. (Декабрь 2009 г.). «Фаза II клинических испытаний онколитического герпесвируса второго поколения, кодирующего гранулоцитарно-макрофагальный колониестимулирующий фактор, у пациентов с неоперабельной метастатической меланомой». Журнал клинической онкологии. 27 (34): 5763–71. Дои:10.1200 / JCO.2009.24.3675. PMID 19884534.
- ^ Andtbacka RH, Collichio FA, Amatruda T, Senzer NN, Chesney J, Delman KA и др. «OPTiM: рандомизированное испытание фазы III талимогена лахерпарепвека (T-VEC) по сравнению с подкожным (SC) гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF) для лечения (tx) нерезецированной меланомы IIIB / C и IV стадии». Журнал клинической онкологии. 31 (приложение): LBA9008.
- ^ «Одобрение FDA США препарата Imlygic является первым препаратом для лечения вирусной онкологии». Журнал точной медицины. 5 ноября 2015.
внешняя ссылка
- «Талимоген лахерпарепвец». Портал информации о наркотиках. Национальная медицинская библиотека США.
