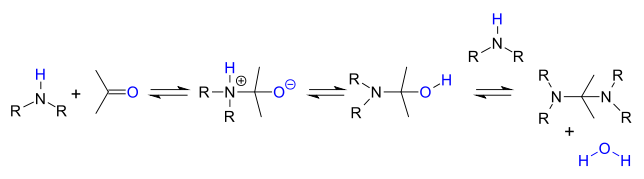Алкилимино-дезоксо-бис-замещение - Alkylimino-de-oxo-bisubstitution
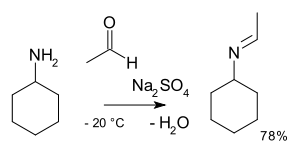
Алкилимино-дезоксо-бис-замещение в органическая химия это органическая реакция из карбонил соединения с амины к имины.[2] Название реакции основано на Номенклатура преобразований ИЮПАК. Реакция кислотный катализатор и тип реакции нуклеофильное присоединение амина в карбонильное соединение с последующим переносом протон от азота до кислорода до стабильного полуаминальный или карбиноламин. С первичными аминами вода теряется в реакция элиминации для я добываю. С арил особенно стабильные амины Базы Шиффа сформированы.
Механизм реакции
Шаги реакции обратимые реакции и реакция доводится до завершения за счет удаления воды за счет азеотропная дистилляция, молекулярные сита или же тетрахлорид титана. Первичные амины реагируют через нестабильную полуаминальный промежуточное соединение, которое затем отщепляет воду.
Вторичные амины нелегко теряют воду, потому что у них нет доступного протона, и вместо этого они часто реагируют дальше на аминальный:
или когда α-карбонильный протон присутствует в енамин:
В кислой среде продукт реакции представляет собой иминий соль за счет потери воды.
Этот тип реакции встречается во многих Гетероцикл подготовка, например, Поварова реакция и Фридлендер-синтез к хинолины.
Поскольку оба компонента настолько реактивны, молекула не несет альдегид и одновременно аминогруппа, если аминогруппа не снабжена защитная группа. В качестве дополнительной демонстрации реактивности одно исследование[3] исследовал свойства α-формил азиридин который был найден димеризовать как оксазолидин по формированию из соответствующих сложный эфир к органическое восстановление с ДИБАЛ:[4]

Образование иминиевого иона запрещено в этой молекуле, потому что азириновая группа и формильная группа считаются ортогональный.
Объем
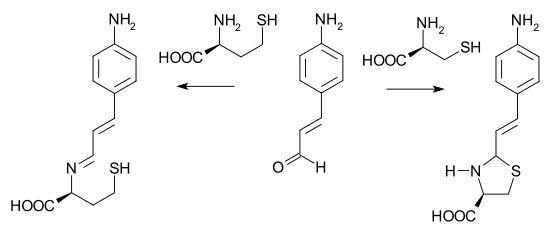
В одном потенциальном приложении[5] п-аминокоричный альдегид умеет различать цистеин и гомоцистеин. В случае цистеина водный буферный раствор альдегида меняет цвет с желтого на бесцветный из-за вторичной реакции замыкания кольца имина. Гомоцистеин не может замкнуть кольцо, и цвет не меняется.
Рекомендации
- ^ Органический синтез, Сб. Vol. 6, p.901 (1988); Vol. 50, стр.66 (1970). Статья В архиве 2012-07-28 в Wayback Machine
- ^ Марш Джерри; (1985). Продвинутая органическая химия: реакции, механизмы и структура (3-е изд.). Нью-Йорк: John Wiley & Sons, inc. ISBN 0-471-85472-7
- ^ Хили, Райан; Юдин, Андрей К. (2006). «Легкодоступные незащищенные аминоальдегиды». Журнал Американского химического общества. 128 (46): 14772–14773. Дои:10.1021 / ja065898s. PMID 17105264.
- ^ Димер реагирует с борогидрид натрия через мономер он находится в равновесие с азиридином алкоголь
- ^ Ван, Вэйхуа; Русин Александр; Сюй, Сянъян; Ким, Кю Кван; Эскобедо, Хорхе О .; Fakayode, Sayo O .; Флетчер, Кристин А .; Лоури, Марк; Schowalter, Corin M .; Лоуренс, Кэндис М .; Fronczek, Frank R .; Уорнер, Исайя М .; Стронгин, Роберт М. (2005). «Обнаружение гомоцистеина и цистеина». Журнал Американского химического общества. 127 (45): 15949–15958. Дои:10.1021 / ja054962n. ЧВК 3386615. PMID 16277539.
внешняя ссылка
- реакция бензальдегид и метиламин в Органический синтез Coll. Vol. 10, стр. 312 (2004 г.); Vol. 76, стр. 23 (1999). Интернет-статья
- реакция метилбензиламин с 2-метилциклогексаноном в Органический синтез, Сб. Vol. 9, стр. 610 (1998); Vol. 70, стр. 35 (1992). Статья
- Реакция ацетофенон с метиламин в Органический синтез, Сб. Vol. 6, стр. 818 (1988); Vol. 54, стр. 93 (1974). Статья
- Хиральный База Шиффа в Молбанк 2005, М435 Статья