Перестановка Курция - Curtius rearrangement
| Перестановка Курция | |
|---|---|
| Названный в честь | Теодор Курций |
| Тип реакции | Реакция перестановки |
| Идентификаторы | |
| Портал органической химии | curtius-перестановка |
| RSC ID онтологии | RXNO: 0000054 |
В Перестановка Курция (или же Курциус реакция или же Курциус деградация), впервые определенная Теодор Курций в 1885 г. термическое разложение из ацилазид для изоцианат с потерей азот газ.[1][2] Затем изоцианат подвергается атаке со стороны различных нуклеофилы например, вода, спирты и амины, чтобы получить первичный амин, карбамат или же производное мочевины соответственно.[3] Опубликовано несколько обзоров.[4][5]

Получение ацилазида
Ацилазид обычно получают по реакции хлорангидриды или же Anydrides[6] с азид натрия или же триметилсилилазид.[7] Ацилазиды также получают при обработке ацилгидразины с азотистая кислота.[8] Альтернативно, ацилазид может быть образован прямой реакцией карбоновой кислоты с дифенилфосфорилазид (DPPA).[9]

Механизм реакции
Считалось, что перегруппировка Курциуса представляет собой двухступенчатый процесс с потерей газообразного азота, образующей ацилнитрен с последующей миграцией R-группы для получения изоцианат. Однако недавние исследования показали, что термическое разложение - это согласованный процесс, причем обе стадии происходят вместе из-за отсутствия каких-либо побочных продуктов введения или добавления нитрена, наблюдаемых или выделяемых в реакции.[10] Термодинамические расчеты также подтверждают согласованный механизм.[11]
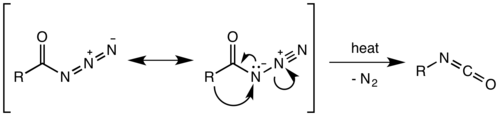
Миграция происходит с полным сохранением конфигурации в R-группе. В способность к миграции R-группы примерно третичный> вторичный арил> первичный. Образовавшийся изоцианат затем может быть гидролизованный дать первичный амин, или пройти нуклеофильная атака с спирты и амины с образованием карбаматы и производные мочевины соответственно.
Модификации
Исследования показали, что перестановка Курция катализированный обоими Brønsted[12] и Кислоты Льюиса, посредством протонирования или координации ацильного атома кислорода соответственно. Например, Фар и Нойман показали, что использование трифторид бора или же трихлорид бора Катализатор снижает температуру разложения, необходимую для перегруппировки, примерно на 100 ° C и значительно увеличивает выход изоцианата.[13]
Фотохимическая перегруппировка
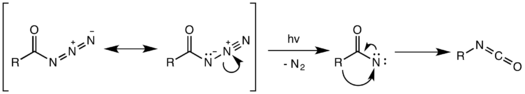
Фотохимический также возможно разложение ацилазида.[14] Однако фотохимическая перестройка не согласована и вместо этого происходит нитрен промежуточный, образованный разрывом слабой связи N – N и потерей газообразного азота. Нитрен с высокой реакционной способностью может претерпевать множество нитреновых реакций, таких как вставка нитрена и кроме того, давая нежелательные побочные продукты.[15] В приведенном ниже примере промежуточный нитрен вставляется в одну из связей C – H циклогексанового растворителя с образованием N-циклогексилбензамида в качестве побочного продукта.

Вариации
Дарапская деградация
В одном из вариантов под названием Дарапская деградация,[16] или же Дарапский синтез, перегруппировка Курциуса имеет место как одна из стадий превращения α-цианоэфира в аминокислота. Гидразин используется для преобразования сложного эфира в ацилгидразин, который реагирует с азотистая кислота с получением ацилазида. Нагрев азида в этиловый спирт дает этилкарбамат через перегруппировку Курциуса. Кислотный гидролиз дает амин из карбамата и карбоновую кислоту из нитрила одновременно, давая продукт аминокислоту.[17]

Реакция Харгера
Фотохимическая Курциус-подобная миграция и перегруппировка фосфинового азида приводит к образованию метафосфонимидата.[18] в том, что также известно как Реакция Харгера (назван в честь доктора Мартина Харгера из Университет Лестера ).[19] За этим следует гидролиз, в примере ниже с метанол, чтобы получить фосфонамидат.

В отличие от перегруппировки Курциуса, существует выбор R-групп фосфинового азида, которые могут мигрировать. Харгер обнаружил, что алкильные группы мигрируют преимущественно в арильные группы, и это предпочтение возрастает в порядке метил <первичный <вторичный <третичный. Вероятно, это происходит из-за стерических и конформационных факторов, поскольку чем больше R-группа, тем менее благоприятна конформация для миграции фенила.[20]
Синтетические приложения
Перегруппировка Курциуса терпима к большому разнообразию функциональные группы, и имеет значительную синтетическую полезность, поскольку может быть включено множество различных групп в зависимости от выбора нуклеофил используется для атаки изоцианата.
Например, при проведении в присутствии терт-бутанол, реакция порождает Boc -защищенный амины, полезные промежуточные соединения в органический синтез.[21][22]Аналогичным образом, когда реакция Курциуса проводится в присутствии бензиловый спирт, КБЗ -защищенные амины.[23]
Перегруппировка Курциуса используется при синтезе лекарств. транилципромин, кандесартан, бромадол, тергурид, бензидамин, габапентин, игмезин и текаденозон.
Трихинацен
Р. Б. Вудворд и другие. использовал перестановку Курция как один из шагов в полный синтез из полихинан трихинацен в 1964 году. После гидролиза сложного эфира в промежуточном продукте (1), перегруппировка Курциуса была проведена для преобразования групп карбоновой кислоты в (2) к метилкарбаматным группам (3) с доходностью 84%. Дальнейшие шаги затем дали трихинацен (4).[24]

Осельтамивир
В своем синтезе противовирусное средство препарат, средство, медикамент осельтамивир, также известный как Тамифлю, Ishikawa et al. использовали перегруппировку Курциуса на одной из ключевых стадий превращения ацилазида в амидную группу в молекуле-мишени. В этом случае изоцианат, образующийся в результате перегруппировки, подвергается атаке карбоновой кислоты с образованием амида. Все последующие реакции могут быть проведены в одном реакционном сосуде с получением конечного продукта с общим выходом 57%. Важное преимущество реакции Курциуса, отмеченное авторами, состояло в том, что ее можно было проводить при комнатной температуре, что сводило к минимуму опасность нагрева. В целом схема была очень эффективной: для производства этого важного и ценного препарата, используемого для лечения птичий грипп.[25]

Диеводиамин
Диеводиамин - это натуральный продукт из растения Evodia rutaecarpa, широко используемого в традиционная китайская медицина. Ансуорт и др. защитная группа -свободный полный синтез диэводиамина использует перегруппировку Курциуса на первой стадии синтеза, катализируемую трифторид бора. Затем активированный изоцианат быстро реагирует с индол кольцо в электрофильное ароматическое замещение реакция дает амид с выходом 94%, и последующие стадии дают диэводамин.[26]

Смотрите также
- Перестановка Бекмана
- Деградация Бергмана
- Перегруппировка Гофмана
- Перестановка Лоссена
- Реакция Шмидта
- Перестановка Тимана
- Перестановка Небера
- Перестановка Вольфа
Рекомендации
- ^ Курций, Т. (1890). "Ueber Stickstoffwasserstoffsäure (Азоимид) N3ЧАС" [О азоимиде азоимидазойной кислоты N3ЧАС]. Berichte der Deutschen Chemischen Gesellschaft zu Berlin. 23 (2): 3023–3033. Дои:10.1002 / cber.189002302232.
- ^ Курций, Т. (1894). "20. Организатор гидразидов и азидов Säuren I. Abhandlung" [Гидразиды и азиды органических кислот I. Статья]. Journal für Praktische Chemie. 50: 275–294. Дои:10.1002 / prac.18940500125.
- ^ Kaiser, C .; Вайншток, Дж. (1988). «Амины из смешанных карбоново-угольных ангидридов: 1-фенилциклопентиламин». Органический синтез.; Коллективный объем, 6, п. 910
- ^ Смит, П.А.С. (1946). «Реакция Курция». Органические реакции. 3: 337–449.
- ^ Скривен, Эрик Ф. В .; Тернбулл, Кеннет (1988). «Азиды: их получение и синтетическое использование». Химические обзоры. 88 (2): 297–368. Дои:10.1021 / cr00084a001.
- ^ Weinstock, J (1961). «Модифицированная реакция Курциуса». J. Org. Chem. 26: 3511. Дои:10.1021 / jo01067a604.
- ^ Warren, J.D .; Press, J. B. (1980). «Образование и перегруппировка Курциуса ацилазидов из инертных хлорангидридов». Synth. Сообщество. 10: 107–110. Дои:10.1080/00397918008061812.
- ^ Позгай, В .; Дженнингс, Х. Дж. (1987). «Синтез азидов со стабильными нитрозильными солями». Tetrahedron Lett. 28 (43): 5091–5092. Дои:10.1016 / s0040-4039 (00) 95598-9.
- ^ Shioiri, T .; Ninomiya, K .; Ямада, С. (1972). «Новый удобный реагент для модифицированной реакции Курциуса и пептидного синтеза». Варенье. Chem. Soc. 94 (17): 6203–6205. Дои:10.1021 / ja00772a052. PMID 5054412.
- ^ Раук, А .; Алевуд, П. Ф. (1977). «Теоретическое исследование перегруппировки Курциуса. Электронная структура и взаимопревращение разновидностей CHNO». Может. J. Chem. 55 (9): 1498–1510. Дои:10.1139 / v77-209.
- ^ Л'Аббе, Г. (1969). «Реакции разложения и присоединения органических азидов». Chem. Rev. 69 (3): 345–363. Дои:10.1021 / cr60259a004.
- ^ Yukawa, Y .; Цуно, Ю. (1959). «Разложение замещенных бензазидов в кислых растворителях, кислотный катализ». Варенье. Chem. Soc. 81: 2007–2012. Дои:10.1021 / ja01517a055.
- ^ Fahr, E .; Нойман, Л. (1965). "Курциус-Реактион мит Бортрихалогениден". Энгью. Chem. 77 (13): 591. Дои:10.1002 / ange.19650771308.
- ^ Wentrup, C .; Борнеманн, Х. (2005). «Повторное обращение к перегруппировке ацилазидов Курциуса - образование цианата». Евро. J. Org. Chem.: 4521–4524. Дои:10.1002 / ejoc.200500545.
- ^ Eibler, E .; Зауэр, Дж. (1974). "Ein Betrag zur Isocyanatbildung bei der Photolyse von Acylaziden". Tetrahedron Lett. 15 (30): 2569–2572. Дои:10.1016 / s0040-4039 (01) 92295-6.
- ^ Август Дарапски (1936) "Дарстеллунг фон α-аминосаурена aus Alkyl-cyanessigsigsäuren" (Получение α-аминокислот из алкилцианоуксусных кислот), Journal für Praktische Chemie, 146 : 250-267.
- ^ Gagnon, P.E .; Бовин, П. А .; Крейг, Х. М. (1951). «Синтез аминокислот из замещенных цианоуксусных эфиров». Может. J. Chem. 29: 70–75. Дои:10.1139 / cjc-29-1-70.
- ^ Бертран, G .; Majoral, J .; Басейредо, А. (1980). «Фотолитическая перегруппировка азида фосфора: свидетельство переходного метафосфонимидата». Tetrahedron Lett. 21 (52): 5015–5018. Дои:10.1016 / s0040-4039 (00) 71119-1.
- ^ Harger, M. J. P .; Вестлейк, С. (1982). «Фотолиз некоторых несимметричных азидов фосфиновой кислоты в метаноле». Тетраэдр. 38 (20): 3073–3078. Дои:10.1016/0040-4020(82)80195-6.
- ^ Harger, M. J. P .; Вестлейк, С. (1982). «Фотолиз некоторых несимметричных азидов фосфиновой кислоты в метаноле». Тетраэдр. 38 (20): 3073–3078. Дои:10.1016/0040-4020(82)80195-6.
- ^ Ам Энде, Дэвид Дж .; Деврис, Кейт М .; Клиффорд, Памела Дж .; Бренек, Стивен Дж. (1998). «Калориметрическое исследование для безопасного увеличения масштабов перегруппировки Курциуса акрилоил азида». Исследования и разработки в области органических процессов. 2 (6): 382–392. Дои:10.1021 / op970115w.
- ^ Lebel, H .; Леоган О. (2005). "Boc-защищенные амины посредством мягкой и эффективной перегруппировки Курциуса в одном реакторе". Органические буквы. 7 (19): 4107–4110. Дои:10.1021 / ol051428b. PMID 16146363.
- ^ Джессап, П. Дж .; Petty, C. B .; Roos, J .; Оверман, Л. Э. (1988). "1-N-Ациламино-1,3-диены из 2,4-пентадиеновых кислот перегруппировкой Курциуса: бензил транс-1,3-бутадиен-1-карбамат ». Органический синтез.; Коллективный объем, 6, п. 95
- ^ Woodward, R. B .; Фукунага, Т .; Келли, Р. К. (1964). «Трихинацен». Варенье. Chem. Soc. 86 (15): 3162–3164. Дои:10.1021 / ja01069a046.
- ^ Ishikawa, H .; Сузуки, Т .; Хаяси, Ю. (2009). «Высокопроизводительный синтез противогриппозного ингибитора нейрамидазы (-) - осельтамивира с помощью трех« однокомпонентных »операций». Энгью. Chem. Int. Эд. 48 (7): 1304–1307. Дои:10.1002 / anie.200804883. PMID 19123206.
- ^ Ансуорт, Уильям П .; Китсиу, Кристиана; Тейлор, Ричард Дж. К. (5 июля 2013 г.). «Целесообразный полный синтез без защитных групп (±) -диеводиамина». Органические буквы. 15 (13): 3302–3305. Дои:10.1021 / ol4013469. PMID 23786450.