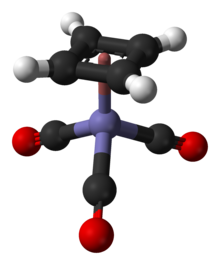
Циклобутадиен, трикарбонил железа - Cyclobutadieneiron tricarbonyl
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol ) | |
| |
| Характеристики | |
| (C4ЧАС4) Fe (CO)3 | |
| Внешность | желтое твердое вещество |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Циклобутадиен, трикарбонил железа или (C4ЧАС4) Fe (CO)3 является железоорганическое соединение с формулой Fe (C4ЧАС4) (CO)3. Это твердое вещество желтого цвета, растворимое в органических растворителях. Он был использован в органическая химия как предшественник циклобутадиен, который в свободном состоянии является неуловимым видом.[1]
Подготовка и состав
Впервые он был получен в 1965 году Петтитом из 3,4-дихлорциклобутена и диирон нонакарбонил:[2][3]
- C4ЧАС4Cl2 + 2 Fe2(CO)9 → (C4ЧАС4) Fe (CO)3 + 2 Fe (CO)5 + 2 СО + 2 FeCl2
Соединение является примером фортепианный табурет комплекс. Расстояния C-C составляют 1,426 Å.[4]
Характеристики
Окислительное разложение из циклобутадиен достигается обработкой трикарбонильного комплекса аммиачная селитра церия. Высвободившийся циклобутадиен улавливается хинон, который функционирует как диенофил.[5]
Циклобутадиен, трикарбонил железа, дисплеи ароматичность о чем свидетельствуют некоторые его реакции, которые можно классифицировать как электрофильное ароматическое замещение:[6]
Он подвергается Ацилирование Фриделя-Крафтса с ацетилхлоридом и хлоридом алюминия с получением ацильного производного 2, с формальдегид и соляная кислота к хлорметильному производному 3, в Реакция Вильсмайера-Хаака с N-метилформанилидом и оксихлоридом фосфора до формил 4, а в Реакция Манниха к производному амина 5.
В механизм реакции идентична EAS:
Родственные соединения
За несколько лет до работы Пети (C4Ph4) Fe (CO)3 был приготовлен по реакции карбонил железа и дифенилацетилен.[7]
(Бутадиен) трикарбонил железа изоэлектронен с циклобутадиен трикарбонилом железа.
Рекомендации
- ^ Д. Сейферт "(Циклобутадиен) трикарбонил железа - Теория перед экспериментом" Металлоорганика 2003, том 22, 2-20.
- ^ Циклобутадиен- и бензоциклобутадиен-трикарбонильные комплексы железа Г. Ф. Эмерсон, Л. Уоттс, Р. Петтит; Варенье. Chem. Soc.; 1965; 87(1); 131-133. Первая страница
- ^ Pettit, R .; Хенери, Дж. (1970). «Циклобутадиен-трикарбонил железа». Органический синтез. 50: 21. Дои:10.15227 / orgsyn.050.0021.
- ^ П. Д. Харви; В. П. Шефер; Х. Б. Грей; Д. Ф. Р. Гилсон; Батлер И.С. (1988). «Структура трикарбонила (η4-циклобутадиенил) железо (0) при -45 ° C ». Неорг. Chem. 27 (1): 57–59. Дои:10.1021 / ic00274a013.
- ^ Л. Бренер, Дж. С. Маккеннис, Р. Петтит (1976). «Циклобутадиен в синтезе: эндо-Трицикло [4.4.0.02,5] дека-3,8-диен-7,10-дион ». Орг. Синтезатор. 55: 43. Дои:10.15227 / orgsyn.055.0043.CS1 maint: использует параметр авторов (связь)
- ^ Циклобутадиен-трикарбонил железа. Новая ароматическая система Дж. Д. Фитцпатрик, Л. Уоттс, Г. Ф. Эмерсон, Р. Петтит Варенье. Chem. Soc.; 1965, т. 87, 3254-3255 Абстрактный
- ^ Р. П. Додж, В. Шомакер, "Кристаллическая структура тетрафенилциклобутадиенового трикарбонила железа", Nature 1960, вып. 186, 798-799.Дои:10.1038 / 186798b0


