Этенон - Ethenone
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Этенон[1] | |
| Другие имена Кетене Карбометен Кето-этилен | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 1098282 | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.006.671 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Свойства | |
| C2ЧАС2О | |
| Молярная масса | 42,037 г / моль |
| Внешность | Бесцветный газ |
| Запах | проникающий |
| Плотность | 1,93 г / см3 |
| Температура плавления | -150,5 ° С (-238,9 ° F, 122,6 К) |
| Точка кипения | -56,1 ° С (-69,0 ° F, 217,1 К) |
| разлагается | |
| Растворимость | растворим в ацетон этиловый спирт этиловый эфир ароматный растворители галоидоуглероды |
| Давление газа | > 1 атм (20 ° C)[2] |
| 1.4355 | |
| Термохимия | |
Теплоемкость (C) | 51,75 Дж / К моль |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -87,24 кДж / моль |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материалов |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -107 ° С (-161 ° F, 166 К) |
| Пределы взрываемости | 5.5-18% |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 1300 мг / кг (перорально, крыса) |
LC50 (средняя концентрация ) | 17 частей на миллион (мышь, 10 мин)[3] |
LCLo (самый низкий опубликованный ) | 23 ppm (мышь, 30 мин) 53 частей на миллион (кролик, 2 часа) 53 частей на миллион (морская свинка, 2 часа) 750 частей на миллион (кошка, 10 мин) 200 частей на миллион (обезьяна, 10 мин) 50 частей на миллион (мышь, 10 мин) 1000 ppm (кролик, 10 мин)[3] |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 0,5 частей на миллион (0,9 мг / м3)[2] |
REL (Рекомендуемые) | TWA 0,5 частей на миллион (0,9 мг / м3) ST 1,5 частей на миллион (3 мг / м3)[2] |
IDLH (Непосредственная опасность) | 5 частей на миллион[2] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Этенон это официальное название для кетен, органическое соединение с формулой C2ЧАС2O или H2С = С = О. Это простейший член кетен класс. Это таутомер из еще менее стабильных этинол.
Свойства
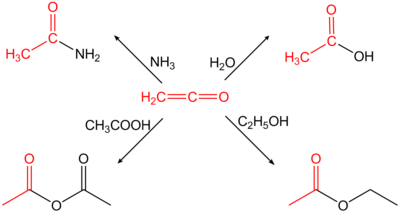
Этенон - газ с высокой реакционной способностью (при стандартные условия ) и имеет резкий раздражающий запах. Он достаточно стабилен только при низких температурах (-80 ° C). Поэтому его всегда нужно готовить для каждого использования и немедленно обрабатывать, в противном случае димеризация дикетен возникает или реагирует на полимеры, с которыми трудно обращаться. Содержание полимера, образующегося во время приготовления, снижается, например, добавлением диоксида серы к газообразному кетену.[4] Из-за своих кумулятивных двойных связей этенон обладает высокой реакционной способностью и реагирует в реакции присоединения H-кислотных соединений с соответствующими производными уксусной кислоты. Например, он реагирует с водой до уксусной кислоты или с первичный или вторичные амины к соответствующему ацетамиды.
Этенон очень ядовит; его токсичность примерно в восемь раз выше, чем у фосген.[5]
Этенон самопроизвольно полимеризовать. Контакт с перекисью водорода приводит к взрывной реакции. Может образовывать с воздухом взрывоопасную смесь.
Растворим в ацетон, этиловый спирт, этиловый эфир, ароматный растворители и галоидоуглероды.
Подготовка
Этенон был открыт в то же время Герман Штаудингер (по реакции бромацетилбромид с металлическим цинк )[6][7]
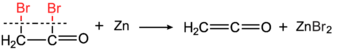
и по Норман Т. М. Уилсмор (термическим разложением уксусного ангидрида).[8]

Этенон производится в промышленных масштабах для использования в производстве уксусный ангидрид. Его можно приготовить пиролиз из ацетон, и раньше это был основной производственный процесс. При пропускании паров ацетона через нагретые трубы или электрически нагретый металл (например, медь ) провода при 500-600 ° С при наличии небольшого сероуглерод (CS2) ацетон разлагается на метан и этенон с выходом 95%.[9][10]

В промышленной химии пиролиз кетонов в значительной степени был заменен дегидратацией уксусная кислота (реакция Шмидлина-Бергмана-Вильсмора).[11]

Естественное явление
Наблюдалось, что этенон встречается в космосе, в кометах или в газе как часть межзвездной среды.[12]
Использовать
Этенон используется для изготовления уксусный ангидрид от уксусная кислота. Обычно он используется для ацетилирование химических соединений.[5]
Этенон реагирует с метанал в присутствии катализаторов, таких как кислоты Льюиса (AlCl3, ZnCl2 или BF3) давать β-пропиолактон.[13] Технически наиболее важным применением этенона является синтез сорбиновая кислота по реакции с 2-бутенал (кротоновый альдегид) в толуол примерно при 50 ° C в присутствии цинковых солей длинноцепочечных карбоновых кислот. Это дает полиэстер 3-гидрокси-4-гексеновой кислоты, которая термически[14] или гидролитически деполимеризованный до сорбиновой кислоты.
Этенон очень реактивен, склонен реагировать с нуклеофилы сформировать ацетильная группа. Например, он реагирует с водой с образованием уксусная кислота;[15] с уксусной кислотой с образованием уксусный ангидрид; с аммиаком и аминами с образованием этанамидов;[16] и с сухим галогениды водорода с образованием ацетилгалогенидов.[17]
Образование уксусной кислоты, вероятно, происходит путем начального образования 1,1-дигидроксиэтен, который затем таутомеризуется дать конечный продукт.[18]
Этенон также будет реагировать сам с собой через [2 + 2] фотоциклоприсоединения образовывать циклический димеры известный как дикетены. По этой причине его не следует хранить в течение длительного времени.[19]
Опасности
Воздействие концентрированных концентраций вызывает у людей раздражение таких частей тела, как глаз, нос, горло и легкие. Расширенные испытания на токсичность на мышах, крысах, морских свинках и кроликах показали, что десятиминутное воздействие свежевыработанного этенона с концентрацией всего 0,2 мг / л (116 промилле ) может привести к высокому проценту гибели мелких животных. Эти данные показывают, что этенон токсикологически идентичен фосген.[20]
Образование кетена в пиролиз из ацетат витамина Е, добавка некоторых электронная жидкость продукты, является одним из возможных механизмов зарегистрированного легочного повреждения[21] вызвано использованием электронных сигарет.[22]В ряде патентов описано каталитическое образование кетена из карбоновых кислот и ацетатов с использованием различных металлов или керамики, некоторые из которых, как известно, встречаются в устройствах для электронных сигарет у пациентов с повреждениями легких, связанными с употреблением электронных сигарет или вейпинга. (ЭВАЛИ).[23][24]
Пределы профессионального воздействия установлены на уровне 0,5 частей на миллион (0,9 мг / м3) по восьмичасовому средневзвешенному по времени.[25] An IDLH предел установлен на уровне 5 частей на миллион, так как это самая низкая концентрация, вызывающая клинически значимый физиологический ответ у людей.[26]
использованная литература
- ^ «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 723. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ а б c d Карманный справочник NIOSH по химической опасности. "#0367". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б "Кетене". Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ EP 0377438, R. Bergamin et al., Выдано 11 июня 1990 г., передано Lonza AG
- ^ а б Вход на Дикетен. в: Römpp Online. Георг Тиме Верлаг, извлечен 16 июня 2014 г.
- ^ Х. Штаудингер Х. В. Клевер (1908): "Keten. Bemerkung zur Abhandlung zur Abhandlung der HHrn. V.T. Wilsmore und A.W. Стюарт". Berichte der deutschen chemischen Gesellschaft, том 41, выпуск 1, страницы 1516-1517. Дои:10.1002 / cber.190804101275
- ^ Тидвелл, Т. Т. (2005), «Эйн Ярхундерт Кетене (1905–2005): умереть Entdeckung einer vielseitigen Klasse reaktiver Intermediate». Angewandte Chemie, том 117, страницы 5926–5933. Дои:10.1002 / ange.200500098
- ^ Норман Томас Мортимер Уилсмор (1907): «Кетен». Журнал химического общества, Сделки, том 91, статья CLXXXVIII (188), страницы 1938-1941. Дои:10.1039 / ct9079101938
- ^ К.-Х. Лаутеншлегер, В. Шретер, А. Ваннингер, "Taschenbuch der Chemie", 20. Aufl. 2006 г., ISBN 978-3-8171-1761-1.
- ^ «Кетене». Органический синтез. Дои:10.15227 / orgsyn.004.0039.
- ^ Дж. Шмидлин, М. Бергман (1910): Berichte der deutschen chemischen Gesellschaft, том 43, страницы 2821-. Дои:10.1002 / cber.19100430340.
- ^ Хадсон, Реджи Л .; Лёффлер, Марк Дж. (2013). "Кетеновая формация в межзвездных льдах: лабораторное исследование". Астрофизический журнал. 773 (2): 109. Дои:10.1088 / 0004-637x / 773/2/109. HDL:2060/20140010162. ISSN 0004-637X.
- ^ Ханс-Юрген Арпе, "Industrielle Organische Chemie", 6. Aufl., 2007, WILEY-VCH Verlag, Weinheim, ISBN 978-3-527-31540-6.
- ^ EP 1295860, D. Decker et al., Выдано 26. März 26.03.2003, переуступлено Nutrinova GmbH
- ^ Тидвелл, п. 11.
- ^ Тидвелл, стр. 560.
- ^ ChemSpider http://www.chemspider.com/Chemical-Structure.9643.html
- ^ Нгуен, Минь Тхо; Распоэт, Привет (1999). «Механизм гидратации кетена: 15 лет спустя». Мочь. J. Chem. 77: 817–829. Дои:10.1139 / v99-090.
- ^ Кристоф Тайшлер:Кетены, димеры кетена и родственные вещества, Кирк-Отмер Энциклопедия химической технологии, John Wiley & Sons, Нью-Йорк, 2010 г.
- ^ Х. А. Вустер; К. С. Лашбо; К. Э. Редеман (1946). «Токсичность кетена и димера кетена при вдыхании». Варенье. Chem. Soc. 68 (12): 2743. Дои:10.1021 / ja01216a526.
- ^ https://time.com/5753947/vaping-lung-disease-outbreak-peak/
- ^ Дэн Ву и Ф. О'Ши "Возможность выделения легочного токсичного кетена в результате пиролиза ацетата витамина Е ", PNAS 24 марта 2020 г. 117 (12) 6349-6355.
- ^ К. Аттфилд, В. Чен, К. Каммингс, П. Джейкоб 3-й, Д. О'Ши, Дж. Вагнер, П. Ван и Дж. Фаулз, https://pubmed.ncbi.nlm.nih.gov/32551843/ Способность этенона (кетена) вызывать электронные сигареты или повреждение легких, связанное с употреблением вейпинга. Am J Respir Crit Care Med, 2020 doi: 10.1164 / rccm.202003-0654LE.
- ^ Патент США № 5475144. Катализатор и способ синтеза кетенов из карбоновых кислот. 12 декабря 1995 г. https://patents.google.com/patent/US5475144A/en
- ^ Центры по контролю и профилактике заболеваний (4 апреля 2013 г.). "Кетене". Карманный справочник NIOSH по химической опасности. Получено 13 ноября 2013.
- ^ Центры по контролю и профилактике заболеваний (Май 1994). "Кетене". Документация по концентрациям, непосредственно опасным для жизни или здоровья (IDLH). Получено 13 ноября 2013.
Литература
внешние ссылки
 СМИ, связанные с Этенон в Wikimedia Commons
СМИ, связанные с Этенон в Wikimedia Commons