Кетене - Ketene

А кетен является органическое соединение вида R′R ″ C = C = O, где R и R '- два произвольных одновалентный химические группы (или два отдельных сайта замещения в одной молекуле).[1] Название может также относиться к конкретному соединению. этенон ЧАС
2С = С = О, простейший кетен.
Хотя они очень полезны, большинство кетенов неустойчивый. При использовании в качестве реагенты в химической процедуре они обычно образуются по мере необходимости и потребляются сразу после (или во время) производства.[1]
История
Кетены были впервые изучены как класс у Герман Штаудингер до 1905 г.[2]
Кетены были систематически исследованы Германом Штаудингером в 1905 году в форме дифенилкетена (превращение -хлордифенилацетилхлорид с цинком). Штаудингер был вдохновлен первыми примерами реакционноспособных органических промежуточных продуктов и стабильных радикалов, открытых Моисей Гомберг в 1900 г. (соединения с трифенилметильной группой).[3]
Подготовка
Этенон, простейший кетен, может быть получен пиролиз (термическое растрескивание) ацетон:[4]
- CH3−CO − CH3 → CH2= C = O + CH4
Эта реакция называется синтезом кетена Шмидлина.[5][6]
Другие кетены можно получить из ацилхлориды по реакция элиминации в котором HCl потерян:
В этой реакции основание, обычно триэтиламин, удаляет кислый протон альфа к карбонил группы, вызывая образование двойной связи углерод-углерод и потерю хлористый ион:

Кетены также могут быть образованы из α-диазокетоны к Перестановка Вольфа.
Другой способ генерировать кетены - это мгновенный вакуумный термолиз (FVT) с 2-пиридиламины. В 1997 году Плюг и Вентруп разработали метод, который улучшил реакции FVT для получения кетенов со стабильным FVT, нечувствительным к влаге, в мягких условиях (480 ° C). N-пиридиламины получают конденсацией с R-малонаты с N-амино (пиридин ) и DCC как растворитель.[7]
Более надежный метод приготовления кетенов - это карбонилирование из металл-карбены, и на месте реакция полученных таким образом высокореакционных кетенов с подходящими реагентами, такими как имины, амины, или же спирты.[8] Этот метод является эффективным горшок тандемный протокол карбонилирования α-диазокарбонильных соединений и различных N-Тозилгидразоны, катализируемые Co (II) -порфирин металлорадикалы, приводящие к образованию кетенов, которые впоследствии вступают в реакцию с различными нуклеофилы и имины формировать сложные эфиры, амиды и β-лактамы. Эта система имеет широкий спектр подложек и может применяться для различных комбинаций карбен предшественники, нуклеофилы и имины.[9]
Реакции и заявки
Благодаря их кумулятивные двойные облигации, кетены очень реактивны.[10]
Образование эфиров карбоновых кислот
По реакции с спирты, сложные эфиры карбоновых кислот формируются:
Образование ангидридов карбоновых кислот
Кетены реагируют с карбоновыми кислотами с образованием ангидриды карбоновых кислот:
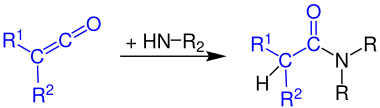
Образование амидов карбоновых кислот
Кетены реагируют с аммиак к первичные амиды:
Реакция кетенов с первичные амины производит вторичные амиды:
Кетены реагируют с вторичные амины дать третичные амиды:
Гидролиз
При реакции с водой карбоновые кислоты образуются из кетенов.
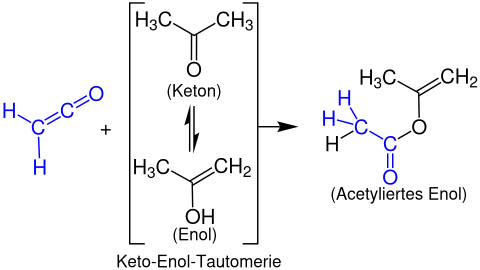
Образование енолацетатов
Энолацетаты образуются из кетенов с енолизируемый карбонильные соединения. В следующем примере показана реакция этенон с ацетон с образованием пропен-2-илацетата:
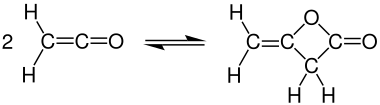
Димеризация
При комнатной температуре кетен быстро димеризуется до дикетен, но кетен можно восстановить при нагревании:
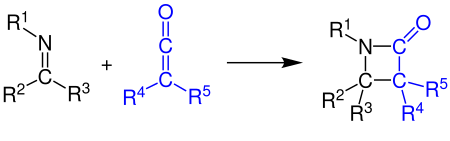
[2 + 2] -циклоприсоединение
Кетены могут реагировать с алкены, карбонильные соединения, карбодиимиды и имины в [2 + 2] циклоприсоединение. На примере показан синтез β-лактам реакцией кетена с имином (см. Синтез Штаудингера ):[11][12]
Приложения
Кетены обычно очень реактивны и участвуют в различных циклоприсоединения. Одним из важных процессов является димеризация с получением пропиолактоны. Конкретный пример - димеризация кетена стеариновая кислота позволить себе димеры алкилкетена, которые широко используются в бумажной промышленности.[1] AKD реагируют с гидроксильными группами целлюлозы через этерификация реакция.
Они также будут претерпевать реакции [2 + 2] циклоприсоединения с электронно-богатыми алкины формировать циклобутеноны, или карбонильные группы с образованием бета-лактоны. С имины бета-лактамы сформированы. Это Синтез Штаудингера, простой путь к этому важному классу соединений. С ацетон, кетен реагирует, давая Изопропенилацетат.[1]
Разнообразие гидроксильный соединения могут добавляться как нуклеофилы, образуя либо энол или же сложный эфир товары. Например, молекула воды легко присоединяется к кетену, давая 1,1-дигидроксиэтен и уксусный ангидрид производится в результате реакции уксусная кислота с кетеном. Реакции между диолы (HO − R − OH) и бис-кетены (O = C = CH − R′ − CH = C = O) дают полиэфиры с повторяющейся единицей (-O-R-O-CO-R'-CO).
Этилацетоацетат, важный исходный материал в органическом синтезе, может быть получен с использованием дикетен в реакции с этиловый спирт. Они непосредственно образуют этилацетоацетат, и выход является высоким при проведении в контролируемых условиях; поэтому этот метод используется в промышленности.
Смотрите также
Рекомендации
- ^ а б c d Миллер Р., Абаечерли С., Саид А., Джексон Б. (2001). «Кетенес». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a15_063. ISBN 978-3527306732.
- ^ Штаудингер H (1905). "Ketene, eine neue Körperklasse" [Кетены, новый класс веществ]. Berichte der Deutschen Chemischen Gesellschaft. 38 (2): 1735–1739. Дои:10.1002 / cber.19050380283.
- ^ Томас Т. Тидвелл, Первый век Кетена (1905-2005): рождение семейства реактивных промежуточных продуктов, Angewandte Chemie, Int. Издание, Band 44, 2005 г., S. 5778–5785
- ^ Вейганд С (1972). Hilgetag G, Martini A (ред.). Препаративная органическая химия Weygand / Hilgetag (4-е изд.). Нью-Йорк: John Wiley & Sons, Inc., стр. 1031–1032. ISBN 978-0471937494.
- ^ Херд CD, Камм О. (1941). «Кетен в органическом синтезе». Органический синтез. Коллектив Vol. 1. п. 330.
- ^ Шмидлин Дж, Бергман М (1910). "Darstellung des Ketens aus Aceton" [Получение кетена из ацетона]. Berichte der Deutschen Chemischen Gesellschaft (на немецком). 43 (3): 2821–2823. Дои:10.1002 / cber.19100430340.
- ^ Карстен Плюг, Хусейн Канаани и Курт Вентруп (12 февраля 2015 г.). «Кетены из N- (2-пиридил) амидов». Австралийский химический журнал. 68 (4): 687. Дои:10.1071 / CH14714.
- ^ Пол Н.Д., Чирила А., Лу Х., Чжан ХР, де Брюин Б. (сентябрь 2013 г.). «Карбеновые радикалы в реакциях карбонилирования карбена, катализируемых кобальтом (II) -порфирином; каталитический подход к кетенам». Химия. 19 (39): 12953–8. Дои:10.1002 / chem.201301731. ЧВК 4351769. PMID 24038393.
- ^ Кирила А., ван Влит К.М., Пол Н.Д., де Брюин Б. (2018). «[Co (MeTAA)] Металлорадикальный каталитический путь к кетенам через карбонилирование карбеновых радикалов» (PDF). Европейский журнал неорганической химии. 2018 (20–21): 2251–2258. Дои:10.1002 / ejic.201800101. ISSN 1099-0682.
- ^ Зигфрид Гауптманн (1985), Organische Chemie: mit 65 Tabellen (на немецком языке), Лейпциг: Deutscher Verlag für Grundstoffindustrie, стр. 410–412, ISBN 3871449024
- ^ Джи Джек Ли (2006), Назовите реакции. Сборник подробных механизмов реакции (на немецком языке) (3-е изд.), Берлин: Springer-Verlag, стр. 561-562, Дои:10.1007/3-540-30031-7, ISBN 9783540300304
- ^ Герман Штаудингер (1907), "Zur Kenntnis der Ketene. Diphenylketen", Юстус Либигс Аннален дер Хеми (на немецком языке), John Wiley & Sons, Inc., 356 (1–2), стр. 51–123, Дои:10.1002 / jlac.19073560106
внешняя ссылка
 СМИ, связанные с Кетены в Wikimedia Commons
СМИ, связанные с Кетены в Wikimedia Commons