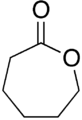
Лактон - Lactone
Лактоны цикличны эфиры карбоновых кислот, содержащий структуру 1-оксациклоалкан-2-она (−C (= O) −O−), или аналоги, имеющие ненасыщенность или гетероатомы замена одного или нескольких атомов углерода кольца.[1]
Лактоны образуются внутримолекулярными этерификация соответствующих гидроксикарбоновых кислот, что происходит спонтанно, когда образующееся кольцо является пяти- или шестичленным. Лактоны с трех- или четырехчленными кольцами (α-лактоны и β-лактоны) очень реактивны, что затрудняет их выделение. Специальные методы обычно требуются для лабораторного синтеза лактонов с малым кольцом, а также тех, которые содержат кольца больше, чем шестичленные.[2]
Номенклатура
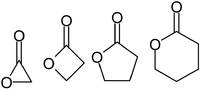
Лактоны обычно называют в соответствии с молекулой-предшественником кислоты (ацето = 2 атома углерода, пропио = 3, Butyro = 4, Валеро = 5, капро = 6 и т. Д.), С -лактон суффикс и Греческая буква префикс, который указывает количество атомов углерода в гетероцикле, то есть расстояние между соответствующими группами -ОН и -СООН вдоль указанной основной цепи. Первый атом углерода после углерода в группе -COOH в исходном соединении обозначен как α, второй будет обозначен как β и так далее. Следовательно, префиксы также указывают размер лактонового кольца: α-лактон = 3-членное кольцо, β-лактон = 4-членное кольцо, γ-лактон = 5-членное кольцо и т. Д. Макроциклический лактоны известны как макролактоны.[3]
Другой суффикс, используемый для обозначения лактона, - -олид, используется в именах классов веществ, например бутенолид, макролид, карденолид или же буфадиенолид.
Чтобы получить предпочтительные названия ИЮПАК, лактоны называют гетероциклическими псевдокетонами путем добавления суффикса «один», «дион», «тион» и т.д. и соответствующих мультипликативных префиксов к названию гетероциклического исходного гидрида.[4]
Этимология
Название «лактон» было придумано в 1844 году французским химиком. Теофиль-Жюль Пелуз, который впервые получил его как производное молочной кислоты.[5] Название лактон происходит от кольцевого соединения, называемого лактид, который образуется при дегидратации 2-гидроксипропановой кислоты (молочная кислота ) CH3-CH (OH) -COOH. Молочная кислота, в свою очередь, получила свое название от первоначального выделения из кислого молока (лат. Lac, lactis). Внутреннее обезвоживание в той же молекуле молочной кислоты привело бы к альфа-пропиолактон, лактон с 3-членным кольцом.
В 1880 году немецкий химик Вильгельм Рудольф Фиттиг расширил название «лактон» на все внутримолекулярные сложные эфиры карбоновых кислот.[6]
Природные источники
Встречающиеся в природе лактоны в основном представляют собой насыщенные и ненасыщенные γ- и δ-лактоны и, в меньшей степени, макроциклические лактоны. Γ- и δ-лактоны представляют собой внутримолекулярные сложные эфиры соответствующих гидроксижирных кислот. Они способствуют аромату фруктов, масла, сыра и других продуктов. Циклопентадеканолид отвечает за мускусный запах корень ангелики масло. Из встречающихся в природе бициклических лактонов, фталиды несут ответственность за запахи сельдерей и любисток масла и кумарин за Woodruff.[7] Лактоны присутствуют в дуб древесины, и они способствуют вкусовому профилю Пиво бочковой выдержки.[8]
Лактоновые кольца широко встречаются в природе в качестве строительных блоков, например, в аскорбиновая кислота, Кавайн, непеталактон, глюконолактон, гормоны (спиронолактон, мевалонолактон ), ферменты (лактоназа ), нейротрансмиттеры (бутиролактон, авермектины ), антибиотики (макролиды подобно эритромицин; амфотерицин B ), противораковые препараты (Вернолепин, эпотилоны ), фитоэстрогены (резорциловая кислота лактоны, сердечные гликозиды ).
Синтез

Многие методы синтеза сложных эфиров также применимы к лактонам. В одном промышленном синтезе оксандролон ключевым этапом образования лактона является органическая реакция - этерификация.[9][10]

В галолактонизация, алкен атакован галоген через электрофильная добавка с катионным промежуточным продуктом, захваченным внутримолекулярно соседним карбоновая кислота (Смотрите также йодолактамизация ).[11]
Конкретные методы включают Ямагути этерификация, Макролактонизация шиины, Окисление Байера-Виллигера и нуклеофильная абстракция.

Γ-лактоны γ-окталактон, γ-ноналактон, γ-декалактон, γ-ундекалактон можно приготовить с хорошим выходом в одноэтапном процессе с помощью радикальное добавление первичного жирные спирты к акриловая кислота, с помощью ди-трет-бутилпероксид как катализатор.[7]
Реакции
Наиболее стабильной структурой для лактонов являются 5-членные γ-лактоны и 6-членные δ-лактоны, потому что, как и во всех органических циклах, 5- и 6-членные кольца минимизируют напряжение валентные углы. γ-лактоны настолько стабильны, что в присутствии разбавленных кислот при комнатной температуре 4-гидроксикислоты (R-CH (OH) - (CH2)2-COOH) немедленно подвергаются спонтанной этерификации и циклизации до лактона. β-лактоны существуют, но их можно получить только специальными методами. α-лактоны могут быть обнаружены как временные частицы в масс-спектрометрии эксперименты.[12]
Реакции лактонов аналогичны реакциям сложных эфиров, как показано на примере гамма-лактона в следующих разделах:
Гидролиз
Нагрев лактона с основой (едкий натр ) буду гидролизовать от лактона до его родительского соединения, бифункционального соединения с прямой цепью. Как и сложные эфиры с прямой цепью, реакция гидролиза-конденсации лактонов представляет собой обратимая реакция, с равновесие. Тем не менее константа равновесия реакции гидролиза лактона ниже, чем у сложного эфира с прямой цепью, т.е. продукты (гидроксикислоты) менее предпочтительны в случае лактонов. Это потому, что хотя энтальпии гидролиза сложных эфиров и лактонов примерно одинаковы, энтропия гидролиза лактонов меньше, чем энтропия сложных эфиров с прямой цепью. Сложные эфиры с прямой цепью при гидролизе дают два продукта, что делает изменение энтропии более благоприятным, чем в случае лактонов, которые дают только один продукт.
Снижение
Лактоны можно восстановить до диолов, используя литийалюминийгидрид в сухом эфире. Реакция восстановления сначала разрывает сложноэфирную связь лактона, а затем восстанавливает альдегидную группу (-CHO) до спиртовой группы (-OH).[нужна цитата ] Например, гамма-лактоны будут восстановлены до бутан-1,4-диола, (CH2(ОН) - (СН2)2-CH2(ОЙ).
Аминолиз
Лактоны также реагируют с этанольным аммиаком, который сначала разрывает сложноэфирную связь, а затем реагирует с кислотной группой -COOH из-за основных свойств аммиака с образованием дифункциональной группы, то есть спирта и амида. Гамма-лактоны будут реагировать с образованием CH2(ОН) - (СН2)2-CO-NH2.
Полимеризация
Лактоны легко образуют сложные полиэфиры в соответствии с формулой, и было показано, что они также олигомеризуются без катализатора:[13][14]

Реакция Майкла
Сесквитерпеновые лактоны, обнаруженный во многих растениях, может реагировать с другими молекулами через Реакция Майкла.
Использует
Ароматизаторы и ароматы
Лактоны вносят значительный вклад в аромат фруктов, неферментированных и ферментированных молочных продуктов,[15] и поэтому используются в качестве ароматизаторов и ароматизаторов.[7] Некоторые примеры γ-декалактон (4-деканолид), имеющий характерный персиковый аромат;[15] δ-декалактон (5-деканолид), имеющий сливочный кокосовый / персиковый вкус; γ-додекалактон (4-додеканолид), который также имеет кокосовый / фруктовый вкус,[15] описание, которое также подходит γ-окталактон (4-октанолид),[16] хотя и имеет травянистый характер;[15] γ-ноналактон, который обладает интенсивным кокосовым ароматом этой серии, несмотря на то, что не содержится в кокосе,[17] и γ-ундекалактон.
Макроциклические лактоны (циклопентадеканолид, 15-пентадек-11/12-енолид ) имеют запах, похожий на запах макроциклических кетонов животного происхождения (Muscone, циветон ), но их легче приготовить, например, деполимеризация соответствующего линейного полиэфиры. Замена метиленовой единицы кислородом практически не влияет на запах этих соединений, а оксалактоны с 15-17-членными кольцами образуются в дополнение к циклопентадеканолиду (например, 12-окса-16-гексадеканолид ).[7]
Пребиотическая химия
Пребиотически правдоподобные лактоны, такие как ε-капролактон и δ-валеролактон, олигомеризуются без использования катализаторов, образующих олигомеры, которые, возможно, были актуальны во время «Происхождения жизни».[18]
Пластмассы
Поликапролактон важный пластик.
Примеры

γ-бутиролактон (ГБЛ)
- Макролиды
- Кавалактоны
дилактоны
- Эллаговая кислота (Дилактон гексагидроксидифеновой кислоты)
- Дилактон флавогаллоновой кислоты можно найти в Rhynchosia volubilis семена и в Shorea laeviforia
- Лактид
- Дилактон тергалловой кислоты можно найти в Rhynchosia volubilis семена
- Дилактон валонеиновой кислоты можно выделить из сердцевины Shorea laeviforia
- Этилен брассилат (Musk T), широко используемый синтетический мускус
Смотрите также
- Лактам, циклический амид
- Лактим, циклический имид
- Лактид, циклический diсложный эфир
- Галолактонизация
- Фталеин
Ссылки и примечания
- ^ «лактоны», Сборник химической терминологии, 2.3.3, Международный союз теоретической и прикладной химии, 2014-02-24, с. 817
- ^ Фрэнсис А. Кэри; Роберт М. Джулиано (2011), Органическая химия (8-е изд.), McGraw-Hill, стр. 798–799.
- ^ Стивен А. Хардинджер. «Иллюстрированный глоссарий органической химии». Кафедра химии и биохимии, UCLA.
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 822. Дои:10.1039/9781849733069-00648. ISBN 978-0-85404-182-4.
- ^ Пелуз, Дж. (9 декабря 1844 г.). "Mémoire sur l'acide lactique" [Воспоминания о молочной кислоте]. Comptes rendus (На французском). 19: 1219–1227.С п. 1223: "Indépendamment de la lactide dont je viens de rappeler l'existence dans les produits de la distllation de l'acide lactique, celui-ci donne encore, par sa décomposition, une autre entity, que je propose d'appeler лактон, parce qu'elle me paraît être à l'acide lactique ce que l'acétone est à l'acide acétique ". (Независимо от лактида, о существовании которого я только что вспомнил, в продуктах перегонки молочной кислоты, эта [то есть молочная кислота] дает в дальнейшем путем разложения другое вещество, которое я предлагаю назвать лактон, потому что мне кажется, что молочная кислота похожа на ацетон на уксусную кислоту.)
- Перепечатано: Пелуз, Дж. (1845). "Mémoire sur l'acide lactique" [Воспоминания о молочной кислоте]. Annals de Chimie et de Physique. 3-я серия (на французском языке). 13: 257–268. ; см. стр. 262.
- Английский перевод: Пелуз, Дж. (15 января 1845 г.). «Исследования по молочной кислоте». Химический вестник. 3 (54): 29–35. ; см. стр. 31.
- Ментен, Пьер де (2013). Dictionnaire de chimie: Une Approche étymologique et Historique [Химический словарь: этимологический и исторический подход] (На французском). Брюссель, Бельгия: де бок. п. 183. ISBN 9782804181758.
- ^ Фиттиг, Рудольф (1880). "Untersuchungen über ungesättige Säuren, dritte Abhandlung" [Исследования ненасыщенных кислот, третья статья]. Annalen der Chemie und Pharmacie (на немецком). 200: 1–96. Дои:10.1002 / jlac.18802000102. С п. 62: "Es ist wünschenswerth, für diese Gruppe von Verbindungen, deren bis jetzt einfachster Repräsentant der im Vorstehenden beschriebene Körper ist, eine allgemeine Bezeichnungsweise zu haben, und da der Name" Lactiνd , так что schlagen wir als Gruppenbezeichnung den Namen "Lactone" vor. " (Желательно, чтобы эта группа соединений, простейшим представителем которой до сих пор было вещество, описанное выше, имела общее обозначение, и поскольку название «лактид» неприменимо, потому что тогда архетипический лактид не будет лактид, поэтому мы предлагаем название «лактон» для обозначения этой группы [соединений].)
- ^ а б c d Карл-Георг Фальбуш; и другие. (2007), «Вкус и ароматизаторы», Энциклопедия промышленной химии Ульмана (7-е изд.), Wiley, стр. 74–78.
- ^ Ремесленное пиво и пивоварение. Бочковая выдержка.
- ^ Разработка коммерческого процесса производства оксандролона Джон Э. Кабадж, Дэвид Кайрис и Томас Р. Бенсон Org. Процесс Res. Dev .; 2007; 11 (3), стр. 378–388; (Статья) Дои:10.1021 / op060231b
- ^ Полная последовательность реакций бромирование к галокетон (не отображается), реакция элиминации с хлорид лития для Enone, органическое окисление к четырехокись осмия и тетраацетат свинца с раскрытием кольца и, наконец, уменьшение альдегид к алкоголь с борогидрид натрия и внутримолекулярное образование лактона
- ^ Органический синтез, Сб. Vol. 7, стр. 164 (1990); Vol. 64, с.175 (1986) Ссылка на статью
- ^ Детлеф Шредер, Норман Голдберг, Вальтрауд Цуммак, Гельмут Шварц, Джон С. Поутсма и Роберт Р. Сквайрс (1997), Образование α-ацетолактона и ацетоксил-бирадикала • CH2COO • в газовой фазе. Международный журнал масс-спектрометрии и ионных процессов, тома 165-166, ноябрьский выпуск, страницы 71-82. Дои:10.1016 / S0168-1176 (97) 00150-X
- ^ Вильгельм Рименшнайдер; Герман М. Болт (2007), «Сложные органические эфиры», Энциклопедия промышленной химии Ульмана (7-е изд.), Wiley
- ^ Чандру, Кухан; Джиа, Тони З .; Мамаджанов, Ирена; Бапат, Нираджа; Кливз, Х. Джеймс (2020-10-16). «Пребиотическая олигомеризация и самосборка структурно разнообразных ксенобиологических мономеров». Научные отчеты. 10 (1): 17560. Дои:10.1038 / s41598-020-74223-5. ISSN 2045-2322. ЧВК 7567815. PMID 33067516.
- ^ а б c d Бергер, Р.Г., изд. (2007). Химия ароматизаторов и ароматизаторов, биопереработка и экологичность. Берлин: Springer. ISBN 9783540493396. Получено 2 июля 2015.
- ^ Mehta, Bhavbhuti M .; Камал-Элдин, Афаф; Ивански, Роберт З., ред. (2012). Влияние ферментации на пищевые свойства. Бока-Ратон: Тейлор и Фрэнсис. п. 74. ISBN 9781439853351. Получено 2 июля 2015.
- ^ Марсили, Рэй, изд. (2007). Сенсорный анализ вкуса. Бока-Ратон, Флорида: CRC / Taylor & Francis. п. 242. ISBN 9781420017045. Получено 2 июля 2015.
- ^ Чандру, Кухан; Мамаджанов, Ирена; Кливз, Х. Джеймс; Джиа, Тони З. (январь 2020 г.). «Полиэфиры как модельная система для построения примитивных биологических препаратов из химии небиологических пребиотиков». Жизнь. 10 (1): 6. Дои:10.3390 / life10010006. ЧВК 7175156. PMID 31963928.