Ароматическое соединение - Aromatic compound
Ароматические соединения те химические соединения (Наиболее часто органический ), которые содержат один или несколько кольца с пи-электроны делокализованы вокруг них. В отличие от соединений, которые проявляют ароматичность, алифатические соединения не хватает этой делокализации. Термин «ароматический» был назначен перед физическим механизмом, определяющим ароматичность был обнаружен и связан просто с тем фактом, что многие такие соединения имеют сладкий или приятный запах; однако не все ароматические соединения имеют сладкий запах, и не все соединения со сладким запахом являются ароматическими. Ароматические углеводороды, или же арены, представляют собой ароматические органические соединения, содержащие только атомы углерода и водорода. Конфигурация из шести атомов углерода в ароматических соединениях называется «бензольным кольцом» в честь простого ароматического соединения. бензол, или фенил группа, когда часть более крупного соединения.
Не все ароматические соединения основаны на бензоле; ароматичность также может проявляться в гетероарены, которые следуют Правило Хюккеля (для моноциклических колец: когда число его π-электронов равно 4п + 2, где п = 0, 1, 2, 3, ...). В этих соединениях по крайней мере один атом углерода заменен одним из гетероатомы кислород, азот, или же сера. Примеры небензольных соединений с ароматическими свойствами: фуран, гетероциклическое соединение с пятичленным кольцом, которое включает один атом кислорода, и пиридин, гетероциклическое соединение с шестичленным кольцом, содержащим один атом азота.[1]
Модель бензольного кольца
Бензол, С6ЧАС6, является наименее сложным ароматическим углеводородом, и он был первым назван так. Природа его связи была впервые признана Август Кекуле в 19 веке. Каждый атом углерода в гексагональном цикле имеет четыре общих электрона. Один идет к атому водорода, и по одному к каждому из двух соседних атомов углерода. Это оставляет один электрон делиться с одним из двух соседних атомов углерода, таким образом создавая двойную связь с одним углеродом и оставляя одинарную связь с другим, вот почему некоторые представления молекулы бензола изображают ее в виде шестиугольника с чередующимися одинарными и двойные связи.
Другие изображения структуры изображают шестиугольник с кругом внутри него, чтобы указать, что шесть электронов плавают по делокализованным молекулярным орбиталям размером с само кольцо. Это представляет собой эквивалентную природу шести углерод-углеродных связей во всех ордер на облигации 1,5; эквивалентность объясняется резонансные формы. Электроны визуализируются плавающими над и под кольцом, а генерируемые ими электромагнитные поля действуют, чтобы кольцо оставалось плоским.
Общие свойства ароматических углеводородов:
- Они отображают ароматичность
- Отношение углерод – водород высокое.
- Они горят сильным дымчатым желтым пламенем из-за высокого соотношения углерода и водорода.
- Они проходят реакции электрофильного замещения и нуклеофильные ароматические замещения
Круглый символ ароматичности был введен Сэр Роберт Робинсон и его ученик Джеймс Армит в 1925 г.[2] и популяризируется, начиная с 1959 года, учебником Моррисона и Бойда по органической химии. Вопрос о правильном использовании символа обсуждается: в некоторых публикациях он используется для любой циклическая π-система, в то время как другие используют ее только для тех π-систем, которые подчиняются Правило Хюккеля. Дженсен[3] утверждает, что в соответствии с первоначальным предложением Робинсона, использование символа круга должно быть ограничено моноциклическими 6 π-электронными системами. Таким образом, символ круга для шестицентровой шестиэлектронной связи можно сравнить с символом Y для трехцентровая двухэлектронная связь.
Синтез арена
Реакция, при которой образуется ареновое соединение из ненасыщенного или частично ненасыщенного циклического предшественника, просто называется ароматизация. Существует множество лабораторных методов для органический синтез аренов из неареновых предшественников. Многие методы полагаются на циклоприсоединение реакции. Тримеризация алкинов описывает [2 + 2 + 2] циклизацию трех алкинов в Реакция Дёца реагентами являются алкин, монооксид углерода и комплекс карбена хрома. Реакции Дильса – Альдера из алкины с пирон или же циклопентадиенон с изгнанием углекислый газ или окись углерода также образуют ареновые соединения. В Циклизация Бергмана реагенты являются Enyne плюс донор водорода.
Еще один комплекс методов - ароматизация циклогексаны и другие алифатические кольца: реагенты - катализаторы, используемые в гидрирование такие как платина, палладий и никель (обратное гидрирование), хиноны и элементы сера и селен.[4]
Реакции
Ароматические кольцевые системы участвуют во многих органических реакциях.
Ароматическая замена
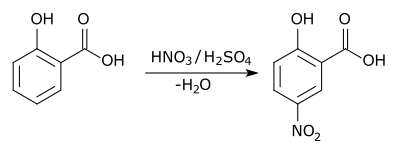
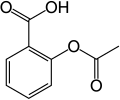
В ароматических замена один заместитель в ареновом кольце, обычно водород, заменен другим заместителем. Два основных типа: электрофильное ароматическое замещение когда активным реагентом является электрофил и нуклеофильное ароматическое замещение когда реагент является нуклеофилом. В радикально-нуклеофильное ароматическое замещение активный реагент - радикал. Примером электрофильного ароматического замещения является нитрование салициловая кислота:[5]
Реакции сцепления
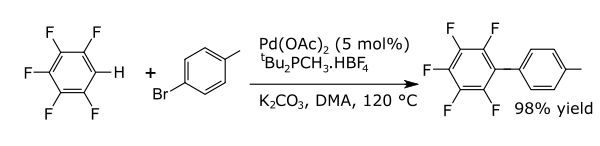
В реакции сочетания металл катализирует сочетание двух формальных радикальных фрагментов. Обычные реакции сочетания с аренами приводят к образованию новых углерод-углеродные связи например, алкиларены, виниларены, бирарилы, новые углеродно-азотные связи (анилины) или новые углерод-кислородные связи (арилокси соединения). Примером может служить прямое арилирование перфторбензолы [6]
Гидрирование
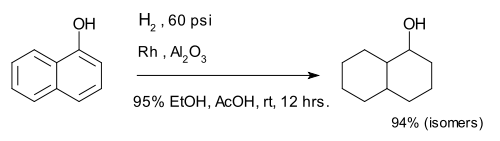
Гидрирование аренов создают насыщенные кольца. Состав 1-нафтол полностью превращается в смесь декалин -ol изомеры.[7]
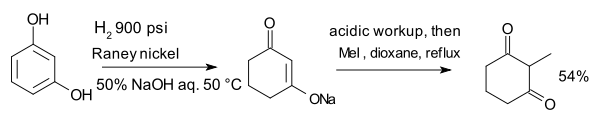
Состав резорцин, гидрированный с Никель Ренея в присутствии водного едкий натр образует энолировать который алкилирован йодистый метил к 2-метил-1,3-циклогександиону:[8]
Циклоприсоединения
Циклоприсоединение реакции не распространены. Необычная термическая реакционная способность аренов по Дильсу – Альдеру обнаруживается в Реакция Вагнера-Яурегга. Другие реакции фотохимического циклоприсоединения с алкенами протекают через эксимеры.
Деароматизация
В реакции деароматизации ароматичность реагента навсегда теряется.
Бензол и производные бензола
Производные бензола имеют от одного до шести заместители прикреплен к центральной бензольной сердцевине. Примеры бензольных соединений только с одним заместителем: фенол, который несет гидроксил группа и толуол с метил группа. Когда в кольце присутствует более одного заместителя, их пространственное соотношение становится важным, для чего паттерны замещения аренов орто, мета, и параграф придуманы. Например, три изомеры существуют для крезол потому что метильная группа и гидроксильная группа могут быть размещены рядом друг с другом (орто), одна позиция удалена друг от друга (мета), либо две удаленные друг от друга позиции (параграф). Ксиленол имеет две метильные группы в дополнение к гидроксильной группе, и для этой структуры существует 6 изомеров.
- Типичные ареновые соединения
Кольцо арена имеет способность стабилизировать заряды. Это видно, например, в феноле (C6ЧАС5–OH), что является кислый у гидроксила (OH), так как заряд этого кислорода (алкоксид –O−) частично делокализован в бензольное кольцо.
Другой моноциклический ароматический углеводород
Другие моноциклические ароматические углеводороды включают: Циклотетрадекагептаен или же Циклооктадеканонаен.
Полициклические ароматические углеводороды
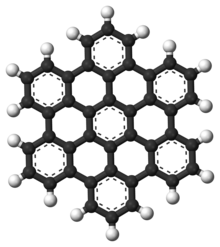
Полициклические ароматические углеводороды (ПАУ) - это ароматические углеводороды, состоящие из конденсированных ароматный кольца и не содержат гетероатомы или нести заместители.[9] Нафталин это простейший пример ПАУ. ПАУ встречаются в масло, каменный уголь, и деготь отложения и образуются как побочные продукты сгорания топлива (будь то ископаемое топливо или биомасса). Как загрязнители, они вызывают озабоченность, поскольку некоторые соединения были идентифицированы как канцерогенный, мутагенный, и тератогенный. ПАУ также содержатся в приготовленной пище. Исследования показали, что высокие уровни ПАУ обнаруживаются, например, в мясе, приготовленном при высоких температурах, таком как жарка на гриле или барбекю, а также в копченой рыбе.[10][11][12]
Они также встречаются в межзвездная среда, в кометы, И в метеориты и являемся молекула-кандидат на роль основы для самых ранних форм жизни. В графен Мотив PAH распространяется на большие 2D-листы.
Смотрите также
- Ароматические заместители: Арил, Арилокси и Аренедиил
- Асфальтен
- Гидродеалкилирование
- Простые ароматические кольца
- Оксид родия-платины, катализатор, используемый для гидрирования ароматических соединений.
Рекомендации
- ^ Энциклопедия HighBeam: ароматические соединения.
- ^ Армит, Джеймс Уилкинс; Робинсон, Роберт (1925). «Полиядерные гетероциклические ароматические типы. Часть II. Некоторые ангидрониевые основания». J. Chem. Soc. Пер. 127: 1604–1618.
- ^ Дженсен, Уильям Б. (апрель 2009 г.). «Круглый символ ароматичности» (PDF). J. Chem. Educ. 86 (4): 423–424. Bibcode:2009JChEd..86..423J. Дои:10.1021 / ed086p423.
- ^ Марш, Джерри (1985), Продвинутая органическая химия: реакции, механизмы и структура (3-е изд.), Нью-Йорк: Wiley, ISBN 0-471-85472-7
- ^ Webb, K .; Сеневиратне В. (1995). «Мягкое окисление ароматических аминов». Буквы Тетраэдра. 36 (14): 2377–2378. Дои:10.1016 / 0040-4039 (95) 00281-Г.
- ^ Lafrance, M .; Rowley, C .; Ву, Т .; Фагну, К. (2006). «Каталитическое межмолекулярное прямое арилирование перфторбензолов». Журнал Американского химического общества. 128 (27): 8754–8756. CiteSeerX 10.1.1.631.607. Дои:10.1021 / ja062509l. PMID 16819868.
- ^ Мейерс, А. И .; Beverung, W. N .; Голт, Р. «1-Нафтол». Органический синтез. 51: 103.; Коллективный объем, 6
- ^ Noland, Wayland E .; Бауде, Фредерик Дж. «Этилиндол-2-карбоксилат». Органический синтез. 41: 56.; Коллективный объем, 5
- ^ Фетцер, Дж. К. (2000). «Химия и анализ крупных полициклических ароматических углеводородов». Полициклические ароматические соединения. Нью-Йорк: Вили. 27 (2): 143. Дои:10.1080/10406630701268255. ISBN 0-471-36354-5.
- ^ «Полициклические ароматические углеводороды - присутствие в продуктах питания, воздействие на рацион и воздействие на здоровье» (PDF). Европейская комиссия, Научный комитет по пищевым продуктам. 4 декабря 2002 г.
- ^ Larsson, B.K .; Зальберг, врач-терапевт; Eriksson, AT; Буск, Л.А. (1983). «Полициклические ароматические углеводороды в блюдах, приготовленных на гриле». J. Agric. Food Chem. 31 (4): 867–873. Дои:10.1021 / jf00118a049. PMID 6352775.
- ^ «Полициклические ароматические углеводороды (ПАУ)». Агентство регистрации токсичных веществ и заболеваний. 1996 г.
внешняя ссылка
 СМИ, связанные с Ароматика в Wikimedia Commons
СМИ, связанные с Ароматика в Wikimedia Commons