Алазоцин - Alazocine - Wikipedia
 | |
| Клинические данные | |
|---|---|
| Другие имена | СКФ-10047; WIN-19631; N-Аллилнорметазоцин; NANM; NAN; ANMC; 2'-гидрокси-5,9-диметил-2-аллил-6,7-бензоморфан |
| Код УВД |
|
| Идентификаторы | |
| |
| Количество CAS |
|
| PubChem CID | |
| ChemSpider | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.162.264 |
| Химические и физические данные | |
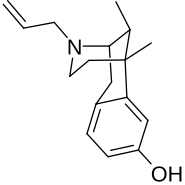
| Формула | C17ЧАС23NО |
| Молярная масса | 257.377 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Алазоцин (кодовое название разработки SKF-10047), также известный как N-аллилнорметазоцин (NANM), это синтетический опиоид обезболивающее из бензоморфан семья, связанная с метазоцин, который никогда не продавался.[1][2][3] Помимо опиоидной активности, препарат является сигма рецептор агонист, и широко использовался в научное исследование в исследованиях этого рецептора.[4][5] Алазоцин описывается как мощный обезболивающее, психотомиметик или же галлюциноген, и морфий или же опиоидный антагонист.[2] Более того, одна из его энантиомеры был первым соединением, которое, как было обнаружено, выборочно метка то σ1 рецептор, и привел к открытию и характеристике рецептора.[4][5]
Фармакология
Фармакодинамика
Алазоцин шоу стереоселективность в его фармакодинамика.[6] (-) - энантиомер является неселективным и высокоактивнымблизость лиганд из μ-, κ-, и дельта-опиоидные рецепторы (Kя = 3,0, 4,7 и 15 нМ дюйм морская свинка мозг мембраны ) с очень низким сродством к сигме σ1 рецептор (Kя = 1,800–4,657 нМ в мембранах мозга морских свинок).[6][7] Он действует как умеренно-эффективность частичный агонист κ-опиоидного рецептора (Kя = 0,4 нМ, EC50 = 24 нМ, и EМаксимум = 66% для (±) -алазоцина против мышь рецептор трансфицированный в HEK293 клетки)[8] и как антагонист μ-опиоидного рецептора (Kя = 1,15 нМ для (±) -алазоцина против рецептора мыши, трансфицированного в клетках HEK293).[9] Это также агонист δ-опиоидного рецептора с гораздо более низкой активностью (Kя = не сообщается, IC50 = 184 нМ, и яМаксимум = 68% для (±) -алазоцина против рецептора мыши, трансфицированного в клетках HEK293).[10]
И наоборот, (+) -стереоизомер мало любит опиоидные рецепторы (Kя для 1900, 1600 и 19000 нМ для μ-, κ-, δ-опиоидных рецепторов в мембранах головного мозга морских свинок), а вместо этого является селективным и высокоаффинным агонист из σ1 рецептор (Kя = 48–66 нМ в мембранах головного мозга морских свинок).[6][7] Однако (+) - энантиомер также проявляет умеренное сродство к дизоцилпин (МК-801) или фенциклидин (PCP) сайт Рецептор NMDA (Kя = 587 нМ дюйм крыса мембраны мозга относительно 45 нМ для σ1 рецептор) и, следовательно, является неконкурентоспособный Антагонист рецептора NMDA а также при более высоких концентрациях.[11] Таким образом, (+) - алазоцин лишь умеренно селективен в качестве лиганда σ1 рецептор.[11]
Оба энантиомера алазоцина имеют очень низкое сродство к сигма σ2 рецептор (Kя = 13 694 нМ и 4581 нМ для (+) - и (-) - энантиомеров, соответственно, в мембранах головного мозга крысы или крысы PC12 ячеек).[11][7][5] Таким образом, из-за его высокого сродства к σ1 рецептор, (+) - алазоцин можно использовать для различения двух подтипов сигма-рецепторов в научных исследованиях, например, в анализы связывания радиолиганда.[11][5]
В совокупности (-) - алазоцин является селективным частичным агонистом κ-опиоидного рецептора, антагонистом μ-опиоидного рецептора и, в гораздо меньшей степени, агонистом δ-опиоидного рецептора.[8][9][10] с очень низким сродством к сигма-рецепторам, а (+) - алазоцин является селективным агонистом сигма-рецепторов1 рецептора и в меньшей (~ 10 раз) степени антагонист рецептора NMDA с низким сродством к опиоиду и сигма σ2 рецепторы.[6][7][11][5]
История
Алазоцин был одним из первых членов бензоморфан семейство опиоидных анальгетиков, подлежащих исследованию.[1] Впервые это было описано в научная литература в 1961 г.[12] Его развитие стало результатом налорфин (N-аллилнорморфин), мощный анальгетик и антагонист опиоидов с аналогичной фармакологией, который был представлен в середине 1950-х годов.[1] Было обнаружено, что алазоцин оказывает сильное психотомиметическое действие на человека, и его дальнейшее клиническое применение не разрабатывалось.[13][1] Впоследствии другие бензоморфаны, такие как пентазоцин (ан N-диметилаллилбензоморфан), циклазоцин (ан N-циклопропилметилбензоморфан), и феназоцин (ан N-фенилэтилбензоморфан), и некоторые из них были проданы для использования в качестве анальгетиков.[1]
Сигма σ1 рецептор был назван в 1976 году, а (+) - алазоцин был описан как его прототипный лиганд.[13][14][15] Первоначально считалось, что рецептор является опиоидным рецептором, а затем какое-то время его путали с рецептором NMDA, но в конечном итоге его отличили от них обоих.[13][14][5] Психотомиметические эффекты алазоцина и других бензоморфинов изначально неправильно приписывались агонизму σ1 рецептор; последующие исследования установили, что эффекты на самом деле вызваны агонизмом κ-опиоидного рецептора и / или антагонизмом рецептора NMDA.[13][5] Сигма σ2 рецептор был открыт и назван в 1990 году и был идентифицирован отчасти из-за резко сниженного сродства алазоцина к рецептору по сравнению с σ1 рецептор (в отличие от неселективных лигандов, таких как галоперидол, дитолилгуанидин, и (+) - 3-ППС, которые показывают сходство для обоих подтипов).[7]
Рекомендации
- ^ а б c d е А.Ф. Кэси; R.T. Парфитт (29 июня 2013 г.). Опиоидные анальгетики: химический состав и рецепторы. Springer Science & Business Media. С. 176–178, 420–421. ISBN 978-1-4899-0585-7.
- ^ а б Китс, Артур С .; Телфорд, Джейн (1964). «Наркотические антагонисты как анальгетики». Молекулярная модификация в Препарат, средство, медикамент Дизайн. Успехи химии. 45. С. 170–176. Дои:10.1021 / ba-1964-0045.ch014. ISBN 0-8412-0046-7. ISSN 0065-2393.
- ^ Ивамото ET (февраль 1981 г.). «Фармакологические эффекты N-аллилнорметазоцина (SKF-10047)». Монография исследования NIDA. 34: 82–8. PMID 6783955.
- ^ а б Нараянан С., Бхат Р., Месанжо С., Поупаерт Дж. Х., Маккарди С. Р. (январь 2011 г.). «Раннее развитие лигандов сигма-рецепторов». Медицинская химия будущего. 3 (1): 79–94. Дои:10.4155 / fmc.10.279. PMID 21428827.
- ^ а б c d е ж грамм Хаяси Т., Су ТП (2004). «Лиганды рецептора сигма-1: потенциал в лечении нервно-психических расстройств». Препараты ЦНС. 18 (5): 269–84. Дои:10.2165/00023210-200418050-00001. PMID 15089113. S2CID 72726251.
- ^ а б c d Tam SW (февраль 1985 г.). «(+) - [3H] SKF 10,047, (+) - [3H] этилкетоциклазоцин, мю, каппа, дельта и сайты связывания фенциклидина в мембранах мозга морских свинок». Европейский журнал фармакологии. 109 (1): 33–41. Дои:10.1016/0014-2999(85)90536-9. PMID 2986989.
- ^ а б c d е Hellewell SB, Bowen WD (сентябрь 1990 г.). «Сигма-подобный сайт связывания в клетках феохромоцитомы крысы (PC12): пониженное сродство к (+) - бензоморфанам и более низкая молекулярная масса указывают на форму сигма-рецептора, отличную от формы мозга морской свинки». Исследование мозга. 527 (2): 244–53. Дои:10.1016/0006-8993(90)91143-5. PMID 2174717. S2CID 24546226.
- ^ а б Gharagozlou P, Hashemi E, DeLorey TM, Clark JD, Lameh J (январь 2006 г.). «Фармакологические профили опиоидных лигандов на каппа-опиоидных рецепторах». BMC Фармакология. 6: 3. Дои:10.1186/1471-2210-6-3. ЧВК 1403760. PMID 16433932.
- ^ а б Гарагозлоу П., Демирчи Х., Дэвид Кларк Дж., Ламех Дж. (Январь 2003 г.). «Активность опиоидных лигандов в клетках, экспрессирующих клонированные мю-опиоидные рецепторы». BMC Фармакология. 3: 1. Дои:10.1186/1471-2210-3-1. ЧВК 140036. PMID 12513698.
- ^ а б Гарагозлоу П., Демирчи Х., Кларк Дж. Д., Ламех Дж. (Ноябрь 2002 г.). «Профили активации опиоидных лигандов в клетках HEK, экспрессирующих дельта-опиоидные рецепторы». BMC Neuroscience. 3: 19. Дои:10.1186/1471-2202-3-19. ЧВК 137588. PMID 12437765.
- ^ а б c d е Чжоу Ю.К., Ляо Д.Ф., Чанг В.Й., Лин М.Ф., Чен С.Ф. (март 1999 г.). «Связывание димеморфана с рецептором сигма-1 и его противосудорожные и локомоторные эффекты у мышей по сравнению с декстрометорфаном и декстрорфаном». Исследование мозга. 821 (2): 516–9. Дои:10.1016 / с0006-8993 (99) 01125-7. PMID 10064839. S2CID 22762264.
- ^ Гордон М., Лафферти Дж. Дж., Тедески Д.Х., Эдди Н.Б., Мэй Э.Л. (декабрь 1961 г.). «Новый мощный антагонист анальгетика». Природа. 192 (4807): 1089. Дои:10.1038 / 1921089a0. PMID 13900480. S2CID 4212447.
- ^ а б c d Осборн Алмейда; Тони С. Шиппенберг (6 декабря 2012 г.). Нейробиология опиоидов. Springer Science & Business Media. С. 356–. ISBN 978-3-642-46660-1.
- ^ а б Юрген Шюттлер; Гельмут Швильден (8 января 2008 г.). Современные анестетики. Springer Science & Business Media. С. 97–. ISBN 978-3-540-74806-9.
- ^ Мартин WR, Идес CG, Томпсон JA, Huppler RE, Gilbert PE (июнь 1976 г.). «Эффекты морфин- и налорфиноподобных препаратов у независимых и морфин-зависимых хронических спинальных собак». Журнал фармакологии и экспериментальной терапии. 197 (3): 517–32. PMID 945347.
