N-метил-D-аспарагиновая кислота - N-Methyl-D-aspartic acid
 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК (2р) -2- (Метиламино) бутандиовая кислота[1] | |
| Другие имена N-Метиласпартат; N-Метил-D-аспартат; NMDA | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 1724431 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| КЕГГ | |
| MeSH | N-метиласпартат |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Свойства | |
| C5ЧАС9NО4 | |
| Молярная масса | 147.130 г · моль−1 |
| Внешность | Белые непрозрачные кристаллы |
| Запах | Без запаха |
| Температура плавления | От 189 до 190 ° C (от 372 до 374 ° F, от 462 до 463 K) |
| журнал п | 1.39 |
| Кислотность (пKа) | 2.206 |
| Основность (пKб) | 11.791 |
| Опасности | |
| S-фразы (устарело) | S22, S24 / 25 |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 137 мг кг−1 (внутрибрюшинно, мышиный) |
| Родственные соединения | |
Родственные производные аминокислот | |
Родственные соединения | Диметилацетамид |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
N-Метил-D-аспарагиновая кислота или N-Метил-D-аспартат (NMDA) является аминокислота производная, которая действует как особый агонист на Рецептор NMDA имитируя действие глутамат, то нейротрансмиттер который обычно действует на этот рецептор. В отличие от глутамата, NMDA только связывается и регулирует рецептор NMDA и не влияет на другие рецепторы глутамата (например, рецепторы для AMPA и каинат ). Рецепторы NMDA особенно важны, когда они становятся сверхактивными, например, во время вывод от алкоголь поскольку это вызывает такие симптомы, как волнение и, иногда, эпилептиформная припадки.
Биологическая функция
В 1962 году Дж. К. Уоткинс сообщил о синтезе NMDA, изомер из ранее известных N-Метил-DL-аспарагиновая кислота (PubChem ID 4376).[2][3] NMDA - водорастворимый D-альфа-аминокислота - аспарагиновая кислота производная с N-метильный заместитель и D-конфигурация - найдено через Animalia от ланцетники к млекопитающие.[4][5] На гомеостатическом уровне NMDA играет важную роль в качестве нейротрансмиттера и нейроэндокринного регулятора.[6] При повышенных, но субтоксичных уровнях NMDA становится нейрозащитным.[нужна цитата ] В чрезмерных количествах NMDA является эксайтотоксином. Исследование поведенческой нейробиологии использует NMDA эксайтотоксичность вызвать поражения в определенных областях животное головной или спинной мозг субъекта для изучения изменений в поведении.[7]
Механизм действия для Рецептор NMDA является специфическим агонистом, связывающимся с его субъединицами NR2, а затем открывается неспецифический катионный канал, который может позволить прохождение Ca2+ и Na+ в ячейку и K+ из клетки. В возбуждающий постсинаптический потенциал (ВПСП), образующийся при активации рецептора NMDA, также увеличивает концентрацию Са2+ в камере. CA2+ может, в свою очередь, действовать в качестве второго мессенджера в различных сигнальных путях.[8][9][10][11] Этот процесс модулируется рядом эндогенных и экзогенных соединений и играет ключевую роль в широком спектре физиологических (таких как память) и патологических процессов (таких как эксайтотоксичность ).
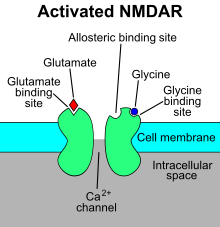
Антагонисты
Примеры антагонисты, или более подходящее название блокаторов рецепторных каналов рецептора NMDA, представляют собой APV, амантадин, декстрометорфан (ДХМ), кетамин, магний,[12] тилетамин, фенциклидин (PCP), рилузол, мемантин, метоксетамин (MXE), метоксфенидин (MXP) и кинуреновая кислота. В то время как дизоцилпин обычно считается прототипом блокатора рецепторов NMDA и является наиболее распространенным агентом, используемым в исследованиях, исследования на животных продемонстрировали некоторое количество нейротоксичность, которые могут встречаться или не встречаться у людей. Эти соединения обычно называют Антагонисты рецепторов NMDA.
Смотрите также
использованная литература
- ^ «N-Метиласпартат - Резюме соединения». PubChem Compound. США: Национальный центр биотехнологической информации. 24 июня 2005 г. Идентификация. Получено 9 января 2012.
- ^ Уоткинс, Дж. К. (ноябрь 1962 г.). «Синтез некоторых кислых аминокислот, обладающих нейрофармакологической активностью». Журнал медицинской и фармацевтической химии. 5 (6): 1187–1199. Дои:10.1021 / jm01241a010. ISSN 1520-4804. PMID 14056452.
- ^ Curtis, D. R .; Уоткинс, Дж. К. (сентябрь 1960 г.). «Возбуждение и угнетение спинномозговых нейронов структурно родственными аминокислотами». Журнал нейрохимии. 6 (2): 117–141. Дои:10.1111 / j.1471-4159.1960.tb13458.x. ISSN 1471-4159. PMID 13718948.
- ^ Тодороки, Нацуми; Шибата, Кимихико; Ямада, Такахиро; Кера, Йошио; Ямада, Рё-хей (май 1999 г.). "Определение N-метил-D-аспарагиновая кислота в тканях двустворчатых моллюсков методом высокоэффективной жидкостной хроматографии ». Журнал хроматографии B: биомедицинские науки и приложения. 728 (1): 41–47. Дои:10.1016 / S0378-4347 (99) 00089-4. ISSN 0378-4347. PMID 10379655.
- ^ Д'Аниелло, Антимо; Де Симона, Антонелла; Спинелли, Патриция; Д'Аниелло, Сальваторе; Бранно, Маргарита; Аниелло, Франческо; Риос, Жаннетт; Цесарская, Мара; Фишер, Джордж (сентябрь 2002 г.). "Специфический метод ферментативной высокоэффективной жидкостной хроматографии для определения N-метил-D-аспарагиновая кислота в биологических тканях ». Аналитическая биохимия. 308 (1): 42–51. Дои:10.1016 / S0003-2697 (02) 00326-3. ISSN 0003-2697. PMID 12234462.
- ^ Д'Аниелло, Антимо; Де Симона, Антонелла; Спинелли, Патриция; Д'Аниелло, Сальваторе; Бранно, Маргарита; Аниелло, Франческо; Риос, Жаннетт; Цесарская, Мара; Фишер, Джордж (2002-09-01). "Специфический метод ферментативной высокоэффективной жидкостной хроматографии для определения N-метил-D-аспарагиновая кислота в биологических тканях ». Аналитическая биохимия. 308 (1): 42–51. Дои:10.1016 / S0003-2697 (02) 00326-3. ISSN 0003-2697. PMID 12234462. Получено 2020-05-02.
- ^ Джонсон, Патриция I .; Паренте, Мэри Энн; Звездный, Джеймс Р. (май 1996 г.). «NMDA-индуцированные поражения прилежащего ядра или вентрального паллидума увеличивают полезную эффективность пищи для лишенных недостатков крыс». Исследование мозга. 722 (1–2): 109–117. Дои:10.1016/0006-8993(96)00202-8. ISSN 0006-8993. PMID 8813355. S2CID 23002111.
- ^ Dingledine, R; Борхес К. (март 1999 г.). «Ионные каналы рецептора глутамата». Pharmacol. Rev. 51 (1): 7–61. PMID 10049997.
- ^ Лю, Y; Чжан Дж (октябрь 2000 г.). «Последние разработки в рецепторах NMDA». Chin Med J (англ.). 113 (10): 948–956. PMID 11775847.
- ^ Калл-Кэнди, S; Брикли С. (июнь 2001 г.). «Субъединицы рецептора NMDA: разнообразие, развитие и болезнь». Текущее мнение в нейробиологии. 11 (3): 327–335. Дои:10.1016 / S0959-4388 (00) 00215-4. PMID 11399431. S2CID 11929361.
- ^ Paoletti, P; Нейтон Дж (февраль 2007 г.). «Субъединицы рецептора NMDA: функции и фармакология». Текущее мнение в фармакологии. 7 (1): 39–47. Дои:10.1016 / j.coph.2006.08.011. PMID 17088105.
- ^ Мерк, Х. (01.01.2002). «Магний и аффективные расстройства». Пищевая неврология. 5 (6): 375–389. Дои:10.1080/1028415021000039194. ISSN 1028-415X. PMID 12509067. S2CID 28550919.
дальнейшее чтение
- Уоткинс, Джеффри С.; Джейн, Дэвид Э. (2006), «История глутамата», Br. J. Pharmacol., 147 (Приложение 1): S100 – S108, Дои:10.1038 / sj.bjp.0706444, ЧВК 1760733, PMID 16402093
- Блез, Матиас-Коста; Соудхамини, Раманатан; Рао, Метпалли Рагху Прасад; Прадхан, Нитянанда (2004), «Эволюционный анализ следов ионотропных последовательностей рецепторов глутамата и моделирование взаимодействий агонистов с различными субъединицами рецепторов NMDA», J. Mol. Модель., 10 (5–6): 305–316, Дои:10.1007 / s00894-004-0196-7, PMID 15597199, S2CID 19993673
