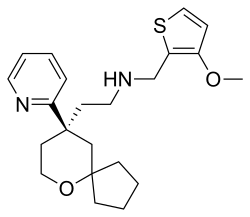
Олицеридин - Oliceridine
 | |
| Клинические данные | |
|---|---|
| Произношение | OH li SER i deen |
| Торговые наименования | Олинвик |
| Другие имена | ТРВ-130, ТРВ130 |
| AHFS /Drugs.com | Факты о профессиональных наркотиках |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Внутривенно[1] |
| Код УВД |
|
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Химические и физические данные | |
| Формула | C22ЧАС30N2О2S |
| Молярная масса | 386.55 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Олицеридин, продается под торговой маркой Олинвик, является опиоид лекарство, которое используется для лечения острого заболевания средней и тяжелой степени боль у взрослых.[2] Это дается внутривенный (IV) инъекция.[2]
Наиболее частые побочные эффекты включают тошноту, рвоту, головокружение, головную боль, запор, кожный зуд и низкий уровень кислорода в крови.[3]
Он был одобрен для медицинского использования в США в августе 2020 года.[3]
Медицинское использование
Олицеридин указал для кратковременного внутривенного применения в больницах или других контролируемых клинических условиях, например, во время стационарных и амбулаторных процедур.[2] Не предназначен для домашнего использования.[2]
Побочные эффекты
Профиль безопасности олицеридина аналогичен профилю безопасности других опиоидов.[2] Как и в случае с другими опиоидами, наиболее частыми побочными эффектами олицеридина являются тошнота, рвота, головокружение, головная боль и запор.[2] Длительное употребление опиоидных анальгетиков во время беременности может привести к развитию синдрома отмены опиоидов у новорожденных.[2]
Олинвик несет предупреждение о зависимости, жестоком обращении и злоупотреблении; опасное для жизни угнетение дыхания; неонатальный синдром отмены опиоидов; и риски от одновременного использования с бензодиазепинами или другими депрессантами центральной нервной системы.[2] В отличие от других опиоидов для внутривенного введения, максимальная рекомендуемая суточная доза Олинвика составляет 27 миллиграммов.[2]
Противопоказания
Олицеридин не следует назначать людям со значительным угнетением дыхания; острая или тяжелая бронхиальная астма в неконтролируемых условиях или при отсутствии реанимационного оборудования; известная или предполагаемая желудочно-кишечная непроходимость; или известная гиперчувствительность к лекарству.[2]
Фармакология
Фармакодинамика
Олицеридин - это μ-опиоидный рецептор предвзятый агонист разработан Trevena. В ячейках (in vitro) исследования, олицеридин вызывает надежные G протеин сигнализация, с потенция и эффективность аналогично тому из морфий, но с меньшим β-аррестин 2 набор и рецепторная интернализация [4]. Однако в недавних отчетах подчеркивается, что это может быть связано с его низкой внутренней эффективностью. [5], а не функциональная селективность или «ошибка G-белка», как сообщалось изначально. В естественных условиях, может быть меньше побочные эффекты (включая угнетение дыхания и запор) по сравнению с морфий.[6][7][8] В целом, in vitro потенция не гарантирует клинической значимости для человека.[9]
История
В контролируемых и открытых исследованиях олицеридин лечили 1535 участников с острой болью от умеренной до тяжелой.[2] Его безопасность и эффективность были установлены путем сравнения олицеридина с плацебо в рандомизированных контролируемых исследованиях участников, перенесших операцию на бурсите или абдоминальную операцию.[2] Участники, которым вводили олицеридин, сообщили об уменьшении боли по сравнению с плацебо в утвержденных дозах.[2]
Соединенные штаты. Управление по контролю за продуктами и лекарствами (FDA) одобрило олицеридин на основании данных трех клинических испытаний (испытание 1 / NCT02815709, испытание 2 / NCT02820324 и испытание 3) с участием 1558 участников в возрасте от 18 до 89 лет, которые нуждались в обезболивающих.[3] Испытания проводились в 53 центрах США.[3]
В испытание 1 были включены участники, перенесшие операцию на косточке.[3] Участники с умеренной и сильной послеоперационной болью были случайным образом распределены для приема олицеридина, плацебо или одобренного препарата для лечения боли (морфина) в течение 48 часов через вену.[3] Ни участники, ни медицинские работники не знали, какое лечение проводится, пока испытание не было завершено.[3] Всем участникам разрешалось использовать обезболивающее, если боль не контролировалась с помощью исследуемых препаратов.[3]
В исследование 2 вошли участники, перенесшие хирургическое удаление жира на брюшной стенке (абдоминопластика) и страдавшие от умеренной до сильной боли.[3] Участники были случайным образом распределены для приема олицеридина, плацебо или одобренного препарата для лечения боли (морфина) в течение 24 часов через вену.[3] Ни участники, ни медицинские работники не знали, какое лечение проводится, пока испытание не было завершено.[3] Всем участникам разрешалось использовать обезболивающее, если боль не контролировалась с помощью исследуемых препаратов.[3]
Чтобы оценить преимущества олицеридина, участники использовали числовую шкалу, чтобы оценить, насколько сильной была боль после операции.[3] Баллы участников, получавших олицеридин, сравнивали с баллами участников, получавших плацебо, и тех, кто получал морфин.[3]
В третьем испытании участники, которые испытывали боль после различных операций или по состоянию здоровья, получали как минимум одну дозу олицеридина.[3] Данные этого исследования использовались только для оценки побочных эффектов олицеридина.[3]
Олицеридин был одобрен для медицинского применения в США в августе 2020 года.[2] FDA предоставило разрешение на использование Олинвик компании Trevena Inc.[2]
Общество и культура
Легальное положение
Консультативный комитет США Управление по контролю за продуктами и лекарствами (FDA) проголосовало против одобрения олицеридина в 2018 году из-за опасений, что польза от препарата не превышает риска. Риски олицеридина включают продление QT интервал на ЭКГ, и угнетение дыхательного драйва (из-за чего человек может перестать дышать).[10] В результате голосования комитета FDA отказалось одобрить олицеридин, сославшись на соображения безопасности.[11]
Олицеридин был одобрен для медицинского применения в США в августе 2020 года.[2] FDA предоставило разрешение на использование Олинвик компании Trevena Inc.[2]
30 октября 2020 года DEA выпустило временное окончательное правило, определяющее олидеридин как Список II CSA (код DEA 9245).
Рекомендации
- ^ «Олинвиколицеридин для инъекций, раствор». DailyMed. 18 августа 2020 г.. Получено 16 сентября 2020.
- ^ а б c d е ж грамм час я j k л м п о п q «FDA одобряет новый опиоид для внутривенного применения в больницах и других контролируемых клинических учреждениях». НАС. Управление по контролю за продуктами и лекарствами (FDA) (Пресс-релиз). 7 августа 2020 г.. Получено 7 августа 2020.
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ а б c d е ж грамм час я j k л м п о п "Снимки испытаний лекарств: Олинвик". НАС. Управление по контролю за продуктами и лекарствами (FDA). 7 августа 2020 г.. Получено 16 сентября 2020.
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ ДеВайр С.М., Ямашита Д.С., Ромингер Д.Х., Лю Дж., Коуэн С.Л., Грачик Т.М. и др. (Март 2013 г.). «Лиганд, связанный с G-белком, у μ-опиоидного рецептора является сильнодействующим обезболивающим с уменьшением желудочно-кишечной и респираторной дисфункции по сравнению с морфином». Журнал фармакологии и экспериментальной терапии. 344 (3): 708–17. Дои:10.1124 / jpet.112.201616. PMID 23300227. S2CID 8785003.
- ^ Гиллис А., Гонден А.Б., Кливер А., Санчес Дж., Лим HD, Аламейн С. и др. (Март 2020 г.). «Низкая внутренняя эффективность активации G-белка может объяснить улучшенные профили побочных эффектов новых опиоидных агонистов». Научная сигнализация. 13 (625): eaaz3140. Дои:10.1126 / scisignal.aaz3140. PMID 32234959. S2CID 214771721.
- ^ Chen XT, Pitis P, Liu G, Yuan C, Gotchev D, Cowan CL, et al. (Октябрь 2013). "Взаимосвязь структура-активность и открытие лиганда опиоидного рецептора, смещенного G-белком, [(3-метокситиофен-2-ил) метил] ({2 - [(9R) -9- (пиридин-2-ил) -6- оксаспиро- [4,5] декан-9-ил] этил}) амин (TRV130) для лечения острой сильной боли ». Журнал медицинской химии. 56 (20): 8019–31. Дои:10.1021 / jm4010829. PMID 24063433.
- ^ Soergel DG, Subach RA, Sadler B, Connell J, Marion AS, Cowan CL, et al. (Март 2014 г.). «Первый клинический опыт с TRV130: фармакокинетика и фармакодинамика у здоровых добровольцев». Журнал клинической фармакологии. 54 (3): 351–7. Дои:10.1002 / jcph.207. PMID 24122908. S2CID 25049515.
- ^ Персонал (1 октября 2015 г.). «Острая послеоперационная боль». Новости генной инженерии и биотехнологии (Бумага). 35 (17): 40.
- ^ Вальдман С.А. (июль 2002 г.). «Предсказывает ли потенция клиническую эффективность? Иллюстрация с помощью антигистаминной модели». Анналы аллергии, астмы и иммунологии. 89 (1): 7–11, викторина 11-2, 77. Дои:10.1016 / S1081-1206 (10) 61904-7. PMID 12141724.
- ^ «Группа FDA проголосовала против обезболивающего олицеридина». www.medpagetoday.com. MedPage Today, LLC. 11 октября 2018 г.. Получено 23 декабря 2018.
- ^ "FDA отклоняет болеутоляющее олицеридин Тревены | FierceBiotech". www.fiercebiotech.com. Questex ООО. Получено 23 декабря 2018.
внешняя ссылка
- «Олицеридин». Портал информации о наркотиках. Национальная медицинская библиотека США.
- Номер клинического исследования NCT02815709 за «Исследование олицеридина (TRV130) для лечения умеренной и тяжелой острой боли после бунионэктомии (APOLLO-1)» в ClinicalTrials.gov
- Номер клинического исследования NCT02820324 за «Исследование олицеридина (TRV130) для лечения умеренной и сильной острой боли после абдоминопластики» в ClinicalTrials.gov
