Смешанное торможение - Mixed inhibition
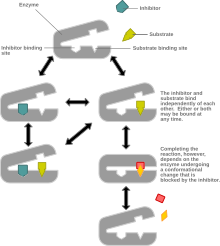

Смешанное торможение это тип ингибирование ферментов в котором ингибитор может связываться с ферментом независимо от того, связал ли фермент уже субстрат или нет, но имеет большее сродство к тому или иному состоянию.[1] Это называется «смешанным», потому что его можно рассматривать как концептуальную «смесь» конкурентное торможение, в котором ингибитор может связывать фермент, только если субстрат не имеет уже связаны, и неконкурентное торможение, в котором ингибитор может связывать фермент, только если субстрат имеет уже связаны. Если способность ингибитора связывать фермент точно так же независимо от того, связывает ли фермент уже субстрат, он известен как неконкурентоспособный ингибитор.[1] [2] Неконкурентное торможение иногда рассматривается как частный случай смешанного торможения.
При смешанном ингибировании ингибитор связывается с аллостерическим сайтом, то есть сайтом, отличным от активный сайт где субстрат связывает. Однако не все ингибиторы, которые связываются в аллостерических сайтах, являются смешанными ингибиторами. [1]
Смешанное ингибирование может привести к:
- Уменьшение видимого сродства фермента к субстрату (значение Km, по-видимому, увеличивается; ) - наблюдается в тех случаях, когда ингибитор способствует связыванию со свободным ферментом. Ближе имитирует конкурентную привязку.
- Повышение очевидного сродства фермента к субстрату (значение Km, по-видимому, уменьшается; ) - наблюдается в случаях, когда ингибитор способствует связыванию с комплексом фермент-субстрат. Ближе имитирует неконкурентную привязку.
В любом случае ингибирование снижает кажущуюся максимальную скорость ферментативной реакции ().[3]
Математически смешанное торможение происходит, когда факторы α и α ’(введенные в Уравнение Михаэлиса-Ментен для учета конкурентного и неконкурентного торможения соответственно) оба больше 1.
В частном случае, когда α = α ’, неконкурентное торможение происходит, и в этом случае уменьшается, но не затронут. На практике это очень необычно.[3]
Биологические примеры
В глюконеогенез, фермент cPEPCK (цистолический фосфоенолпируваткарбоксикиназа ) отвечает за преобразование оксалоацетат в фосфоенолпировиноградная кислота, или PEP, когда гуанозинтрифосфат, GTP, присутствует. Этот этап является исключительным для глюконеогенеза, который происходит при голодании из-за истощения организма глюкозой. cPEPCK, как известно, регулируется Геништейн, изофлавон, который естественным образом содержится в ряде растений. [4] Впервые было доказано, что генистеин подавляет активность cPEPCK. В одном исследовании присутствие этого изофлавона привело к снижению уровня сахара в крови. Пониженный уровень сахара в крови означает, что в крови меньше глюкозы. Если это происходит у голодающего субъекта, это происходит из-за того, что глюконеогенез ингибируется, предотвращая повышенное производство глюкозы. Способность генистеина снижать уровень сахара в крови человека позволяет называть его антидиабетическим свойством. [4] Механизм, в котором генистеин ингибирует фермент cPEPCK, был дополнительно оценен. Во-первых, cPEPCK был размещен в присутствии 3-меркаптопропионовая кислота или 3-МПА, известный ингибитор фермента. Его сравнивали с результатами размещения cPEPCK в присутствии генистеина, которые показали, что для снижения активности cPEPCK использовался механизм смешанного ингибирования. [4] cPEPCK претерпевает несколько конфигураций, катализируя образование PEP. Он может быть несвязанным, привязанным к GDP или привязанным к GTP. Был проведен эксперимент по изучению сродства к генистеину в этих различных конфигурациях. Было обнаружено, что гейнштейн предпочитает связывание cPEPCK со связанным GTP, чем фермент со связанным GDP, который оказался менее стабильным.[4] Это произошло потому, что связанная с GTP cPEPCK обнаружила расширенный сайт связывания для генистеина.[4] Это тот же сайт связывания, что и предполагаемый субстрат фермента, оксалоацетат, в то время как в других конфигурациях этого не происходило в присутствии генистеина. [4] Это свидетельствует о том, что механизм ингибирования cPEPCK генистеином представляет собой смесь конкурентного и неконкурентного ингибирования.
А калликреин это тип сериновая протеаза, который расщепляет пептидные связи после определенных аминокислот в белке. Эти 15 калликрейнов, KLK1 к KLK15, находятся в тканях человека. Способность этой молекулы расщеплять белки приводит к эффективной активации рецепторов клеточной поверхности, что делает их ключевыми элементами многих путей передачи биологических сигналов и их амплификации с помощью каскадов. Это семейство сериновых протеаз часто является биомаркером заболеваний и, следовательно, становится мишенью для ингибирования. [5] Ингибирование этих калликреинов приводит к возможной терапии таких заболеваний, как метастатический рак или болезнь Альцгеймера. [5] Фукугетин, или (+) -мореллофлавон, это вид растений бифлавоноид изолирован от Гарциния бразильская. [5] После выделения фукугетина его поместили с KLK1, KLK2, KLK3, KLK4, KLK5, KLK6, и KLK7 в разных концентрациях.[5] Это позволило провести анализ кинетика ферментов путем получения параметров Km и Vmax. Через модель Кинетика Михаэлиса-Ментен, то Диаграмма Иди-Хофсти был нанесен.[5] Он подтвердил, что фукугетин действует как смешанный ингибитор, проявляя различное, но имеющееся сродство к ферменту одному и комплексу фермент-субстрат. Анализируя кинетику, фукугетин уменьшал Vmax, в то время как он увеличивал Km для этих KLK.[5] Обычно в конкурентное торможение, Vmax остается неизменной при увеличении Km, а в неконкурентное торможение, Vmax уменьшается, а Km остается прежним. Изменение обеих этих переменных - еще один результат, согласующийся с эффектами смешанного ингибитора.
Рекомендации
- ^ а б c «Типы торможения». Архивировано из оригинал 8 сентября 2011 г.. Получено 2 апреля 2012.
- ^ «Подавление ферментов». Лондонский университет Южного берега. Архивировано из оригинал 19 марта 2012 г.. Получено 2 апреля 2012.
- ^ а б Стори, Кеннет Б. (2004). Функциональный метаболизм: регуляция и адаптация. Wiley-IEEE. п. 12. ISBN 978-0-471-41090-4.
- ^ а б c d е ж Катияр, Шашанк Пракаш (2015). «Смешанное ингибирование cPEPCK по Гейнштейну с использованием расширенного сайта связывания, расположенного рядом с его каталитической щелью». PLOS ONE. 10 (11): e0141987. Дои:10.1371 / journal.pone.0141987. ЧВК 4631375. PMID 26528723 - через NCBI.
- ^ а б c d е ж Сантос, Хорхе А. Н. (2016). «Натуральный флавон фукугетин как ингибитор смешанного типа калликреинов ткани человека». Письма по биоорганической и медицинской химии. 26 (5): 1485–9. Дои:10.1016 / j.bmcl.2016.01.039. PMID 26848109.
| Этот биохимия статья - это заглушка. Вы можете помочь Википедии расширяя это. |





