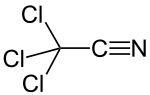
Трихлорацетонитрил - Trichloroacetonitrile
 | |
| Имена | |
|---|---|
| Название ИЮПАК Трихлорацетонитрил | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.008.078 |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C2Cl3N | |
| Молярная масса | 144.38 г · моль−1 |
| Внешность | бесцветная жидкость |
| Плотность | 1,44 г / мл |
| Температура плавления | -42 ° С |
| Точка кипения | От 83 до 84 ° C (от 181 до 183 ° F, от 356 до 357 K) |
| нерастворимый | |
| Опасности | |
| Основной опасности | GHS06, GHS09 |
| Паспорт безопасности | MSDS |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 195 ° С (383 ° F, 468 К) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Трихлорацетонитрил является органическое соединение с формулой CCl3CN. Это бесцветная жидкость, хотя коммерческие образцы часто имеют коричневатый оттенок. Он используется в коммерческих целях в качестве предшественника фунгицида. этридиазол. Готовится путем обезвоживания трихлорацетамид.[1] Как бифункциональное соединение, трихлорацетонитрил может реагировать как по трихлорметильной, так и по нитрильной группе. В эффект удаления электронов из трихлорметильная группа активирует нитрильную группу для нуклеофильных добавок. Высота реактивность делает трихлорацетонитрил универсальным реагент, но также обуславливает его склонность к гидролизу.
Синтез
Производство трихлорацетонитрила дегидратацией трихлорацетамид был впервые описан в 1873 г. Л. Бишопинком на Katholieke Universiteit Leuven.[2]

Трихлорацетонитрил можно получить хлорирование из ацетонитрил на катализаторе с активированным углем, пропитанном Zn, Cu и галогенидами щелочноземельных металлов, при 200-400 ° C с выходом 54%.[3]
Высокие температуры, необходимые для этого процесса, способствуют образованию побочных продуктов, таких как тетрахлорметан. Напротив, хлорирование ацетонитрила, насыщенного хлористый водород приводит к чистому трихлорацетонитрилу даже при 50-80 ° C с хорошими выходами.[4]
Как и другие галогенированные ацетонитрилы, трихлорацетонитрил получают из органических веществ, таких как водоросли, гуминовые кислоты и белковые вещества, при дезинфицирующем хлорировании воды из природных источников.[5][6]
Свойства

Свежеперегнанный трихлорацетонитрил представляет собой бесцветную жидкость с резким запахом, которая быстро меняет цвет от желтоватого до светло-коричневого. Чувствителен к воде, кислотам и щелочам.
В длина облигаций 146,0 вечера (C-C), 116,5 пм (C-N) и 176,3 пм (C-Cl). Угол связи составляет 110,0 ° (ClCCl).[7]
Использовать
Замена всех электроотрицательных заместителей в трихлорацетонитриле путем нуклеофильной атаки анионов алкоксида дает эфиры ортокарбоновой кислоты с высокой урожайностью.
Из-за высокой реакционной способности атомов хлора можно использовать трихлорацетонитрил (особенно в сочетании с трифенилфосфин ) для превращения аллиловых спиртов в соответствующие хлориды аллилов.[8]

С карбоновыми кислотами, ацилхлориды получены.[9]
Благодаря мягким условиям реакции Cl3CCN / PPh3 Система также подходит для активации карбоновых кислот и их связывания с аминосоединениями на носителе с амидами (пептидами) в твердофазном синтезе.[10] Из сульфокислот аналогично образуются соответствующие сульфохлориды.[11] Аналогичным образом активация дифенилфосфорной кислоты Cl3CCN / PPh3 и реакция со спиртами или аминами протекает с образованием соответствующих эфиров или амидов фосфорной кислоты в мягкой и эффективной реакции в одном реакторе.[12]
Кроме того, фенольные гидроксильные группы в азотсодержащих ароматических соединениях могут быть преобразованы в соединения хлора.[13]

В Реакция Хёша, ароматические гидроксикетоны образуются в реакции замещенных фенолов с трихлорацетонитрилом, например, из 2-метилфенол 2-трихлорацилпроизводное с выходом 70%.[14]

В электроноакцепторный эффект из трихлорметильная группа активирует нитрильную группу трихлорацетонитрила для атаки нуклеофильных соединений кислорода, азота и серы. Например, спирты при щелочном катализе дают прямое и обратимое присоединение. О-алкилтрихлорацетимидаты,[15] которые можно выделить как стабильные и менее чувствительные к гидролизу аддукты.

С первичными и вторичными аминами, N-замещенные трихлорацетамидины образуются в ходе гладкой реакции с хорошими выходами, которые могут быть очищены вакуумной перегонкой и получаются в виде бесцветных жидкостей с неприятным запахом.[16] Реакция с аммиаком, а затем с безводным хлористым водородом дает твердый гидрохлорид трихлорацетамидина, исходное соединение для фунгицид этридиазол.
В академических исследованиях трихлорацетонитрил используется как реагент в Перестройка сверхчеловека, преобразование аллильный спирты в аллильный амины.[17][18][19] Реакция основана на [3,3] -сигматропной и диастереоселективной перегруппировке.
Бензилтрихлорацетимидат легко доступен из бензилового спирта и трихлорацетонитрила.[20] Бензилтрихлорацетимидат полезен в качестве реагента для бензилирования чувствительных спиртов в мягких условиях и для сохранения хиральности.[21]
О-Гликозил-трихлорацетимидаты для активации углеводов
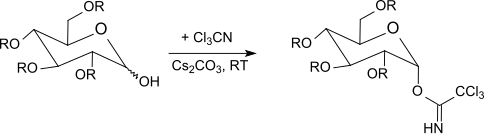
Р. Р. Шмидт и его сотрудники[22] описали выборочные аномерный активация О-защищенные гексопиранозы (глюкоза, галактоза, манноза, глюкозамин, галактозамин ), гексофуранозы и пентопиранозы с трихлорацетонитрилом в присутствии основания, а также гликозилирование при кислотном катализе.[23][24][25]
Под кинетическим контролем[26] с карбонатом калия в качестве основания, β-трихлорацетимидаты образуются селективно, тогда как с гидридом натрия, карбонатом цезия или гидроксидом калия[27] и в присутствии катализаторов межфазного переноса[28] получают только α-трихлорацетимидаты (термодинамически контролируемые).
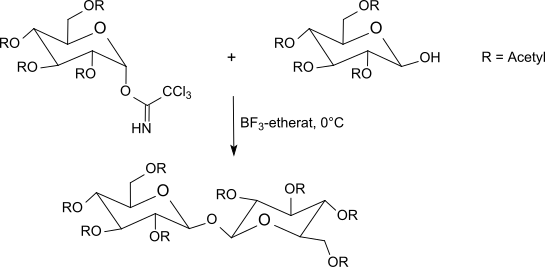
Трихлорацетимидаты реагируют от -40 ° C до комнатной температуры с эфират трифторида бора в дихлорметан с участием О-защищенные сахара. Этот метод обычно дает лучшие результаты, чем метод Кенигса-Кнорра с использованием солей серебра или метод Гельфериха, который использует проблемные соли ртути. Поскольку инверсия происходит в аномерном центре, реакция приводит к β-O-гликозидам (при использовании α-трихлорацетимидатов). Метод трихлорацетимидата часто дает стерически однородные гликозиды в мягких условиях реакции с очень хорошими выходами.
Тиоуксусная кислота реагирует с ацетил-защищенным α-галактозилтрихлорацетимидатом даже без дополнительного кислотного катализа до тиогликозида, из которого (после отщепления защитных групп) легко доступна 1-тио-β-D-галактоза, что полезно для отделения рацематы из аминокислоты.[29]

Трихлорацетонитрил был важным фумигант в первой половине 20 века, но сегодня он стал устаревший для этого приложения.[30]
Смотрите также
использованная литература
- ^ Питер Поллак, Жерар Ромедер, Фердинанд Хагедорн, Хайнц-Петер Гельбке «Нитрилы» в Энциклопедия промышленной химии Ульмана, 2002, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a17_363
- ^ Бишопинк, Л. (1873). "Ueber die gechlorten Acetonitrile". Berichte der Deutschen Chemischen Gesellschaft. 6: 731–734. Дои:10.1002 / cber.187300601227.
- ^ США 2375545, Р. Т. Фостер, "Процесс получения трихлорацетонитрила", выпущенный 1945-05-08, передан Imperial Chemical Industries
- ^ США 2745868, Г. Кебиш, "Процесс производства трихлорацетонитрила", выпущенный 1956-05-15, назначенный Deutsche Gold- und Silber-Scheideanstalt, vormals Roessler
- ^ Рекомендации по качеству питьевой воды, 3. Auflage, Vol. 1, Рекомендации, Всемирная организация здравоохранения, Genf, 2004 г., ISBN 9-2415-4638-7, PDF.
- ^ Фрэнк Бернсдорф (2007), Untersuchungen zur abiotischen Bildung von Acetonitril, Haloacetonitrilen und Trichlornitromethan (на немецком языке), GRIN, p. 5, ISBN 9783638383431}}
- ^ Дэвид Р. Лиде (Hrsg.): CRC Справочник по химии и физике. 90. Auflage. (Интернет-версия: 2010 г.), CRC Press / Taylor and Francis, Boca Raton, FL, Структура свободных молекул в газовой фазе. С. 9-46.
- ^ Матвеева Е.Д. и др., Региоселективное и стереоселективное замещение гидроксильной группы галогена в аллиловых спиртах, Ж. Орг. Хим., 31, (8), 1121–1125 (1995).
- ^ Д. О. Джанг и др., Мягкий и эффективный способ получения хлорангидридов из карбоновых кислот., Tetrahedron Lett., 40, (29), 5323–5326 (1999).
- ^ Дж. Ваго, Дж. Грейнер, Полезный метод ацилирования с использованием трихлорацетонитрила и трифенилфосфина для твердофазного органического синтеза, Tetrahedron Lett., 43, (34), 6039–6041 (2002).
- ^ О. Чантарасривонг и др., Практичный и эффективный метод получения сульфаниламидов с использованием Cl3CCN / PPh3, Tetrahedron Lett., 47, (42), 7489–7492 (2006).
- ^ A. Kasemsuknimit et al., Эффективное амидирование и этерификация фосфорной кислоты с использованием Cl3CCN / Ph3п, Бык. Korean Chem. Soc., 32, (9), 3486–3488 (2011).
- ^ W. Kijrungphaiboon et al., Cl3CCN / PPh3 и CBr4/ PPh3: две эффективные системы реагентов для получения N-гетероароматических галогенидов., Tetrahedron Lett., 53, 674–677 (2006).
- ^ Р. Мартин (2011), Ароматические гидроксикетоны: получение и физические свойства. Vol. 1 Гидроксибензофеноны (на немецком языке) (3-е изд.), Springer, Дои:10.1007/978-1-4020-9787-4, ISBN 978-1-4020-9787-4
- ^ J. U. Nef, Ann. Chem., 287, 274 (1895).
- ^ Гривас, Джон С .; Таурины, Альфред (1958-05-01). «Реакция трихлорацетонитрила с первичными и вторичными аминами: часть I. Получение некоторых трихлорацетамидинов». Канадский химический журнал. 36 (5): 771–774. Дои:10.1139 / v58-113. ISSN 0008-4042.
- ^ Т. Нисикава; М. Асаи; Н. Охьябу; М. Исобе (1998). «Улучшенные условия для легкой перестановки сверхчеловека (1)». J. Org. Chem. 63 (1): 188–192. Дои:10.1021 / jo9713924. PMID 11674062.
- ^ "Перестановка сверхчеловека". Портал органической химии. organic-chemistry.org. Получено 15 ноября, 2012.
- ^ Ю. К. Чен. А. Э. Лурайн, П. Дж. Уолш (2002). «Общий высокоэнантиоселективный метод синтеза D- и L-альфа-аминокислот и аллильных аминов». Варенье. Chem. Soc. 124 (41): 12225–12231. Дои:10.1021 / ja027271p. PMID 12371863.
- ^ Schaefer, Fred C .; Питерс, Грейс А. (1961). «Катализируемая основанием реакция нитрилов со спиртами. Удобный путь к имидатам и солям амидина». Журнал органической химии. 26 (2): 412–418. Дои:10.1021 / jo01061a034.
- ^ E. P. Eckenberg et al., Полезное применение бензилтрихлорацетимидата для бензилирования спиртов, Тетраэдр, 49, 1619–1624 (1993).
- ^ Р. Р. Шмидт, Ж. Мишель, Einfache Synthese von α- и β-О-Гликозилимидатин. Herstellung von Glykosiden und Disacchariden, Энгью. Chem., 92, 763–764 (1980).
- ^ Р. Р. Шмидт, Neue Methoden zur Glycosid- und Oligosaccharidsynthese - gibt es Alternativen zur Koenigs-Knorr-Methode?, Энгью. Chem. 98, 213–236 (1986)
- ^ Р. Р. Шмидт, В. Кинзи, Активация аномерного кислорода для синтеза гликозидов - метод трихлорацетимидата, Adv. Carbohydr. Chem. Биохим., 50, 21–123 (1994).
- ^ Р. Р. Шмидт, К.-Х. Юнг, Осинтез лигосахаридов с трихлорацетимидатами, В: Препаративная химия углеводов, С. Ханессиан, ред., Марсель Деккер, Нью-Йорк, 283–312 (1997), ISBN 0-8247-9802-3.
- ^ Р. Р. Шмидт, Ж. Мишель, Liebigs Ann. Chem., 1343–1357 (1984).
- ^ Ф. Дж. Урбан и др., Tetrahedron Lett., 31, 4421–4424 (1990)
- ^ В. Дж. Патил, Tetrahedron Lett., 37, 1481–1484 (1996).
- ^ А. Егоров и др., 1-Тио-β-D-галактоза как хиральный дериватизирующий агент для разделения D,Lэнантиомеры аминокислот, J. Chromatogr. А, 673(2), 286–290 (1994).
- ^ Н. М. Сакс, Р. Дж. Льюис, Краткий химический словарь Хоули, 11-е изд., Van Nostrand Reinhold, New York, S. 261, 1175 (1987).

