Количественная оценка вирусов - Virus quantification
Количественная оценка вирусов предполагает подсчет количества вирусы в определенном объеме для определения концентрации вируса. Он используется как в исследованиях и разработках (НИОКР), так и в коммерческих и академических лабораториях, а также в производственных ситуациях, когда количество вируса на различных этапах является важной переменной. Например, производство вирусных вакцина, рекомбинантные белки с использованием вирусных векторов и вирусных антигены Все они требуют количественной оценки вирусов для постоянной адаптации и мониторинга процесса с целью оптимизации производительности и реагирования на постоянно меняющиеся потребности и приложения. Примеры конкретных случаев, когда необходимо количественно оценить известные вирусы, включают скрининг клонов, множественность заражения (MOI) оптимизация и адаптация методов к культуре клеток. На этой странице обсуждаются различные методы, используемые в настоящее время для количественного определения вирусов в жидких образцах. Эти методы делятся на две категории: традиционные и современные. Традиционные методы - это стандартные в отрасли методы, которые использовались десятилетиями, но, как правило, медленные и трудоемкие. Современные методы представляют собой относительно новые коммерчески доступные продукты и наборы, которые значительно сокращают время количественной оценки. Это не исчерпывающий обзор всех потенциальных методов, а скорее репрезентативное сечение традиционных методов и новых, коммерчески доступных методов. Хотя могут существовать и другие опубликованные методы количественной оценки вирусов, некоммерческие методы здесь не обсуждаются.
Традиционные методы
Анализ зубного налета
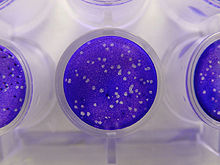
Анализы на основе бляшек - это стандартный метод, используемый для определения концентрации вируса с точки зрения инфекционная доза. Вирусный налет анализы определяют количество блоки формирования зубного налета (БОЕ) в образце вируса, который является одним из показателей количества вируса. Этот анализ основан на микробиологическом методе, проведенном в чашки Петри или многолуночные планшеты. В частности, сливной монослой хозяин клетки инфицированы вирусом в различных разведениях и покрыты полутвердой средой, такой как агар или же карбоксиметилцеллюлоза, чтобы предотвратить беспорядочное распространение вирусной инфекции. Вирусная бляшка образуется, когда вирус заражает клетку внутри фиксированного монослоя клеток.[1] Клетка, инфицированная вирусом, будет лизировать и распространять инфекцию на соседние клетки, где цикл от инфицирования до лизиса повторяется. Зона инфицированных клеток образует бляшку (область инфекции, окруженная неинфицированными клетками), которую можно увидеть в оптический микроскоп или визуально (слить верхнюю среду и добавить кристально-фиолетовый раствор в течение 15 минут, пока он не окрасит цитоплазму, аккуратно удалив излишки водой, покажет неокрашенные места мертвых клеток[2]). Образование налета может занять от 3 до 14 дней, в зависимости от анализируемого вируса. Бляшки обычно подсчитываются вручную, и результаты в сочетании с коэффициентом разбавления, используемым для приготовления планшета, используются для расчета количества бляшкообразующих единиц на единицу объема образца (БОЕ / мл). Результат БОЕ / мл представляет собой количество инфекционных частиц в образце и основан на предположении, что каждая образовавшаяся бляшка представляет одну инфекционную вирусную частицу.[3][4]
Анализ формирования фокуса (FFA)
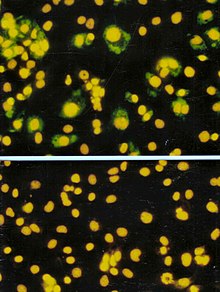
Анализ формирования фокуса (FFA) представляет собой разновидность анализа бляшек, но вместо того, чтобы полагаться на лизис клеток для обнаружения образования бляшек, FFA использует иммуноокрашивание методы с использованием флуоресцентно меченых антитела специфический для вирусного антиген для обнаружения инфицированных клеток-хозяев и инфекционных вирусных частиц до образования фактического налета. FFA особенно полезен для количественного определения классов вирусов, которые не лизируют клеточные мембраны, поскольку эти вирусы не поддаются анализу на бляшки. Как и в случае анализа с бляшками, монослои клеток-хозяев инфицированы различными разведениями образца вируса и инкубируются в течение относительно короткого периода инкубации (например, 24–72 часа) в полутвердой наложенной среде, которая ограничивает распространение инфекционного вируса, создавая локализованные скопления (очаги) инфицированных клеток. Затем планшеты зондируют флуоресцентно меченными антителами против вирусного антигена, и для подсчета и количественного определения количества очагов используют флуоресцентную микроскопию. Метод FFA обычно дает результаты за меньшее время, чем доза зубного налета или 50-процентная инфекционная доза культуры ткани (TCID50), но он может быть более дорогим с точки зрения требуемых реагентов и оборудования. Время завершения анализа также зависит от размера области, которую считает пользователь. Для большей площади потребуется больше времени, но она может обеспечить более точное представление образца. Результаты FFA выражаются в единицах формирования фокуса на миллилитр или FFU / мл.[5]
Анализ конечного разведения
Пятидесятипроцентная инфекционная доза культуры ткани (TCID50) является мерой инфекционного вируса титр. Этот анализ разведения конечной точки позволяет количественно оценить количество вируса, необходимое для уничтожения 50% инфицированных хозяев или для получения вируса. цитопатический эффект в 50% инокулированных клеток тканевой культуры. Этот анализ может быть более распространен в клинических исследованиях, где необходимо определить летальную дозу вируса или если вирус не образует бляшек. При использовании в контексте культуры ткани клетки-хозяева высевают на чашки и добавляют серийные разведения вируса. После инкубации вручную наблюдают и записывают процент гибели клеток (т.е. инфицированных клеток) для каждого разведения вируса, а результаты используются для математического расчета TCID.50 результат.[5][6] Из-за явных различий в методах и принципах анализа TCID50 и БОЕ / мл или результаты других анализов на инфекционность не эквивалентны. Этот метод может занять до недели из-за времени инфицирования клеток.[7]
Два метода, обычно используемых для расчета TCID50 (также может использоваться для расчета других типов конечной точки 50%, например EC50, IC50, и LD50 ) находятся:
- Спирмен-Карбер[8]
- Метод Рида-Мюнча
В теоретический связь между TCID50 и PFU составляет приблизительно 0,69 PFU = 1 TCID.50 на основе распределение Пуассона,[9] а распределение вероятностей который описывает, сколько случайных событий (вирусных частиц), происходящих с известной средней скоростью (титр вируса), вероятно, произойдет в фиксированном пространстве (количество вирусной среды в лунке). Однако следует подчеркнуть, что на практике эта взаимосвязь может не соблюдаться даже для одной и той же комбинации вирус + клетка, поскольку два типа анализа настроены по-разному, и инфекционность вируса очень чувствительна к различным факторам, таким как возраст клеток, наложенные среды, и т. д. Но следующая ссылка определяет взаимосвязь по-разному: предполагая, что используется одна и та же клеточная система, что вирус образует бляшки на этих клетках и что не добавляются никакие процедуры, которые ингибировали бы образование бляшек, ожидается, что 1 мл исходного вируса имеют примерно половину количества бляшкообразующих единиц (PFU) как TCID50. Это только оценка, но основывается на том, что предельное разведение, которое могло бы инфицировать 50% зараженных слоев клеток, часто может первоначально привести к образованию единственной бляшки в инфицированных слоях клеток. В некоторых случаях случайно могут образоваться две или более бляшек, и поэтому фактическое количество PFU следует определять экспериментально.
Математически ожидаемые PFU будут несколько больше половины TCID.50, так как отрицательные трубки в TCID50 представляют собой блоки, образующие нулевой зубной налет, а каждая положительная трубка представляет собой один или несколько узлов формирования зубного налета. Более точная оценка получается применением распределения Пуассона. Где P (o) - это доля отрицательных пробирок, а m - среднее количество инфекционных единиц в объеме (БОЕ / мл), P (o) = e (-m). Для любого титра, выраженного как TCID50, P (o) = 0,5. Таким образом, e (-m) = 0,5 и m = -ln 0,5, что составляет ~ 0,7.
Следовательно, можно было умножить TCID50 титр (на мл) на 0,7, чтобы предсказать среднее количество БОЕ / мл. При фактическом применении таких вычислений помните, что вычисленное среднее значение будет действительным только в том случае, если изменения в протоколе, необходимые для визуализации бляшек, не изменяют экспрессию инфекционного вируса по сравнению с экспрессией в условиях, используемых для TCID.50.
Таким образом, в качестве рабочей оценки можно принять материал с TCID.50 из 1 × 105 TCID50/ мл даст 0,7 × 105 БОЕ / мл.
(из: ATCC - преобразование TCID50 в устройства формирования налета PFU-124 )
Протеиновые анализы
Существует несколько вариантов количественного анализа вирусов на основе белков. Как правило, эти методы определяют количество либо всего белка, либо количество конкретного вирусного белка в образце, а не количество инфицированных клеток или вирусных частиц. Количественная оценка чаще всего основана на флуоресценция обнаружение. Некоторые варианты анализа позволяют количественно определять белок непосредственно в образце, в то время как другие варианты требуют инфицирования клетки-хозяина и инкубации, чтобы обеспечить рост вируса до количественного определения белка. Используемый вариант зависит в первую очередь от количества белка (т. Е. Вируса) в исходном образце и чувствительности самого анализа. Если требуется инкубация и рост вируса, перед анализом часто проводят лизис / расщепление клеток и / или вирусов. Большинство методов на основе белков относительно быстры и чувствительны, но требуют стандартов качества для точной калибровки и количественного определения белка, а не фактических концентраций вирусных частиц. Ниже приведены конкретные примеры широко используемых анализов на основе белков.
Анализ гемагглютинации
Анализ гемагглютинации (НА) - это обычный нефлуоресцентный количественный анализ белков, специфичный для грипп. Он основан на том, что гемагглютинин, поверхностный белок вирусов гриппа, агглютинирует красные кровяные тельца (то есть заставляет красные кровяные тельца слипаться). В этом анализе разведения пробы гриппа инкубируются с 1% эритроцит раствор в течение одного часа и визуально определяют разведение вируса, при котором происходит первая агглютинация. Анализ дает результат в единицах гемагглютинации (HAU) с типичным соотношением БОЕ к HAU в 106 классифицировать.[10][11][12] Этот анализ занимает ~ 1-2 часа, а результаты могут сильно отличаться в зависимости от технических знаний оператора.
Анализ ингибирования гемагглютинации - это обычная разновидность анализа HA, используемого для измерения уровней грипп-специфических антител в сыворотке крови. В этом варианте сывороточные антитела к вирусу гриппа будут препятствовать прикреплению вируса к эритроцитам. Следовательно, гемагглютинация подавляется, когда антитела присутствуют в достаточной концентрации.[13]
Анализ бицинхониновой кислоты
В бицинхониновая кислота анализ (BCA) основан на простом колориметрический измерения и является наиболее распространенным методом количественного определения белка. BCA похож на Лоури или же Брэдфорд протеиновые анализы и впервые были коммерчески доступны компанией Pierce, которая в настоящее время принадлежит Thermo Fisher Scientific. В анализе BCA пептидные связи белка количественно снижают Cu2+ к Cu1+, что дает светло-голубой цвет. BCA хелаты Cu1+ при соотношении 2: 1, что приводит к более интенсивному окрашиванию частиц, поглощающих при 562 нм. Абсорбция образца при 562 нм используется для определения основной концентрации белка в образце. Результаты анализа сравнивают с известными стандартными кривыми после анализа с помощью спектрофотометр или планшетный ридер.[14] Общее время анализа составляет от 30 минут до одного часа. Хотя этот анализ является повсеместным и быстрым, ему не хватает специфичности, поскольку он учитывает весь белок, препарат вируса, подлежащий количественной оценке, должен содержать очень низкие уровни белков клетки-хозяина.
Одинарный радиальный иммунодиффузионный анализ
Одинокий радиальная иммунодиффузия анализ (SRID), также известный как метод Манчини, представляет собой анализ белка, который определяет количество специфического вирусного антигена путем иммунодиффузии в полутвердой среде (например, агаре). Среда содержит антисыворотка специфичен для интересующего антигена, и этот антиген помещается в центр диска. По мере того, как антиген диффундирует в среду, он создает кольцо осадка, которое растет до тех пор, пока не будет достигнуто равновесие. Время анализа может составлять от 10 часов до дней в зависимости от времени уравновешивания антигена и антитела. Диаметр зоны от кольца линейно связан с логарифмом концентрации белка и сравнивается с диаметрами зоны для известных стандартов белка для количественного определения.[15] Для этого анализа коммерчески доступны наборы и сыворотки (например, The Binding Site Inc.).
Просвечивающая электронная микроскопия (ПЭМ)


ТЕМ представляет собой специализированный тип микроскопии, в котором для изображения образца используется пучок электронов, сфокусированный магнитным полем. ПЭМ обеспечивает визуализацию с пространственным разрешением в 1000 раз больше, чем световой микроскоп (разрешение до 0,2 нм).[16] Ультратонкий, отрицательно окрашенный требуется образец. Приготовление образцов включает нанесение образцов на сетку ПЭМ с покрытием и отрицательное окрашивание электронно-непрозрачной жидкостью.[17] Образцы залитых тканей также можно исследовать, если они сделаны тонкими срезами. Подготовка образцов зависит от протокола и пользователя, но обычно требует часов. ПЭМ-изображения могут отображать отдельные вирусные частицы и количественные анализ изображений может использоваться для определения концентрации вируса. Эти изображения с высоким разрешением также предоставляют информацию о морфологии частиц, недоступную большинству других методов. Количественные результаты ПЭМ часто бывают лучше, чем результаты других анализов, поскольку все частицы, независимо от инфекционности, количественно определяются в сообщенном результате вирусоподобных частиц на мл (vlp / мл). Количественный ПЭМ обычно хорошо работает при концентрациях вируса более 106 частиц / мл. Из-за высокой стоимости инструментов и необходимого количества места и вспомогательного оборудования оборудование ТЕА доступно в ограниченном количестве объектов.
Современные методы
Настраиваемый резистивный импульсный датчик (TRPS)
Настраиваемое резистивное импульсное зондирование (TRPS) - это метод, который позволяет проводить высокопроизводительные измерения отдельных частиц отдельных вирусных частиц, поскольку они проходят через настраиваемый размер нанопора, один за раз.[18] Преимущество метода заключается в одновременном определении размера и концентрации вирусных частиц в растворе с высоким разрешением. Это можно использовать для оценки стабильности образца и вклада агрегатов, а также общей концентрации вирусных частиц (vp / мл).[19]
Измерение на основе TRPS происходит в ионном буфере, и предварительное окрашивание образцов перед анализом не требуется, поэтому этот метод более быстрый, чем методы, требующие предварительной обработки флуоресцентными красителями, с общим временем подготовки и измерения менее 10 минут на образец. Анализ вирусов на основе TRPS коммерчески доступен через системы qViro-X, которые могут подвергаться химической дезинфекции путем автоклавирования после измерения.
Проточной цитометрии
Хотя большинство проточных цитометров не обладают достаточной чувствительностью, существует несколько коммерчески доступных проточных цитометров, которые можно использовать для количественного определения вирусов. Счетчик вирусов количественно определяет количество интактных вирусных частиц в образце, используя флуоресценцию для обнаружения колокализованных белков и нуклеиновых кислот. Образцы окрашивают двумя красителями, один для белков, а другой для нуклеиновых кислот, и анализируют, когда они проходят через лазерный луч. Количество частиц, вызывающих одновременные события на каждом из двух отдельных каналов флуоресценции, определяется вместе с измеренной скоростью потока пробы для расчета концентрации вирусных частиц (объемных частиц / мл).[20] Результаты обычно аналогичны по абсолютной величине результату ПЭМ. Анализ имеет линейный рабочий диапазон 105–109 vp / мл и время анализа ~ 10 мин с коротким временем пробоподготовки.
Количественная полимеразная цепная реакция (КПЦР)

Количественная ПЦР использует полимеразной цепной реакции химия для усиления вирусного ДНК или же РНК для получения достаточно высоких концентраций для обнаружения и количественного определения по флуоресценции. Как правило, количественная оценка с помощью qPCR основана на серийных разведениях стандартов известной концентрации, анализируемых параллельно с неизвестными образцами для калибровки и сравнения. Количественное обнаружение может быть достигнуто с использованием широкого спектра стратегий обнаружения флуоресценции, включая зонды, специфичные для последовательности, или неспецифические флуоресцентные красители, такие как SYBR Зеленый.[21] Зонды, специфичные для последовательности, такие как TaqMan (разработан Applied Biosystems), Molecular Beacons или Scorpion связываются только с ДНК соответствующей последовательности, образующейся в ходе реакции. Краситель SYBR Green связывается со всей двухцепочечной ДНК[22] производится во время реакции. Хотя SYBR Green прост в использовании, его недостаточная специфичность и низкая чувствительность побуждают большинство лабораторий использовать схемы обнаружения количественной ПЦР на основе зондов. Существует множество вариантов qPCR, включая метод сравнительного порога, который позволяет относительную количественную оценку путем сравнения значений Ct (циклы PCR, которые показывают статистически значимое увеличение продукта) из нескольких образцов, которые включают внутренний стандарт.[23] ПЦР усиливает всю мишень нуклеиновая кислота, в том числе происходящие из интактных инфекционных вирусных частиц, из дефектных вирусных частиц, а также из свободной нуклеиновой кислоты в растворе. Из-за этого результаты кПЦР (выраженные в количестве копий генома / мл), вероятно, будут выше по количеству, чем результаты ПЭМ. Для количественной оценки вирусов отношение целых вирионов к количеству копий нуклеиновой кислоты редко бывает один к одному. Это связано с тем, что во время репликации вируса нуклеиновая кислота и вирусные белки не всегда продуцируются в соотношении 1: 1, а процесс сборки вируса приводит к образованию полных вирионов, а также пустых капсидов и / или избыточных свободных вирусных геномов. В примере с вирусом ящура отношение целых вирионов к количеству копий РНК в активно реплицирующейся клетке-хозяине составляет приблизительно 1: 1000.[24] Продукты для титрования вирусов на основе количественной ПЦР коммерчески доступны через множество компаний (например, Invitrogen, Roche или Qiagen). Преимущества титрования с помощью кПЦР включают быстрое время обработки (1–4 часа) и чувствительность (позволяет обнаруживать гораздо более низкую концентрацию вирусов, чем другие методы).
Иммуноферментный анализ (ELISA)
ELISA представляет собой более современный вариант анализа белка, в котором используются специфические антитела, связанные с ферментом, для обнаружения неизвестного количества антигена (т. е. вируса) в образце. Событие связывания антитело-антиген детектируется и / или количественно определяется по способности фермента преобразовывать реагент в детектируемый сигнал, который можно использовать для вычисления концентрации антигена в образце.[25] Пероксидаза хрена (HRP) - распространенный фермент, используемый в схемах ELISA из-за его способности усиливать сигнал и повышать чувствительность анализа. Существует множество разновидностей или типов анализов ELISA, но их обычно можно классифицировать как косвенный, конкурентный, бутерброд или же обеспечить регресс.[26] Наборы для ELISA коммерчески доступны от множества компаний, и количественная оценка обычно осуществляется через хромогенный репортеры или флуоресценция (например, Invitrogen, Santa Cruz Biotechnology Inc.). Этот метод намного менее трудоемок, чем традиционные методы, и может занять от 4 до 24 часов в зависимости от времени инкубации антител.
Рекомендации
- ^ Kaufmann, S.H .; Кабелиц, Д. (2002). Методы в микробиологии Том 32: Иммунология инфекции. Академическая пресса. ISBN 0-12-521532-0.
- ^ Баер, Алан; Кен-Холл, Килен (4 ноября 2014 г.). «Определение концентрации вирусов с помощью анализов налета: с использованием традиционных и новых систем наложения». Журнал визуализированных экспериментов (93): e52065. Дои:10.3791/52065. ЧВК 4255882. PMID 25407402.
- ^ Мартин, С.Дж. (1978). Биохимия вирусов. Издательство Кембриджского университета. ISBN 0-12-402033-X.
- ^ Якимович Артур; Андриасян, Вардан; Витте, Роберт; Ван, И.-Сюань; Прасад, вибху; Суомалайнен, Маарит; Гребер, Урс Ф. (28 сентября 2015 г.). «Plaque2.0 - высокопроизводительная аналитическая платформа для оценки передачи вирусных клеток и клонального роста клеток». PLOS ONE. 10 (9): e0138760. Bibcode:2015PLoSO..1038760Y. Дои:10.1371 / journal.pone.0138760. ISSN 1932-6203. ЧВК 4587671. PMID 26413745.
- ^ а б Flint, S.J .; Enquist, W .; Racaniello, V.R .; Скалка, А. (2009). «Вирусологические методы». Принципы вирусологии. ASM Press. ISBN 978-1-55581-443-4.
- ^ Линденбах, Бретт Д. "Калькулятор Рида и Мюнха".
- ^ «Архивная копия» (PDF). Архивировано из оригинал (PDF) на 2011-09-27. Получено 2010-02-26.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Кербер, Г. (1931). "Beitrag zur kollektiven Behandlung Pharmakologischer Reihenversuche". Архив ф. Экспериментируйте. Патол. У. Фармакол. Springer-Verlag. 162 (4): 480–483. Дои:10.1007 / BF01863914. S2CID 46017573.
- ^ thneedle (16 апреля 2002 г.). «TCID50 и блок формирования зубного налета (PFU)». Получено 29 мая 2014.
- ^ Киллиан, М. (2008). «Анализ гемагглютинации вируса птичьего гриппа». В Spackman, Эрика (ред.). Вирус птичьего гриппа. 436. Humana Press. С. 47–52. Дои:10.1007/978-1-59745-279-3_7. ISBN 978-1-58829-939-0. PMID 18370040.
- ^ Rimmelzwaan, G.F .; Baars, M .; Claas, E.C.J .; Остерхаус, A.D.M.E. (1998). «Сравнение гибридизации РНК, анализа гемагглютинации, титрования инфекционного вируса и иммунофлуоресценции как методов мониторинга репликации вируса гриппа» In vitro". Журнал вирусологических методов. 74 (1): 57–66. Дои:10.1016 / S0166-0934 (98) 00071-8. PMID 9763129.
- ^ Като, А .; Киётани, К .; Sakai, Y .; Yoshida, T .; Нагаи, Ю. (1997). «Парамиксовирус, вирус Сендай, V-белок кодирует роскошную функцию, необходимую для вирусного патогенеза». Журнал EMBO. 16 (3): 578–587. Дои:10.1093 / emboj / 16.3.578. ЧВК 1169661. PMID 9034340.
- ^ «Анализ ингибирования гемагглютинации гриппа».
- ^ "Биология протеина Пирса".
- ^ Родда, С.Дж .; Gallichio, H.A .; Хэмпсон, A.W (1981). «Анализ однократной радиальной иммунодиффузии выявляет небольшие антигенные различия между гемагглютининами вируса гриппа». Журнал клинической микробиологии. 14 (5): 479–482. Дои:10.1128 / JCM.14.5.479-482.1981. ЧВК 273972. PMID 6171580.
- ^ Шерман, И. «Разрешение электронного микроскопа». Книга фактов по физике. Получено 25 февраля, 2010.
- ^ Стеффенс, W.L. (1998). «Использование просвечивающей электронной микроскопии для вирусной диагностики у птиц пситтацинов». Материалы международных виртуальных конференций по ветеринарной медицине: болезни птиц-пситтацинов. Афины, Грузия.
- ^ Стивен Дж. Сауерби, Мюррей Ф. Брум, Джордж Б. Петерсен. «Динамически изменяемые апертуры нанометрового масштаба для молекулярного зондирования» Датчики и приводы B: Chemical Volume 123, Issue 1 (2007), страницы 325-330
- ^ G. Seth Roberts, Sam Yu, Qinglu Zeng, Leslie C.L. Чан, Уилл Андерсон, Аарон Х. Колби, Марк У. Гринстафф, Стивен Рид, Роберт Фогель. «Настраиваемые поры для измерения концентраций синтетических и биологических дисперсий наночастиц» Биосенсоры и биоэлектроника, 31 стр. 17-25, (2012).
- ^ Stoffel, C.L .; Finch, R .; Christensen, K .; Эдвардс, Д .; Роулен, К. (2005). «Быстрое определение титра бакуловирусов с помощью двухканального счетчика вирусов». Американская биотехнологическая лаборатория. 37 (22): 24–25.
- ^ «Протоколы ПЦР / ПЦР в реальном времени».
- ^ «Прикладные биосистемы - США» (PDF).
- ^ О'Лири, Дж. Дж .; Sheils, O .; Martin, C .; Кроули, А. (2003). «Технология Taqman и полимеразная цепная реакция в реальном времени». В Crocker, J .; Мюррей, П. (ред.). Молекулярная биология в клеточной патологии. Джон Уайли и сыновья. С. 251–268. ISBN 978-0-470-84475-5.
- ^ Каллахан Дж. Д. и др., Использование портативного анализа полимеразной цепной реакции обратной транскриптазы в режиме реального времени для быстрого обнаружения вируса ящура. J Am Vet Med Assoc. 2002, 1 июня; 220 (11): 1636-42.
- ^ Kemeny, D.M .; Challacombe, S.J. (1988). ELISA и другие твердофазные иммуноанализы: теоретические и практические аспекты. Джон Уайли и сыновья. ISBN 0-471-90982-3.
- ^ Kuby, J .; Kindt, T.J .; Goldsby, R.A .; Осборн, Б.А. (2007). Кубы Иммунология 6-е издание. W.H. Freeman и компания. ISBN 978-1-4292-0211-4.
