Апамин - Apamin
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.041.969 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C79ЧАС131N31О24S4 | |
| Молярная масса | 2027,33874 г / моль |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
| Препропротеин апамина | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | Апамин | ||||||
| Количество CAS | |||||||
| Ген NCBI | 406135 | ||||||
| UniProt | P01500 | ||||||
| |||||||
Апамин представляет собой глобулярную группу из 18 аминокислот пептид нейротоксин нашел в апитоксин (пчела яд ).[2] Сухой пчелиный яд на 2–3% состоит из апамина.[3] Апамин избирательно блокирует SK каналы, тип Ca2+-активированный K+ канал выраженный в Центральная нервная система. Токсичность вызывают всего несколько аминокислот, это цистеин.1, лизин4, аргинин13, аргинин14 и гистидин18. Эти аминокислоты участвуют в связывании апамина с Ca2+-активированный K+ канал. Из-за своей специфичности для SK-каналов апамин используется в качестве лекарственного средства в биомедицинских исследованиях для изучения электрических свойств SK-каналов и их роли в постгиперполяризации происходит сразу после потенциал действия.[4]
Источник
Первые симптомы апитоксина (пчелиного яда), которые, как сейчас полагают, вызываются апамином, были описаны еще в 1936 году Ганом и Ледичке. Апамин был впервые выделен Хаберманом в 1965 г. Apis mellifera, то Западная медоносная пчела. Апамин был назван в честь этой пчелы. Пчела яд содержит много других соединений, таких как гистамин, фосфолипаза А2, гиалуронидаза, Пептид MCD, а основной активный компонент мелиттин. Апамин отделяли от других соединений с помощью гель-фильтрации и ионообменной хроматографии.[2]
Структура и активный сайт
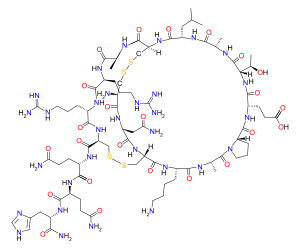
Апамин - это полипептид обладающий аминокислота последовательность H-Cys-Asn-Cys-Lys-Ala-Pro-Glu-Thr-Ala-Leu-Cys-Ala-Arg-Arg-Cys-Gln-Gln-His-NH2 (с дисульфидные связи между Cys1-Cys11 и Cys3-Cys15). Апамин очень жесткий из-за двух дисульфидных мостиков и семи водородных связей. Трехмерная структура апамина была изучена с помощью нескольких спектроскопических методов: HNMR, Круговой дихроизм, Рамановская спектроскопия, FT-IR. Предполагается, что структура состоит из альфа-спирали и бета-витков, но точная структура до сих пор неизвестна.[5]
Путем местных переделок можно найти аминокислоты которые участвуют в токсичности апамина. Это было обнаружено Винсентом и соавт. что гуанидирование ε-аминогруппы лизина4 не снижает токсичность. Когда ε-аминогруппа лизина4 и α-аминогруппа цистеина1 ацетилированы или обработаны флуорескамином, токсичность снижается в 2,5 и 2,8 раза соответственно. Это лишь небольшое уменьшение, которое указывает на то, что ни ε-аминогруппа лизина4 ни α-аминогруппа цистеина1 необходим для токсичности апамина. Глутамин7 был изменен путем образования амидной связи с этиловым эфиром глицина, это привело к снижению токсичности в 2,0 раза. Глутамин7 также не имеет значения для токсичности. Когда гистидин18 изменяется при карбетоксилировании, токсичность снижается только в 2,6 раза. Но когда гистидин18, ε-аминогруппа лизина4 и α-аминогруппа цистеина1 все они карбетоксилированы, и токсичность при ацетилировании резко снижается. Это означает, что эти три аминокислоты сами по себе не являются существенными для токсичности, но три из них вместе взятые. Химическое изменение аргинина13 и аргинин14 лечением 1,2-циклогександион и расщепление трипсин снижает токсичность более чем в 10 раз. Аминокислоты, вызывающие токсичность апамина, - цистеин.1, лизин4, аргинин13, аргинин14 и гистидин18.[6]
Токсикодинамика
Апамин - самый маленький из известных полипептидов нейротоксина и единственный, который проходит через гематоэнцефалический барьер.[6] Таким образом, апамин достигает своего органа-мишени, центральной нервной системы. Здесь он препятствует малой проводимости Ca2+-активированный K+ каналы (Каналы SK) в нейронах. Эти каналы отвечают за постгиперполяризации, которые следуют за потенциалами действия, и, следовательно, регулируют частоту повторяющихся импульсов.[7]Три разных типа каналов SK имеют разные характеристики. Только SK2 и SK3 блокируются апамином, тогда как SK1 нечувствителен к апамину. Каналы SK функционируют как тетрамер субъединиц. Гетеромеры обладают промежуточной чувствительностью.[7] SK каналы активируются за счет связывания внутриклеточного Ca2+ к белку кальмодулин, который конститутивно связан с каналом.[8] Транспорт ионов калия из клетки по градиенту их концентрации приводит к тому, что мембранный потенциал становится более отрицательным. Каналы SK присутствуют в широком диапазоне возбудимых и невозбудимых клеток, включая клетки центральной нервной системы, кишечные миоциты, эндотелиальные клетки и гепатоциты.
Связывание апамина с SK-каналами опосредуется аминокислотами в области пор, а также внеклеточными аминокислотами SK-канала.[9] Вероятно, что ингибирование SK-каналов вызвано блокированием области поры, что затрудняет транспорт ионов калия. Это повысит возбудимость нейронов и снизит порог генерации потенциал действия. Другие токсины, блокирующие каналы SK: тамапин и сцилатоксин.
Токсикокинетика
Кинетика меченых производных апамина изучалась in vitro и in vivo на мышах Cheng-Raude et al. Это пролило свет на кинетику самого апамина. Ключевым органом выделения, вероятно, будет почка, поскольку там обнаружено обогащение меченых производных. Пептид апамин достаточно мал, чтобы пройти через клубочковый барьер, способствующий почечной экскреции. Центральная нервная система, напротив, содержала очень небольшое количество апамина. Это неожиданно, так как это орган-мишень для нейротоксичности, вызванной апамином. Таким образом, эта низкая концентрация оказалась достаточной, чтобы вызвать токсические эффекты.[10]
Однако эти результаты не согласуются с исследованием Винсента и соавт. После введения мышам сверхлетальной дозы радиоактивного ацетилированного апамина было обнаружено обогащение спинной мозг, который является частью органа-мишени. Некоторые другие органы, включая почки и мозг, содержали лишь небольшое количество производного апамина.[6]
Симптомы
Симптомы после укуса пчелы могут включать:
- местные эффекты: жжение или покалывание боль, припухлость, покраснение.
- тяжелые системные реакции: отек язык и горло, сложность дыхание, и шок.
- развитие оптический неврит и атрофия.
- мерцательная аритмия, инфаркт мозга, острый инфаркт миокарда, Синдром Фишера, острое воспалительное полирадикулопатия (Синдром Гийена-Барре ), коготь руки (благодаря центральному действию апамина на спинной мозг и периферическое действие в виде медианы и локтевой неврит, вызывая спазмы длительного сгибатели в предплечье ).[11]
Больных, отравленных пчелиным ядом, можно лечить противовоспалительное средство медикамент, антигистаминные препараты и устный преднизолон.[11]
Апамин является элементом пчела яд. Вы можете контактировать с апамином через пчелиный яд, поэтому известные симптомы вызваны не апамином напрямую, а ядом в целом. Апамин - единственный нейротоксин, действующий исключительно на центральную нервную систему. Симптомы отравления апамином малоизвестны, потому что людям нелегко подвергнуться воздействию одного токсина.[12]
Благодаря исследованиям нейротоксичности апамина были обнаружены некоторые симптомы. У мышей инъекция апамина вызывает судороги и длительную спастичность позвоночника. Также известно, что у кошек растормаживаются полисинаптические спинномозговые рефлексы.[12] Полисинаптический рефлекс - это рефлекторное действие, которое передает импульс от сенсорного нейрона к двигательному нейрону через интернейрон в спинном мозге.[13] Было обнаружено, что у крыс апамин вызывает тремор и атаксию, а также драматические геморрагические эффекты в легкие.[14]
Кроме того, было обнаружено, что апамин в 1000 раз более эффективен при введении в желудочковую систему, а не в периферическую нервную систему. Желудочковая система - это совокупность структур головного мозга, содержащих спинномозговую жидкость. Периферическая нервная система содержит нервы и ганглии вне головного и спинного мозга.[12] Эту разницу в эффективности легко объяснить. Апамин связывается с SK-каналами, которые незначительно различаются в разных тканях. Таким образом, связывание апамина, вероятно, сильнее в SK-каналах желудочковой системы, чем в других тканях.
Показатели токсичности
Раньше считалось, что апамин является довольно нетоксичным соединением (LD50 = 15 мг / кг для мышей) по сравнению с другими соединениями пчелиного яда.[15] Текущие значения летальных доз апамина, измеренные у мышей, приведены ниже.[16] Нет никаких известных данных, специфичных для людей.
Внутрибрюшинный (мышиный) LD50: 3,8 мг / кг
Подкожный (мышиный) LD50: 2,9 мг / кг
Внутривенный (мышиный) LD50: 4 мг / кг
Интрацеребральный (мышиный) LD50: 1800 нг / кг
Парентерально (мышь) LD50: 600 мг / кг
Терапевтическое использование
Недавние исследования показали, что каналы SK не только регулируют постгиперполяризацию, они также влияют на синаптическая пластичность. Это зависимая от активности адаптация силы синаптической передачи. Синаптическая пластичность - важный механизм, лежащий в основе процессов обучения и памяти. Ожидается, что апамин будет влиять на эти процессы, ингибируя каналы SK. Было показано, что апамин улучшает обучение и память у крыс и мышей.[7][17] Это может служить основанием для использования апамина для лечения нарушений памяти и когнитивной дисфункции. Однако из-за риска токсических эффектов терапевтическое окно очень узкое.[17]
Блокаторы SK каналов могут оказывать терапевтическое действие на болезнь Паркинсона. Дофамин, который истощается при этом заболевании, будет высвобождаться из дофаминергических нейронов среднего мозга, когда эти SK-каналы подавлены. Каналы SK также были предложены в качестве целей для лечения эпилепсия, эмоциональные расстройства и шизофрения.[17]
Рекомендации
- ^ Апамин - Резюме соединения, PubChem.
- ^ а б Хаберманн Э (1984). «Апамин». Фармакология и терапия. 25 (2): 255–70. Дои:10.1016/0163-7258(84)90046-9. PMID 6095335.
- ^ Сын DJ, Ли Дж. У., Ли Й., Сон Х. С., Ли СК, Хонг Дж. Т. (август 2007 г.) «Терапевтическое применение противоартритного, болеутоляющего и противоракового действия пчелиного яда и входящих в его состав соединений». Фармакология и терапия. 115 (2): 246–70. Дои:10.1016 / j.pharmthera.2007.04.004. PMID 17555825.
- ^ Castle NA, Haylett DG, Jenkinson DH (февраль 1989 г.). «Токсины в характеристике калиевых каналов». Тенденции в неврологии. 12 (2): 59–65. Дои:10.1016/0166-2236(89)90137-9. PMID 2469212.
- ^ Кастин А.Ю. «Апамин». Справочник по биологически активным пептидам (Изд. 2013): 417–418.
- ^ а б c Винсент Дж. П., Швейц Х., Лаздунски М. (июнь 1975 г.). «Взаимосвязи между структурой и функцией и место действия апамина, нейротоксического полипептида пчелиного яда, который действует на центральную нервную систему». Биохимия. 14 (11): 2521–5. Дои:10.1021 / bi00682a035. PMID 1138869.
- ^ а б c М. Стокер; М. Краузе; П. Педарзани (1999). "Апамин-чувствительный Ca2+-активированный K+ ток в пирамидных нейронах гиппокампа ». PNAS. 96 (8): 4662–4667. Дои:10.1073 / пнас.96.8.4662. ЧВК 16389. PMID 10200319.
- ^ Stocker M (октябрь 2004 г.). «Ca (2 +) - активированные K + каналы: молекулярные детерминанты и функция семейства SK». Обзоры природы. Неврология. 5 (10): 758–70. Дои:10.1038 / номер 1516. PMID 15378036.
- ^ Нолтинг А., Ферраро Т., Д'хоэдт Д., Стокер М. (февраль 2007 г.). «Аминокислота вне области поры влияет на чувствительность к апамину в K + каналах с небольшой проводимостью, активированных Ca2 +». Журнал биологической химии. 282 (6): 3478–86. Дои:10.1074 / jbc.M607213200. ЧВК 1849974. PMID 17142458.
- ^ Cheng-Raude D, Treloar M, Habermann E (1976). «Приготовление и фармакокинетика меченых производных апамина». Токсикон. 14 (6): 467–76. Дои:10.1016/0041-0101(76)90064-7. PMID 1014036.
- ^ а б Сараванан Р., Кинг Р., Уайт Дж. (Апрель 2004 г.). «Преходящая когтистая рука из-за укуса пчелы. Отчет о двух случаях». Журнал костной и суставной хирургии. Британский том. 86 (3): 404–5. Дои:10.1302 / 0301-620x.86b3.14311. PMID 15125129.
- ^ а б c Habermann E (ноябрь 1977 г.). «Нейротоксичность апамина и пептида MCD при центральном применении». Архив фармакологии Наунин-Шмидеберг. 300 (2): 189–91. Дои:10.1007 / bf00505050. PMID 593441.
- ^ «полисинаптический рефлекс».
- ^ Lallement G, Fosbraey P, Baille-Le-Crom V, Tattersall JE, Blanchet G, Wetherell JR, Rice P, Passingham SL, Sentenac-Roumanou H (декабрь 1995 г.). «Сравнительная токсичность блокаторов калиевых каналов, апамина и дендротоксина». Токсикология. 104 (1–3): 47–52. Дои:10.1016 / 0300-483X (95) 03120-5. PMID 8560501.
- ^ отдел армейской биодемической лаборатории Edgewood Arsenal (1972). «Бета-адренергическое и антиаритмическое действие апамина, компонента пчелиного яда». Цитировать журнал требует
| журнал =(помощь) - ^ «Апамин» (PDF). Паспорт безопасности материала.
- ^ а б c Faber ES, Sah P (октябрь 2007 г.). «Функции SK каналов в центральных нейронах». Клиническая и экспериментальная фармакология и физиология. 34 (10): 1077–83. Дои:10.1111 / j.1440-1681.2007.04725.x. PMID 17714097.
внешняя ссылка
- Апамин в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
