Ретровирус овец Jaagsiekte - Jaagsiekte sheep retrovirus
| Ретровирус овец Jaagsiekte | |
|---|---|
 | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область: | Рибовирия |
| Королевство: | Парарнавиры |
| Тип: | Artverviricota |
| Учебный класс: | Revtraviricetes |
| Заказ: | Ортервиралес |
| Семья: | Retroviridae |
| Род: | Бетаретровирус |
| Разновидность: | Ретровирус овец Jaagsiekte |
Ретровирус овец Jaagsiekte (JSRV) это бетаретровирус который является возбудителем заразного рака легких у овец, называемого легочная аденокарцинома овцы.
Естественная история
JSRV - это вирус, вызывающий заразные опухоли легких у овец. легочная аденокарцинома овцы (OPA). Болезнь также получила название «jaagsiekte», в честь африкаанс слова для "погони" (jaag) и "болезнь" (siekte), чтобы описать респираторный дистресс, наблюдаемый у животного, запыхавшегося от преследования, что указывает на затрудненное дыхание, испытываемое инфицированной овцой. Передача вируса через аэрозоль распространяется между овцами.
В экзогенный инфекционная форма JSRV имеет эндогенный аналог, который присутствует в геномах всех овец и коз.[1] Овца геном имеет около 27 копий эндогенных ретровирусов (enJSRV), которые тесно связаны с JSRV. Эндогенный JSRV играет несколько ролей в эволюции домашних овец, поскольку они способны блокировать JSRV. репликация цикл и играют решающую роль в овцах концептус развитие и плацентарный морфогенез.[2]
Хотя OPA напоминает рак легких человека, неизвестно, что рак легких человека вызывается бетаретровирусы.[3] Несмотря на то, что возможность вирусной причины бронхоальвеолярного рака устранена, понимание молекулярных механизмов, ведущих к трансформации эпителия легких под действием JSRV, может представлять интерес в контексте терапевтических подходов к лечению рака легких у человека в целом и бронхоальвеолярной аденокарциномы (BAC). особенно.[4]
Классификация
JSRV принадлежит семье Retroviridae, в подсемейство Orthoretrovirinae и род Бетаретровирус.
Патогенез
JSRV передается респираторным путем, а также может инфицировать лимфоциты и миелоидный клетки, помимо эпителия легких. Экспрессия белка оболочки JSRV активирует сигнальные каскады, которые способствуют клеточной распространение и злокачественный трансформация клеток. Вначале опухолевые клетки растут по альвеолярный стены по узору напоминают человеческий BAC, но впоследствии становятся более инвазивный и метастазировать к местным лимфатический узел. Более крупные опухоли могут быть некротический и фиброматозный в их центре. По мере роста опухоли производство жидкости в легких увеличивается, что может способствовать распространению вируса на других овец. Только когда опухоль достигает размера, достаточного для нарушения функции легких, появляются клинические признаки. Важно отметить, что большинство инфицированных животных в эндемичных районах никогда не проявляют внешних признаков инфекции, но они могут выделять вирус, тем самым способствуя непреднамеренному занесению болезни в ранее не пораженные стада и новые географические районы.[5]
Структура генома
Геном экзогенного вируса составляет 7462 основания и имеет классическое расположение генома «gag», «pol», «env» и фланкируется длинный терминальный повтор (LTR) на каждом конце. Есть 4 гена, кодирующих структурные белки вируса. Они представляют собой «затычку», кодирующую структурную внутреннюю вирион белки, содержащие «матрицу» (MA), «капсид» (CA) и «нуклеокапсид» (NC); "pro", который кодирует аспарагиновый протеаза (PR); «pol», который кодирует ферменты «RT» и «интеграза» (IN); и «env», который кодирует «поверхностный» (SU) и «трансмембранный» (TM) конверт. гликопротеины. Вирусные белки сначала синтезируются в виде крупных предшественников, а затем превращаются в зрелые белки с помощью протеолитический расщепление.[5] Дополнительный открытая рамка чтения (ORF) наблюдалась в вирусном геноме и была названа orfX, и ее функция не определена.[1]
Цикл репликации
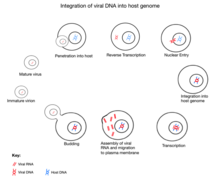
Первоначальное прикрепление JSRV к его клетке-мишени опосредовано связыванием субъединицы SU Env. гликопротеин к специфической молекуле рецептора клеточной поверхности "Hyal2". Вхождение ядра JSRV в цитоплазма активирует обратная транскрипция, при котором геном одноцепочечной РНК превращается в двухцепочечный ДНК формируется и интегрируется как провирус в хост. После интеграции экспрессия РНК JSRV из вирусного промоутер в LTR контролируется транскрипционной машиной хозяина. Следующий транскрипция и перевод вирусного генома, новый потомство вирус собирается на плазматической мембране и отделяется от клетки-хозяина, приобретая липидную оболочку и их гликопротеины "env". После высвобождения из клетки полипротеины «Gag» - «Pro» - «Pol» расщепляются до зрелых форм посредством протеаза. Этот шаг созревание необходим для формирования заразный частицы.[5]
Рецептор и вход
Сотовый рецептор для JSRV - это гиалуронидаза 2 (Hyal2), гликофосфатидилинол (GPI) -зависимый белок, принадлежащий к гиалуронидаза семья. Как правило, онкогенные ретровирусы вызывают трансформация клеток-хозяев в основном за счет инсерционной активации хозяина протоонкоген в онкоген. Но JSRV отличается в этом аспекте, поскольку его гликопротеин оболочки («env») сам по себе является онкогеном, и было показано, что этот единственный белок необходим и достаточен для индукции опухолей легких у овец.[6] В отличие от большинства ретровирусы, Проникновение JSRV в клетку-хозяина зависит от pH. Таким образом, онкогенный JSRV для проникновения заимствовал свойства как pH-зависимых, так и pH-независимых вирусов, что включает как связывание с рецептором, так и низкий pH для трансформации слияния клеток-хозяев.[7]
Иммунный ответ хозяина
Важной особенностью инфекции JSRV является отсутствие какого-либо специфического иммунного ответа со стороны хозяина. Вероятное объяснение состоит в том, что овцы иммунологически толерантны к антигенам JSRV из-за экспрессии близкородственных эндогенных белков JSRV в плод вилочковая железа во время развития Т-лимфоцитов и любые JSRV-реактивные Т-клетки должны распознаваться как «анти-собственные» и выборочно удаляться. Другая гипотеза заключается в том, что опухолевые клетки подавляют экспрессию своего основного класса гистосовместимости I, что, возможно, является причиной отсутствия какого-либо вирусоспецифического цитотоксического ответа Т-клеток (CTL).[5]
Эндогенный ретровирус овец jaagsiekte
В процессе эволюции овца геном включены части ретровируса овец Яагксиете, ныне известного как эндогенный Ретровирус овец Jaagsiekte (enJSRV).[8] Существует 27 известных копий enJSRV в геноме овец, пять из которых имеют интактные последовательности, обнаруженные во всех ретровирусы.[2][9] Похоже, они были заимствованы геномом овец как вспомогательные средства enJSRV. плацентарный разработка и обеспечивает защиту от подобных ретровирусов.[8][9] Анализы in vitro показали, что enJSRV делает это, блокируя различные стадии цикл репликации вируса.[2][9][10] Примером этой защиты является эпителий эндометрия овцы, где высокая экспрессия enJSVR предотвращает проникновение экзогенного JSVR в клетки посредством блокирования общего рецептора для обоих, HYAL2.[9] Однако вирус Jaagsiekte иногда может мутировать чтобы преодолеть эту защиту, и есть свидетельства того, что это имело место в последние 200 лет.[8] Есть также признаки того, что эндогенизация вируса Jaagsiekte все еще происходит сегодня.[2]
Механизм enJSRV в воспроизведении

У овец enJSRV высоко экспрессируются в эпителий выстилает различные репродуктивные ткани, в том числе влагалище, матка и яйцевод. В РНК enJSRV впервые обнаруживается в концептусе на 12 день.[11] Эксперименты показали, что enJSRV конверт регулирует трофобласт рост и дифференциация в пределах периимплантация концептус.[12] Было обнаружено, что enJSRV выражаются в трофэктодерма клетки плаценты. Их выражение совпадает с ключевыми событиями удлинения концептуса и наступлением трофобласт гигант двуядерные клетки (BNC) дифференциация.[11] Кроме того, было замечено, что инъекция морфолино (ингибитор образования оболочки enJSRV) в матку беременной овцы на 8-й день беременности приводил к снижению концептус удлинение и ингибирование дифференцировки гигантских BNC трофобластов.[11] Удлинение концепта овцы - важный процесс, так как он приводит к образованию интерферон тау (IFNT), который является сигналом распознавания беременности, необходимым для выживания концептуса.[13] Это стимулирует как желтое тело продолжать секретировать прогестерон и наступление имплантация.[13] После инъекции морфолино было замечено, что выкидыш наступил через 12 дней.[12] Эта работа поддерживает гипотезу о том, что enJSRV имеют решающее значение для воспроизводства овец и плацентарной морфогенез.
HYAL2
Гиалуронидаза 2 (HYAL2) служит рецептором на клеточной поверхности как для экзогенной, так и для эндогенной оболочки JSRV (env). МРНК HYAL2 может быть обнаружена в BNC и многоядерных синцитиях плацентомов овец во время беременности, но не в клетках трофэктодермы или каких-либо клетках эндометрия.[12] Гибридизация in situ анализ показал, что HYAL2 мРНК был обнаружен только в двухъядерных клетках и многоядерных синцитиальных бляшках.[10] Предполагается, что взаимодействия enJSRV с HYAL2 жизненно важны для роста и дифференцировки плаценты.[11] Хотя клеточный и молекулярный механизм все еще неясен, очевидно, что он играет роль в защите матки от вирусной инфекции и морфогенеза плаценты.[10]
Совместная экспрессия оболочки enJSRV и HYAL2 в одних и тех же типах клеток поддерживает гипотезу, что HYAL2 связывается с enJSRVs env на двуядерных клетках и способствует их слиянию в многоядерные синцитии.[8]
Сравнительная физиология человека и мышей
Представляет интерес для сравнительная физиология заключается в том, что наличие экспрессии белка оболочки enJSRV в развивающейся плаценте овцы очень похоже на то, что наблюдается для синцитина у людей и мышей.[14] Во время формирования плаценты человека синцитиотрофобласт, путем синтеза одноядерных цитотрофобласты, специфически экспрессируются синцитины человека. Синцитины фузогенный когда выражено in vitro, что подтверждает гипотезу о том, что они участвуют в морфогенезе плаценты.[8] Эти наблюдения подтверждают теорию о том, что древние ретровирусный инфекция имела важные последствия для млекопитающих эволюция.[8] Участие бета-ретровируса enJSRV в трофобластах концептуальных клеток овец является дополнительным аргументом в пользу его участия в плацентации овец.[8]
Будущие направления и резюме
Исследования эндогенных ретровирусов подтверждают идею о том, что они могут играть решающую роль в росте концептуальных клеток, дифференцировке плаценты и слиянии клеток у млекопитающих. Морфологические аспекты дифференцировки двуядерных клеток у жвачные животные такие как овцы, хорошо охарактеризованы, но механизмы четко не определены - хотя данные показывают, что enJSRV РНК и мРНК HYAL2 коэкспрессируются в двухъядерных клетках и многоядерных синцитиотрофобластах на протяжении всей беременности.
Смотрите также
Рекомендации
- ^ а б Йорк Д.Ф., Керат Г. (2003). «История аденокарциномы легких овец (jaagsiekte) и эксперименты, ведущие к вычету нуклеотидной последовательности JSRV». Актуальные темы микробиологии и иммунологии. 275: 1–23. Дои:10.1007/978-3-642-55638-8_1. PMID 12596893.
- ^ а б c d Арно Ф, Варела М, Спенсер Т.Э., Пальмарини М (ноябрь 2008 г.). «Коэволюция эндогенных бета-вирусов овец и их хозяев». Клеточные и молекулярные науки о жизни. 65 (21): 3422–32. Дои:10.1007 / s00018-008-8500-9. ЧВК 4207369. PMID 18818869.
- ^ Хопвуд П., Уоллес В.А., Коузенс С., Дьюар П., Малдун М., Норвал М., Гриффитс Д.Д. (ноябрь 2010 г.). «Отсутствие маркеров бетаретровирусной инфекции в аденокарциноме легких человека». Патология человека. 41 (11): 1631–40. Дои:10.1016 / j.humpath.2010.05.013. PMID 20825971.
- ^ Леру К., Жирар Н., Коттин В., Гренландия Т., Морнекс Дж. Ф., Арчер Ф (2007). «Ретровирус овец Jaagsiekte (JSRV): от вируса к раку легких у овец». Ветеринарные исследования. 38 (2): 211–28. Дои:10.1051 / ветрес: 2006060. PMID 17257570.
- ^ а б c d Гриффитс DJ, Мартино Х.М., Cousens C (май 2010 г.). «Патология и патогенез аденокарциномы легких овец». Журнал сравнительной патологии. 142 (4): 260–83. Дои:10.1016 / j.jcpa.2009.12.013. PMID 20163805.
- ^ Caporale M, Cousens C, Centorame P, Pinoni C, De las Heras M, Palmarini M (август 2006 г.). «Экспрессия гликопротеина оболочки ретровируса овец jaagsiekte достаточна для индукции опухолей легких у овец». Журнал вирусологии. 80 (16): 8030–7. Дои:10.1128 / JVI.00474-06. ЧВК 1563803. PMID 16873259.
- ^ Côté M, Zheng YM, Liu SL (ноябрь 2009 г.). «Связывание рецептора и низкий pH коактивируют слияние, опосредованное оболочкой онкогенного ретровируса». Журнал вирусологии. 83 (22): 11447–55. Дои:10.1128 / JVI.00748-09. ЧВК 2772678. PMID 19726505.
- ^ а б c d е ж грамм Армеццани А., Варела М., Спенсер Т.Э., Пальмарини М., Арно Ф. (декабрь 2014 г.). ""Ménage à Trois ": эволюционное взаимодействие между JSRV, enJSRV и домашними овцами". Вирусы. 6 (12): 4926–45. Дои:10.3390 / v6124926. ЧВК 4276937. PMID 25502326.
- ^ а б c d Варела М., Спенсер Т.Э., Пальмарини М., Арно Ф. (октябрь 2009 г.). «Дружественные вирусы: особые отношения между эндогенными ретровирусами и их хозяином». Летопись Нью-Йоркской академии наук. 1178: 157–72. Дои:10.1111 / j.1749-6632.2009.05002.x. ЧВК 4199234. PMID 19845636.
- ^ а б c Данлэп К.А., Пальмарини М., Адельсон Д.Л., Спенсер Т.Э. (август 2005 г.). «Эндогенные бета-ретровирусы овец (enJSRV) и рецептор гиалуронидазы 2 (HYAL2) в матке и концептусе овцы». Биология размножения. 73 (2): 271–9. Дои:10.1095 / биолрепрод.105.039776. PMID 15788753.
- ^ а б c d Блэк С.Г., Арно Ф., Пальмарини М., Спенсер Т.Е. (октябрь 2010 г.). «Эндогенные ретровирусы в дифференцировке трофобластов и развитии плаценты». Американский журнал репродуктивной иммунологии. 64 (4): 255–64. Дои:10.1111 / j.1600-0897.2010.00860.x. ЧВК 4198168. PMID 20528833.
- ^ а б c Данлэп К.А., Палмарини М., Варела М., Бургхардт Р.С., Хаяши К., Фармер Дж. Л., Спенсер Т. Э. (сентябрь 2006 г.). «Эндогенные ретровирусы регулируют периимплантационный рост и дифференцировку плаценты». Труды Национальной академии наук Соединенных Штатов Америки. 103 (39): 14390–5. Дои:10.1073 / pnas.0603836103. ЧВК 1599973. PMID 16980413.
- ^ а б Брукс К., Бернс Г., Спенсер Т.Э. (2014). «Удлинение концептуса у жвачных: роль прогестерона, простагландина, тау-интерферона и кортизола». Журнал зоотехники и биотехнологии. 5 (1): 53. Дои:10.1186/2049-1891-5-53. ЧВК 4373033. PMID 25810904.
- ^ Данлэп К.А., Пальмарини М., Спенсер Т.Э. (апрель 2006 г.). «Эндогенные бета-ретровирусы овец (enJSRV) и плацентарный морфогенез». Плацента. 27 (Приложение A): S135-40. Дои:10.1016 / j.placenta.2005.12.009. PMID 16533524.
дальнейшее чтение
- Пальмарини М, Фан Х (2003). «Молекулярная биология ретровируса овец jaagsiekte». Актуальные темы микробиологии и иммунологии. Актуальные темы микробиологии и иммунологии. 275: 81–115. Дои:10.1007/978-3-642-55638-8_4. ISBN 978-3-642-62897-9. PMID 12596896.
- Шарп Дж. М., ДеМартини Дж. С. (2003). «Естественная история JSRV у овец». Актуальные темы микробиологии и иммунологии. 275: 55–79. Дои:10.1007/978-3-642-55638-8_3. PMID 12596895.
