Нейроферритинопатия - Neuroferritinopathy
| Нейроферритинопатия | |
|---|---|
| Другие имена | Заболевание базальных ганглиев у взрослых |
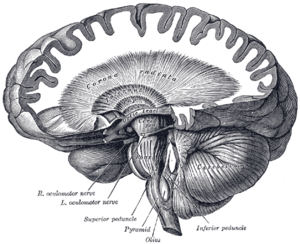 | |
| Мозжечок и базальные ганглии | |
| Специальность | Неврология |
Нейроферритинопатия генетический нейродегенеративное расстройство характеризуется накоплением утюг в базальный ганглий, мозжечок, и моторная кора человеческого мозга. Симптомы, которые экстрапирамидный в природе прогрессирует медленно и обычно не проявляется до взрослого возраста.[1] Эти симптомы включают: хорея, дистония и когнитивный дефицит, который ухудшается с возрастом.[2][3]
Это расстройство аутосомный доминирующий[4] и вызвано мутациями в гене, кодирующем легкая цепь подразделение ферритин белок. Ферритин дикого типа действует как буфер для железа, изолируя его и контролируя его высвобождение. Таким образом, мутации в легкой цепи ферритина приводят к накоплению железа в головном мозге, что можно визуализировать с помощью МРТ.[2] В настоящее время нейроферритинопатия - единственное нейродегенеративное заболевание с накоплением железа в головном мозге, классифицируемое как аутосомно-доминантный синдром.[4]
Лечение нейроферритинопатии направлено на устранение симптомов, связанных с хореей и дистонией, с использованием стандартных лекарств для каждого из них.[2] Расстройство прогрессирует, и с возрастом симптомы ухудшаются. С момента ее выявления в 2001 году было зарегистрировано менее 100 случаев нейроферритинопатии.[2] Заболеваемость в основном локализована в Северо-Восточной Англии.[4] предлагая эффект основателя.[2] Из-за его генетической природы текущие исследования сосредоточены на терапевтическом лечении симптомов, вызванных расстройством.[4]
Признаки и симптомы
Нейроферритинопатия имеет несколько отличительных признаков и симптомов. Они делятся на две категории: диагностические данные и физически видимые симптомы.
Результаты диагностики
Симптомы, отнесенные к категории протестированных и диагностированных с медицинской точки зрения, включают накопление железа в головном мозге, базальных ганглиях. кавитация, и нейродегенерация.[4] Пациенты с диагнозом нейроферритинопатия имеют аномальное накопление железа в головном мозге в пределах нейроны и глия из полосатое тело и коры мозжечка.[3] Наряду с накоплением железа в головном мозге нейроферритинопатия также обычно вызывает серьезную потерю нейронов.[3] Также могут возникнуть вторичные симптомы. Возможно, что первоначальное накопление железа вызовет дополнительное повреждение нейронов и гибель нейронов.[3] Поврежденные нейроны могут быть заменены другими клетками, чтобы обратить вспять нейродегенерацию. Эти клетки часто имеют более высокое содержание железа. Распад гематоэнцефалический барьер также может произойти из-за потери нейронов и впоследствии позволит большему количеству железа поступить в мозг и со временем накапливаться.[3]
Нейроферритинопатия в основном наблюдается у лиц, достигших позднего взросления, и, как правило, наблюдается медленное прогрессирование на протяжении многих десятилетий в течение жизни, средний возраст начала составляет 39 лет.[1] Потеря познания обычно наблюдается только на поздних стадиях заболевания.[1] У диагностированных пациентов сохраняется большая часть когнитивных функций до тех пор, пока не наступят наиболее прогрессивные стадии болезни.[1]
Физические симптомы
Симптомы, классифицируемые как физически видимые, включают: хорея, дистония, спастичность, и жесткость, все физические симптомы организма, связанные с двигательные расстройства.[3] Симптомы нейроферритинопатии, влияющие на движение, также прогрессируют и со временем становятся все более обобщенными.[4] Обычно в течение первых десяти лет от начала болезни напрямую поражаются только одна или две конечности.[4]Отличительными симптомами нейроферритинопатии являются хорея, обнаруживаемая у 50% диагностированных пациентов, дистония, обнаруживаемая у 43% пациентов, и паркинсонизм, обнаружен у 7,5% пациентов.[1] Полный контроль над верхними конечностями на теле обычно сохраняется до позднего начала болезни.[1] Со временем симптомы, наблюдаемые у пациента, могут меняться с одной стороны тела на противоположную, прыгая слева направо или наоборот.[1] Другой путь, по которому наблюдаются физически видимые симптомы, - это появление, исчезновение, а затем повторное появление специфических симптомов.[1]
Хотя эти симптомы являются классическими индикаторами нейроферритинопатии, симптомы могут варьироваться от пациента к пациенту.[1]
Причины
Нейроферритинопатия возникает в результате аномального накопления железа в мозге. Это накопление железа происходит из-за мутаций полипептида FTL, который отвечает за кодирование белков, участвующих в метаболизме железа. Нейроферритинопатия чаще всего вызывается однократной вставкой нуклеотида аденина в ген ферритина L-цепи, который, в свою очередь, изменяет карбоксил конец всей белковой цепи.[3] Однако точное расположение вставки в экзон зависит от семьи.[4] Нейроферритинопатия также может быть вызвана вставкой двух дополнительных нуклеотидных оснований. Встраивание оснований в ген ферритина L-цепи заставляет цепь удлиняться и изменять последовательность аминокислот, обнаруженных в гене, также известную как мутация сдвига рамки.[3]
Эти мутации приводят к снижению способности связывать железо.[1] Окислительное повреждение, вызванное повышенным содержанием железа, приводит к апоптоз, или запрограммированная гибель клеток.[1] Накопление железа в головном мозге чрезвычайно опасно, поскольку избыток железа катализирует образование свободные радикалы, которые оказывают вредное воздействие на мозг.[1] Накопление железа, характерное для нейроферритинопатии, особенно влияет на мозжечок, базальные ганглии и моторную кору головного мозга.[1]
Механизм
Протеин ферритин функции секвестра и высвобождения железа, действуя как буферная система железа в клетках. Железо необходимо для работы мозга, например, для транспорта кислорода и клеточного метаболизма. Тем не менее, тщательный контроль железа важен, поскольку повышенный уровень железа в головном мозге катализирует образование свободные радикалы которые создают окислительные молекулы через Реакция Фентона.[5] Эти окислительные молекулы могут вызывать окислительное повреждение мозга. Железо, связанное с ферритином, не реагирует.[1]
Реакция Фентона
(1) Fe2+ + H2О2 → Fe3+ + HO • + OH−
(2) Fe3+ + H2О2 → Fe2+ + HOO • + H+
Белок ферритин состоит из тяжелая цепь (H) и легкая цепь (L) субъединицы. При нейроферритинопатии происходит мутация гена, кодирующего легкую цепь. Несколько различных вариаций мутаций привели к диагнозу нейроферритинопатии; все эти мутации происходят в легкой цепи. Полагают, что мутированная легкая цепь подавляет способность ферритина эффективно связывать и удерживать железо. Без контроля железа оно может вызвать окислительное повреждение мозга, как описано выше.[6]
Концентрация железа в здоровом мозге сильно варьируется от региона к региону. Определенные области мозга, связанные с двигательными функциями, по-видимому, имеют больше накоплений железа, чем области, не связанные с двигателем. Это наблюдение различных концентраций железа является возможным объяснением корреляции между двигательными расстройствами и дисбалансом железа в центральной нервной системе.[3]
Диагностика
Нейроферритинопатия в первую очередь диагностируется у пожилых людей, особенно у взрослых, страдающих Болезнь Альцгеймера или же болезнь Паркинсона, поскольку железо накапливается в мозге в течение длительного времени.[3] Нейроферритинопатия диагностируется с помощью методов нейровизуализации, физиологических тестов или генетических тестов.
Классификация
Все нарушения мозгового железа ранее были помечены нейродегенерация, связанная с пантотенаткиназой ранее известный как синдром Халлервордена-Шпатца, в честь ученых, впервые обнаруживших людей с аномальным уровнем железа в 1922 году (впоследствии переименованных после обнаружения их Нацистская партия галстуки).[1] Заболевания, связанные с железом в головном мозге, в настоящее время делятся на три категории: генетическая нейродегенерация с накоплением железа в мозге, генетическое системное накопление железа с неврологическими особенностями и приобретенные заболевания, связанные с избытком или дефицитом железа. Нейроферритинопатия классифицируется по первой категории - генетическая нейродегенерация с накоплением железа в мозге.[7] Нейроферритинопатия классифицируется как болезнь с поздним началом. базальный ганглий болезнь и является доминантно наследуемым нейродегенеративным заболеванием.[3] Четыре разных аллели несут ответственность за нейроферритинопатию. Три возникают из нуклеотид вставки в легкая цепь ферритина (FTL) полипептидный ген, а четвертый - результат миссенс-мутации в гене FTL.[4]
Нейровизуализация

Нейроферритинопатия чаще всего диагностируется с помощью МРТ и другие методы нейровизуализации.[1] МРТ помогает определить отложения железа в мозжечке, базальных ганглиях и моторной коре, характерные для нейроферритинопатии.[8] МРТ пораженных людей также показывает легкие мозжечковые и церебральная атрофия, или разрушение ткани, и образование газовой полости в скорлупа.[8] Что наиболее важно, МРТ показывает неправильно свернутые белки ферритина и отложения железа в глиальных клетках хвостатого тела, скорлупы, бледного шара, коры головного мозга, таламуса и клетки Пуркинье, вызывая гибель нейронов в этих областях.[8]
Физиологическое тестирование
Анализы крови обычно возвращаются к норме у пораженных людей, поэтому они не служат надежным средством диагностики.[1] Анализы крови могут показать низкие сыворотка уровни ферритина. Однако это ненадежный метод диагностики, поскольку у некоторых пациентов уровень ферритина в сыворотке крови типичен даже на последних стадиях нейроферритинопатии.[1] Анализы спинномозговой жидкости также обычно в норме.[8]Ферритин агрегаты в коже, печени, почках и мышцах может помочь в диагностике нейроферритинопатии.[8] Более цитохром с оксидаза -отрицательные волокна также часто встречаются в мышцах биопсия пострадавших людей.[8]
Генетическое тестирование
Генетическое тестирование может подтвердить диагноз нейроферритинопатии. Диагноз может быть поставлен путем анализа белковых последовательностей пораженных людей и сравнения их с известными последовательностями нейроферритинопатии.[4]
Уход
В связи с генетической этиологией нейроферритинопатии заболевание в настоящее время неизлечимо. Более того, невозможно эффективно остановить прогрессирование заболевания.[1] Таким образом, текущее лечение направлено на устранение симптомов заболевания. Нет лекарств для лечения всех симптомов.[1] Ботокс было показано, что помогает при очаговой дистонии.[1] Истощитель дофамина Тетрабеназин показано, чтобы помочь с непроизвольными движениями.[1] Симптомы, влияющие на движение (дистония), также лечили с помощью L-допа, орфенадрин, бензгексол, сульпирид, диазепам, клоназепам, и деанол.[4] Симптомы паркинсонизма не уменьшились на L-допа.[1] Следует избегать приема добавок железа.[4]
Эпидемиология

Нейроферритинопатия была впервые обнаружена в 2001 году, и ее первый случай был зарегистрирован в Камбрии из Северной Англии.[1] Открытие нейроферритинопатии было опосредовано исследованием, проведенным на большой семье, страдающей от доминантно наследуемой болезни базальных ганглиев.[1] Сообщалось, что заболевание вызвано мутацией полипептида легкой цепи ферритина (FTL1) и, как было установлено, вызывает накопление железа в головном мозге и нейродегенерацию.[1] Судя по местонахождению первого случая нейроферритинопатии, большинство пациентов с диагнозом этого заболевания также были обнаружены в Северной и Северо-Восточной Англии.[1] Локализация большинства случаев в Северной и Северо-Восточной Англии предполагает, что общий предок может быть ответственным за многие или, возможно, все случаи.[4] Несмотря на то, что было зарегистрировано менее 100 случаев и общее местонахождение болезни в Северной и Северо-Восточной Англии, за последние годы во всем остальном мире было диагностировано еще несколько случаев нейроферритинопатии.[4]
Исследование
Исследуются новые возможные варианты лечения: венесекция (удаление красных кровяных телец), хелатирование железа с помощью деферипрон, и Коэнзим Q10 (убихинон).[4]
Рекомендации
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа Лен, А; Бойл, Р; Коричневый, H; Эйри, К; Меллик, Дж. (Сентябрь 2012 г.). «Нейроферритинопатия». Паркинсонизм и связанные с ним расстройства. 18 (8): 909–15. Дои:10.1016 / j.parkreldis.2012.06.021. PMID 22818529.
- ^ а б c d е Чиннери, ПФ; Пагон, РА; Адам, депутат; Ardinger, HH; Птица, ТД; Долан, CR; Фонг, Коннектикут; Смит, RJH; Стивенс, К. (2010). «Нейроферритинопатия». PMID 20301320. Цитировать журнал требует
| журнал =(помощь) - ^ а б c d е ж грамм час я j k Zecca, L; Юдим, МБ; Riederer, P; Коннор, младший; Крайтон, Р.Р. (ноябрь 2004 г.). «Железо, старение мозга и нейродегенеративные расстройства». Обзоры природы Неврология. 5 (11): 863–73. Дои:10.1038 / nrn1537. PMID 15496864.
- ^ а б c d е ж грамм час я j k л м п о Кио, MJ; Моррис, CM; Чиннери, ПФ (2013). «Нейроферритинопатия». Международный обзор нейробиологии. 110: 91–123. Дои:10.1016 / B978-0-12-410502-7.00006-5. ISBN 9780124105027. PMID 24209436.
- ^ Батиста-Насименто, Лилиана; Пиментель, Катарина; Андраде Менезеш, Регина; Родригес-Поузада, Клаудина (2012). «Железо и нейродегенерация: от клеточного гомеостаза к болезни». Окислительная медицина и клеточное долголетие. 2012: 128647. Дои:10.1155/2012/128647. ЧВК 3369498. PMID 22701145.
- ^ Руо, Трейси А. (3 июля 2013 г.). «Метаболизм железа в ЦНС: последствия для нейродегенеративных заболеваний». Обзоры природы Неврология. 14 (8): 551–564. Дои:10.1038 / nrn3453. PMID 23820773.
- ^ Woimant, F; Трочелло, Дж. М. (2014). «Заболевания тяжелых металлов». Справочник по клинической неврологии. 120: 851–64. Дои:10.1016 / B978-0-7020-4087-0.00057-7. ISBN 9780702040870. PMID 24365357.
- ^ а б c d е ж Леви, Соня; Финацци, Дарио (7 мая 2014 г.). «Нейродегенерация с накоплением железа в мозге: обновленная информация о патогенетических механизмах». Границы фармакологии. 5: 99. Дои:10.3389 / fphar.2014.00099. ЧВК 4019866. PMID 24847269.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
