Реперфузионная терапия - Reperfusion therapy - Wikipedia
| Реперфузионная терапия | |
|---|---|
 Тромб материал (в чашке, в верхнем левом углу), удаленный из коронарной артерии во время ангиопластики для прерывания инфаркта миокарда. Показаны пять частей тромба (стрелки). |
Реперфузионная терапия - это лечение для восстановления кровотока, проходящего через закупоренные артерии или вокруг них, обычно после сердечного приступа (инфаркт миокарда (MI)). Реперфузионная терапия включает: наркотики и хирургия. Лекарства тромболитики и фибринолитики используется в процессе, называемом тромболизис. Проведенные операции могут быть малоинвазивный эндоваскулярные процедуры например, чрезкожное коронарное вмешательство (PCI), за которым следует коронарная ангиопластика. При ангиопластике используется вставка воздушный шар для открытия артерии с возможным дополнительным использованием одного или нескольких стенты.[1] Другие выполняемые операции более инвазивны. обходные операции которые пересаживают артерии вокруг закупорки.
Если ИМ представлен ЭКГ свидетельство Элевация ST известный как ИМпST, или если межжелудочковая блокада аналогичным образом представлена реперфузионная терапия. При отсутствии элевации ST, ИМ без элевации ST, известный как NSTEMI, или нестабильная стенокардия можно предположить (оба они неразличимы при первоначальной оценке симптомов). Повышение сегмента ST указывает на полностью заблокированную артерию, требующую немедленной реперфузии. При NSTEMI кровоток присутствует, но ограничен стеноз. При ИМбпST следует избегать применения тромболитиков, поскольку нет явной пользы от их использования. [2]. Если состояние остается стабильным сердечный стресс-тест могут быть предложены, а при необходимости последующие реваскуляризация будет проводиться для восстановления нормального кровотока. Если кровоток становится нестабильным, может потребоваться срочная ангиопластика. В этих нестабильных случаях применение тромболитиков противопоказано.[3]
По крайней мере, в 10% пролеченных случаев ИМпST не развиваются. некроз из сердечная мышца. Успешное восстановление кровотока называется прерыванием сердечного приступа. Около 25% ИМпST можно прервать, если лечить в течение часа после появления симптомов.[4]
Тромболитическая терапия
Инфаркт миокарда
Тромболитическая терапия показан для лечения ИМпST - если оно может начаться в течение 12 часов с момента появления симптомов, и человек имеет право на лечение на основании критериев исключения, и коронарная ангиопластика не доступен сразу.[5] Тромболизис наиболее эффективен в первые 2 часа. Через 12 часов риск внутричерепное кровотечение связанные с тромболитической терапией перевешивают любую пользу.[3][6][7] Поскольку необратимое повреждение происходит в течение 2–4 часов после инфаркта, для реперфузии имеется ограниченное время.
Тромболитические препараты противопоказаны для лечения нестабильной стенокардии и ИМбпST.[3][8] и для лечения лиц с доказательствами кардиогенный шок.[9]
Хотя идеального тромболитического средства не существует, в идеале он должен приводить к быстрой реперфузии, иметь высокую устойчивую проходимость, быть специфичным для недавно возникших тромбов, легко и быстро вводиться, создавать низкий риск внутримозговое кровотечение и системные кровотечения, не имеют антигенность, неблагоприятный гемодинамические эффекты, или клинически значимый лекарственные взаимодействия, и быть экономически эффективным.[10] Доступные в настоящее время тромболитические средства включают: стрептокиназа, урокиназа, и альтеплаза (рекомбинантный тканевый активатор плазминогена, rtPA). Совсем недавно тромболитические агенты, похожие по структуре на rtPA, такие как ретеплаза и тенектеплаза был использован. Эти новые агенты обладают не меньшей эффективностью, чем rtPA, при значительно более простом введении. Тромболитический агент, используемый конкретным человеком, зависит от предпочтений учреждения и возраста пациента.
В зависимости от применяемого тромболитического средства дополнительные антикоагулянт с гепарин или же низкомолекулярный гепарин может принести пользу.[11][12] С tPa и родственными агентами (ретеплаза и тенектеплаза) гепарин необходим, чтобы коронарная артерия оставалась открытой. Из-за антикоагулянтного эффекта истощения фибриногена стрептокиназой[13] и урокиназа[14][15][16] лечение, там меньше необходимости.[11]
Отказ
Тромболитическая терапия для прерывания инфаркта миокарда не всегда эффективна. Степень эффективности тромболитика зависит от времени, прошедшего с начала инфаркта миокарда, при этом наилучшие результаты достигаются, если тромболитик применяется в течение двух часов после появления симптомов.[17][18] Частота неудач тромболитиков может достигать 50%.[19] В случае неспособности тромболитического средства открыть коронарную артерию, связанную с инфарктом, пациенту затем проводят консервативное лечение антикоагулянтами и позволяют «завершить инфаркт» или чрезкожное коронарное вмешательство (и коронарная ангиопластика). Чрескожное коронарное вмешательство в этом случае известно как «спасательное ЧКВ» или «спасительное ЧКВ». Осложнения, особенно кровотечения, значительно выше при экстренном ЧКВ, чем при первичном ЧКВ из-за действия тромболитика.
Побочные эффекты
Внутричерепное кровотечение (ICB) и последующее Инсульт это серьезный побочный эффект тромболитического использования. В факторы риска для развития внутричерепного кровотечения включают предыдущий эпизод внутричерепного кровотечения, преклонный возраст человека и используемый тромболитический режим. В целом риск ICB из-за тромболитиков составляет от 0,5 до 1 процента.[11]
Коронарная ангиопластика
Преимущество быстрой первичной ангиопластики перед тромболитической терапией при остром ИМпST в настоящее время хорошо известно.[20][21][22] При быстром выполнении ангиопластика восстанавливает кровоток в закупоренной артерии более чем у 95% пациентов по сравнению со скоростью реперфузии около 65%, достигнутой при тромболизисе.[20] Логистические и экономические препятствия, кажется, препятствуют более широкому применению ангиопластики.[23] хотя возможность проведения регионарной ангиопластики при ИМпST в настоящее время изучается в США.[24] Использование коронарной ангиопластики для прерывания инфаркта миокарда предшествует первичной чрезкожное коронарное вмешательство. Целью быстрой ангиопластики является открытие артерии как можно скорее и предпочтительно в течение 90 минут после обращения пациента в отделение неотложной помощи. Это время называется от двери до воздушного шара время. Немногие больницы могут провести ангиопластику в течение 90 минут.[25] что побудило Американский колледж кардиологии (ACC) о запуске национальной инициативы Door to Balloon (D2B) в ноябре 2006 года. По состоянию на 16 марта 2007 года к D2B Alliance присоединились более 800 больниц.[26]
Одна особенно успешная реализация основного протокола PCI находится в Калгари, область здравоохранения под эгидой Институт сердечно-сосудистой системы им. Либина в Альберте. Согласно этой модели, EMS бригады, принимающие экстренную помощь, могут передавать ЭКГ непосредственно в систему цифрового архивирования, которая позволяет персоналу отделения неотложной помощи немедленно подтвердить диагноз. Это, в свою очередь, позволяет перенаправить бригад неотложной помощи в те учреждения, которые готовы к проведению срочной ангиопластики. В результате этого протокола среднее время до лечения составило 62 минуты.[27]
Текущие руководящие принципы в Соединенных Штатах ограничивают ангиопластику больницами с доступной операцией экстренного шунтирования в качестве резервного,[5] но это не так в других частях мира.[28]
ЧКВ включает выполнение коронарного ангиограмма для определения местоположения инфарктного сосуда с последующим баллонная ангиопластика (и часто установка интракоронарного стента) стенозированный артериальный сегмент. В некоторых условиях экстракционный катетер может использоваться для попытки аспирации (удаления) тромба перед баллонной ангиопластикой. При использовании интракоронарного стенты не улучшают краткосрочные результаты первичного ЧКВ, использование стентов широко распространено из-за меньшего количества процедур для лечения рестеноза по сравнению с баллонной ангиопластикой.[29]
Адъювантная терапия во время ангиопластики включает внутривенное гепарин, аспирин, и клопидогрель. Ингибиторы гликопротеина IIb / IIIa часто используются при первичной ангиопластике, чтобы снизить риск ишемических осложнений во время процедуры.[30][31] Из-за количества антитромбоцитарных агентов и антикоагулянтов, используемых во время первичной ангиопластики, риск кровотечения, связанный с процедурой, выше, чем во время плановой процедуры.[32]
Аортокоронарное шунтирование
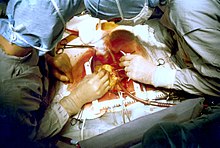
Экстренное шунтирование для лечения острого инфаркта миокарда (ИМ) встречается реже, чем ЧКВ или тромболизис. С 1995 по 2004 год процент людей с кардиогенный шок леченных первичным ЧКВ увеличилось с 27,4% до 54,4%, в то время как увеличение операция по аортокоронарному шунтированию (АКШ) было всего от 2,1% до 3,2%.[33] Экстренная АКШ обычно проводится для одновременного лечения механических осложнений, таких как разрыв сосочковой мышцы или дефекта межжелудочковой перегородки, с последующим кардиогенным шоком.[34] При неосложненном ИМ смертность может быть высоким, если операция проводится сразу после инфаркта.[35] Если этот вариант поддерживается, пациент должен быть стабилизирован до операции с помощью поддерживающих вмешательств, таких как использование внутриаортальный баллонный насос.[36] У пациентов, у которых после инфаркта миокарда развивается кардиогенный шок, как ЧКВ, так и АКШ являются удовлетворительными вариантами лечения с аналогичными показателями выживаемости.[37][38]
Операция по аортокоронарному шунтированию включает в себя имплантацию артерии или вены пациента для шунтирования. сужения или окклюзии коронарных артерий. Однако можно использовать несколько артерий и вен. внутренняя артерия молочной железы трансплантаты продемонстрировали значительно лучшую долгосрочную проходимость, чем большая подкожная вена прививки.[39] У пациентов с поражением двух или более коронарных артерий операция шунтирования связана с более длительным сроком службы. выживаемость по сравнению с чрескожными вмешательствами.[40] У пациентов с поражением одного сосуда операция сравнительно безопасна и эффективна и в отдельных случаях может быть вариантом лечения.[41] Первоначально шунтирование обходится дороже, но становится экономически эффективным в долгосрочной перспективе.[42] Хирургический шунт больше инвазивный первоначально, но несет меньший риск повторных процедур (но они могут быть минимально инвазивный ).[41]
Реперфузионная аритмия
Ускоренный идиовентрикулярный ритм что выглядит медленно вентрикулярная тахикардия это признак успешной реперфузии.[43] Лечение этого ритма не требуется, так как он редко переходит в более серьезный ритм.[44]
Смотрите также
- Перфузионное сканирование
- Реперфузионная травма
- Реваскуляризация
- ТИМИ
- Ишемически-реперфузионное повреждение аппендикулярно-мышечной системы
Рекомендации
- ^ McCoy SS, Crowson CS, Maradit-Kremers H, Therneau TM, Roger VL, Matteson EL, Gabriel SE (май 2013 г.). «Долгосрочные исходы и лечение после инфаркта миокарда у пациентов с ревматоидным артритом». Журнал ревматологии. 40 (5): 605–10. Дои:10.3899 / jrheum.120941. ЧВК 3895921. PMID 23418388.
- ^ «Эффекты тканевого активатора плазминогена и сравнение ранних инвазивных и консервативных стратегий при нестабильной стенокардии и миокарде без зубца Q ... - PubMed - NCBI».
- ^ а б c Совместная группа специалистов по фибринолитической терапии (FTT) (1994). «Показания к фибринолитической терапии при подозрении на острый инфаркт миокарда: совместный обзор результатов ранней смертности и основных заболеваний по всем рандомизированным исследованиям с участием более 1000 пациентов». Ланцет. 343 (8893): 311–22. Дои:10.1016 / с0140-6736 (94) 91161-4. PMID 7905143.
- ^ Ферхойгт Ф.В., Герш Б.Дж., Армстронг П.В. (2006). «Прерывистый инфаркт миокарда: новая мишень реперфузионной терапии». Eur Heart J. 27 (8): 901–4. Дои:10.1093 / eurheartj / ehi829. PMID 16543251.
- ^ а б Антман Э.М., Анбе Д.Т., Армстронг П.В., Бейтс Э.Р., Грин Л.А., Хэнд М., Хохман Д.С., Крумхольц Х.М., Кушнер Ф.Г., Ламас Г.А., Маллани С.Дж., Орнато Дж. П., Пирл Д. "Рекомендации ACC / AHA по ведению пациентов с инфарктом миокарда с подъемом сегмента ST: отчет Целевой группы Американского колледжа кардиологов / Американской кардиологической ассоциации по практическим рекомендациям (Комитет по пересмотру рекомендаций 1999 года по ведению пациентов с острым инфарктом миокарда. ) ". J Am Coll Cardiol. 44 (3): 671–719. Дои:10.1016 / j.jacc.2004.07.002. PMID 15358045. Архивировано из оригинал на 2010-05-09.
- ^ Boersma E, Maas AC, Deckers JW, Simoons ML (1996). «Раннее тромболитическое лечение острого инфаркта миокарда: переоценка золотого часа». Ланцет. 348 (9030): 771–5. Дои:10.1016 / S0140-6736 (96) 02514-7. HDL:1765/58599. PMID 8813982. S2CID 36710069.
- ^ ПОЗДНЕЕ испытание intestigatos. (1993). «Исследование поздней оценки тромболитической эффективности (LATE) с альтеплазой через 6-24 часа после начала острого инфаркта миокарда». Ланцет. 342 (8874): 759–66. Дои:10.1016 / 0140-6736 (93) 91538-В. PMID 8103874. S2CID 26840289.
- ^ «Эффекты тканевого активатора плазминогена и сравнение ранних инвазивных и консервативных стратегий при нестабильной стенокардии и инфаркте миокарда без зубца Q. Результаты исследования TIMI IIIB. Тромболизис при ишемии миокарда». Тираж. 89 (4): 1545–56. Апрель 1994 г. Дои:10.1161 / 01.cir.89.4.1545. PMID 8149520.
- ^ Хохман Дж. С., Слипер Л. А., Уэбб Дж. Г., Сэнборн Т. А., Уайт HD, Тэлли Дж. Д., Буллер К. Э., Джейкобс А. К., Слейтер Дж. Н., полковник Дж., Маккинлей С. М., ЛеДжемтель Т.Х. (1999). «Ранняя реваскуляризация при остром инфаркте миокарда, осложненном кардиогенным шоком. Исследователи ШОКА. Следует ли срочно реваскуляризовать окклюзированные коронарные сосуды для кардиогенного шока». N Engl J Med. 341 (9): 625–34. Дои:10.1056 / NEJM199908263410901. PMID 10460813.
- ^ Белый HD, Ван де Верф FJ (1998). «Тромболизис при остром инфаркте миокарда». Тираж. 97 (16): 1632–46. Дои:10.1161 / 01.cir.97.16.1632. PMID 9593569.
- ^ а б c Следователи GUSTO (1993). «Международное рандомизированное исследование по сравнению четырех тромболитических стратегий при остром инфаркте миокарда. Исследователи GUSTO». N Engl J Med. 329 (10): 673–82. Дои:10.1056 / NEJM199309023291001. HDL:1765/5468. PMID 8204123.
- ^ Sabatine MS, Morrow DA, Montalescot G, Dellborg M, Leiva-Pons JL, Keltai M, Murphy SA, McCabe CH, Gibson CM, Cannon CP, Antman EM, Braunwald E (2005). Клопидогрель как дополнительная реперфузионная терапия (CLARITY) - тромболизис при инфаркте миокарда (TIMI) 28 исследователей. «Ангиографические и клинические результаты у пациентов, получавших низкомолекулярный гепарин по сравнению с нефракционированным гепарином при инфаркте миокарда с подъемом сегмента ST, получавших фибринолитики в исследовании CLARITY-TIMI 28». Тираж. 112 (25): 3846–54. Дои:10.1161 / CIRCULATIONAHA.105.595397. PMID 16291601.
- ^ Коули MJ, Hastillo A, Vetrovec GW, Fisher LM, Garrett R, Hess ML (1983). «Фибринолитические эффекты интракоронарного введения стрептокиназы у пациентов с острым инфарктом миокарда и коронарной недостаточностью». Тираж. 67 (5): 1031–8. Дои:10.1161 / 01.cir.67.5.1031. PMID 6831667.
- ^ Лоуренко Д.М., Досне А.М., Хер А., Самама М. (1989). «Влияние стандартного гепарина и низкомолекулярного гепарина на тромболитическую и фибринолитическую активность одноцепочечного активатора плазминогена урокиназы» in vitro". Тромб Хемост. 62 (3): 923–6. Дои:10.1055 / с-0038-1651029. PMID 2556812.
- ^ Ван де Верф Ф., Ванхаек Дж., Де Гест Х., Верстрате М., Коллен Д. (1986). «Коронарный тромболизис рекомбинантным одноцепочечным активатором плазминогена урокиназного типа у пациентов с острым инфарктом миокарда». Тираж. 74 (5): 1066–70. Дои:10.1161 / 01.cir.74.5.1066. PMID 2429783.
- ^ Боде С., Шенермарк С., Шулер Г., Циммерманн Р., Шварц Ф., Кюблер В. (1988). «Эффективность внутривенного введения проурокиназы и комбинации проурокиназы и урокиназы при остром инфаркте миокарда». Am J Cardiol. 61 (13): 971–4. Дои:10.1016/0002-9149(88)90108-7. PMID 2452564.
- ^ Моррисон LJ, Verbeek PR, McDonald AC, Sawadsky BV, Cook DJ (2000). «Смертность и догоспитальный тромболизис при остром инфаркте миокарда: метаанализ». JAMA. 283 (20): 2686–92. Дои:10.1001 / jama.283.20.2686. PMID 10819952.
- ^ Boersma E, Maas AC, Deckers JW, Simoons ML (1996). «Раннее тромболитическое лечение острого инфаркта миокарда: переоценка золотого часа». Ланцет. 348 (9030): 771–5. Дои:10.1016 / S0140-6736 (96) 02514-7. HDL:1765/58599. PMID 8813982. S2CID 36710069.
- ^ Кац, Ричард; Перселл, Х. (2006). Острые коронарные синдромы. Elsevier Health Sciences. п. 96. ISBN 0443102961.
- ^ а б Кили Э. К., Бура Дж. А., Гринес С. Л. (2003). «Первичная ангиопластика по сравнению с внутривенной тромболитической терапией при остром инфаркте миокарда: количественный обзор 23 рандомизированных исследований». Ланцет. 361 (9351): 13–20. Дои:10.1016 / S0140-6736 (03) 12113-7. PMID 12517460. S2CID 9480846.
- ^ Гринс К.Л., Браун К.Ф., Марко Дж., Ротбаум Д., Стоун Г.В., О'Киф Дж., Оверли П., Донохью Б., Челлия Н., Тиммис Г.К. и др. (1993). «Сравнение немедленной ангиопластики с тромболитической терапией острого инфаркта миокарда. Первичная ангиопластика в группе исследования инфаркта миокарда». N Engl J Med. 328 (10): 673–9. Дои:10.1056 / NEJM199303113281001. PMID 8433725.
- ^ Глобальное использование стратегий открытия окклюзированных коронарных артерий при острых коронарных синдромах (GUSTO IIb) Исследователи подгруппы по ангиопластике. (1997). «Клиническое испытание по сравнению первичной коронарной ангиопластики с тканевым активатором плазминогена при остром инфаркте миокарда». N Engl J Med. 336 (23): 1621–8. Дои:10.1056 / NEJM199706053362301. HDL:1765/5545. PMID 9173270.
- ^ Boersma E, Первичная коронарная ангиопластика против группы тромболизиса (2006). «Имеет ли значение время? Объединенный анализ рандомизированных клинических испытаний, сравнивающих первичное чрескожное коронарное вмешательство и внутрибольничный фибринолиз у пациентов с острым инфарктом миокарда». Eur Heart J. 27 (7): 779–88. Дои:10.1093 / eurheartj / ehi810. PMID 16513663.
- ^ Рокос И.К., Ларсон Д.М., Генри Т.Д. и др. (2006). «Обоснование создания региональных сетей центров приема инфаркта миокарда с подъемом сегмента ST». Я сердце J. 152 (4): 661–7. Дои:10.1016 / j.ahj.2006.06.001. PMID 16996830.
- ^ Bradley EH, Herrin J, Wang Y, Barton BA, Webster TR, Mattera JA, Roumanis SA, Curtis JP, Nallamothu BK и др. (2006). «Стратегии сокращения времени от двери до баллона при остром инфаркте миокарда». N Engl J Med. 355 (22): 2308–20. Дои:10.1056 / NEJMsa063117. PMID 17101617. S2CID 1360936.
- ^ «D2B: Альянс за качество». Американский колледж кардиологии. 2006 г.. Получено 15 апреля, 2007.
- ^ Де Вилльерс Дж. С., Андерсон Т., МакМикин Дж. Д. и др. (2007). «Ускоренный перевод для первичного чрескожного коронарного вмешательства: оценка программы». CMAJ. 176 (13): 1833–8. Дои:10.1503 / cmaj.060902. ЧВК 1891117. PMID 17576980.
- ^ Аверсано Т. и др. (2002). «Тромболитическая терапия по сравнению с первичным чрескожным коронарным вмешательством по поводу инфаркта миокарда у пациентов, поступающих в больницы без кардиохирургии на месте: рандомизированное контролируемое исследование». JAMA. 287 (15): 1943–51. Дои:10.1001 / jama.287.15.1943. PMID 11960536.
- ^ Гринес К.Л., Кокс Д.А., Стоун Г.В., Гарсия Е., Маттос Л.А., Джамбартоломей А., Броди Б.Р., Мадонна О., Эйджгельшовен М., Лански А.Дж., О'Нил В.В., Морис М.С. (1999). «Коронарная ангиопластика с имплантацией стента или без него при остром инфаркте миокарда. Первичная ангиопластика стента в группе исследования инфаркта миокарда». N Engl J Med. 341 (26): 1949–56. Дои:10.1056 / NEJM199912233412601. PMID 10607811.
- ^ Бренер С.Дж., Барр Л.А., Бурченал Дж.Э., Кац С., Джордж Б.С., Джонс А.А., Коэн Э.Д., Гейни П.С., Уайт Х.Дж., Чик Х.Б., Моисей Дж. В., Молитерно Д. Д., Эффрон МБ, Тополь Э.Д. «Рандомизированное плацебо-контролируемое испытание блокады тромбоцитов гликопротеина IIb / IIIa с первичной ангиопластикой при остром инфаркте миокарда. Исследователи ReoPro и первичной PTCA. Организация и рандомизированное исследование (RAPPORT)». Тираж. 98 (8): 734–41. Дои:10.1161 / 01.cir.98.8.734. PMID 9727542.
- ^ Tcheng JE, Kandzari DE, Grines CL, Cox DA, Effron MB, Garcia E, Griffin JJ, Guagliumi G, Stuckey T., Turco M, Fahy M, Lansky AJ, Mehran R, Stone GW (2003). «Преимущества и риски использования абциксимаба при первичной ангиопластике при остром инфаркте миокарда: исследование контролируемого абциксимаба и устройств для лечения поздних осложнений ангиопластики нижних конечностей (CADILLAC)». Тираж. 108 (11): 1316–23. Дои:10.1161 / 01.CIR.0000087601.45803.86. PMID 12939213.
- ^ Мукерджи, Дебабрата (2006). 900 вопросов: обзор совета по интервенционной кардиологии. Липпинкотт Уильямс и Уилкинс. ISBN 0-7817-7349-0.
- ^ Бабаев А, Фредерик П.Д., Pasta DJ, Every N, Сичровский Т, Хохман Дж.С. (2005). «Тенденции ведения и исходы пациентов с острым инфарктом миокарда, осложненным кардиогенным шоком». JAMA. 294 (4): 448–54. Дои:10.1001 / jama.294.4.448. PMID 16046651.
- ^ Таунсенд, Кортни М .; Beauchamp D.R .; Evers M.B .; Маттокс К.Л. (2004). Учебник хирургии Сабистона - Биологические основы современной хирургической практики. Филадельфия, Пенсильвания: Elsevier Saunders. п. 1871 г. ISBN 0-7216-0409-9.
- ^ Каул Т.К., Филдс Б.Л., Риггинс С.Л., Дакумос Г.К., Вятт Д.А., Джонс С.Р. (1995). «Аортокоронарное шунтирование в течение 30 дней после острого инфаркта миокарда». Анна. Грудной. Surg. 59 (5): 1169–76. Дои:10.1016/0003-4975(95)00125-5. PMID 7733715.
- ^ Кресвелл Л.Л., Моултон М.Дж., Кокс Д.Л., Розенблум М. (1995). «Реваскуляризация после острого инфаркта миокарда». Анна. Грудной. Surg. 60 (1): 19–26. Дои:10.1016 / с0003-4975 (95) 00351-7. PMID 7598589.
- ^ Белый HD, Ассманн С.Ф., Санборн Т.А. и др. (2005). «Сравнение чрескожного коронарного вмешательства и аортокоронарного шунтирования после острого инфаркта миокарда, осложненного кардиогенным шоком: результаты исследования« Должны ли мы срочно реваскуляризовать окклюзированные коронарные сосуды для кардиогенного шока (ШОК) »». Тираж. 112 (13): 1992–2001. Дои:10.1161 / CIRCULATIONAHA.105.540948. PMID 16186436.
- ^ Хохман Дж. С., Слипер Л. А., Уэбб Дж. Г., Дзавик В., Буллер К. Э., Эйлуорд П., Кол Дж., Белый HD (2006). «Ранняя реваскуляризация и длительная выживаемость при кардиогенном шоке, осложнившем острый инфаркт миокарда». JAMA. 295 (21): 2511–5. Дои:10.1001 / jama.295.21.2511. ЧВК 1782030. PMID 16757723.
- ^ Раджа С.Г., Хайдер З., Ахмад М., Заман Х. (2004). «Трансплантаты подкожной вены: использовать или не использовать?». Сердце легкого Circ. 13 (4): 403–9. Дои:10.1016 / j.hlc.2004.04.004. PMID 16352226.
- ^ Ханнан Э.Л., Рач М.Дж., Уолфорд Дж. И др. (2005). «Отдаленные результаты коронарного шунтирования по сравнению с имплантацией стента». N. Engl. J. Med. 352 (21): 2174–83. Дои:10.1056 / NEJMoa040316. PMID 15917382. S2CID 18308025.
- ^ а б Бурасса М.Г. (2000). «Клинические испытания коронарной реваскуляризации: коронарная ангиопластика против коронарного шунтирования». Curr. Мнение. Кардиол. 15 (4): 281–6. Дои:10.1097/00001573-200007000-00013. PMID 11139092. S2CID 36950994.
- ^ Хлатки М.А., Бутройд Д.Б., Мелсоп К.А. и др. (2004). «Медицинские расходы и качество жизни от 10 до 12 лет после рандомизации к ангиопластике или шунтированию по поводу многососудистой коронарной болезни». Тираж. 110 (14): 1960–6. Дои:10.1161 / 01.CIR.0000143379.26342.5C. PMID 15451795.
- ^ Османчик П.П., Строс П., Герман Д. (2008). «Госпитальные аритмии у пациентов с острым инфарктом миокарда - отношение к стратегии реперфузии и их прогностическое влияние». Острый уход за картой. 10 (1): 15–25. Дои:10.1080/17482940701474478. PMID 17924228. S2CID 24957172.
- ^ Далзелл-младший, Джексон К.Э. (апрель 2009 г.). «Когда ритм ставит диагноз». J Emerg Med. 41 (2): 182–4. Дои:10.1016 / j.jemermed.2009.02.028. PMID 19345050.
