Транскраниальный допплер - Transcranial Doppler - Wikipedia
| Транскраниальный допплер | |
|---|---|
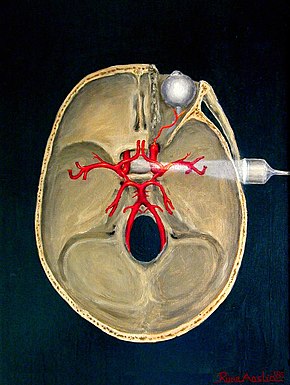 Транскраниальное допплеровское зондирование мозгового кровообращения | |
| Синонимы | Транскраниальный цветной допплер |
| МКБ-9-СМ | 88.71 |
| MeSH | D017585 |
| LOINC | 24733-8, 39044-3, 30880-9 |
Транскраниальный допплер (TCD) и транскраниальный цветной допплер (TCCD) являются типами Допплерография которые измеряют скорость кровоток сквозь мозг с кровеносный сосуд измеряя эхо УЗИ волны, движущиеся транскраниально (через череп ). Эти способы медицинская визуализация проводят спектральный анализ принимаемых акустических сигналов и поэтому могут быть классифицированы как методы активного акустоцеребрография. Они используются как тесты чтобы помочь диагностировать эмболы, стеноз, вазоспазм из субарахноидального кровоизлияние (кровотечение из разорванной аневризма ) и другие проблемы. Популярность этих относительно быстрых и недорогих тестов растет.[нужна цитата ] Тесты эффективны для обнаружения серповидноклеточная анемия, ишемический цереброваскулярные заболевания, субарахноидальное кровоизлияние, артериовенозные мальформации, и остановка мозгового кровообращения. Возможно, тесты будут полезны для периоперационный мониторинг и менингеальная инфекция.[1] Оборудование, используемое для этих тестов, становится все более портативным, что позволяет клиницисту ездить в больницу, в кабинет врача или в дом престарелых как для стационарных, так и для амбулаторных исследований. Эти тесты часто используются вместе с другими тестами, такими как МРТ, MRA, сонная артерия дуплекс УЗИ и Компьютерная томография. Тесты также используются для исследований в когнитивная нейробиология (см. Функциональный транскраниальный допплер, ниже).
Методы
Для этой процедуры можно использовать два метода записи. Первое использование Визуализация в "B-режиме", который отображает двумерное изображение черепа, головного мозга и кровеносных сосудов, как видно УЗИ зонд. Однажды желаемое кровеносный сосуд обнаружена, скорость кровотока может быть измерена с помощью импульсного Эффект Допплера зонд, который отображает скорость во времени. Вместе они составляют дуплексный тест. Второй метод регистрации использует только функцию второго датчика, вместо этого полагаясь на подготовку и опыт врача в поиске правильных сосудов. Современные машины TCD всегда допускают оба метода.[нужна цитата ]
Как это устроено
Ультразвуковой датчик излучает высокочастотную звуковую волну (обычно кратную 2 МГц ), который отскакивает от различных веществ в организме. Эти эхо обнаруживаются датчиком в зонде. В случае крови в артерия, эхо-сигналы имеют разные частоты в зависимости от направления и скорости кровотока из-за Эффект Допплера.[2]Если кровь удаляется от зонда, то частота эха ниже, чем частота излучаемого; если кровь движется к зонду, то частота эха выше, чем частота испускания. Эхо-сигналы анализируются и преобразуются в скорости, которые отображаются на мониторе компьютера устройства. Фактически, поскольку на зонд подается импульсная частота до 10 кГц, информация о частоте отбрасывается из каждого импульса и восстанавливается по фазовым изменениям от одного импульса к другому.
Потому что кости череп блокируют большую часть передачи ультразвука, для анализа необходимо использовать области с более тонкими стенками (так называемые окна озвучивания), которые обеспечивают наименьшее искажение звуковых волн. По этой причине запись ведется во временной области выше скула /скуловая дуга через глаза, под челюстью и с затылка. Возраст, пол, раса и другие факторы пациента влияют на толщину и пористость кости, что затрудняет или даже делает некоторые обследования невозможными. Большинство из них все еще может быть выполнено для получения приемлемых ответов, иногда требуя использования альтернативных участков для обзора судов.
Имплантируемый транскраниальный допплер
Иногда история болезни пациента и клинические признаки указывают на очень высокий риск инсульта. Окклюзионный удар вызывает необратимое повреждение тканей в течение следующих трех часов (возможно, даже 4,5 часов).[3]), но не сразу. Различные препараты (например, аспирин, стрептокиназа и активатор тканевого плазминогена (TPA) в порядке возрастания эффективности и стоимости)[4][5][6] может полностью изменить ход хода. Проблема в том, как сразу узнать, что случился инсульт. Одним из возможных способов является использование имплантируемого транскраниального допплеровского устройства, «оперативно связанного с системой доставки лекарств».[7] Работая от батареи, он будет использовать радиочастотную связь с портативным компьютером, выполняющим процедуру спектрального анализа вместе с данными от оксиметра (мониторинг степени оксигенации крови, которую может нарушить инсульт), чтобы принять автоматическое решение о введении препарата.
Функциональный транскраниальный допплер (fTCD)
Функциональная транскраниальная допплерография (fTCD) - это инструмент нейровизуализации для измерения изменений скорости мозгового кровотока из-за активации нейронов во время когнитивных задач.[8]Функциональная ТКД использует технологию пульсово-волнового допплера для регистрации скорости кровотока в передней, средней и задней церебральных артериях. Подобно другим методам нейровизуализации, таким как функциональная магнитно-резонансная томография (фМРТ) и позитронно-эмиссионная томография (ПЭТ), fTCD основан на тесной связи между региональными изменениями мозгового кровотока и нервной активацией. Благодаря постоянному мониторингу скорости кровотока, TCD предлагает лучшее временное разрешение, чем фМРТ и ПЭТ. Техника неинвазивна и проста в применении. Измерения скорости кровотока устойчивы к артефактам движения. С момента своего появления этот метод внес значительный вклад в выяснение полушарной организации когнитивных, моторных и сенсорных функций у взрослых и детей.[9][10]fTCD использовался для изучения церебральной латерализации основных функций мозга, таких как речь,[11][12][13]обработка лица,[14]обработка цвета,[15]и интеллект.[16]Более того, большинство установленных нейроанатомических субстратов для функции мозга перфузируются основными церебральными артериями, которые могут быть напрямую озвучены. Наконец, fTCD использовался как интерфейс мозг-компьютер модальность.[17]
Функциональная транскраниальная доплеровская спектроскопия (fTCDS)
Этот раздел может требовать уборка встретиться с Википедией стандарты качества. Конкретная проблема: слишком плотный и техничный (Сентябрь 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
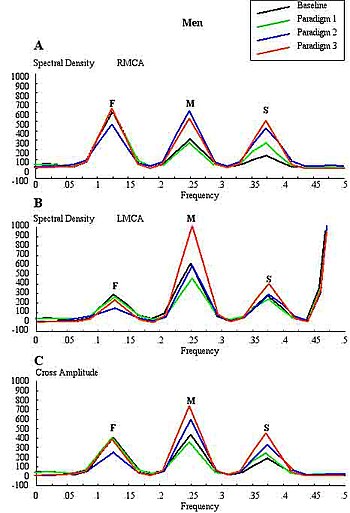
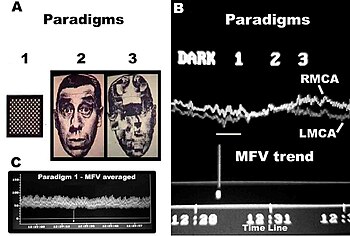
Обычный FTCD имеет ограничения для изучения церебральной латерализации. Например, он может не отличать латерализующие эффекты, обусловленные характеристиками стимула, от эффектов, обусловленных световой реакцией, и не различает сигналы потока, исходящие от корковых и подкорковых ветвей церебральных артерий Виллизиевского круга. Каждая базальная мозговая артерия Виллизиева круга дает начало двум различным системам вторичных сосудов. Более короткий из этих двух называется ганглиозной системой, и принадлежащие ей сосуды снабжают таламус и полосатые тела; чем длиннее кортикальная система, а ее сосуды разветвляются в мягкой мозговой оболочке и снабжают кору и находящееся под ней вещество мозга. Кроме того, корковые ветви делятся на два класса: длинные и короткие. Длинные или мозговые артерии проходят через серое вещество и проникают в нижележащее белое вещество на глубину 3–4 см. Короткие сосуды ограничены корой. И корковые, и ганглиозные системы не взаимодействуют ни в какой точке своего периферического распределения, но полностью независимы друг от друга, имея между частями, снабжаемыми двумя системами, границу снижения питательной активности.[18] В то время как сосуды ганглиозной системы являются конечными сосудами, сосуды корковой артериальной системы не так строго «конечны». Кровоток в этих двух системах на территории средней мозговой артерии (СМА) снабжает 80% обоих полушарий,[19] включая большинство нейронных субстратов, участвующих в обработке лица, речи и интеллекта в корковых и подкорковых структурах. Измерения средней скорости кровотока (MFV) в главном стволе СМА могут потенциально предоставить информацию об изменениях ниже по течению в корковых и подкорковых участках в пределах территории СМА. Каждое дистальное плечо сосудистой системы MCA можно разделить на «ближние» и «дальние» дистальные участки отражения для корковой и ганглионарной (подкорковой) систем соответственно. Для достижения этой цели можно применить Анализ Фурье к периодическим временным рядам MFV, полученным во время когнитивных стимуляций. Анализ Фурье даст пики, представляющие пульсирующую энергию от мест отражения на различных гармониках, которые кратны основной частоте.[20][21] Макдональд в 1974 году показал, что первые пять гармоник обычно содержат 90% всей пульсирующей энергии в системе колебаний давления / потока в периферической циркуляции. Можно предположить, что каждое плечо сосудистой системы представляет собой одну вязкоупругую трубку, оканчивающуюся импедансом, создающую единое место отражения.[22] Психофизиологическая стимуляция, вызванная вазомоторной активностью в каждом терминальном участке, вызывает колебание стоячей синусоидальной волны, состоящее из суммирования волн из-за эффектов падающих, отраженных и повторно отраженных волн от дистальной к проксимальной точке измерения. Исследования fTCDS проводятся с участником, находящимся в положении лежа на спине с поднятой головой примерно на 30 градусов. Головной убор с держателем зонда (например, LAM-RAK, DWL, Sipplingen, Германия) используется с базовой опорой на двух затычках для ушей и на носовом гребне. Два зонда с частотой 2 МГц закрепляются в держателе зонда, и выполняется озвучивание для определения оптимального положения для непрерывного мониторинга обоих основных стержней MCA на глубине 50 мм от поверхности зонда. Производится серийная запись MFV для каждого стимула, которая используется для анализа Фурье. преобразование Фурье алгоритм использует стандартное программное обеспечение (например, модуль временных рядов и прогнозирования, СТАТИСТИКА, StatSoft, Inc. ). Наиболее эффективный стандартный алгоритм Фурье требует, чтобы длина входного ряда была равна степени 2. Если это не так, необходимо выполнить дополнительные вычисления. Чтобы получить требуемый временной ряд, данные были усреднены по 10-секундным сегментам для 1-минутной продолжительности или каждого стимула, что дало 6 точек данных для каждого участника и в общей сложности 48 точек данных для всех восьми мужчин и женщин, соответственно. Сглаживание значений периодограммы осуществлялось с помощью преобразования взвешенного скользящего среднего. Окно Хэмминга применялось как сглаживание.[23][24] Были нанесены оценки спектральной плотности, полученные из анализа Фурье отдельных серий, и области частот с наивысшими оценками были отмечены как пики. Происхождение пиков представляет интерес для определения надежности настоящего метода. Основной (F), корковый (C) или пики памяти (M) и подкорковые (S) пики возникали с регулярными частотными интервалами 0,125, 0,25 и 0,375 соответственно. Эти частоты можно было преобразовать в Гц, если предположить, что основная частота сердечных колебаний была средней частотой сердечных сокращений. Основная частота (F) первой гармоники может быть определена из средней частоты сердечных сокращений в секунду. Например, частота сердечных сокращений 74 удара в минуту предполагает 74 цикла / 60 или 1,23 Гц. Другими словами, F-, C- и S-пики возникли на частотах, кратных первой гармонике, на второй и третьей гармониках соответственно. Можно предположить, что расстояние до места отражения для F-пика исходит от места в D1 = длина волны / 4 = cf / 4 = 6,15 (м / с) / (4 × 1,23 Гц) = 125 см, где c - предполагаемая скорость распространения волны периферического артериального дерева согласно McDonald, 1974. Учитывая извитость сосудов, расчетное расстояние приблизительно соответствует расстоянию от места измерения в основной штанге MCA до воображаемого места суммированных отражений от верхних конечностей, близко к кончикам пальцев при растяжении в стороны.[25] C-пик возник на второй гармонике, так что расчетная длина артерии (с использованием общей сонной артерии = 5,5 м / с)[26] было дано D2 = длина волны / 8 = cf2/ 8 = 28 см, а частота f равна 2,46 Гц. Расстояние приблизительно соответствует видимой длине артерии от основного ствола СМА через извитость сосудов и вокруг выпуклости головного мозга до концевых сосудов в дистальных отделах коры головного мозга, таких как затылочно-височное соединение на каротидных ангиограммах взрослых.[25] S-пик возник на третьей гармонике и, возможно, возник в предполагаемом месте в D3= длина волны / 16 = cf3/ 16 = 9,3 см и частота f3 3,69 Гц. Последняя аппроксимирует видимую артериальную длину лентикулостриарных сосудов от основного ствола СМА на каротидных ангиограммах.[27] Хотя это и не отображается, четвертая гармоника может возникнуть в результате разветвления MCA в непосредственной близости от места измерения в главном стержне MCA. Длина предбифуркации от точки измерения будет равна D4 = длина волны / 32 = cf4/ 32 = 3,5 см и частота f4 4,92 Гц. Рассчитанное расстояние приблизительно соответствует расстоянию от сегмента основной ножки СМА сразу после бифуркации сонной артерии, где, вероятно, был помещен объем ультразвукового образца, до разветвления СМА. Таким образом, эти оценки являются приблизительными фактическими длинами. Однако было высказано предположение, что расчетные расстояния могут не точно коррелировать с известными морфометрическими размерами артериального дерева согласно Кэмпбеллу и др., 1989. Метод был впервые описан Филипом Нджеманзе в 2007 году и был назван функциональным транскраниальным допплером. спектроскопия (fTCDS).[25] fTCDS исследует оценки спектральной плотности периодических процессов, вызываемых умственными задачами, и, следовательно, предлагает гораздо более полную картину изменений, связанных с воздействием данного умственного стимула. На оценки спектральной плотности в наименьшей степени будут влиять артефакты, у которых отсутствует периодичность, а фильтрация уменьшит влияние шума.[28] Изменения на C-пике могут указывать на долгосрочный потенциал коры головного мозга (CLTP) или долгосрочную депрессию коры головного мозга (CLTD), что было предложено в качестве эквивалента активности коры во время обучения.[25] и когнитивные процессы. Отслеживание скорости потока отслеживается во время парадигмы 1, содержащей квадрат шахматной доски, поскольку восприятие объекта сравнивается с целым лицом (парадигма 2) и задачей сортировки лицевых элементов (парадигма 3). Расчеты быстрого преобразования Фурье используются для получения графиков спектральной плотности и кросс-амплитуды в левой и правой средних мозговых артериях. С-пик, также называемый кортикальным пиком памяти (М-пик), можно увидеть, возникающий во время парадигмы 3, задачи сортировки лицевых элементов, требующей повторного вызова памяти, поскольку субъект постоянно пространственно вписывается в головоломку, сопоставляя каждый лицевой элемент в парадигме 3 с сохраненным в памяти (Парадигма 2) перед тем, как приступить к формированию картины всего лица.
Точность
Хотя TCD не так точен из-за относительной скорости кровотока, он все же полезен для диагностики артериальных окклюзий у пациентов с острым ишемическим инсультом, особенно для средней мозговой артерии. Было проведено исследование для сравнения Power Motion Doppler TCD (PMD-TCD) с CT. ангиография (CTA), оба действительны, но точность PMD-TCD не превышает 85 процентов. Преимущества PMD-TCD - портативный, поэтому его можно использовать в постели или в отделении неотложной помощи, без облучения, как CTA, поэтому его можно повторять, если необходимо для мониторинга, и он дешевле, чем CTA или магнитно-резонансная ангиография.[29]
Смотрите также
Рекомендации
- ^ «Транскраниальный допплер: обзор его клинического применения». Архивировано из оригинал 25 апреля 2015 г.. Получено 3 июня, 2013.
- ^ «Как работает ультразвук». Получено 11 сентября, 2015.
- ^ ДеНун, Дэниел Дж. (2009). Немедленное лечение Лучшее, но даже позднее лечение с помощью tPA может помочь. Новости здоровья WebMD.
- ^ HP Adams Jr, BH Bendixen, LJ Kappelle, J Biller, BB Love, DL Gordon и EE Marsh 3d (1993). «Классификация подтипа острого ишемического инсульта. Определения для использования в многоцентровом клиническом исследовании. TOAST. Испытание Org 10172 в лечении острого инсульта». Гладить. 24 (1): 35–41. Дои:10.1161 / 01.STR.24.1.35. PMID 7678184.CS1 maint: несколько имен: список авторов (связь)
- ^ «Рандомизированное контролируемое исследование стрептокиназы, аспирина и их комбинации в лечении острого ишемического инсульта. Многоцентровое исследование острого инсульта - Италия (MAST-I) Группа». Ланцет. 346 (8989): 1509–14. 1995. Дои:10.1016 / с0140-6736 (95) 92049-8. PMID 7491044.
- ^ Zeumer, H; Freitag, HJ; Занелла, Ф; Thie, A; Арнинг, С. (1993). «Местная внутриартериальная фибринолитическая терапия у пациентов с инсультом: урокиназа против рекомбинантного тканевого активатора плазминогена (r-TPA)». Нейрорадиология. 35 (2): 159–62. Дои:10.1007 / bf00593977. PMID 8433796.
- ^ Нджеманзе, Филип Чиди (2003). Имплантируемый телеметрический транскраниальный допплеровский аппарат. Патент США 6,468,219.
- ^ Душек, С; Шандри, Р. (2003). «Функциональная транскраниальная допплерография как инструмент психофизиологических исследований». Психофизиология. 40 (3): 436–454. Дои:10.1111/1469-8986.00046. PMID 12946117.
- ^ Строобант, Н; Vingerhoets, G (2000). «Транскраниальный допплерографический мониторинг церебральной гемодинамики при выполнении когнитивных задач: обзор». Обзор нейропсихологии. 10 (4): 213–231. Дои:10.1023 / А: 1026412811036. PMID 11132101.
- ^ Блтон, Н; Перера, S; Сейдич, Э (2016). «Когнитивные задачи и церебральный кровоток через передние мозговые артерии: исследование с помощью функциональных транскраниальных записей ультразвукового допплера». BMC Medical Imaging. 16: 22–1–22–12. Дои:10.1186 / s12880-016-0125-0. ЧВК 4788871. PMID 26969112.
- ^ Колер М., Кейдж Х. А. Д., Спунер Р., Флиттон А., Хофманн Дж., Чёрчерс О. Ф. и др. (2015). «Вариабельность реакции латерализованного кровотока на язык связана с языковым развитием у детей в возрасте 1–5 лет». Обзор нейропсихологии. 145–146: 34–41. Дои:10.1016 / j.bandl.2015.04.004. PMID 25950747.CS1 maint: использует параметр авторов (связь)
- ^ Knecht, S .; Деппе, М; Dräger, B; Бобе, L; Ломанн, Н; Рингельштейн, Э; Хеннингсен, Х (2000). «Латерализация языка у здоровых правшей». Мозг. 123: 74–81. Дои:10.1093 / мозг / 123.1.74. PMID 10611122.
- ^ Njemanze, PC (1991). «Церебральная латерализация в языковом и нелингвистическом восприятии: анализ когнитивных стилей в слуховой модальности». Мозг и язык. 41 (3): 367–80. Дои:10.1016 / 0093-934х (91) 90161-с. PMID 1933263.
- ^ Нджеманзе, PC (2004). «Асимметрия скорости мозгового кровотока при обработке изображений лица во время отдыха головой вниз» (PDF). Авиация, космос и экологическая медицина. 75 (9): 800–5. PMID 15460633.
- ^ Njemanze, PC; Гомес, CR; Хоренштейн, S (1992). «Церебральная латерализация и восприятие цвета: транскраниальное допплеровское исследование». Кора. 28 (1): 69–75. Дои:10.1016 / s0010-9452 (13) 80166-9. PMID 1572174.
- ^ Нджеманзе, PC (2005). «Церебральная латерализация и общий интеллект: гендерные различия в транскраниальном допплеровском исследовании» (PDF). Мозг и язык. 92 (3): 234–9. CiteSeerX 10.1.1.532.5734. Дои:10.1016 / j.bandl.2004.06.104. PMID 15721956.
- ^ Мирден, А; Кушки, А; Сейдич, Э; Гергерский, А-М; Чау, Т. (2011). «Интерфейс мозг-компьютер на основе двустороннего транскраниального допплера». PLoS ONE. 6 (9): e24170–1–8. Bibcode:2011PLoSO ... 624170M. Дои:10.1371 / journal.pone.0024170. ЧВК 3168473. PMID 21915292.
- ^ Грей Х. и Клементе К. Д. (1984). Анатомия человеческого тела Грея. 30-е американское издание .Филадельфия: Липпинкотт Уильямс и Уилкинс.
- ^ Тул, Дж. Ф. (1990). Цереброваскулярные нарушения. Нью-Йорк: Raven Press.
- ^ Макдональд, Д. А. (1974). Кровоток в артериях с. 311–350. Балтимор: Williams & Wilkins Co.
- ^ Нджеманзе, П. К., Бек, О. Дж., Гомес, К. Р., и Хоренштейн, С. (1991). «Фурье-анализ цереброваскулярной системы». Гладить. 22 (6): 721–726. Дои:10.1161 / 01.STR.22.6.721. PMID 2057969.CS1 maint: несколько имен: список авторов (связь)
- ^ Кэмпбелл, К. Б., Ли, Л. С., Фраш, Х. Ф., & Noordergraaf, А. (1989). «Места отражения импульсов и эффективная длина артериальной системы». Американский журнал физиологии. 256 (6, часть 2): H1684 – H1689. Дои:10.1152 / ajpheart.1989.256.6.H1684. PMID 2735437.CS1 maint: несколько имен: список авторов (связь)
- ^ Питер Блумфилд (1 апреля 2004 г.). Фурье-анализ временных рядов: введение. Wiley-IEEE. ISBN 978-0-471-65399-8. Получено 22 октября 2011.
- ^ Бригам, Э. О. (1974). Быстрое преобразование Фурье. Нью-Йорк: Прентис-Холл.
- ^ а б c d Нджеманзе, PC (2007). «Церебральная латерализация для обработки лица: когнитивные стили, связанные с полом, определенные с использованием анализа Фурье средней скорости мозгового кровотока в средних церебральных артериях» (PDF). Латеральность. 12 (1): 31–49. Дои:10.1080/13576500600886796. PMID 17090448.
- ^ Майндерс, Дж. М.; Корнет, Л; Бренды, PJ; Хукс, AP (2001). «Оценка локальной скорости пульсовой волны в артериях с использованием 2D кривых растяжения». Ультразвуковая визуализация. 23 (4): 199–215. Дои:10.1177/016173460102300401. PMID 12051275.
- ^ Канг, HS; Хан, MH; Квон, Би Джей; Квон, хорошо; Kim, SH; Чанг, К. Х. (2005). «Оценка лентикулостриарных артерий с ротационной ангиографией и 3D реконструкцией». AJNR. Американский журнал нейрорадиологии. 26 (2): 306–12. PMID 15709128.
- ^ Ньеманзе П.С., Транскраниальная допплеровская спектроскопия для оценки когнитивных функций мозга. Патент США 20,040,158,155, 12 августа 2004 г.
- ^ Алехандро М. Брунсер, доктор медицины; Пабло М. Лавадос, доктор медицины; Арнольд Хоппе, доктор медицины; Хавьера Лопес, доктор медицины; Марсела Валенсуэла, доктор медицины; Родриго Ривас, доктор медицины. «Точность транскраниального допплера по сравнению с КТ-ангиографией в диагностике артериальной обструкции при остром ишемическом инсульте» (PDF). Получено 2 апреля, 2015.
