Ацилирование - Acylation
В химия, ацилирование (или алканоилирование) - это процесс добавления ацил группа в соединение. Соединение, обеспечивающее ацильную группу, называется ацилирующий агент.
Потому что они образуют сильную электрофил при обработке некоторым металлом катализаторы, ацилгалогениды обычно используются в качестве ацилирующих агентов. Например, Ацилирование Фриделя-Крафтса использует ацетилхлорид (этаноилхлорид), CH3COCl, в качестве агента и хлорид алюминия (AlCl3) в качестве катализатора для добавления этаноила (ацетил ) группа в бензол:
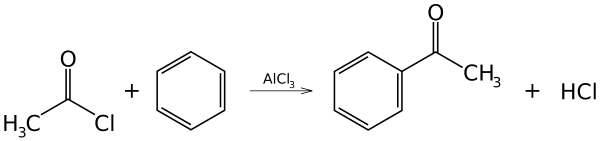
Механизм этой реакции электрофильное ароматическое замещение.
Ацилгалогениды и ангидриды из карбоновые кислоты также обычно используются ацилирующие агенты. В некоторых случаях, активные эфиры демонстрируют сопоставимую реактивность. Все реагируют с амины формировать амиды и спирты формировать сложные эфиры к нуклеофильное ацильное замещение.
Ацилирование можно использовать для предотвращения реакции перегруппировки это обычно происходит в алкилирование. Для этого проводят реакцию ацилирования, затем карбонил удаляют путем Редукция Клемменсена или аналогичный процесс.[1]
Ацилирование в биологии
Ацилирование белков - это посттрансляционная модификация белков за счет присоединения функциональные группы через ацильные связи. Ацилирование белков наблюдалось как механизм, контролирующий передачу биологических сигналов.[2] Одним из наиболее заметных типов является ацилирование жирных кислот, добавление жирных кислот к определенным аминокислотам (например, миристоилирование, пальмитоилирование или же пальмитолеоилирование ).[3] В глобальном ацилировании белка участвуют различные типы жирных кислот.[4] Пальмитолеоилирование - это тип ацилирования, при котором мононенасыщенная жирная кислота пальмитолеиновая кислота ковалентно присоединяется к сериновым или треониновым остаткам белков.[5][6] Пальмитолеоилирование, по-видимому, играет важную роль в торговле, нацеливании и функционировании Wnt белки.[7][8]
Смотрите также
Рекомендации
- ^ Воллхардт, Питер; Шор, Нил (2014). Органическая химия: структура и функции (7-е изд.). Нью-Йорк, штат Нью-Йорк: W.H. Фримен и компания. С. 714–715. ISBN 978-1-4641-2027-5.
- ^ Towler, D.A.; Гордон, Дж. Я; Адамс, С. П.; Глейзер, L (1988). «Биология и энзимология ацилирования эукариотических белков». Ежегодный обзор биохимии. 57 (1): 69–97. Дои:10.1146 / annurev.bi.57.070188.000441. PMID 3052287.
- ^ Реш, М. Д. (1999). «Жировое ацилирование белков: новый взгляд на мембранную направленность миристоилированных и пальмитоилированных белков». Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1451 (1): 1–16. Дои:10.1016 / S0167-4889 (99) 00075-0. PMID 10446384.
- ^ Мохаммадзаде, Фатемех; Хоссейни, Вахид; Мехдизаде, Амир; Дэни, Кристиан; Дараби, Масуд (2019). «Метод общего анализа ацилирования белков методом газожидкостной хроматографии». IUBMB Life. 71 (3): 340–346. Дои:10.1002 / iub.1975. ISSN 1521-6551. PMID 30501005.
- ^ Ханнуш, Рами Н. (октябрь 2015 г.). «Липидирование синтетических белков». Современное мнение в области химической биологии. 28: 39–46. Дои:10.1016 / j.cbpa.2015.05.025. ISSN 1879-0402. PMID 26080277.
- ^ Пелегри, Франсиско; Данильчик, Михаил; Сазерленд, Энн (13 декабря 2016 г.). Развитие позвоночных: от матери до зиготического контроля. Чам, Швейцария. ISBN 9783319460956. OCLC 966313034.
- ^ Хоссейни, Вахид; Дэни, Кристиан; Геранмайе, Мохаммад Хоссейн; Мохаммадзаде, Фатемех; Назари Солтан Ахмад, Саид; Дараби, Масуд (20.10.2018). «Липидация Wnt: роль в торговле, модуляции и функции». Журнал клеточной физиологии. 234 (6): 8040–8054. Дои:10.1002 / jcp.27570. ISSN 1097-4652. PMID 30341908.
- ^ Нил, Аарон Х .; Ханнуш, Рами Н. (февраль 2016 г.). «Жировое ацилирование белков Wnt». Природа Химическая Биология. 12 (2): 60–69. Дои:10.1038 / nchembio.2005. ISSN 1552-4469. PMID 26784846.
