Трифторид мышьяка - Arsenic trifluoride
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Фторид мышьяка (III) | |||
| Другие имена Трифторид мышьяка, трифторарсан | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.145 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| AsF3 | |||
| Молярная масса | 131,9168 г / моль | ||
| Внешность | бесцветная жидкость | ||
| Плотность | 2,666 г / см3[1] | ||
| Температура плавления | -8,5 ° С (16,7 ° F, 264,6 К) | ||
| Точка кипения | 60,4 ° С (140,7 ° F, 333,5 К) | ||
| разлагается | |||
| Растворимость | растворим в алкоголь, эфир, бензол и аммиак решение | ||
| Опасности | |||
| Главный опасности | Токсичный, коррозионный | ||
| Пиктограммы GHS |  | ||
| Сигнальное слово GHS | Опасность | ||
| H301, H311, H331 | |||
| P261, P264, P270, P271, P280, P301 + 310, P302 + 352, P304 + 340, P311, P312, P321, P322, P330, P361, P363, P403 + 233, P405, P501 | |||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | [1910.1018] TWA 0,010 мг / м3[2] | ||
REL (Рекомендуемые) | Ca C 0,002 мг / м3 [15 минут][2] | ||
IDLH (Непосредственная опасность) | Ca [5 мг / м3 (как As)][2] | ||
| Термохимия | |||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -821,3 кДж / моль | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
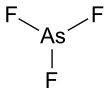
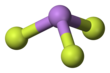
Трифторид мышьяка это химическое соединение из мышьяк и фтор с химической формулой AsF3. Это бесцветная жидкость, легко вступающая в реакцию с водой.[3]
Подготовка и свойства
Его можно приготовить, реагируя фтороводород, ВЧ, с триоксид мышьяка:[3]
- 6HF + As2О3 → 2AsF3 + 3H2О
Он имеет пирамидальную молекулярную структуру в газовой фазе, которая также присутствует в твердом теле.[3] В газовой фазе длина связи As-F составляет 170,6 пм, а валентный угол F-As-F 96,2 °.[4]
Трифторид мышьяка используется в качестве фторирующих хлоридов неметаллов до фторидов, в этом отношении он менее реакционноспособен, чем SbF.3.[3]
Соли, содержащие AsF4− анион можно получить, например, CsAsF4.[5] калиевая соль КА2F7 приготовлено из KF и AsF3 содержит AsF4− и AsF3 молекулы с признаками взаимодействия между AsF3 молекула и анион.[6]
AsF3 реагирует с SbF5. Полученный продукт можно описать как ионный аддукт AsF2+ SbF6−. Однако авторы приходят к выводу, что образовавшийся продукт нельзя рассматривать только как ионное соединение или полностью как нейтральный аддукт AsF.3SbF5. Кристаллическая структура образованного соединения демонстрирует характеристики как ионной пары, так и структурных мотивов нейтрального аддукта, занимая промежуточное положение между обеими моделями описания молекул. [7]
Рекомендации
- ^ Прадёт Патнаик. Справочник неорганических химикатов. Макгроу-Хилл, 2002 г., ISBN 0-07-049439-8
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0038". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б c d Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Уэллс А.Ф. (1984) Структурная неорганическая химия 5-е издание Oxford Science Publications ISBN 0-19-855370-6
- ^ Новые тетрафторарсенаты щелочных металлов и тетраметиламмония (III), их колебательные спектры и кристаллическая структура тетрафторарсената цезия (III) Клампфер П., Бенкич П., Лесар А., Волавшек Б., Пониквар М., Йесих А., Collect. Чешский. Chem. Commun. 2004, 69, 339-350 Дои:10.1135 / cccc20040339
- ^ Гептафтордиарсенаты щелочных металлов (III): их получение и кристаллическая структура калиевой соли, Edwards A.J., Patel S.N., J. Chem. Soc., Dalton Trans., 1980, 1630-1632, Дои:10.1039 / DT9800001630
- ^ Кристаллические структуры фторидов. Часть XV. Трифторид мышьяка – пентафторид сурьмы, Edwards A. J., Sills R. J. C. J. Chem. Soc. А, 1971 г., 942 - 945, Дои:10.1039 / J19710000942