Динамическое равновесие - Dynamic equilibrium
В химия, И в физика, а динамическое равновесие существует однажды обратимая реакция происходит. Вещества переходят между реагентами и продуктами с одинаковой скоростью, что означает отсутствие чистых изменений. Реагенты и продукты образуются с такой скоростью, что их концентрация не меняется. Это частный пример системы в устойчивое состояние. В термодинамика, а закрытая система в термодинамическое равновесие когда реакции происходят с такой скоростью, что состав смеси не меняется со временем. Реакции действительно происходят, иногда бурно, но до такой степени, что изменения в составе невозможно наблюдать. Константы равновесия могут быть выражены через константы скорости обратимых реакций.
Примеры
В новой бутылке газировки концентрация углекислый газ в жидкой фазе имеет особое значение. Если вылить половину жидкости и закрыть бутылку, углекислый газ будет выходить из жидкой фазы с постоянно уменьшающейся скоростью, и частичное давление диоксида углерода в газовой фазе будет увеличиваться до тех пор, пока не будет достигнуто равновесие. В этот момент из-за теплового движения молекула CO2 может покинуть жидкую фазу, но в течение очень короткого времени другая молекула CO2 перейдет из газа в жидкость и наоборот. При равновесии скорость переноса CO2 от газа к жидкой фазе равна скорости перехода от жидкости к газу. В этом случае равновесная концентрация CO2 в жидкости определяется выражением Закон Генри, который утверждает, что растворимость газа в жидкости прямо пропорциональна частичное давление этого газа над жидкостью.[1] Это отношение записывается как
куда k - константа, зависящая от температуры, п парциальное давление и c - концентрация растворенного газа в жидкости. Таким образом, парциальное давление CO2 газа увеличилось, пока не соблюдается закон Генри. Концентрация углекислого газа в жидкости снизилась, и напиток немного потерял газообразность.
Закон Генри можно вывести, установив химические потенциалы диоксида углерода в двух фазах равны друг другу. Равенство химического потенциала определяет химическое равновесие. Другие константы динамического равновесия, включающие фазовые изменения, включают: Коэффициент распределения и произведение растворимости. Закон Рауля определяет равновесие давление газа из идеальное решение
Динамическое равновесие может существовать и в однофазной системе. Простой пример происходит с кислотно-щелочной равновесие, такое как диссоциация уксусная кислота, в водном растворе.
- CH3CO2ЧАС CH3CO2− + H+
В состоянии равновесия концентрация частное K, то константа диссоциации кислоты, постоянно (при некоторых условиях)
В этом случае прямая реакция предполагает высвобождение некоторых протоны от молекул уксусной кислоты, и обратная реакция включает образование молекул уксусной кислоты, когда ацетат-ион принимает протон. Равновесие достигается, когда сумма химических потенциалов компонентов в левой части выражения равновесия равна сумме химических потенциалов компонентов в правой части. При этом скорости прямой и обратной реакции равны между собой. Равновесия с образованием химические комплексы также являются динамическими равновесиями, а концентрации регулируются константы устойчивости комплексов.
В газовой фазе также могут возникать динамические равновесия, например, когда диоксид азота димеризуется.
- 2НО2 N2О4;
В газовой фазе квадратные скобки указывают парциальное давление. В качестве альтернативы парциальное давление вещества можно записать как P (вещество).[2]
Связь между константами равновесия и скоростью
В простой реакции, такой как изомеризация:
необходимо рассмотреть две реакции: прямая реакция, в которой компонент A превращается в B, и обратная реакция, в которой B превращается в A. Если обе реакции элементарные реакции, то скорость реакции дан кем-то[3]
куда kж это константа скорости для прямой реакции и kб - константа скорости обратной реакции, квадратные скобки, [..] обозначают концентрация . Если в начале присутствует только A, время т= 0, с концентрацией [A]0, сумма двух концентраций, [A]т и [B]т, вовремя т, будет равно [A]0.
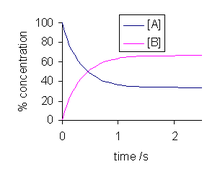
Решение этого дифференциального уравнения есть
и показан справа. Когда время стремится к бесконечности, концентрации [A]т и [B]т стремятся к постоянным значениям. Позволять т приближаются к бесконечности, то есть т→ ∞ в приведенном выше выражении:
На практике изменения концентрации невозможно измерить после . Поскольку после этого концентрации не меняются, они определение, равновесные концентрации. Теперь константа равновесия для реакции определяется как
Отсюда следует, что константа равновесия численно равна отношению констант скорости.
Как правило, это может быть более одной прямой реакции и более одной обратной реакции. Аткинс заявляет[4] что для общей реакции общая константа равновесия связана с константами скорости элементарных реакций соотношением
- .
Смотрите также
Рекомендации
Аткинс, P.W .; де Паула, Дж. (2006). Физическая химия (8-е изд.). Издательство Оксфордского университета. ISBN 0-19-870072-5.



![K_c = mathrm { frac {[CH_3CO_2 ^ -] [H ^ +]} {[CH_3CO_2H]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d49d8d7ac315ab55173bef33931a289f7471d638)
![{ displaystyle K_ {p} = mathrm { frac {[N_ {2} O_ {4}]} {[NO_ {2}] ^ {2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/80decc2ee0b634b53f773302e89bfcfbdf5d6fcc)

![frac {d [A]} {dt} = - k_f [A] _t + k_b [B] _t](https://wikimedia.org/api/rest_v1/media/math/render/svg/7b9dae97de8aca04a52600698bac66b295a3a234)
![frac {d [A]} {dt} = -k_f [A] _t + k_b left ([A] _0- [A] _t right)](https://wikimedia.org/api/rest_v1/media/math/render/svg/2afda28c6572264af0a80c5f3bb141cbc5a5fb8a)
![[A] _t = frac {k_b + k_fe ^ {- left (k_f + k_b right) t}} {k_f + k_b} [A] _0](https://wikimedia.org/api/rest_v1/media/math/render/svg/41477d519e2f9006e57aae00bb6e80de4b50640f)
![[A] _ infty = frac {k_b} {k_f + k_b} [A] _0; [B] _ infty = frac {k_f} {k_f + k_b} [A] _0](https://wikimedia.org/api/rest_v1/media/math/render/svg/7a11974608637eafa142d4c7aee65c56d96af964)

![K = frac {[B] _ {eq}} {[A] _ {eq}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/78dbaca6d95fad47ff4d24baee56d9eac377b72b)
![K = frac { frac {k_f} {k_f + k_b} [A] _0} { frac {k_b} {k_f + k_b} [A] _0} = frac {k_ {f}} {k_ {b} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/ff234cde522c7e054eed178f987a0acd19ba615e)
