Лабораторная диагностика вирусных инфекций - Laboratory diagnosis of viral infections
| Лабораторная диагностика вирусных инфекций | |
|---|---|
| Цель | тест на вирусную инфекцию |
В диагностической лаборатории вирус инфекции могут быть подтверждены множеством методов. Диагностическая вирусология быстро изменилась благодаря появлению молекулярных методов и повышенной клинической чувствительности серологических тестов.[1]
Отбор проб
Для вирусологического тестирования можно использовать самые разные образцы. Тип образца, отправляемого в лабораторию, часто зависит от типа диагностируемой вирусной инфекции и требуемого теста. Правильная техника отбора проб важна, чтобы избежать потенциальных преаналитических ошибок. Например, разные типы образцов необходимо собирать в соответствующие пробирки, чтобы сохранить целостность образца, и хранить при соответствующих температурах (обычно 4 ° C) для сохранения вируса и предотвращения роста бактерий или грибков. Иногда также может быть выбрано несколько сайтов.
Типы образцов включают:
- Мазок из носоглотки
- Кровь
- Кожа
- Мокрота, полоскания и бронхиальные промывания
- Моча
- Сперма
- Кал
- Спинномозговая жидкость
- Ткани (биопсия или же вскрытие )
- Засохшие пятна крови
- Носовая слизь на риновирус, например[2]
Изоляция вирусов
Вирусы часто выделяют из первоначальной выборки пациентов. Это позволяет увеличивать количество образцов вируса и запускать на них большее количество тестов. Это особенно важно для образцов, содержащих новые или редкие вирусы, диагностические тесты для которых еще не разработаны.
Многие вирусы можно выращивать в культура клеток в лаборатории. Для этого образец вируса смешивается с клетками. Этот процесс называется адсорбция, после чего клетки заражаются и производят новые копии вируса.[3] Хотя разные вирусы часто растут только в определенных типах клеток, существуют клетки, которые поддерживают рост большого количества различных вирусов и являются хорошей отправной точкой, например линия клеток почек африканских обезьян (Клетки Vero ), фибробласты легких человека (MRC-5 ) и клетки эпидермоидной карциномы человека (HEp-2 ). Одним из способов определения того, успешно ли клетки реплицируют вирус, является проверка изменения морфологии клеток или наличия вируса. смерть клетки с помощью микроскопа.
Для роста других вирусов могут потребоваться альтернативные методы, такие как инокуляция куриных яиц с эмбрионами (например, вирусы птичьего гриппа[4]) или внутричерепной инокуляции вируса с использованием новорожденных мышей (например, лиссавирусы[5]).
Методы на основе нуклеиновых кислот
Молекулярные методы являются наиболее специфическими и чувствительными диагностическими тестами.[6] Они способны обнаруживать либо весь вирусный геном, либо части вирусного генома. В прошлом тесты на нуклеиновую кислоту в основном использовались как вторичный тест для подтверждения положительных серологических результатов.[3] Однако по мере того, как они становятся более дешевыми и автоматизированными, они все чаще становятся основным инструментом диагностики.[3]
Полимеразной цепной реакции
Обнаружение вирусных РНК и ДНК геномов может быть выполнено с использованием полимеразной цепной реакции. Этот метод создает множество копий вирусного генома с помощью вирус-специфичных зондов. Варианты ПЦР, такие как вложенная ПЦР с обратной транскриптазой и ПЦР в реальном времени также может использоваться для определения вирусной нагрузки в сыворотке крови пациента. Это часто используется для отслеживания успеха лечения ВИЧ случаи.
Последовательность действий
Секвенирование - единственный диагностический метод, который позволяет получить полную последовательность вирусного генома. Следовательно, он предоставляет больше всего информации об очень небольших различиях между двумя вирусами, которые будут выглядеть одинаково при использовании других диагностических тестов. В настоящее время он используется только тогда, когда требуется такая глубина информации. Например, секвенирование полезно при тестировании конкретных мутаций у пациента с целью определения противовирусная терапия и восприимчивость к инфекции. Однако по мере того, как тесты становятся дешевле, быстрее и автоматизированнее, секвенирование, вероятно, станет основным диагностическим инструментом в будущем.
Методы на основе микроскопии
Иммунофлуоресценция или иммунопероксидаза
Иммунофлуоресценция или же иммунопероксидаза Анализы обычно используются для определения наличия вируса в образце ткани. Эти тесты основаны на том принципе, что если ткань инфицирована вирусом, антитело, специфичное к этому вирусу, сможет связываться с ним. Для этого к образцу ткани примешивают антитела, специфичные к разным типам вирусов. После того, как ткань подвергается воздействию света определенной длины волны или химического вещества, которое позволяет визуализировать антитело.
Для этих тестов требуются специализированные антитела, которые производятся и покупаются в коммерческих компаниях. Эти коммерческие антитела обычно хорошо охарактеризованы и, как известно, связываются только с одним конкретным типом вируса. Они также связаны со специальным типом метки, которая позволяет визуализировать антитело в лаборатории, то есть излучать флуоресценцию или цвет. Следовательно, иммунофлуоресценция относится к обнаружению флуоресцентных антител (иммуно), а иммунопероксидаза относится к обнаружению окрашенных антител (пероксидаза дает темно-коричневый цвет).
| Иммунофлуоресцентный анализ | Иммунопероксидазный анализ |
|---|---|
Электронная микроскопия
Электронная микроскопия - это метод, с помощью которого можно сфотографировать весь вирус и выявить его форму и структуру. Обычно он не используется в качестве стандартного диагностического теста, поскольку требует высокоспециализированной подготовки проб, микроскопа и технических знаний. Однако электронная микроскопия очень универсальна из-за ее способности анализировать любой тип образца и идентифицировать любой тип вируса. Таким образом, он остается золотым стандартом для выявления вирусов, которые не обнаруживаются при обычных диагностических тестах или для которых стандартные тесты дают противоречивые результаты.[7]
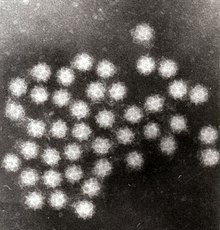 Электронная микроскопия Саповирус |
Обнаружение антител хозяина
Человек, который недавно был заражен вирусом, вырабатывает в крови антитела, которые распознают этот вирус. Это называется гуморальный иммунитет. Важны два типа антител. Первый позвонил IgM очень эффективно нейтрализует вирусы, но вырабатывается клетками иммунной системы только в течение нескольких недель. Второй, названный, IgG производится на неопределенный срок. Таким образом, наличие IgM в крови хозяина используется для проверки на острую инфекцию, тогда как IgG указывает на инфекцию, которая произошла когда-то в прошлом.[8] Оба типа антител измеряются при тестировании на иммунитет осуществляются.[9]
Тестирование на антитела стало широко доступным. Это можно сделать для отдельных вирусов (например, с помощью анализа ELISA), но все более распространенными становятся автоматизированные панели, которые могут одновременно проверять множество вирусов.
Анализ гемагглютинации
Некоторые вирусы прикрепляются к молекулам, присутствующим на поверхности эритроцитов, например, вирусу гриппа.[10] Следствием этого является то, что - при определенных концентрациях - суспензия вируса может связываться вместе (агглютинировать ) красные кровяные тельца, тем самым предотвращая их выпадение из суспензии.
Смотрите также
Рекомендации
- ^ Leland, D. S .; Джиноккио, К. С. (2007). «Роль клеточной культуры в обнаружении вирусов в век технологий». Обзоры клинической микробиологии. 20 (1): 49–78. Дои:10.1128 / CMR.00002-06. ЧВК 1797634. PMID 17223623.
- ^ Гвалтни Дж. М., Хайден Ф. Г. (февраль 1992 г.). «Психологический стресс и простуда». N Engl J Med. 326 (9): 644–5, ответ автора 645–6. Дои:10.1056 / NEJM199202273260915. PMID 1310349.
- ^ а б c «Диагностические методы в вирусологии, вирусологические методы, культура вирусов, выделение вирусов». virology-online.com. Получено 2018-01-03.
- ^ Брауэр, Рена; Чен, Питер (2015). «Распространение вируса гриппа в куриных яйцах с эмбрионами». Журнал визуализированных экспериментов (97). Дои:10.3791/52421. ЧВК 4401370. PMID 25867050.
- ^ Кузьмин, Иван В. (2015). «Выделение вирусов у животных». Современные лабораторные методы диагностики, исследования и профилактики бешенства, Том 2. С. 13–23. Дои:10.1016 / B978-0-12-801919-1.00002-6. ISBN 9780128019191.
- ^ Дхамад, AE; Абдал Рида, Массачусетс (2020). «COVID-19: молекулярные и серологические методы обнаружения». PeerJ. 8: e10180. Дои:10.7717 / peerj.10180. PMID 33083156.
- ^ Hazelton, Paul R .; Гелдерблом, Ханс Р. (2003). «Электронная микроскопия для быстрой диагностики новых инфекционных агентов1». Возникающие инфекционные заболевания. 9 (3): 294–303. Дои:10.3201 / eid0903.020327. ЧВК 2958539. PMID 12643823.
- ^ Грир, Шон; Александр, Грэм Дж. М. (1995). «4 Вирусная серология и обнаружение». Клиническая гастроэнтерология Байера. 9 (4): 689–721. Дои:10.1016/0950-3528(95)90057-8. PMID 8903801.
- ^ Лоуренс, Джеффри С. (2005). «Иммунизация против гепатита А и В лиц, инфицированных вирусом иммунодефицита человека». Американский журнал медицины. 118 (10): 75–83. Дои:10.1016 / j.amjmed.2005.07.024. PMID 16271546.
- ^ «Анализ ингибирования гемагглютинации гриппа». www.virology.ws. Получено 19 октября 2020.

