История вирусологии - History of virology
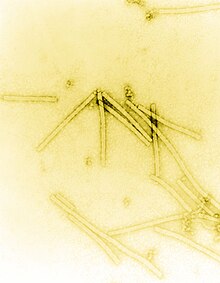
В история вирусологии - научное изучение вирусы и инфекции они вызывают - начались в последние годы 19 века. Несмотря на то что Луи Пастер и Эдвард Дженнер разработал первый вакцина чтобы защититься от вирусных инфекций, они не знали о существовании вирусов. Первые доказательства существования вирусов были получены в результате экспериментов с фильтрами, у которых были достаточно маленькие поры, чтобы удерживать бактерии. В 1892 г. Дмитрий Ивановский использовал один из этих фильтров, чтобы показать, что сок больного табачное растение оставался заразным для здоровых растений табака, несмотря на фильтрацию. Мартинус Бейеринк назвал отфильтрованное инфекционное вещество "вирусом", и это открытие считается началом вирусология.
Последующее открытие и частичная характеристика бактериофаги от Фредерик Творт и Феликс д'Эрель дальнейшее развитие этой области, и к началу 20 века было обнаружено множество вирусов. В 1926 г. Томас Милтон Риверс определил вирусы как облигатных паразитов. Доказано, что вирусы - это частицы, а не жидкость. Венделл Мередит Стэнли, и изобретение электронный микроскоп в 1931 г. позволили визуализировать их сложные структуры.
Пионеры


Несмотря на другие его успехи, Луи Пастер (1822–1895) не смог найти возбудителя бешенство и предположил, что патоген слишком мал, чтобы его можно было обнаружить с помощью микроскопа.[1] В 1884 году французы микробиолог Чарльз Чемберленд (1851–1931) изобрел фильтр, известный сегодня как Фильтр Чемберленда - у которых были поры меньше, чем у бактерий. Таким образом, он мог пропустить раствор, содержащий бактерии, через фильтр и полностью удалить их из раствора.[2]
В 1876 г. Адольф Майер, руководивший Сельскохозяйственной опытной станцией в г. Вагенинген, был первым, кто показал, что то, что он называл «болезнью табачной мозаики», было заразным. Он думал, что это было вызвано токсином или очень маленькой бактерией. Позже, в 1892 г., русский биолог Дмитрий Ивановский (1864–1920) использовал фильтр Чемберленда для изучения того, что сейчас известно как вирус табачной мозаики. Его эксперименты показали, что экстракты измельченных листьев инфицированных растений табака остаются заразными после фильтрации. Ивановский предположил, что инфекция может быть вызвана токсин производится бактериями, но не преследовал эту идею.[3]
В 1898 году голландский микробиолог Мартинус Бейеринк (1851–1931), учитель микробиологии Сельскохозяйственной школы в г. Вагенинген повторные эксперименты Адольф Майер и убедился, что фильтрат содержит новую форму инфекционного агента.[4] Он заметил, что агент размножается только в делящихся клетках, и назвал это contagium vivum fluidum (растворимый живой микроб) и повторно ввел слово вирус.[3] Бейеринк утверждал, что вирусы имеют жидкую природу - теория, впоследствии дискредитированная американским биохимиком и вирусологом. Венделл Мередит Стэнли (1904–1971), которые доказали, что они на самом деле частицы.[3] В том же 1898 г. Фридрих Лёффлер (1852–1915) и Пол Фрош (1860–1928) пропустил первый вирус животных через аналогичный фильтр и обнаружил причину ящур.[5]
Первым идентифицированным человеческим вирусом был вирус желтой лихорадки.[6] В 1881 г. Карлос Финлей (1833–1915), кубинский врач, впервые провел и опубликовал исследование, которое показало, что москиты являются переносчиками желтой лихорадки,[7] теория, подтвержденная в 1900 г. комиссией во главе с Уолтер Рид (1851–1902). В 1901 и 1902 гг. Уильям Кроуфорд Горгас (1854–1920) организовал уничтожение мест размножения комаров на Кубе, что резко снизило распространенность болезни.[8] Позже Горгас организовал уничтожение комаров из Панамы, что позволило Панамский канал откроется в 1914 году.[9] В итоге вирус был изолирован Макс Тайлер (1899–1972) в 1932 году, который разработал успешную вакцину.[10]
К 1928 году о вирусах было известно достаточно, чтобы опубликовать Фильтруемые вирусы, сборник эссе по всем известным вирусам под редакцией Томас Милтон Риверс (1888–1962). Риверс, оставшийся в живых брюшной тиф заразился в возрасте двенадцати лет, сделал выдающуюся карьеру в вирусологии. В 1926 году его пригласили выступить на встрече, организованной Обществом американской бактериологии, где он впервые сказал: «Вирусы кажутся облигатными паразитами в том смысле, что их размножение зависит от живых клеток».[11]
Представление о том, что вирусы представляют собой частицы, не считалось неестественным и хорошо вписывалось в теория микробов. Предполагается, что д-р Дж. Буист из Эдинбурга был первым человеком, который увидел вирусные частицы в 1886 году, когда он сообщил, что видел «микрококки» в вакциной лимфе, хотя он, вероятно, наблюдал скопления вируса. вакцина.[12] В последующие годы по мере совершенствования оптических микроскопов «тельца включения» наблюдались во многих инфицированных вирусом клетках, но эти агрегаты вирусных частиц были все еще слишком малы, чтобы выявить какую-либо детальную структуру. Так было до изобретения электронный микроскоп в 1931 году немецкими инженерами Эрнст Руска (1906–1988) и Макс Нолл (1887–1969),[13] что вирусные частицы, особенно бактериофаги, были показаны сложные структуры. Размеры вирусов, определенные с помощью этого нового микроскопа, хорошо совпадали с размерами вирусов, определенными с помощью экспериментов по фильтрации. Ожидалось, что вирусы будут небольшими, но их размер оказался неожиданным. Некоторые из них были лишь немного меньше самых мелких известных бактерий, а вирусы меньшего размера были аналогичны размерам сложных органических молекул.[14]
В 1935 году Венделл Стэнли исследовал вирус табачной мозаики и обнаружил, что он в основном состоит из белка.[15] В 1939 году Стэнли и Макс Лауффер (1914) разделили вирус на белок и нуклеиновая кислота,[16] докторант Стэнли Хьюберт С. Лоринг показал, что РНК.[17] Открытие РНК в частицах было важным, потому что в 1928 г. Фред Гриффит (c.1879–1941) предоставил первое свидетельство того, что его «двоюродный брат», ДНК, сформированный гены.[18]
Во времена Пастера и в течение многих лет после его смерти слово «вирус» использовалось для описания любой причины инфекционного заболевания. Много бактериологи вскоре обнаружил причину многочисленных инфекций. Тем не менее, некоторые инфекции остались, многие из них были ужасными, для которых не удалось найти бактериальную причину. Эти агенты были невидимы и могли выращиваться только на живых животных. Открытие вирусов было ключом, открывшим дверь, утаивавшую секреты причины этих загадочных инфекций. И хотя Постулаты Коха не могли быть выполнены для многих из этих инфекций, это не помешало вирусологам-пионерам искать вирусы в инфекциях, для которых не было найдено других причин.[19]
Бактериофаги

Открытие
Бактериофаги это вирусы, которые заражают и размножаются в бактериях. Они были открыты в начале 20 века английским бактериологом. Фредерик Творт (1877–1950).[20] Но до этого, в 1896 году, бактериолог Эрнест Хэнбери Хэнкин (1865–1939) сообщил, что что-то в водах Река Ганг мог убить Холерный вибрион - причина холера. Содержащийся в воде агент мог проходить через фильтры, удаляющие бактерии, но уничтожался кипячением.[21] Творт обнаружил действие бактериофагов на стафилококки бактерии. Он заметил, что при выращивании на питательном агаре некоторые колонии бактерий становились водянистыми или «стекловидными». Он собрал некоторые из этих водянистых колоний и пропустил их через фильтр Чемберленда, чтобы удалить бактерии, и обнаружил, что когда фильтрат добавляли к свежим культурам бактерий, они, в свою очередь, становились водянистыми.[20] Он предположил, что агентом может быть «амеба, ультрамикроскопический вирус, живая протоплазма или фермент, обладающий способностью к росту».[21]
Феликс д'Эрель (1873–1949) был в основном французско-канадским микробиологом-самоучкой. В 1917 году он открыл этот «невидимый антагонист», когда добавил к бактериям на агар, будет производить участки мертвых бактерий.[20] Антагонист, известный теперь как бактериофаг, может проходить через фильтр Чемберленда. Он точно разбавил суспензию этих вирусов и обнаружил, что самые высокие разведения (самые низкие концентрации вируса), вместо того, чтобы убивать все бактерии, образовывали отдельные области мертвых организмов. Подсчет этих площадей и умножение на коэффициент разведения позволили ему рассчитать количество вирусов в исходной суспензии.[22] Он понял, что открыл новую форму вируса и позже ввел термин «бактериофаг».[23][24]Между 1918 и 1921 годами д'Эрель обнаружил различные типы бактериофагов, которые могли инфицировать несколько других видов бактерий, включая Холерный вибрион.[25] Бактериофаги были объявлены потенциальным средством лечения таких заболеваний, как брюшной тиф и холера, но их обещание было забыто с развитием пенициллин.[23] С начала 1970-х бактерии продолжали вырабатывать устойчивость к антибиотики такие как пенициллин, и это привело к возобновлению интереса к использованию бактериофаги для лечения серьезных инфекций.[26]
Ранние исследования 1920–1940 гг.
Д'Эрелл много путешествовал, чтобы продвигать использование бактериофагов в лечении бактериальных инфекций. В 1928 году он стал профессором биологии в Йель и основал несколько исследовательских институтов.[27] Он был убежден, что бактериофаги - это вирусы, несмотря на противодействие известных бактериологов, таких как лауреат Нобелевской премии. Жюль Борде (1870–1961). Борде утверждал, что бактериофаги - это не вирусы, а просто ферменты выпущенный из «лизогенный» бактерии. Он сказал, что «невидимого мира d'Herelle не существует».[28] Но в 1930-х годах доказательство того, что бактериофаги были вирусами, было предоставлено Кристофер Эндрюс (1896–1988) и другие. Они показали, что эти вирусы различались по размеру, химическому и химическому составу. серологический свойства.В 1940 г. электронная микрофотография бактериофага, и это заставило замолчать скептиков, которые утверждали, что бактериофаги были относительно простыми ферментами, а не вирусами.[29]Было быстро обнаружено множество других типов бактериофагов, которые, как было показано, заражают бактерии везде, где они встречаются. Ранние исследования были прерваны Вторая Мировая Война. д'Эрелль, несмотря на его канадское гражданство, был интернирован Правительство Виши до конца войны.[30]
Современная эра
Знания о бактериофагах расширились в 1940-х годах после образования Фаговая группа учеными США. Среди участников были Макс Дельбрюк (1906–1981), который основал курс по бактериофагам в Лаборатория Колд-Спринг-Харбор.[26] Среди других ключевых членов Phage Group: Сальвадор Лурия (1912–1991) и Альфред Херши (1908–1997). В 1950-х годах Херши и Чейз сделали важные открытия в отношении репликации ДНК во время своих исследований бактериофага, называемого Т2. Вместе с Дельбрюком они были совместно удостоены Нобелевской премии 1969 года по физиологии и медицине «за открытия, касающиеся механизма репликации и генетической структуры вирусов».[31] С тех пор изучение бактериофагов дало понимание включения и выключения генов, а также полезный механизм введения чужеродных генов в бактерии и многие другие фундаментальные механизмы молекулярная биология.[32]
Вирусы растений
В 1882 г. Адольф Майер (1843–1942) описал состояние табачных растений, которое он назвал «мозаичной болезнью» («mozaïkziekte»). Больные растения имели пестрый листья, которые были пестрый.[33] Он исключил возможность грибковой инфекции и не смог обнаружить какие-либо бактерии, предположив, что "замешан растворимый ферментоподобный инфекционный принцип".[34] Он не стал развивать свою идею дальше, и именно эксперименты по фильтрации Ивановского и Бейеринка показали, что причиной был ранее нераспознанный инфекционный агент. После того, как табачная мозаика была признана вирусной болезнью, были обнаружены вирусные инфекции многих других растений.[34]
Невозможно переоценить значение вируса табачной мозаики в истории вирусов. Это был первый обнаруженный вирус и первый кристаллизованный и его структура подробно показана. Первый дифракция рентгеновских лучей фотографии кристаллизованного вируса были получены Бернал и Fankuchen в 1941 году. По ее картинам, Розалинд Франклин открыл полную структуру вируса в 1955 году.[35] В том же году, Хайнц Френкель-Конрат и Робли Уильямс показали, что очищенная РНК вируса табачной мозаики и его белок оболочки могут собираться сами по себе, чтобы сформировать функциональные вирусы, предполагая, что этот простой механизм, вероятно, был средством, с помощью которого вирусы были созданы в их клетках-хозяевах.[36]
К 1935 году считалось, что многие болезни растений вызываются вирусами. В 1922 г. Джон Канкель Смолл (1869–1938) обнаружили, что насекомые могут действовать как векторов и передают вирус растениям. В следующее десятилетие было показано, что многие болезни растений вызываются вирусами, переносимыми насекомыми, а в 1939 г. Фрэнсис Холмс пионер вирусологии растений,[37] описано 129 вирусов, вызывающих болезни растений.[38] Современное интенсивное сельское хозяйство обеспечивает богатую среду для многих вирусов растений. В 1948 году в Канзасе, США, 7% урожая пшеницы было уничтожено вирус мозаики полос пшеницы. Вирус распространяли клещи, называемые Aceria tulipae.[39]
В 1970 году российский вирусолог растений Иосиф Атабеков обнаружил, что многие вирусы растений поражают только один вид растения-хозяина.[37] В Международный комитет по таксономии вирусов теперь распознает более 900 вирусов растений.[40]
20 век
К концу XIX века вирусы были определены с точки зрения их заразительность, их способность фильтроваться и их требования к живым хозяевам. До этого времени вирусы выращивали только на растениях и животных, но в 1906 г. Росс Грэнвилл Харрисон (1870–1959) изобрел метод выращивания ткань в лимфа,[41] а в 1913 году Э. Стейнхардт, К. Израэли и Р. А. Ламберт использовали этот метод для выращивания вакцина вирус во фрагментах ткани роговицы морской свинки.[42] В 1928 г. HB и MC Maitland выращивали вирус осповакцины в суспензиях из измельченных почек кур.[43] Их метод не получил широкого распространения до 1950-х годов, когда полиовирус был выращен в больших масштабах для производства вакцины.[44] В 1941–42 гг. Джордж Хёрст (1909–94) разработали тесты, основанные на гемагглютинация для количественного определения широкого спектра вирусов, а также вирус-специфических антител в сыворотке.[45][46]
Грипп

Хотя вирус гриппа это вызвало 1918–1919 Пандемия гриппа не была обнаружена до 1930-х годов, описания болезни и последующие исследования доказали, что виновата она.[47]Пандемия унесла жизни 40–50 миллионов человек менее чем за год.[48] но доказательства того, что это было вызвано вирусом, были получены только в 1933 году.[49] Haemophilus influenzae является условно-патогенной бактерией, которая обычно развивается после гриппа; это привело выдающегося немецкого бактериолога Ричард Пфайффер (1858–1945), чтобы сделать неправильный вывод о том, что эта бактерия была причиной гриппа.[50] Большой прорыв произошел в 1931 году, когда американский патологоанатом Эрнест Уильям Гудпастур вырастил грипп и несколько других вирусов в оплодотворенных куриных яйцах.[51] Херст идентифицировал ферментативную активность, связанную с вирусной частицей, позже охарактеризованную как нейраминидаза, первая демонстрация того, что вирусы могут содержать ферменты. Фрэнк Макфарлейн Бернет в начале 1950-х годов показал, что вирус рекомбинирует с высокой частотой, а позже Херст пришел к выводу, что у него сегментированный геном.[52]
Полиомиелит
В 1949 г. Джон Ф. Эндерс (1897–1985) Томас Веллер (1915–2008) и Фредерик Роббинс (1916–2003) впервые вырастил вирус полиомиелита на культивируемых клетках человеческого эмбриона, это был первый вирус, который был выращен без использования твердых тканей животных или яиц. Инфекции, вызванные полиовирусом, чаще всего вызывают самые легкие симптомы. Это было неизвестно до тех пор, пока вирус не был выделен в культивируемых клетках, и у многих людей не было показано, что у них были легкие инфекции, которые не привели к полиомиелиту. Но, в отличие от других вирусных инфекций, заболеваемость полиомиелитом - более редкой тяжелой формой инфекции - увеличилась в 20 веке и достигла пика примерно в 1952 году. культура клеток система для выращивания вируса включена Йонас Солк (1914–1995), чтобы вакцина от полиомиелита.[53]
Вирус Эпштейна-Барра
Денис Парсонс Беркитт (1911–1993) родился в Эннискиллене, графство Фермана, Ирландия. Он был первым, кто описал тип рака, который теперь носит его имя. Лимфома Беркитта. Этот тип рака был эндемическим в экваториальной Африке и был самым распространенным злокачественным заболеванием у детей в начале 1960-х годов.[54] В попытке найти причину рака Беркитт отправил клетки из опухоли в Энтони Эпштейн (р. 1921) британский вирусолог, который вместе с Ивонн Барр и Берт Ачонг (1928–1996), и после многих неудач обнаружил вирусы, похожие на вирус герпеса, в жидкости, окружающей клетки. Позже было показано, что этот вирус представляет собой ранее нераспознанный вирус герпеса, который теперь называется Вирус Эпштейна-Барра.[55] Удивительно, но вирус Эпштейна – Барра - очень распространенная, но относительно легкая инфекция европейцев. Почему это может вызвать такую разрушительную болезнь у африканцев, до конца не понятно, но снижение иммунитета к вирусу, вызванное малярия может быть виноват.[56] Вирус Эпштейна-Барра важен в истории вирусов как первый вирус, вызывающий рак у людей.[57]
Конец 20-го и начало 21-го века

Вторая половина 20-го века была золотым веком открытия вирусов, и большинство из 2000 признанных видов животных, растений и бактериальных вирусов были обнаружены в течение этих лет.[58][59] В 1946 г. диарея, вызванная вирусом крупного рогатого скота был открыт,[60] который до сих пор является наиболее распространенным возбудителем крупного рогатого скота во всем мире.[61] а в 1957 г. конский артеривирус был открыт.[62] В 1950-х годах усовершенствования методов выделения и обнаружения вирусов привели к открытию нескольких важных человеческих вирусов, включая вирус ветряной оспы,[63] то парамиксовирусы,[64] - который включает в себя корь вирус,[65] и респираторно-синцитиальный вирус[64] - и риновирусы что вызывает простуда.[66] В 1960-х годах было обнаружено больше вирусов. В 1963 г. вирус гепатита В был обнаружен Барух Блумберг (р. 1925).[67] Обратная транскриптаза, ключевой фермент, который ретровирусы используют для перевести их РНК в ДНК, была впервые описана в 1970 году независимо Говардом Темином и Дэвид Балтимор (р. 1938).[68] Это было важно для развития противовирусные препараты - ключевой поворотный момент в истории вирусных инфекций.[69] В 1983 г. Люк Монтанье (р. 1932) и его команда на Институт Пастера во Франции впервые выделили ретровирус, который теперь называется ВИЧ.[70] В 1989 г. Майкл Хоутон команда в Корпорация Chiron обнаружил гепатит С.[71]Новые вирусы и штаммы вирусов открывались каждое десятилетие второй половины 20 века. Эти открытия продолжились в 21 веке в виде новых вирусных заболеваний, таких как ОРВИ[72] и вирус нипах[73] появились. Несмотря на достижения ученых за последние сто лет, вирусы продолжают создавать новые угрозы и проблемы.[74]
Смотрите также
использованная литература
- ^ Борденаве G (май 2003 г.). «Луи Пастер (1822–1895)». Микробы и инфекции / Institut Pasteur. 5 (6): 553–60. Дои:10.1016 / S1286-4579 (03) 00075-3. PMID 12758285.
- ^ Шорс 2008, стр. 76–77
- ^ а б c Топли и Уилсон 1998, п. 3
- ^ Леппард, Кейт; Найджел Диммок; Истон, Эндрю (2007). Введение в современную вирусологию. Blackwell Publishing Limited. С. 4–5. ISBN 978-1-4051-3645-7.
- ^ Феннер, Ф. (2009). «История вирусологии: вирусы позвоночных». В Mahy, B.W.J .; Ван Регенмортал, M.H.V. (ред.). Настольная энциклопедия общей вирусологии. Оксфорд, Великобритания: Academic Press. п. 15. ISBN 978-0-12-375146-1.
- ^ Staples JE, Monath TP (27 августа 2008 г.). «Желтая лихорадка: 100 лет открытий». JAMA: журнал Американской медицинской ассоциации. 300 (8): 960–2. Дои:10.1001 / jama.300.8.960. PMID 18728272.
- ^ Чионг М.А. (декабрь 1989 г.). «Доктор Карлос Финли и желтая лихорадка». Журнал Канадской медицинской ассоциации. 141 (11): 1126. ЧВК 1451274. PMID 2684378.
- ^ Лициос С (2001). "Уильям Кроуфорд Горгас (1854–1920)". Перспективы биологии и медицины. 44 (3): 368–78. Дои:10.1353 / pbm.2001.0051. ЧВК 1089739. PMID 11482006.
- ^ Паттерсон Р. (сентябрь 1989 г.). «Доктор Уильям Горгас и его война с комарами». Журнал Канадской медицинской ассоциации. 141 (6): 596–7, 599. ЧВК 1451363. PMID 2673502.
- ^ Фриерсон Дж. Г. (июнь 2010 г.). «Вакцина против желтой лихорадки: история». Йельский журнал биологии и медицины. 83 (2): 77–85. ЧВК 2892770. PMID 20589188.
- ^ Хорсфолл FL (1965). «Томас Милтон Риверс, 3 сентября 1888 г. - 12 мая 1962 г.» (PDF). Biogr Mem Natl Acad Sci. 38: 263–94. PMID 11615452.
- ^ * В 1887 году Буист визуализировал один из крупнейших вирусов осповакцины с помощью оптической микроскопии после его окрашивания. В то время не было известно, что вирус осповакцины является вирусом. Буист, Дж. Б. (1887). Вакциния и оспа: изучение истории их жизни. Лондон: Черчилль.
- ^ От Ekspång, Gösta, ed. (1993). Нобелевские лекции по физике 1981–1990 гг.. World Scientific. ISBN 978-9810207281.
- ^ Carr, N.G .; Mahy, B.W.J .; Pattison, J. R .; Келли, Д. П. (1984). Микроб 1984: Тридцать шестой симпозиум Общества общей микробиологии, проведенный в Уорикском университете, апрель 1984 г.. Симпозиумы Общества общей микробиологии. 36. Издательство Кембриджского университета. п. 4. ISBN 978-0-521-26056-5. OCLC 499302635.
- ^ Стэнли WM, Лоринг HS (1936). «Выделение кристаллического белка вируса табачной мозаики из больных растений томата». Наука. 83 (2143): 85. Bibcode:1936Научный .... 83 ... 85С. Дои:10.1126 / science.83.2143.85. PMID 17756690.
- ^ Стэнли WM, Lauffer MA (1939). «Распад вируса табачной мозаики в растворах мочевины». Наука. 89 (2311): 345–347. Bibcode:1939Sci .... 89..345S. Дои:10.1126 / наука.89.2311.345. PMID 17788438.
- ^ Лоринг HS (1939). «Свойства и продукты гидролиза нуклеиновой кислоты вируса табачной мозаики». Журнал биологической химии. 130 (1): 251–258.
- ^ Бертон Э. Тропп (2007). Молекулярная биология: гены в белки. Бертон Э. Тропп. Садбери, Массачусетс: Jones & Bartlett Publishers. п. 12. ISBN 978-0-7637-5963-6.
- ^ Микроб 1984, п. 3
- ^ а б c d е Шорс, Тери (2008). Понимание вирусов. Садбери, Массачусетс: Jones & Bartlett Publishers. п. 589. ISBN 978-0-7637-2932-5.CS1 maint: ref = harv (ссылка на сайт)
- ^ а б Акерманн, HW (2009). «История вирусологии: бактериофаги». Настольная энциклопедия общей вирусологии. п. 3.
- ^ а б D'Herelle F (сентябрь 2007 г.). «О невидимом микробе, антагонистическом дизентерийным бациллам: краткая записка г-на Ф. Д'Эрелля, представленная г-ном Ру ☆». Исследования в области микробиологии. 158 (7): 553–4. Дои:10.1016 / j.resmic.2007.07.005. PMID 17855060.
- ^ а б Акерманн, HW (2009). «История вирусологии: бактериофаги». Настольная энциклопедия общей вирусологии. п. 4.
- ^ «Антагонистический микроб никогда нельзя культивировать в среде без дизентерийной палочки. Он не атакует уничтоженные нагреванием дизентерийные палочки, но идеально культивируется в суспензии промытых клеток в физиологическом растворе. Это указывает на то, что антидизентерийный микроб является облигатный бактериофаг ». Феликс д'Эрель (1917) Невидимый микроб, антагонистичный дизентерийной палочке. (1917) Comptes rendus Acad. Sci. Paris Проверено 2 декабря 2010 г.
- ^ Акерманн, HW (2009). «История вирусологии: бактериофаги». Настольная энциклопедия общей вирусологии. п. 4 Таблица 1.
- ^ а б Шорс 2008, п. 591
- ^ Шорс 2008, п. 590
- ^ Цитируется в: Акерманн, HW (2009). «История вирусологии: бактериофаги». Настольная энциклопедия общей вирусологии. п. 4.
- ^ Акерманн, HW (2009). «История вирусологии: бактериофаги». Настольная энциклопедия общей вирусологии. С. 3–5.
- ^ Акерманн, HW (2009). «История вирусологии: бактериофаги». Настольная энциклопедия общей вирусологии. п. 5.
- ^ Нобелевская организация
- ^ Акерманн, HW (2009). «История вирусологии: бактериофаги». Настольная энциклопедия общей вирусологии. С. 5–10 Таблица 1.
- ^ Mayer A (1882) Over de moza¨ıkziekte van de tabak: voorloopige mededeeling. TijdschrLandbouwkunde Groningen 2: 359–364 (на немецком языке)
- ^ а б Цитируется в: ван дер Вант, Дж. П., Дейкстра Дж. (август 2006 г.). «История вирусологии растений». Архив вирусологии. 151 (8): 1467–98. Дои:10.1007 / s00705-006-0782-3. PMID 16732421.
- ^ Creager AN, Morgan GJ (июнь 2008 г.). "После двойной спирали: исследование Розалинды Франклин вируса табачной мозаики". Исида. 99 (2): 239–72. Дои:10.1086/588626. PMID 18702397.
- ^ Леппард, Кейт; Найджел Диммок; Истон, Эндрю (2007). Введение в современную вирусологию. Blackwell Publishing Limited. п. 12. ISBN 978-1-4051-3645-7.
- ^ а б Pennazio S, Roggero P, Conti M (октябрь 2001 г.). «История вирусологии растений. Менделирующая генетика и устойчивость растений к вирусам». Новая микробиология. 24 (4): 409–24. PMID 11718380.
- ^ Шорс 2008, п. 563
- ^ Hansing, D .; Johnston, C.O .; Melchers, L.E .; Товарищи, Х. (1949). «Канзасские фитопатологические заметки». Труды Канзасской академии наук. 52 (3): 363–369. Дои:10.2307/3625805. JSTOR 3625805.
- ^ Шорс 2008, п. 564
- ^ Николас, Дж. (1961). Росс Грэнвилл Харрисон 1870–1959 Биографические воспоминания (PDF). Национальная академия наук.
- ^ Steinhardt, E .; Израильский, C .; Ламберт, Р.А. (1913). «Исследования по выращиванию вируса коровьей оспы» (PDF). Дж. Инф Дис. 13 (2): 294–300. Дои:10.1093 / infdis / 13.2.294.
- ^ Maitland HB, Magrath DI (сентябрь 1957 г.). «Рост in vitro вируса коровьей оспы в хорио-аллантоисной мембране куриного эмбриона, измельченных эмбрионах и клеточных суспензиях». Журнал гигиены. 55 (3): 347–60. Дои:10.1017 / S0022172400037268. ЧВК 2217967. PMID 13475780.
- ^ Сассман, Макс; Topley, W.W.C .; Уилсон, Грэм К .; Collier, L.H .; Balows, Альберт (1998). Микробиология и микробные инфекции Топли и Уилсона. Лондон: Арнольд. п. 4. ISBN 978-0-340-66316-5.
- ^ Йоклик В.К. (май 1999 г.). «Когда два лучше, чем один: мысли о трех десятилетиях взаимодействия вирусологии и журнала вирусологии». J. Virol. 73 (5): 3520–3. ЧВК 104123. PMID 10196240.
- ^ Шлезингер RW, Гранофф A (1994). «Джордж К. Херст (1909–1994)». Вирусология. 200 (2): 327. Дои:10.1006 / viro.1994.1196.
- ^ Шорс 2008, стр. 238–344
- ^ Олдстон, Майкл Б. А. (2009). Вирусы, эпидемии и история: прошлое, настоящее и будущее. Издательство Оксфордского университета. п. 306. ISBN 978-0-19-532731-1.CS1 maint: ref = harv (ссылка на сайт)
- ^ Cunha BA (март 2004 г.). «Грипп: исторические аспекты эпидемий и пандемий». Клиники инфекционных болезней Северной Америки. 18 (1): 141–55. Дои:10.1016 / S0891-5520 (03) 00095-3. PMID 15081510.
- ^ Олдстон 2009, п. 315
- ^ Goodpasture EW, Вудрафф AM, Буддинг GJ (1931). «Культивирование вакцины и других вирусов в хориоаллантоисной мембране куриных эмбрионов». Наука. 74 (1919): 371–2. Bibcode:1931Научный .... 74..371Г. Дои:10.1126 / science.74.1919.371. PMID 17810781.
- ^ Килбурн ED (ноябрь 1975 г.). "Вручение медали Академии доктору медицины Джорджу К. Херсту". Bull N Y Acad Med. 51 (10): 1133–6. ЧВК 1749565. PMID 1104014.
- ^ Розен Ф.С. (2004). «Изоляция полиовируса - Джон Эндерс и Нобелевская премия». Медицинский журнал Новой Англии. 351 (15): 1481–83. Дои:10.1056 / NEJMp048202. PMID 15470207.
- ^ Маграт I (сентябрь 2009 г.). «Уроки клинических испытаний африканской лимфомы Беркитта». Текущее мнение в области онкологии. 21 (5): 462–8. Дои:10.1097 / CCO.0b013e32832f3dcd. PMID 19620863.
- ^ Эпштейн, М. Энтони (2005). «1. Истоки исследования ВЭБ: открытие и характеристика вируса». В Робертсоне, Эрл С. (ред.). Вирус Эпштейна-Барра. Троубридж: Cromwell Press. С. 1–14. ISBN 978-1-904455-03-5. Получено 18 сентября 2010.
- ^ Bornkamm GW (апрель 2009 г.). «Вирус Эпштейна-Барра и патогенез лимфомы Беркитта: больше вопросов, чем ответов». Международный журнал рака. 124 (8): 1745–55. Дои:10.1002 / ijc.24223. PMID 19165855.
- ^ Торли-Лоусон Д.А. (август 2005 г.). «ВЭБ - прототип вируса опухоли человека - насколько он плох?». Журнал аллергии и клинической иммунологии. 116 (2): 251–61, тест 262. Дои:10.1016 / j.jaci.2005.05.038. PMID 16083776.
- ^ Норрби Э. (2008). «Нобелевские премии и новая концепция вирусов». Архив вирусологии. 153 (6): 1109–23. Дои:10.1007 / s00705-008-0088-8. PMID 18446425.
- ^ «Первооткрыватели и открытия - файлы и обсуждения ICTV». 11 ноября 2009 г. Архивировано с оригинал 11 ноября 2009 г.. Получено 5 ноября 2017.
- ^ Олафсон П., Маккаллум А.Д., Фокс Ф.Х. (июль 1946 г.). «Очевидно новое трансмиссионное заболевание крупного рогатого скота». Ветеринар Корнелла. 36: 205–13. PMID 20995890.
- ^ Петерханс Э., Бахофен С., Сталдер Н, Швейцер М. (2010). «Цитопатические вирусы вирусной диареи крупного рогатого скота (BVDV): новые пестивирусы, обреченные на исчезновение». Ветеринарные исследования. 41 (6): 44. Дои:10.1051 / vetres / 2010016. ЧВК 2850149. PMID 20197026.
- ^ Bryans JT, Crowe ME, Doll ER, McCollum WH (январь 1957). «Выделение фильтруемого агента, вызывающего артериит лошадей и аборты кобылами; его дифференциация от вируса аборта лошадей (гриппа)». Ветеринар Корнелла. 47 (1): 3–41. PMID 13397177.
- ^ а б Веллер TH (декабрь 1995 г.). «Вирус ветряной оспы: история, перспективы и возникающие проблемы». Неврология. 45 (12 Дополнение 8): S9–10. Дои:10.1212 / wnl.45.12_suppl_8.s9. PMID 8545033.
- ^ а б c Schmidt AC, Johnson TR, Openshaw PJ, Braciale TJ, Falsey AR, Anderson LJ, Wertz GW, Groothuis JR, Prince GA, Melero JA, Graham BS (ноябрь 2004 г.). «Респираторно-синцитиальный вирус и другие пневмовирусы: обзор международного симпозиума - RSV 2003». Вирусные исследования. 106 (1): 1–13. Дои:10.1016 / j.virusres.2004.06.008. PMID 15522442.
- ^ а б Гриффин Д.Е., Пан СН (2009). Корь: старые вакцины, новые вакцины. Актуальные темы микробиологии и иммунологии. 330. С. 191–212. Дои:10.1007/978-3-540-70617-5_10. ISBN 978-3-540-70616-8. PMID 19203111.
- ^ а б Тиррелл Д.А. (август 1987 г.). «Простуда - моя любимая инфекция. Лекция памяти Стивенсона восемнадцатого большинства». Журнал общей вирусологии. 68 (8): 2053–61. Дои:10.1099/0022-1317-68-8-2053. PMID 3039038.
- ^ Zetterström R (март 2008 г.). «Нобелевская премия Баруху Блумбергу за открытие этиологии гепатита B». Acta Paediatrica. 97 (3): 384–7. Дои:10.1111 / j.1651-2227.2008.00669.x. PMID 18298788.
- ^ Темин HM, Балтимор Д. (1972). РНК-направленный синтез ДНК и РНК опухолевых вирусов. Достижения в вирусных исследованиях. 17. С. 129–86. Дои:10.1016 / S0065-3527 (08) 60749-6. ISBN 9780120398171. PMID 4348509.
- ^ Бродер С. (январь 2010 г.). «Развитие антиретровирусной терапии и ее влияние на пандемию ВИЧ-1 / СПИДа». Противовирусные исследования. 85 (1): 1–18. Дои:10.1016 / j.antiviral.2009.10.002. ЧВК 2815149. PMID 20018391.
- ^ Барре-Синусси Ф., Шерманн Дж. К., Рей Ф., Нугейр М. Т., Шамарэ С., Грюст Дж., Доге С., Акслер-Блин С., Везине-Брун Ф., Рузиу С., Розенбаум В., Монтанье Л. (май 1983 г.). «Выделение Т-лимфотропного ретровируса от пациента с риском синдрома приобретенного иммунодефицита (СПИД)». Наука. 220 (4599): 868–71. Bibcode:1983Научный ... 220..868B. Дои:10.1126 / science.6189183. PMID 6189183.
- ^ Houghton M (ноябрь 2009 г.). «Долгая и извилистая дорога, ведущая к выявлению вируса гепатита С». Журнал гепатологии. 51 (5): 939–48. Дои:10.1016 / j.jhep.2009.08.004. PMID 19781804.
- ^ Пейрис Дж. С., Пун Л. Л. (2011). Обнаружение коронавируса SARS. Методы молекулярной биологии. 665. С. 369–82. Дои:10.1007/978-1-60761-817-1_20. ISBN 978-1-60761-816-4. PMID 21116811.
- ^ Поле Х, Янг П., Йоб Дж. М., Миллс Дж., Холл Л., Маккензи Дж. (Апрель 2001 г.). «Естественная история вирусов Hendra и Nipah». Микробы и инфекции / Institut Pasteur. 3 (4): 307–14. Дои:10.1016 / S1286-4579 (01) 01384-3. PMID 11334748.
- ^ Мэхи, Б.В.Дж. (2009). Настольная энциклопедия человеческой и медицинской вирусологии. Бостон: Academic Press. С. 583–7. ISBN 978-0-12-375147-8.CS1 maint: ref = harv (ссылка на сайт)
- ^ Скерн Т. (сентябрь 2010 г.). «100 лет полиовирусу: от открытия до искоренения. Отчет о встрече». Архив вирусологии. 155 (9): 1371–81. Дои:10.1007 / s00705-010-0778-х. PMID 20683737.
- ^ Бексей-Килборн Э (2010). «Научное открытие и научная репутация: прием открытия Пейтоном Раусом вируса саркомы кур». Журнал истории биологии. 43 (1): 111–57. Дои:10.1007 / s10739-008-9171-у. PMID 20503720.
- ^ Гарднер С.Л., Райман К.Д. (март 2010 г.). «Желтая лихорадка: новая угроза». Клиники лабораторной медицины. 30 (1): 237–60. Дои:10.1016 / j.cll.2010.01.001. ЧВК 4349381. PMID 20513550.
- ^ а б Закс М.А., Паесслер С. (январь 2010 г.). «Энцефалитные альфавирусы». Ветеринарная микробиология. 140 (3–4): 281–6. Дои:10.1016 / j.vetmic.2009.08.023. ЧВК 2814892. PMID 19775836.
- ^ Джонсон CD, Goodpasture EW (январь 1934 г.). «Исследование этиологии паротита». Журнал экспериментальной медицины. 59 (1): 1–19. Дои:10.1084 / jem.59.1.1. ЧВК 2132344. PMID 19870227.
- ^ Мисра Великобритания, Калита Дж. (Июнь 2010 г.). «Обзор: японский энцефалит». Прогресс в нейробиологии. 91 (2): 108–20. Дои:10.1016 / j.pneurobio.2010.01.008. PMID 20132860.
- ^ Росс TM (март 2010 г.). «Вирус денге». Клиники лабораторной медицины. 30 (1): 149–60. Дои:10.1016 / j.cll.2009.10.007. ЧВК 7115719. PMID 20513545.
- ^ Мельник JL (декабрь 1993 г.). «Открытие энтеровирусов и классификация среди них полиовирусов». Биологические препараты. 21 (4): 305–9. Дои:10.1006 / биол.1993.1088. PMID 8024744.
- ^ Мартин, Малькольм А .; Книп, Дэвид М .; Поля, Бернард Н .; Хоули, Питер М .; Гриффин, Дайан; Лэмб, Роберт (2007). Вирусология Филдса. Филадельфия: Wolters Kluwer Health / Lippincott Williams & Wilkins. п. 2395. ISBN 978-0-7817-6060-7.
- ^ Дуглас Н., Дамбелл К. (декабрь 1992 г.). «Независимая эволюция вирусов оспы обезьян и натуральной оспы». Журнал вирусологии. 66 (12): 7565–7. ЧВК 240470. PMID 1331540.
- ^ Купер Л.З. (1985). «История и медицинские последствия краснухи». Отзывы об инфекционных заболеваниях. 7 Дополнение 1: S2–10. Дои:10.1093 / Clinids / 7.supplement_1.s2. PMID 3890105.
- ^ Яп SF (июнь 2004 г.). «Гепатит B: обзор развития от открытия« Австралийского антигена »до конца двадцатого века». Малазийский журнал патологии. 26 (1): 1–12. PMID 16190102.
- ^ Эпштейн М.А., Ачонг Б.Г., Барр Ю.М., Зажак Б., Хенле Г., Генле В. (октябрь 1966 г.). «Морфологические и вирусологические исследования культивированных лимфобластов опухоли Беркитта (штамм Raji)». Журнал Национального института рака. 37 (4): 547–59. Дои:10.1093 / jnci / 37.4.547. PMID 4288580.
- ^ Карпас А (ноябрь 2004 г.). «Человеческие ретровирусы при лейкемии и СПИДе: размышления об их открытии, биологии и эпидемиологии». Биологические обзоры Кембриджского философского общества. 79 (4): 911–33. Дои:10.1017 / S1464793104006505. PMID 15682876.
- ^ Кертис Н. (2006). Вирусные геморрагические лихорадки, вызываемые вирусами Ласса, Эбола и Марбург. Успехи экспериментальной медицины и биологии. 582. С. 35–44. Дои:10.1007/0-387-33026-7_4. ISBN 978-0-387-31783-0. PMID 16802617.
- ^ Хартман А.Л., Таунер Дж.С., Никол С.Т. (март 2010 г.). «Эбола и марбургская геморрагическая лихорадка». Клиники лабораторной медицины. 30 (1): 161–77. Дои:10.1016 / j.cll.2009.12.001. PMID 20513546.
- ^ Капикян А.З. (май 2000 г.). «Открытие 27-нм вируса Norwalk: историческая перспектива». Журнал инфекционных болезней. 181 Приложение 2: S295–302. Дои:10.1086/315584. PMID 10804141.
- ^ Епископ РФ, Кэмерон DJ, Барнс Г.Л., Холмс И.Х., Рак Б.Дж. (1976). Этиология диареи у новорожденных. Симпозиум Фонда Ciba. Симпозиумы Фонда Новартис. С. 223–36. Дои:10.1002 / 9780470720240.ch13. ISBN 9780470720240. PMID 186236.
- ^ Gust ID, Coulepis AG, Feinstone SM, Locarnini SA, Moritsugu Y, Najera R, Siegl G (1983). «Таксономическая классификация вируса гепатита А». Интервирология. 20 (1): 1–7. Дои:10.1159/000149367. PMID 6307916.
- ^ Cossart Y (Октябрь 1981 г.). «Парвовирус В19 обнаруживает болезнь». Ланцет. 2 (8253): 988–9. Дои:10.1016 / S0140-6736 (81) 91185-5. PMID 6117755.
- ^ Фельдманн Х., Гейсберт Т.В. (ноябрь 2010 г.). «Геморрагическая лихорадка Эбола». Ланцет. 377 (9768): 849–862. Дои:10.1016 / S0140-6736 (10) 60667-8. ЧВК 3406178. PMID 21084112.
- ^ а б Gallo RC (сентябрь 2005 г.). «История открытия первых ретровирусов человека: HTLV-1 и HTLV-2». Онкоген. 24 (39): 5926–30. Дои:10.1038 / sj.onc.1208980. PMID 16155599.
- ^ Монтанье Л. (февраль 2010 г.). «Через 25 лет после открытия ВИЧ: перспективы лечения и вакцины». Вирусология. 397 (2): 248–54. Дои:10.1016 / j.virol.2009.10.045. PMID 20152474.
- ^ Де Болле Л., Нейсенс Л., Де Клерк Э. (январь 2005 г.). «Обновленная информация о биологии, клинических характеристиках и терапии человеческого герпесвируса 6». Обзоры клинической микробиологии. 18 (1): 217–45. Дои:10.1128 / CMR.18.1.217-245.2005. ЧВК 544175. PMID 15653828.
- ^ Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M (апрель 1989 г.). «Выделение клона кДНК, полученного из передающегося с кровью генома вирусного гепатита не-A, не-B». Наука. 244 (4902): 359–62. Bibcode:1989Наука ... 244..359C. CiteSeerX 10.1.1.469.3592. Дои:10.1126 / science.2523562. PMID 2523562.
- ^ Биль Ф., Негр Ф. (май 2010 г.). «Вирус гепатита Е: зооноз, адаптирующийся к человеку». Журнал антимикробной химиотерапии. 65 (5): 817–21. Дои:10.1093 / jac / dkq085. PMID 20335188.
- ^ Wild TF (март 2009 г.). «Генипавирусы: новое семейство появляющихся парамиксовирусов». Патология-биология. 57 (2): 188–96. Дои:10.1016 / j.patbio.2008.04.006. PMID 18511217.
- ^ Окамото Х (2009). История открытий и патогенность вирусов TT. Актуальные темы микробиологии и иммунологии. 331. С. 1–20. Дои:10.1007/978-3-540-70972-5_1. ISBN 978-3-540-70971-8. PMID 19230554.


