История биохимии - History of biochemistry
| Часть серии по |
| Биохимия |
|---|
 |
| Ключевые компоненты |
| История биохимии |
| Глоссарии |
| Порталы: Биохимия |
В история биохимии можно сказать, что они начались с древних греков, которые интересовались составом и процессами жизни, хотя биохимия как особая научная дисциплина берет свое начало примерно в начале 19 века.[1] Некоторые утверждали, что началом биохимии могло быть открытие первых фермент, диастаза (сегодня звонил амилаза ), в 1833 г. Ансельм Пайен,[2] в то время как другие считали Эдуард Бюхнер первая демонстрация сложного биохимического процесса спиртовое брожение в бесклеточных экстрактах - рождение биохимии.[3][4] Некоторые могут также указать на влиятельную работу Юстус фон Либих с 1842 г., Химия животных или органическая химия в ее приложениях к физиологии и патологии, который представил химическую теорию метаболизма,[1] или даже раньше, в 18 веке исследования ферментации и дыхания Антуан Лавуазье.[5][6]
Период, термин "биохимия »Происходит от комбинированной формы био-, что означает "жизнь", и химия. Слово впервые записано на английском языке в 1848 году,[7] а в 1877 г. Феликс Хоппе-Зейлер использовал термин (Биохимия на немецком языке) в предисловии к первому выпуску Zeitschrift für Physiologische Chemie (Journal of Physiological Chemistry) как синоним слова физиологическая химия и выступал за создание институтов, посвященных его исследованиям.[8][9] Тем не менее, некоторые источники ссылаются на немецкий химик Карл Нойберг как введя термин для новой дисциплины в 1903 году,[10][11] и некоторые считают это Франц Хофмайстер.[12]
Предметом изучения биохимии являются химические процессы в живых организмах, и ее история включает открытие и понимание сложных компонентов жизни и выяснение путей биохимических процессов. Большая часть биохимии имеет дело со структурами и функциями клеточных компонентов, таких как белки, углеводы, липиды, нуклеиновые кислоты и другие биомолекулы; их метаболические пути и поток химической энергии через метаболизм; как биологические молекулы вызывают процессы, происходящие в живых клетках; он также фокусируется на биохимических процессах, участвующих в контроле информационного потока через биохимические сигналы, и на том, как они связаны с функционированием целых организмов. За последние 40 лет эта область добилась успеха в объяснении жизненных процессов, так что теперь почти все области наук о жизни, от ботаники до медицины, занимаются биохимическими исследованиями.
Среди огромного количества различных биомолекул многие представляют собой сложные и большие молекулы (называемые полимерами), которые состоят из одинаковых повторяющихся субъединиц (называемых мономерами). Каждый класс полимерных биомолекул имеет свой набор типов субъединиц. Например, белок - это полимер, субъединицы которого выбраны из набора из двадцати или более аминокислот, углеводы образуются из сахаров, известных как моносахариды, олигосахариды и полисахариды, липиды образуются из жирных кислот и глицеринов, а образуются нуклеиновые кислоты. из нуклеотидов. Биохимия изучает химические свойства важных биологических молекул, таких как белки, и, в частности, химию реакций, катализируемых ферментами. Биохимия клеточного метаболизма и эндокринной системы подробно описана. Другие области биохимии включают генетический код (ДНК, РНК), синтез белка, перенос клеточной мембраны, и преобразование сигнала.
Протобиохимия
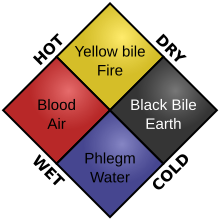
В некотором смысле можно считать, что изучение биохимии началось в древние времена, например, когда биология впервые начали интересовать общество - когда древние китайцы разработали систему медицины, основанную на Инь и Янь, а также пять фаз,[13] которые оба были результатом алхимических и биологических интересов. Его зарождение в древнеиндийской культуре было связано с интересом к медицине, поскольку они разработали концепцию трех юморов, которые были похожи на четыре юмора у греков (см. юморизм ). Они также интересовались тем, что тела состоят из ткани. Представление древних греков о «биохимии» было связано с их представлениями о материи и болезнях, где считалось, что хорошее здоровье достигается за счет баланса четыре элемента и четыре юмора в теле человека.[14] Как и в большинстве ранних наук, исламский мир внес значительный вклад в ранние биологические достижения, а также в достижения алхимии; особенно с введением клинические испытания и клиническая фармакология представлен в Авиценна с Канон медицины.[15] Что касается химии, ранние достижения в значительной степени были связаны с исследованиями алхимических интересов, но также включали: металлургия, научный метод, и ранние теории атомизм. В более поздние времена изучение химии ознаменовалось такими важными вехами, как развитие теории Менделеева. периодическая таблица, Далтона атомная модель, а сохранение массы теория. Последнее упоминание является наиболее важным из трех, потому что этот закон переплетает химию с термодинамика интеркалированным образом.
Ферменты
Еще в конце 18 - начале 19 века переваривание мяса желудочными выделениями[16] и преобразование крахмал к сахару экстрактами растений и слюна были известны. Однако механизм, с помощью которого это произошло, не установлен.[17]
В 19 веке при изучении ферментация сахара в спирт дрожжи, Луи Пастер пришел к выводу, что это брожение катализируется жизненной силой дрожжевых клеток, называемой ферменты, который, как он считал, функционирует только внутри живых организмов. Он писал, что «алкогольное брожение - это действие, связанное с жизнью и организацией дрожжевых клеток, а не со смертью или гниением клеток».[18]
В 1833 г. Ансельм Пайен обнаружил первый фермент, диастаза,[19] а в 1878 г. немецкий физиолог Вильгельм Кюне (1837–1900) ввел термин фермент, который исходит из Греческий ενζυμον «на закваске», чтобы описать этот процесс. Слово фермент позже использовался для обозначения неживых веществ, таких как пепсин, и слово брожение используется для обозначения химической активности, производимой живыми организмами.
В 1897 г. Эдуард Бюхнер начали изучать способность дрожжевых экстрактов сбраживать сахар, несмотря на отсутствие живых дрожжевых клеток. В серии экспериментов на Берлинский университет, он обнаружил, что сахар ферментировался, даже когда в смеси не было живых дрожжевых клеток.[20] Он назвал фермент, вызывающий ферментацию сахарозы "зимаза ".[21] В 1907 г. он получил Нобелевская премия по химии «За биохимические исследования и открытие бесклеточной ферментации». По примеру Бюхнера; Ферменты обычно называют в соответствии с той реакцией, которую они проводят. Обычно суффикс -ase добавляется к названию субстрат (например, лактаза это фермент, который расщепляет лактоза ) или тип реакции (например, ДНК-полимераза образует полимеры ДНК).

После того, как было показано, что ферменты могут функционировать вне живой клетки, следующим шагом было определение их биохимической природы. Многие первые исследователи отметили, что ферментативная активность связана с белками, но некоторые ученые (например, лауреат Нобелевской премии) Ричард Вильштеттер ) утверждал, что белки были просто носителями настоящих ферментов и что белки как таковой были неспособны к катализу. Однако в 1926 г. Джеймс Б. Самнер показали, что фермент уреаза был чистым белком и кристаллизовал его; Самнер поступил так же с ферментом каталаза в 1937 г. Заключение о том, что чистые белки могут быть ферментами, было окончательно доказано Northrop и Стэнли, который работал над пищеварительными ферментами пепсином (1930), трипсином и химотрипсином. Эти трое ученых были удостоены Нобелевской премии по химии 1946 года.[22]
Это открытие, что ферменты могут быть кристаллизованы, означало, что ученые в конечном итоге могли решить их структуры с помощью рентгеновская кристаллография. Впервые это было сделано для лизоцим, фермент, содержащийся в слезах, слюне и яичные белки который переваривает оболочку некоторых бактерий; структура была решена группой во главе с Дэвид Чилтон Филлипс и опубликовано в 1965 году.[23] Эта структура лизоцима с высоким разрешением положила начало области структурная биология и попытка понять, как работают ферменты, на атомарном уровне детализации.
Метаболизм
Ранний метаболический интерес

Период, термин метаболизм происходит из Греческий Μεταβολισμός - метаболизм для «изменения» или «ниспровержения».[24] История научного изучения метаболизма насчитывает 800 лет. Самые ранние из всех метаболических исследований начались в начале тринадцатого века (1213–1288) мусульманским ученым из Дамаска по имени Ибн ан-Нафис. ан-Нафис заявил в своем самом известном произведении Теолог Автодидактус что «это тело и все его части находятся в непрерывном состоянии растворения и питания, поэтому они неизбежно претерпевают постоянные изменения».[25] Хотя ан-Нафис был первым задокументированным врачом, проявившим интерес к биохимическим концепциям, первые контролируемые эксперименты по метаболизму человека были опубликованы Санторио Санторио в 1614 г. в своей книге Ars de statica medecina.[26] В этой книге описывается, как он взвешивался до и после еды, сна, работы, секса, голодания, питья и выделения. Он обнаружил, что большая часть еды, которую он принимал, была потеряна из-за того, что он называл "бесчувственный пот ".
Обмен веществ: 20 век - настоящее время
Один из самых плодовитых современных биохимиков был Ганс Кребс кто внес огромный вклад в изучение обмена веществ.[27] Кребс был учеником чрезвычайно важного Отто Варбурга и написал под этим названием биографию Варбурга, в которой он представляет Варбурга как человека, получившего образование в области биологической химии так, как Фишер сделал для органической химии. Что он и сделал. Кребс открыл цикл мочевины и позже, работая с Ханс Корнберг, цикл лимонной кислоты и цикл глиоксилата.[28][29][30] Эти открытия привели к тому, что Кребс был удостоен награды Нобелевская премия по физиологии в 1953 г.,[31] который поделился с немецким биохимиком Фриц Альберт Липманн кто также совместно открыл существенный кофактор кофермент А.
Абсорбция глюкозы
В 1960 году биохимик Роберт К. Крейн раскрыл свое открытие натрий-глюкозы перевозка как механизм всасывания глюкозы в кишечнике.[32] Это было самое первое предложение о связи между потоками иона и субстрата, которое было замечено как начало революции в биологии. Однако это открытие было бы невозможным, если бы не открытие молекулы. глюкоза строение и химический состав. Эти открытия во многом приписываются немецкому химику. Эмиль Фишер кто получил Нобелевская премия в химии почти 60 лет назад.[33]
Гликолиз

Поскольку метаболизм направлен на разрушение (катаболические процессы) молекул и создание более крупных молекул из этих частиц (анаболические процессы), использование глюкозы и ее участие в образовании аденозинтрифосфат (АТФ) имеет фундаментальное значение для этого понимания. Самый частый вид гликолиз найденный в теле, является типом, который следует по Пути Эмбден-Мейерхоф-Парнас (EMP), который был обнаружен Густав Эмбден, Отто Мейерхоф, и Якоб Кароль Парнас. Эти трое мужчин обнаружили, что гликолиз в значительной степени определяет эффективность и производство человеческого тела. Значение пути, показанного на соседнем изображении, заключается в том, что, идентифицируя отдельные шаги в этом процессе, врачи и исследователи могут точно определить места метаболических нарушений, таких как дефицит пируваткиназы что может привести к тяжелой анемии. Это наиболее важно, потому что клетки и, следовательно, организмы не способны выжить без надлежащего функционирования метаболических путей.
Инструментальные достижения (20 век)
С тех пор биохимия продвинулась вперед, особенно с середины 20 века, с развитием новых методов, таких как хроматография, дифракция рентгеновских лучей, ЯМР-спектроскопия, радиоизотопное мечение, электронная микроскопия и молекулярная динамика симуляции. Эти методы позволили открыть и детально проанализировать многие молекулы и метаболические пути из клетка, Такие как гликолиз и Цикл Кребса (цикл лимонной кислоты). Пример прибора ЯМР показывает, что некоторые из этих приборов, например HWB-ЯМР, может быть очень большим по размеру и стоить от нескольких сотен до миллионов долларов (16 миллионов долларов за показанный здесь).
Полимеразной цепной реакции

Полимеразная цепная реакция (ПЦР) - это метод амплификации первичных генов, который произвел революцию в современной биохимии. Полимеразная цепная реакция была разработана Кэри Маллис в 1983 г.[34] Правильная полимеразная цепная реакция состоит из четырех этапов: 1) денатурация 2) удлинение 3) вставка (экспрессируемого гена) и, наконец, 4) амплификация вставленного гена. Эти шаги с простыми иллюстративными примерами этого процесса можно увидеть на изображении ниже и справа от этого раздела. Этот метод позволяет амплифицировать копию одного гена до сотен или даже миллионов копий и стал краеугольным камнем протокола для любого биохимика, который хочет работать с бактериями и экспрессией генов. ПЦР используется не только для исследования экспрессии генов, но также может помочь лабораториям в диагностике определенных заболеваний, таких как лимфомы, некоторые виды лейкемия, и другие злокачественный болезни, которые иногда могут озадачить врачей. Без развития полимеразной цепной реакции есть много достижений в области изучения бактерий и экспрессии белков, которые не были бы реализованы.[35] Развитие теории и процесса полимеразной цепной реакции важно, но изобретение термоциклер не менее важен, потому что без этого инструмента процесс был бы невозможен. Это еще одно свидетельство того факта, что развитие технологий столь же важно для таких наук, как биохимия, как и кропотливые исследования, ведущие к развитию теоретических концепций.

Открытия
Смотрите также
- Агрохимия # История
- История биологии
- История химии
- История молекулярной биологии
- История хроматографии
- История биологии РНК
- Метаболизм
- Цикл лимонной кислоты
Рекомендации
- ^ а б Тон ван Хелворт (2000). Арне Хессенбрух (ред.). Справочник по истории науки. Издательство Фицрой Дирборн. п. 81.
- ^ Хантер (2000), стр. 75.
- ^ Джейкоб Дарвин Хэмблин. Наука начала двадцатого века: энциклопедия. ABC-CLIO. п. 26. ISBN 978-1-85109-665-7.
- ^ Хантер (2000), стр. 96–98.
- ^ Кларенс Питер Берг (1980). «Университет Айовы и биохимия с момента их появления». Биохимия Айовы: 1 –2. ISBN 9780874140149. Цитировать журнал требует
| журнал =(помощь) - ^ Фредерик Лоуренс Холмс (1987). Лавуазье и химия жизни: исследование научного творчества. Университет Висконсин Press. п. XV. ISBN 978-0299099848.
- ^ "биохимия, сущ." OED Online. Oxford University Press. Получено 8 апреля 2015.
- ^ Анн-Катрин Зисак; Ханс-Роберт Крам (18 октября 1999 г.). Издательство Вальтера де Грюйтера, 1749–1999.. Walter de Gruyter & Co. стр. 169. ISBN 978-3110167412.
- ^ Хорст Кляйнкауф, Ганс фон Дёрен, Лотар Янике (1988). Корни современной биохимии: закорючка Фрица Липпмана и ее последствия. Walter de Gruyter & Co. стр. 116. ISBN 9783110852455.CS1 maint: использует параметр авторов (связь)
- ^ Марк Амслер (1986). Языки творчества: модели, решение проблем, дискурс. University of Delaware Press. п. 55. ISBN 978-0874132809.
- ^ Достижения в химии и биохимии углеводов, том 70. Академическая пресса. 28 ноября 2013. с. 36. КАК В B00H7E78BG.
- ^ Кочак Маруяма (1988). Хорст Кляйнкауф; Ганс фон Дёрен; Лотар Яникем (ред.). Корни современной биохимии: закорючка Фрица Липпмана и ее последствия. Walter de Gruyter & Co. стр. 43. ISBN 9783110852455.
- ^ Магнер. История наук о жизни. п. 4.
- ^ В. Ф. Байнум; Рой Портер (ред.). Сопутствующая энциклопедия истории медицины. Рутледж. ISBN 9781136110443.
- ^ Братер, Д. Крейг; Уолтер Дж. Дэйли (2000). «Клиническая фармакология в средние века: принципы, предвещающие 21 век». Клиническая фармакология и терапия. 67 (5): 447–450. Дои:10.1067 / mcp.2000.106465. PMID 10824622.
- ^ де Реомюр, RAF (1752 г.). «Наблюдения за пищеварением уазов». Histoire de l'académie royale des Sciences. 1752: 266, 461.
- ^ Уильямс, Х.С. (1904) История науки: в пяти томах. Том IV: Современное развитие химических и биологических наук Харпер и братья (Нью-Йорк)
- ^ Дубош Ж. (1951). «Луи Пастер: Свободное копье науки, Голланц. Цитируется в Manchester K. L. (1995) Луи Пастер (1822–1895) - случай и подготовленный ум». Тенденции биотехнологии. 13 (12): 511–515. Дои:10.1016 / S0167-7799 (00) 89014-9. PMID 8595136.
- ^ А. Пайен, Ж.-Ф. Персоз (1833) «Память о диастазе, основных продуктах реакций и прикладных искусствах» (Воспоминания о диастазе, основных продуктах ее реакций и их приложениях в промышленном искусстве), Анналы химии и тела, 2-я серия, т. 53, страницы 73–92.
- ^ Биография Нобелевского лауреата Эдуарда Бухнера на http://nobelprize.org
- ^ Текст Нобелевской лекции Эдуарда Бухнера 1907 г. на http://nobelprize.org
- ^ Нобелевская премия 1946 г. для лауреатов по химии на http://nobelprize.org
- ^ Блейк С.К., Кениг Д.Ф., Майр Г.А., Северный АС, Филлипс, округ Колумбия, Сарма В.Р. (1965). "Структура лизоцима куриного яйца-белка. Трехмерный синтез Фурье с разрешением 2 ангстрем". Природа. 206 (4986): 757–761. Bibcode:1965Натура.206..757Б. Дои:10.1038 / 206757a0. PMID 5891407.
- ^ «Обмен веществ». Интернет-словарь этимологии. Получено 20 февраля 2007.
- ^ Теолог Автодидактус
- ^ Экноян Г (1999). «Санторио Санкториус (1561-1636) - отец-основатель исследований метаболического баланса». Am J Nephrol. 19 (2): 226–33. Дои:10.1159/000013455. PMID 10213823.
- ^ Корнберг Х (2000). «Кребс и его троица циклов». Нат Рев Мол Cell Biol. 1 (3): 225–8. Дои:10.1038/35043073. PMID 11252898.
- ^ Krebs, H.A .; Хенселейт, К. (1932). "Untersuchungen über die Harnstoffbildung im tierkorper". Z. Physiol. Chem. 210: 33–66. Дои:10.1515 / bchm2.1932.210.1-2.33.
- ^ Кребс H, Джонсон W (1 апреля 1937 г.). «Метаболизм кетоновых кислот в тканях животных». Biochem J. 31 (4): 645–60. Дои:10.1042 / bj0310645. ЧВК 1266984. PMID 16746382.
- ^ Корнберг Х, Кребс Х (1957). «Синтез компонентов клетки из C2-звеньев с помощью модифицированного цикла трикарбоновых кислот». Природа. 179 (4568): 988–91. Bibcode:1957 г., природа 179..988 тыс.. Дои:10.1038 / 179988a0. PMID 13430766.
- ^ Кребс, Ганс. «Нобелевский фонд». Получено 22 ноября 2013.
- ^ Роберт К. Крейн, Д. Миллер и И. Билер. «Ограничения возможных механизмов кишечного транспорта сахаров». В: Мембранный транспорт и метаболизм. Материалы симпозиума, проходившего в Праге 22–27 августа 1960 г. Под редакцией А. Кляйнцеллера и А. Котыка. Чешская Академия Наук, Прага, 1961, с. 439-449.
- ^ Фишер, Эмиль. «Нобелевский фонд». Получено 2 сентября 2009.
- ^ Бартлетт, Стирлинг (2003). Краткая история полимеразной цепной реакции. С. 3–6. ISBN 1-59259-384-4.
- ^ Ямамото, Ёсимаса (9 мая 2002 г.). «ПЦР в диагностике инфекции: обнаружение бактерий в спинномозговой жидкости». Clin Diagn Lab Immunology. 9 (3): 508–14. Дои:10.1128 / CDLI.9.3.508-514.2002. ЧВК 119969. PMID 11986253.
дальнейшее чтение
- Фрутон, Джозеф С. Белки, ферменты, гены: взаимодействие химии и биологии. Издательство Йельского университета: Нью-Хейвен, 1999. ISBN 0-300-07608-8
- Колер, Роберт. От медицинской химии к биохимии: создание биомедицинской дисциплины. Издательство Кембриджского университета, 1982.




