Риккетсия тифа - Rickettsia typhi
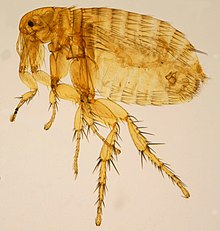
Риккетсия тифа маленький, аэробный, облигатный внутриклеточный, палочковидный грамотрицательный бактерии.[1] Он принадлежит к группе тифа Риккетсия род, наряду с R. prawazekii.[2] R. typhi имеет неопределенную историю, так как, возможно, уже давно ушел в тень эпидемического тифа (Р. prowazekii).[3] Эта бактерия признана биосдерживание уровень 2/3 организма.[1][4] R. typhi это блоха перенесенное заболевание, которое, как известно, является возбудителем болезни мышиный тиф, что является эндемичный тиф у людей, распространенный во всем мире.[3] Как и все риккетсиозные организмы, R. typhi является зоонозным агентом, вызывающим заболевание Мышиный сыпной тиф, проявляющие неспецифические легкие симптомы лихорадки, головных болей, болей и сыпи.[5][6][7] Однако более серьезные осложнения могут привести к заболеваниям почек, дыхательной системы, печени, сердца и центральной нервной системы.[6] Есть два цикла R. typhi передача из резервуаров для животных, содержащих R. typhi для людей: классический цикл крыса-блоха-крыса, который наиболее хорошо изучен и распространен, и вторичный периодо-домашний цикл, который может включать кошек, собак, опоссумов, овец и их блох.[8]
R. typhi когда-то была одной из самых распространенных причин риккетсиозных заболеваний во всем мире, но с тех пор количество зарегистрированных случаев сократилось благодаря внедрению вредитель управляющие программы.[9][10][11] В микроорганизм сконцентрирован в более теплом климате и в прибрежных портах, где много крыс и их блох, которые являются предпочтительными хозяевами для возбудитель.[9][10][12] R. typhi передается между компетентными хозяевами блох и млекопитающих через укусы блох и контакт с инфицированными кал и ткани.[9][12][13]
Есть несколько лаборатория тесты доступны для диагноз из Риккетсиоз видов, с традиционным диагнозом, основанным на серология.[9] Однако более новые лабораторные методы, например, в реальном времени ПЦР и микроиммунофлуоресценция может использоваться для идентификации Риккетсия быстрее и до Риккетсия тифа разновидность уровень.[10][12]
| Риккетсия тифа | |
|---|---|
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Протеобактерии |
| Учебный класс: | Alphaproteobacteria |
| Заказ: | Риккетсиалес |
| Семья: | Риккетсовые |
| Род: | Риккетсия |
| Группа видов: | Группа сыпного тифа |
| Разновидность: | R. typhi |
| Биномиальное имя | |
| Риккетсия тифа (Вольбах и Тодд, 1920) Филипп, 1943 | |
История и таксономия
В начале 20 века эпидемия тиф (Р. prowazekii) распространилась по всему миру. Это было связано с высокой смертностью, высокой вирулентность, и считается, что передается через вшей.[14] В этот период стали появляться менее серьезные и неотслеживаемые случаи.[14] Эти случаи характеризовались лихорадкой, сыпью, головной болью, а также опорно-двигательный аппарат и желудочно-кишечные симптомы.[15] Эпидемиолог Кеннет Ф. Макси осознал это и начал расспрашивать и выявлять присутствие другого человека. тиф в Соединенных Штатах, кроме Р. prowazekii, он подробно описал это в статье, опубликованной в 1926 году.[14] Макси предположил присутствие другого членистоногие вектор передающий эту новую форму тифа, которая позже была обнаружена как R. typhi.[14] Считается, что R. typhi исторически не диагностировался по сравнению с членом группы тифа Р. prowazekii.[16] Открытие R. typhi привели к созданию группы тифа Rickettsia, которая содержит R. typhi и Р. prowazekii.[2] Виды риккетсий обычно делятся на 3 группы: группа пятнистой лихорадки, группа сыпного тифа и группа кустарникового тифа.[2]
Морфология и подвижность клеток
Риккетсия тифа маленький, аэробный, облигатная внутриклеточная, палочковидная, грамм отрицательный бактерии.[1] R. typhi это зоонозный бактерии, признанные биосдерживание уровень 2/3 организма (в зависимости от ткани, с которой работает).[1][17] Как облигатные внутриклеточные патогены R. тиф может быть трудно изолировать, и они не могут быть культурный используя стандартные методы гальванизации, характерные для большинства других организмов.[18] R. typhi находятся подвижный, создавая движение через подвижность на основе актина, с небольшим контролем над направлением и скоростью и часто движутся по круговой схеме.[19]
Вирулентность
Риккетсия тифа является возбудителем болезни, переносимой блохами, и широко распространен во всем мире.[20] Есть два цикла в R. typhi передача от животных-резервуаров человеку: классический цикл крыса-блоха-крыса и перидоместический цикл с участием кошек, собак, опоссумов, овец и их блох.[8]
Классический цикл крыса-блоха-крыса
R. typhi циркулирует среди крыс (Раттус раттус или же Раттус норвегикус ) и крысиные блохи (Xenopyslla cheopis ),[21] но другие грызуны и их эктопаразиты также играют роль в поддержании R. typhi в природе.[22] Пока крысиная блоха - главная вектор из R. typhi, П. ч. humanus, полипакс вши и кровососущие клещи крыс, как сообщается, способны приобретать R. typhi, естественно или экспериментально.[21][3]
Передача R. typhi от блох крыс поражается при контакте с фекалиями блох, содержащих риккетсию, во время или после кормления кровью, а также через укусы блох.[16] Риккетсии не оказывают вредного воздействия на фитнес вектора или крысы, показывая истинное мутуализм отношение.[23] Зараженные блохи могут поддерживать R. typhi на всю жизнь, что дает им возможность заразить большое количество восприимчивый хосты.[23]
Перидоместический цикл
До сих пор проводилось не так много исследований цикла передачи инфекции у домашних животных, большинство из которых было сосредоточено на кошках.
Было показано, что R. typhi может присутствовать у кошек и кошачьей блохи, Ctenocephalides felis, который представляет собой вид блох, который охотно кусает людей.[24] До сих пор не было прямого человеческого R. typhi инфекции от кошек, но вместо этого существует связь между высоким уровнем инфицированных кошек, связанных с человеческими случаями мышиный тиф в том же географическом месте.[25][26]
Есть также некоторые свидетельства того, что другие домашние животные, такие как собаки и овцы [27] а также опоссумы[25] может быть вовлечен в R. typhi цикл передачи, но исследования в настоящее время ограничены.
Патогенез
Rickettsia spp. включая R. typhi проникают в кожу и распространяются через кровоток, заражая эндотелий выстилает кровеносные сосуды. Это приводит к сосудистому воспаление, повреждение целостности сосудов и нарушение сосудистая проницаемость, известный как «риккетсиозный васкулит» [8]
Болезнь
Мышиный тиф (эндемический сыпной тиф) у человека
Риккетсия тифа является возбудителем мышиный тиф (эндемический сыпной тиф) у людей и распространен по всему миру.[28] Это острый, фебрильный болезнь, которая в основном передается блохами грызунов, обычно связанными с городами и портами, где городские крысы (Раттус раттус и Раттус норвегикус ) в изобилии.[28] Люди заражаются путем вдыхания или самозаражения инфицированных блох или фекалий блох в кожу, когда они посещают болезнь -эндемичный районы, зараженные крысами.[22][29] У большинства пациентов наблюдается жар, а у многих - сыпь и головная боль.[28] хотя это также может привести к распространен, мультисистемное заболевание, включая инфекции эндотелия мозга, легких, печени, почек и сердца.[30][31] Как эти знаки и симптомы аналогичны болезням, вызываемым другими заболеваниями, включая другие риккетсии, мышиный тиф трудно диагностировать клинически.[29] Помимо неоднородных и неспецифических симптомов, отсутствуют диагностические тесты эффективен во время острых стадий заболевания, приводящих к отсрочке соответствующего лечения.[1] Мышиный сыпной тиф может быть клинически легким, но сообщалось о тяжелых и даже смертельных случаях.[23] Серьезность мышиный тиф инфекция была связана с возрастом, расой и поздней диагностикой.[23] Доксициклин является антибиотиком выбора, так как показано, что он сокращает течение болезни,[28] хотя 99% инфицированных излечиваются от болезни в течение нескольких недель без специального лечения.[1]
Эпидемиология
Географическое и временное распространение
Риккетсия тифа маленький, грамотрицательный внутриклеточный бактерия, которая устанавливает мышиный тиф инфекция у млекопитающих и блох.[32] Мышиный сыпной тиф когда-то был одним из самых распространенных риккетсиозный болезни в мире,[9][10][11] изолировав R. typhi возбудитель почти со всех континентов земного шара, кроме Антарктиды.[16][13] Помимо широкого распространения, бактерия особенно сконцентрирована в регионах с более теплым климатом круглый год и на побережьях.[9][10][16] Это пристрастие связано с благоприятными климатическими условиями этих регионов для выживания блох и диких животных. хозяева, что приводит к их большему обилию и способности поддерживать риккетсиозный организм в качестве резервуары в окружающей среде.[9][11][10][16] Морские порты - исключительные центры для R. typhi как зараженные грызуны и их эктопаразиты могут быть введены через международное движение судов.[16] Эти порты могут впоследствии передавать возбудитель в близлежащие города, по которым проходят основные торговые пути.[16] Всплески в R. typhi Инфекции также регистрируются с конца весны до начала осени, когда популяция блох особенно высока.[9][16]
Исторически сложилось так, что ежегодно в Соединенных Штатах регистрировались тысячи случаев мышиного тифа;[9][10][11][16] однако заболеваемость этой болезнью резко снизилась в 1940-х годах с введением борьба с вредителями программы по удалению резервуаров блох и грызунов, ответственных за передачу риккетсиоза в городских жилищах.[9][16] Инфекции мышиного сыпного тифа в настоящее время более спорадические и нечастые: в США ежегодно регистрируется менее 100 случаев.[10][16] Тем не менее, R. typhi до сих пор считается бактериями, имеющими большое значение для общественного здравоохранения, и вспышки этого заболевания обычно регистрируются в южных штатах США, Южной Европе, Азии, Африке и Австралии.[9][10][11][16] Считается, что R. typhi распространенность на самом деле выше, чем измеренное значение, поскольку о мышином сыпном тифе часто не сообщают и неправильно диагностируют из-за его неспецифических и легких клинических проявлений (лихорадка, головная боль, общая боль и сыпь).[10][11][16][27] По прогнозам, количество недиагностированных инфекций превысит количество зарегистрированных случаев в 4: 1.[16]
Диапазон хоста и передача
В R. typhi микроорганизм обязательно проживает в эпителиальный ячейки средняя кишка в блоха хозяева, а эндотелиальный ячейки, выстилающие сосудистая сеть из млекопитающее разновидность.[32] Жизненный цикл бактерии классически включает восточную крысиную блоху (Xenopsylla cheopis ) и черный (Раттус раттус ) и коричневый (Раттус норвегикус ) крысы.[9][10][11][16] Эти глобально распределенные хосты особенно хорошо переносят эту риккетсию по многим причинам: X. cheopis имеет невероятно широкий круг хозяев и, таким образом, может передавать бактерию широкому набору млекопитающих-хозяев, включая человека;[16] Члены рода Раттус включить R. typhi пройти массовые раунды двойное деление в эукариотический клетки и увеличить количество бактерий, доступных для заражения блох векторов.[16] Помимо крыс и их блох, было замечено, что другие хозяева естественным образом переносят микропаразит а также кошек и их блох (Ctenocephalides felis ), опоссумы, землеройки, скунсы, домовые мыши и их блохи (Leptopsylla segnis),[9][16] и редко собаки.[27] Кошки и опоссумы считаются довольно значительными резервуарами мышиного тифа в городских условиях из-за их непривередливых эктопаразитов и тесной связи с людьми.[11][16]
Бактерия передается от инфицированной крысы (или другого млекопитающего-хозяина) к чувствительной крысиной блохе (или другому хозяину). членистоногие вектор) через кровяной корм, а затем передается от инфицированной блохи другой восприимчивой крысе через прямой контакт с инфекционными фекалиями или тканями переносчика.[9][16][13] Передача при контакте с фекалиями членистоногих может происходить через открытую рану, дыхательные пути (вдыхание) или конъюнктива млекопитающего-хозяина.[16] Есть свидетельства того, что передача укусов блох возможна также после того, как бактерия подвергнется определенному воздействию. период инкубации в векторе членистоногих.[16] Самки блох также могут передавать инфекцию потомству через трансовариальная передача.[9][16] R. typhi кажется в истинном комменсализм с этими насекомыми и нечеловеческими хозяевами, поскольку он производит только бессимптомный инфекция, не влияющая на продолжительность жизни или репродуктивную способность хозяина.[16] Благодаря универсальности трансмиссии R. typhi бактерия очень успешно увековечивает свою численность в эндемичный регионы.[16]
Зоонозный потенциал
Как и у всех видов риккетсий, R. typhi это зоонозный с людьми, выступающими в качестве аберрантных тупиковых хозяев, и, следовательно, не играют экологической роли в передаче и жизненном цикле бактерий.[16][33] Люди чаще всего заражаются от блох и крыс. R. typhi перевозчики[необходимо разрешение неоднозначности ] в помещениях, обычно поражая людей, работающих или живущих в условиях, в которых обитают крупные популяции грызунов и блох.[16] Мышиный сыпной тиф обычно считается легким заболеванием с 4% коэффициент летальности у нелеченных пациентов.[11][34] Помимо общей лихорадки, головных болей, боли и высыпаний, могут возникнуть более серьезные осложнения. R. typhi инфекции, такие как почечная, респираторная, ЦНС, печень и сердечные заболевания.[34] Надлежащий надзор за мышиным тифом особенно важен для пожилых пациентов, которым часто требуется госпитализация по мере прогрессирования заболевания.[11][16]
Диагностика и идентификация
Лабораторные тесты, доступные для диагноз из Риккетсиоз виды включают в себя: пробу в оболочке флакона, ПЦР- обнаружение на основе, иммунодетекция, циркулирующая эндотелиальный клетки и серодиагностические тесты, такие как тест Вейля-Феликса, тест CF, ELISA, микроиммунофлуоресценция, иммунопероксидаза, линейный блот и Вестерн иммуноблот тесты.[7]
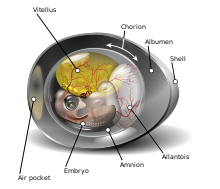
Традиционно диагноз из Риккетсия был основан на серология [35] Однако серологические тесты проходят примерно через 15 дней после появления симптомов, чтобы выявить диагностически значимые титры Р. тыхпи.[36] И поэтому диагноз часто подтверждается после того, как пациент выздоровел или умер.[7] R. typhi не могут расти в аксенический или в стерильных условиях и должны выращиваться в ткани, или эмбрион образцы.[18] Даже при соблюдении строгих физиологических условий при выращивании в среде, имитирующей среду хозяина. цитоплазма, активность патогена не может сохраняться очень долго.[18] Распространенный способ выращивания R. typhi проходит через желточные мешки эмбриональных яиц.[18]
Лабораторные методы, такие как ПЦР в реальном времени и микроиммунофлуоресценция, могут использоваться для идентификации Риккетсия вплоть до видового уровня.[37][5] Микроиммунофлуоресценция - это высокочувствительный тест, который часто используется в эндемичных районах для подтверждения инфекции, вызванной R. typhi.[11] Использование ПЦР в реальном времени может позволить обнаруживать и подтверждать R. typhi раньше, чем серологические тесты.[37] Также используются методы на основе ПЦР и мембранные белки ompB и prsA. ген было показано, что фрагменты являются идентифицируемыми маркерами в qPCR для R. typhi.[38]
Отличие от R. prowazekii
Симптомы из R. typhi и Р. prowazekii может быть очень похожим, с R. typhi инфекции обычно менее тяжелые. R. typhi и член его группы тифа Р. prowazekii состоят из очень похожих геномы, R. typhi можно отличить от Р. prowazekii к 12000 пар оснований вставлен в R. prowazekii.[1] Существуют различные методы дифференциации членов группы тифа. Один из методов заключается в полиморфизме длины рестрикционных фрагментов (RFLP), который позволяет дифференцировать два вида на основе гена ompB и связанных ферменты, который имеет уникальную последовательность для каждого вида.[39] Также полезны серологические методы. Было показано, что использование непрямого флуоресцентного антитело анализы и вестерн-блоттинг вместе обеспечивают надежную дифференциацию между видами.[40] Сам по себе кросс-адсорбционный анализ сыворотки также является надежным методом дифференциации, поскольку перекрестная реакция между двумя видами является обычным явлением.[40]
Библиография
- ^ а б c d е ж грамм Маклеод, Майкл П .; Цинь, Сян; Karpathy, Sandor E .; Джоя, Джейсон; Горец, Сара К .; Фокс, Джордж Э .; Макнил, Томас З .; Цзян, Хуайян; Музны, Донна; Джейкоб, Лени S .; Хоуз, Алисия К. (2004-09-01). «Полная последовательность генома Rickettsia typhi и сравнение с последовательностями других Rickettsiae». Журнал бактериологии. 186 (17): 5842–5855. Дои:10.1128 / JB.186.17.5842-5855.2004. ISSN 0021-9193. ЧВК 516817. PMID 15317790.
- ^ а б c Мансуэто, Паскуале; Витале, Джустина; Cascio, Антонио; Сейдита, Аурелио; Пепе, Илениа; Карроччо, Антонио; ди Роса, Сальваторе; Рини, Джовам Баттиста; Чиллари, Энрико (06.09.2011). "Новое понимание иммунитета и иммунопатологии риккетсиозов". Клиническая иммунология и иммунология развития. Получено 2020-09-09.
- ^ а б c Azad, A. F .; Трауб, Р. (октябрь 1989 г.). «Экспериментальная передача мышиного тифа от укусов блох Xenopsylla cheopis». Медицинская и ветеринарная энтомология. 3 (4): 429–433. Дои:10.1111 / j.1365-2915.1989.tb00251.x. ISSN 0269-283X. PMID 2519693.
- ^ Раух, Джессика; Эйзерманн, Филипп; Ноак, Бернд; Мехлхуп, Юте; Мунтау, Биргит; Шефер, Йоханнес; Таппе, Деннис (июль 2018 г.). «Typhus Group Rickettsiosis, Германия, 2010–20171». Возникающие инфекционные заболевания. 24 (7): 1213–1220. Дои:10.3201 / eid2407.180093. ISSN 1080-6040. ЧВК 6038764. PMID 29912688.
- ^ а б Schriefer, M E; Sacci, JB; Дамлер, Дж. С.; Bullen, MG; Азад, А Ф (1994). «Выявление новой риккетсиозной инфекции у пациента с диагнозом мышиный сыпной тиф». Журнал клинической микробиологии. 32 (4): 949–954. Дои:10.1128 / см. 32.4.949-954.1994. ISSN 0095-1137.
- ^ а б Батиста-Сикейра, Родриго (2016). «Риккетсиоз человека: новые эпидемиологические и клинические данные» (PDF). Журнал тропических болезней. 4: 1–9.
- ^ а б c Скола, Б. Ла; Рауль, Д. (1997-11-01). «Лабораторная диагностика риккетсиозов: современные подходы к диагностике старых и новых риккетсиозов». Журнал клинической микробиологии. 35 (11): 2715–2727. Дои:10.1128 / jcm.35.11.2715-2727.1997. ISSN 0095-1137. PMID 9350721.
- ^ а б c Сахни, Санджив К.; Рыдкина, Елена (30.03.2009). «Взаимодействие клетки-хозяина с патогенными видами Rickettsia». Будущая микробиология. 4 (3): 323–339. Дои:10.2217 / fmb.09.6. ISSN 1746-0913. ЧВК 2775711. PMID 19327117.
- ^ а б c d е ж грамм час я j k л м п о Еремеева, Марина Е .; Даш, Грегори А. (01.01.2012), Лонг, Сара С. (ред.), «179 - Другие виды риккетсий», Принципы и практика детских инфекционных болезней (четвертое издание), London: Content Repository Only !, pp. 930–938.e4, ISBN 978-1-4377-2702-9, получено 2020-10-06
- ^ а б c d е ж грамм час я j k Уайтфорд, Сара Ф .; Тейлор, Джеффри П .; Дамлер, Дж. Стивен (2001-03-01). «Клинические, лабораторные и эпидемиологические особенности мышиного тифа у 97 детей Техаса». Архивы педиатрии и подростковой медицины. 155 (3): 396. Дои:10.1001 / архпеди.155.3.396. ISSN 1072-4710.
- ^ а б c d е ж грамм час я j k Schriefer, M.E .; Sacci, J. B .; Dumler, J. S .; Bullen, M. G .; Азад, А. Ф. (1994-04-01). «Выявление новой риккетсиозной инфекции у пациента с диагнозом мышиный сыпной тиф». Журнал клинической микробиологии. 32 (4): 949–954. ISSN 0095-1137. PMID 8027348.
- ^ а б c Ошибка цитирования: указанная ссылка
:32был вызван, но не определен (см. страница помощи). - ^ а б c Абдад, Мохаммад Язид; Абдалла, Рита Абу; Фурнье, Пьер-Эдуар; Стенос, Джон; Васу, Шон (2018-08-01). «Краткий обзор эпидемиологии и диагностики риккетсиозов: виды Rickettsia и Orientia». Журнал клинической микробиологии. 56 (8). Дои:10.1128 / JCM.01728-17. ISSN 0095-1137. PMID 29769278.
- ^ а б c d Максси, Кеннет Ф. (1926). «Эпидемиологическое исследование эндемического тифа (болезни Брилла) на юго-востоке США: особое внимание уделяется способу передачи». Отчеты об общественном здравоохранении (1896-1970). 41 (52): 2967. Дои:10.2307/4578110.
- ^ Уайтфорд, Сара Ф .; Тейлор, Джеффри П .; Дамлер, Дж. Стивен (2001-03-01). «Клинические, лабораторные и эпидемиологические особенности мышиного тифа у 97 детей Техаса». Архивы педиатрии и подростковой медицины. 155 (3): 396. Дои:10.1001 / archpedi.155.3.396. ISSN 1072-4710.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Икс у z аа ab Азад, АФ (январь 1990 г.). «Эпидемиология мышиного тифа». Ежегодный обзор энтомологии. 35 (1): 553–570. Дои:10.1146 / annurev.en.35.010190.003005. ISSN 0066-4170.
- ^ Раух, Джессика; Эйзерманн, Филипп; Ноак, Бернд; Мехлхуп, Юте; Мунтау, Биргит; Шефер, Йоханнес; Таппе, Деннис (июль 2018 г.). «Typhus Group Rickettsiosis, Германия, 2010–20171». Возникающие инфекционные заболевания. 24 (7): 1213–1220. Дои:10.3201 / eid2407.180093. ISSN 1080-6040. ЧВК 6038764. PMID 29912688.
- ^ а б c d «Риккетсия». Молекулярная медицинская микробиология: 2043–2056. 2015-01-01. Дои:10.1016 / B978-0-12-397169-2.00111-6.
- ^ Хайнцен, Роберт А. (2003). «Риккетсиозная подвижность на основе актина». Летопись Нью-Йоркской академии наук. 990 (1): 535–547. Дои:10.1111 / j.1749-6632.2003.tb07424.x. ISSN 1749-6632.
- ^ Azad, A. F .; Радулович, С .; Хиггинс, Дж. А .; Noden, B.H .; Тройер, Дж. М. (1997). «Блошиные риккетсиозы: экологические соображения». Возникающие инфекционные заболевания. 3 (3): 319–327. ISSN 1080-6040. ЧВК 2627639. PMID 9284376.
- ^ а б TRAUB, R; R, TRAUB; JR, WISSEMAN CL; АЗАД, АБДУЛРАХМАН ФАРХАНГ (1978). «ЭКОЛОГИЯ MURINE TYPHUS. КРИТИЧЕСКИЙ ОБЗОР». ЭКОЛОГИЯ MURINE TYPHUS. КРИТИЧЕСКИЙ ОБЗОР.
- ^ а б Еремеева, Марина Е .; Warashina, Wesley R .; Осетр, Мишель М .; Buchholz, Arlene E .; Олмстед, Грегори К .; Парк, Сара Й .; Effler, Paul V .; Карпаты, Шандор Э. (октябрь 2008 г.). «Rickettsia typhi и R. felis в крысиных блох (Xenopsylla cheopis), Оаху, Гавайи». Возникающие инфекционные заболевания. 14 (10): 1613–1615. Дои:10.3201 / eid1410.080571. ISSN 1080-6040. ЧВК 2609893. PMID 18826827.
- ^ а б c d Гиллеспи, Джозеф Дж .; Аммерман, Николь С .; Байер-Секстон, Магда; Sobral, Bruno S .; Азад, Абду Ф. (2009-03-01). «Риккетсиозы, переносимые вошами и блохами: биологические и геномные анализы». Ветеринарные исследования. 40 (2): 1. Дои:10.1051 / ветрес: 2008050. ISSN 0928-4249.
- ^ Ногерас Мария Мерседес; Pons, Immaculada; Ортуньо, Ана; Мирет, Хайме; Пла, Юлия; Кастелла, Жоаким; Сегура, Ферран (2013-08-06). «Молекулярное определение тифа риккетсии у кошек и блох». PLOS ONE. 8 (8): e71386. Дои:10.1371 / journal.pone.0071386. ISSN 1932-6203. ЧВК 3735526. PMID 23940746.
- ^ а б Аджемян, Дженнифер; Парки, Шарын; МакЭлрой, Кристина; Кэмпбелл, Джилл; Еремеева, Марина Е .; Николсон, Уильям Л .; Маккуистон, Дженнифер; Тейлор, Джеффри. «Мышиный тиф в Остине, штат Техас, США, 2008 г. - Том 16, номер 3 - март 2010 г. - журнал Emerging Infectious Diseases - CDC». Дои:10.3201 / eid1603.091028. Цитировать журнал требует
| журнал =(помощь) - ^ Сорвильо, Франк Дж .; Гондо, Барбара; Эммонс, Ричард; Райан, Патрик; Уотерман, Стивен Х .; Тильзер, Артур; Андерсен, Эллен М .; Мюррей, Роберт А .; Барр, А. Ральф (1 февраля 1993 г.). «Пригородный фокус эндемического тифа в округе Лос-Анджелес: ассоциация с серопозитивными домашними кошками и опоссумами». Американский журнал тропической медицины и гигиены. 48 (2): 269–273. Дои:10.4269 / ajtmh.1993.48.269. ISSN 0002-9637.
- ^ а б c Ногерас, Мария-Мерседес; Pons, Immaculada; Пла, Джулия; Ортуньо, Анна; Мирет, Хайме; Санфелиу, Изабель; Сегура, Ферран (2013-04-12). «Роль собак в экоэпидемиологии Rickettsia typhi, этиологического возбудителя мышиного тифа». Ветеринарная микробиология. 163 (1–2): 97–102. Дои:10.1016 / j.vetmic.2012.11.043. ISSN 1873-2542. PMID 23290118.
- ^ а б c d Сивен, Рэйчел; Нго, Ван (15 марта 2008 г.). «Мышиный сыпной тиф: нераспознанное переносимое пригородом заболевание». Клинические инфекционные болезни. 46 (6): 913–918. Дои:10.1086/527443. ISSN 1058-4838.
- ^ а б Генри, Кэтрин М .; Цзян, Цзюй; Розмайзл, Патрик Дж .; Азад, Абду Ф .; Macaluso, Kevin R .; Ричардс, Аллен Л. (2007-02-01). «Разработка количественных ПЦР-тестов в реальном времени для обнаружения Rickettsia typhi и Rickettsia felis, возбудителей мышиного тифа и пятнистой лихорадки, переносимой блохами». Молекулярные и клеточные зонды. 21 (1): 17–23. Дои:10.1016 / j.mcp.2006.06.002. ISSN 0890-8508.
- ^ Уокер, Д. Х .; Feng, H.M .; Ladner, S .; Биллингс, А. Н .; Zaki, S. R .; Wear, D. J .; Хайтауэр, Б. (октябрь 1997 г.). «Иммуногистохимическая диагностика тифозного риккетсиоза с использованием моноклональных антител против липополисахаридов». Современная патология: официальный журнал США и Канадской академии патологии, Inc.. 10 (10): 1038–1042. ISSN 0893-3952. PMID 9346184.
- ^ Уокер, Дэвид Х .; Парки, Фрэнсис М .; Betz, Thomas G .; Тейлор, Джеффри П .; Мюльбергер, Джоан В. (1 июня 1989 г.). «Гистопатология и иммуногистологическая демонстрация распространения Rickettsia typhi у мышей со смертельным исходом». Американский журнал клинической патологии. 91 (6): 720–724. Дои:10.1093 / ajcp / 91.6.720. ISSN 0002-9173.
- ^ а б Blanton, Lucas S .; Дамлер, Дж. Стивен; Уокер, Дэвид Х. (01.01.2015), Беннетт, Джон Э .; Долин, Рафаэль; Блазер, Мартин Дж. (Ред.), «192 - Rickettsia typhi (Мышиный тиф)», Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета (восьмое издание), Philadelphia: Content Repository Only !, стр. 2221–2224.e2, ISBN 978-1-4557-4801-3, получено 2020-09-10
- ^ Уокер, Д. Х .; Фишбейн, Д. Б. (1991-05-01). «Эпидемиология риккетсиозов». Европейский журнал эпидемиологии. 7 (3): 237–245. Дои:10.1007 / BF00145672. ISSN 1573-7284.
- ^ а б Батиста-Сикейра, Родриго (2016). «Риккетсиоз человека: новые эпидемиологические и клинические данные» (PDF). Журнал тропических болезней. 4: 1–9.
- ^ «Rickettsia typhi (мышиный сыпной тиф) - инфекционное заболевание и противомикробные агенты». www.antimicrobe.org. Получено 2020-09-23.
- ^ Дамлер, Дж. С. (1991-09-11). «Клинические и лабораторные особенности мышиного тифа на юге Техаса, 1980–1987». JAMA: журнал Американской медицинской ассоциации. 266 (10): 1365–1370. Дои:10.1001 / jama.266.10.1365. ISSN 0098-7484.
- ^ а б Джульери, Стефано; Джатон, Катя; Кометта, Ален; Trellu, Laurence T .; Greub, Гилберт (2012-02-01). «Разработка дуплексной ПЦР в реальном времени для обнаружения Rickettsia spp. И риккетсий группы сыпного тифа в клинических образцах». FEMS Иммунология и медицинская микробиология. 64 (1): 92–97. Дои:10.1111 / j.1574-695X.2011.00910.x. ISSN 0928-8244.
- ^ Папп, Стефани; Раух, Джессика; Кюль, Свенья; Ричард, Ульрике; Келлер, Кристиан; Остерло, Анке (февраль 2017 г.). «Сравнительная оценка двух количественных ПЦР в реальном времени, специфичных для Rickettsia typhi, для исследовательских и диагностических целей». Медицинская микробиология и иммунология. 206 (1): 41–51. Дои:10.1007 / s00430-016-0480-z. ISSN 0300-8584.
- ^ Пенише-Лара, Гаспар; Завала-Веласкес, Хорхе; Дзул-Росадо, Карла; Walker, D.H .; Завала-Кастро, Хорхе (2013). «Простой метод дифференциации видов риккетсий». Журнал молекулярной микробиологии и биотехнологии. 23 (3): 203–208. Дои:10.1159/000348298. ISSN 1660-2412. ЧВК 4714558. PMID 23595041.
- ^ а б Ла Скола, Бернар; Рыдкина, Лена; Ндихокубвайо, Жан-Боско; Vene, Sirkka; Рауль, Дидье (01.07.2000). «Серологическая дифференциация мышиного сыпного тифа и эпидемического тифа с использованием перекрестной адсорбции и вестерн-блоттинга». Клинико-диагностическая лаборатория иммунологии. 7 (4): 612–616. Дои:10.1128 / CDLI.7.4.612-616.2000. ISSN 1098-6588. ЧВК 95923. PMID 10882661.