Триптофансинтаза - Tryptophan synthase
| Триптофан-синтаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
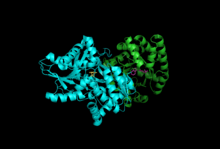 Подразделения: Бета-субъединица, Альфа-субъединица с PLP, IGP | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 4.2.1.20 | ||||||||
| Количество CAS | 9014-52-2 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Триптофансинтаза или же триптофансинтетаза является фермент который катализирует два последних этапа биосинтеза триптофан.[1] Обычно встречается в Эубактерии,[2] Архебактерии,[3] Протиста,[4] Грибы,[5] и Plantae.[6] Однако его нет в Animalia.[7] Обычно встречается как тетрамер α2β2. Субъединицы α катализируют обратимое образование индол и глицеральдегид-3-фосфат (G3P) из индол-3-глицеринфосфата (IGP). Субъединицы β катализируют необратимую конденсацию индола и серин образовать триптофан в пиридоксальфосфат (PLP) зависимая реакция. Каждый α-активный сайт связан с β-активным сайтом гидрофобным каналом длиной 25 ангстрем, содержащимся внутри фермента. Это облегчает диффузию индола, образованного в α-активных центрах, непосредственно в β-активные центры в процессе, известном как канал субстрата.[8] Активные центры триптофансинтазы: аллостерически спаренный.[9]
Структура фермента
Подразделения: Триптофансинтаза обычно существует в виде комплекса α-ββ-α. Субъединицы α и β имеют молекулярные массы 27 и 43 кДа соответственно. Субъединица α имеет ТИМ ствол конформация. Субъединица β имеет складчатую конформацию типа II и сайт связывания, расположенный рядом с активным сайтом для одновалентных катионов.[10] Их сборка в комплекс приводит к структурным изменениям обеих субъединиц, что приводит к реципрокной активации. Существует два основных механизма межсубъединичной коммуникации. Во-первых, домен COMM β-субъединицы и α-петля2 α-субъединицы взаимодействуют. Кроме того, существуют взаимодействия между остатками αGly181 и βSer178.[11] Активные сайты регулируются аллостерически и претерпевают переходы между открытым, неактивным и закрытым, активным состояниями.[9]
Сайт связывания индол-3-глицерина: См. Изображение 1.
Сайт связывания индола и серина: См. Изображение 1.
Гидрофобный канал: Активные центры α и β разделены отрезком длиной 25 ангстрем. гидрофобный канал внутри фермента, обеспечивающий диффузию индола. Если бы канал не существовал, индол, образованный в активном центре α, быстро диффундировал бы и был бы потерян в клетке, поскольку он гидрофобен и может легко проникать через мембраны. Таким образом, канал необходим для функционирования комплекса ферментов.[12]

Ферментный механизм
α субъединица реакция: Субъединица α катализирует образование индола и G3P в результате ретроальдольного расщепления IGP. Считается, что αGlu49 и αAsp60 непосредственно участвуют в катализе, как показано.[8] Стадия ограничения скорости - изомеризация IGP.[13] Смотрите изображение 2.
реакция субъединицы β: Субъединица β катализирует реакцию β-замещения, в которой индол и серин конденсируются с образованием триптофана в PLP-зависимой реакции. Считается, что βLys87, βGlu109 и βSer377 непосредственно участвуют в катализе, как показано.[8] Опять же, точный механизм не был окончательно определен. Смотрите изображение 2.
Чистая реакция: См. Изображение 3.


Биологическая функция
Триптофансинтаза обычно содержится в Eubacteria, Archaebacteria, Protista, Fungi и Plantae. Он отсутствует у таких животных, как человек. Триптофан один из двадцати стандартных аминокислоты и один из девяти незаменимые аминокислоты для людей. Таким образом, триптофан является необходимым компонентом рациона человека.
Объем субстрата
Также известно, что триптофансинтетаза принимает аналоги индола, например фторированные или метилированные индолы, в качестве субстратов, генерируя соответствующие аналоги триптофана.[14]
Актуальность болезни
Поскольку у людей нет триптофансинтазы, этот фермент исследовался как потенциальный мишень для наркотиков.[15] Однако считается, что у бактерий есть альтернативные механизмы производства аминокислот, которые могут сделать этот подход менее эффективным. В любом случае, даже если препарат только ослабляет бактерии, он все равно может быть полезен, поскольку бактерии уже уязвимы во враждебной среде хозяина. Таким образом, ингибирование триптофансинтазы вместе с другими ферментами PLP в метаболизме аминокислот может помочь решить медицинские проблемы.[16]
Подавление триптофансинтазы и других ферментов PLP в метаболизме аминокислот было предложено для:
- Лечение туберкулез[15]
- Лечение окуляр и генитальный инфекции[17]
- Лечение криптоспоридиоз[15]
- Гербицид использовать[18]
Эволюция
Считается, что на ранней стадии эволюции ген trpB2 был продублирован. Один экземпляр вошел в trp оперон как trpB2i с учетом его экспрессии с trpA. TrpB2i образует временные комплексы с TrpA и в процессе однонаправленно активирует TrpA. Другая копия осталась снаружи как trpB2o и выполняла существующую роль или играла новую роль, например, выступая в качестве белка-спасателя для индола. TrpB2i превратился в TrpB1, который образовывал постоянные комплексы с trpA, что приводило к двунаправленной активации. Преимущество спасительного белка индола уменьшилось, и ген TrpB был потерян. Наконец, гены TrpB1 и TrpA были слиты, что привело к образованию бифункционального фермента.[19]
Историческое значение
Триптофансинтаза была первым идентифицированным ферментом, у которого было два каталитический возможности, которые были тщательно изучены. Он также был первым, кто использовал субстратные каналы. Таким образом, этот фермент широко изучен и представляет большой интерес.[8]
Смотрите также
Рекомендации
- ^ Данн М.Ф., Никс Д., Нго Х., Барендс Т.Р., Шлихтинг I (июнь 2008 г.). «Триптофансинтаза: работа канальной наномашины». Тенденции в биохимических науках. 33 (6): 254–64. Дои:10.1016 / j.tibs.2008.04.008. PMID 18486479.
- ^ Яблонски П., Яблонски Л., Пинтадо О., Шриранганатан Н., Хоуд С. (сентябрь 1996 г.). «Триптофансинтаза: идентификация B-субъединицы триптофансинтазы Pasteurella multocida с помощью антисыворотки против штамма PI059». Микробиология. 142: 115–21. Дои:10.1099/13500872-142-1-115. PMID 8581158.
- ^ Ласкано А., Диас-Вильгомес Э, Миллс Т., Оро Дж. (Март 1995 г.). «Об уровнях специфичности ферментных субстратов: значение для ранней эволюции метаболических путей». Успехи в космических исследованиях. 15 (3): 345–56. Дои:10.1016 / S0273-1177 (99) 80106-9. PMID 11539248.
- ^ Андерсон И., Уоткинс Р., Самуэльсон Дж., Спенсер Д., Майорос В., Грей М., Лофтус Б. (август 2005 г.). «Открытие генов в геноме Acanthamoeba castellanii». Протист. 156 (2): 203–14. Дои:10.1016 / j.protis.2005.04.001. PMID 16171187.
- ^ Ирландия К., Пикхаус Н., Лу П., Сангари Р., Чжан А., Масурекар П., Ан З (апрель 2008 г.). «Ген TRP1 триптофансинтетазы Nodulisporium sp: молекулярная характеристика и его связь с продуцированием нодулиспоровой кислоты A». Appl Microbiol Biotechnol. 79 (3): 451–9. Дои:10.1007 / s00253-008-1440-3. PMID 18389234.
- ^ Санджая, Сяо П.Й., Су Р.С., Ко С.С., Тонг К.Г., Ян Р.Й., Чан М.Т. (апрель 2008 г.). «Избыточная экспрессия триптофансинтазы бета 1 Arabidopsis thaliana (AtTSB1) в Arabidopsis и томатах придает устойчивость к кадмиевому стрессу». Растительная клеточная среда. 31 (8): 1074–85. Дои:10.1111 / j.1365-3040.2008.01819.x. PMID 18419734.CS1 maint: несколько имен: список авторов (связь)
- ^ Eckert SC, Kubler E, Hoffmann B, Braus GH (июнь 2000 г.). «Кодирующий триптофансинтазу ген trpB Aspergillus nidulans регулируется системой контроля перекрестного пути». Мол Джен Генет. 263 (5): 867–76. Дои:10.1007 / s004380000250. PMID 10905354.
- ^ а б c d Рабони С., Беттати С., Моцарелли А. (апрель 2009 г.). «Триптофансинтаза: кладезь энзимологов». Cell Mol Life Sci. 66 (14): 2391–403. Дои:10.1007 / s00018-009-0028-0. HDL:11381/2293687. PMID 19387555.
- ^ а б Фатми М.К., Ай Р., Чанг, Калифорния (сентябрь 2009 г.). «Синергетическая регуляция и лиганд-индуцированные конформационные изменения триптофансинтазы». Биохимия. 48 (41): 9921–31. Дои:10.1021 / bi901358j. PMID 19764814.
- ^ Гришин Н.В., Филлипс М.А., Голдсмит Э.Дж. (июль 1995 г.). «Моделирование пространственной структуры орнитиндекарбоксилаз». Белковая наука. 4 (7): 1291–304. Дои:10.1002 / pro.5560040705. ЧВК 2143167. PMID 7670372.
- ^ Schneider TR, Gerhardt E, Lee M, Liang PH, Anderson KS, Schlichting I (апрель 1998 г.). «Замыкание петли и межсубъединичная коммуникация в триптофансинтазе». Биохимия. 37 (16): 5394–406. Дои:10.1021 / bi9728957. PMID 9548921.
- ^ Хуанг X, Холден HM, Raushel FM (2001). "Направление субстратов и промежуточных продуктов в реакции ферментативных катализаторов". Анну Рев Биохим. 70: 149–80. Дои:10.1146 / annurev.biochem.70.1.149. PMID 11395405.
- ^ Андерсон К.С., Майлз Е.В., Джонсон К.А. (май 1991 г.). «Серин модулирует субстратные каналы в триптофансинтазе. Новый межсубъединичный механизм запуска». J Biol Chem. 266 (13): 8020–33. PMID 1902468.
- ^ Уилкокс, Майкл (1974-06-01). «Ферментативный синтез аналогов l-триптофана». Аналитическая биохимия. 59 (2): 436–440. Дои:10.1016/0003-2697(74)90296-6. PMID 4600987.
- ^ а б c Чаудхари К., Роос Д.С. (сентябрь 2005 г.). «Геномика простейших для открытия лекарств». Nat Biotechnol. 23 (9): 1089–91. Дои:10.1038 / nbt0905-1089. ЧВК 7096809. PMID 16151400.
- ^ Беккер Д., Зельбах М., Ролленхаген С., Баллмайер М., Мейер Т.Ф., Манн М., Буман Д. (март 2006 г.). «Устойчивый метаболизм сальмонелл ограничивает возможности для новых противомикробных препаратов». Природа. 440 (7082): 303–7. Дои:10.1038 / природа04616. PMID 16541065.
- ^ Caldwell HD, Wood H, Crane D, Baily R (июнь 2003 г.). «Полиморфизмы генов триптофансинтазы Chlamydia trachomatis различают генитальные и глазные изоляты». J Clin Invest. 111 (11): 1757–69. Дои:10.1172 / JCI17993. ЧВК 156111. PMID 12782678.
- ^ Кулик В., Хартманн Э., Вейанд М., Фрей М., Гирл А., Никс Д., Данн М. Ф., Шлихтинг I (сентябрь 2005 г.). «На структурной основе каталитического механизма и регуляции α-субъединицы триптофансинтазы из Salmonella typhimurium и BXI из кукурузы, двух эволюционно связанных ферментов». Дж Мол Биол. 352 (3): 608–20. Дои:10.1016 / j.jmb.2005.07.014. PMID 16120446.
- ^ Леопольдседер С., Хеттвер С., Штернер Р. (ноябрь 2006 г.). «Эволюция мультиферментных комплексов: случай триптофансинтазы». Биохимия. 45 (47): 14111–9. Дои:10.1021 / bi061684b. PMID 17115706.
