ACTG1 - ACTG1
Гамма-актин это белок что у людей кодируется ACTG1 ген.[5] Гамма-актин широко экспрессируется в клеточных цитоскелеты из многих тканей; во взрослом поперечно-полосатые мышцы клетки, гамма-актин локализуется в Z-диски и Costamere структуры, которые отвечают за передачу и передачу силы в мышечных клетках. Мутации в ACTG1 были связаны с несиндромная потеря слуха и синдром Барайцера-Винтера, а также восприимчивость подростков к винкристин токсичность.
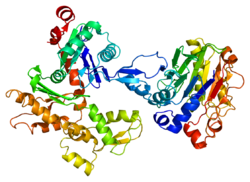
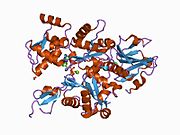
Структура
Гамма-актин человека имеет молекулярную массу 41,8 кДа и 375 кДа. аминокислоты в длину.[6] Актины - это высококонсервативные белки, которые участвуют в различных типах подвижности клеток и поддержании цитоскелета. В позвоночные, три основные группы актина изоформы были определены альфа, бета и гамма.[7]
Альфа-актины содержатся в мышечных тканях и являются основным компонентом саркомер сократительный аппарат. Бета- и гамма-актины сосуществуют в большинстве типов клеток как компоненты цитоскелет, и как медиаторы внутренней подвижности клеток. Актин гамма-1, кодируемый этим геном, обнаруживается в немышечных клетках в цитоплазма, а в мышечных клетках при Costamere структуры или поперечные точки межклеточной адгезии, которые проходят перпендикулярно длинной оси миоциты.[8][9][10]
Функция
В миоциты, саркомеры придерживаться сарколемма через костамеры, которые выравниваются по Z-диски и М-линии.[11] Два основных цитоскелет компоненты костамеры находятся десмин промежуточные нити и гамма-актиновые микрофиламенты.[12] Было показано, что гамма-актин, взаимодействуя с другим костамерический белок дистрофин имеет решающее значение для костамеры формирование механически прочных связей между цитоскелет и сарколеммаль мембрана.[13][14] Дополнительные исследования показали, что гамма-актин колокализуется с альфа-актинин и GFP -меченого гамма-актина, локализованного в Z-диски, в то время как GFP -альфа-актин локализуется на заостренных концах тонких филаментов, что указывает на то, что гамма-актин специфически локализуется в Z-диски в поперечно-полосатые мышцы клетки.[15][16][17]
Во время разработки миоциты считается, что гамма-актин играет роль в организации и сборке развивающихся саркомеры, о чем частично свидетельствует его ранняя совместная локализация с альфа-актинин.[18] Гамма-актин со временем заменяется саркомерный альфа-актин изоформы,[19][20][21] с низким уровнем гамма-актина, сохраняющимся у взрослых миоциты которые связаны с Z-диск и Costamere домены.[15][22][23]
Понимание функции гамма-актина в мышцах было получено в результате исследований с использованием трансгенеза. В скелетные мышцы -специфический нокаут гамма-актина у мышей, у этих животных не обнаруживались отклонения в развитии; однако мыши с нокаутом показали мышечную слабость и волокно некроз, наряду с уменьшением изометрическая сила подергивания, нарушены внутрифибриллярные и межфибриллярные связи между миоциты, и миопатия.[24]
Клиническое значение
Аутосомно-доминантная мутация в ACTG1 в локусе DFNA20 / 26 на 17q25-qter был идентифицирован у пациентов с потерей слуха. А Thr 278Иль мутация была обнаружена в спирали 9 гамма-актина белок, который, как ожидается, изменит белок структура. Это исследование выявило первую мутацию, вызывающую заболевание в гамма-актине, и обосновало важность гамма-актина как структурных элементов волосковых клеток внутреннего уха.[25] С тех пор другие ACTG1 мутации были связаны с несиндромная потеря слуха, включая Встретились 305Thr.[26]
Миссенс-мутация в ACTG1 в Сер 155Phe также был выявлен у пациентов с Синдром Барайцера-Винтера, которое представляет собой нарушение развития, характеризующееся врожденным птоз, чрезмерно изогнутые брови, гипертелоризм, окуляр колобомы, лиссэнцефалия, низкий рост, судороги и потеря слуха.[27][28]
Дифференциальное выражение ACTG1 мРНК также был выявлен у пациентов с Спорадический боковой амиотрофический склероз, разрушительное заболевание с неизвестной причинно-следственной связью, используя сложную биоинформатика подход с использованием Affymetrix Длинноолигонуклеотидные методы BaFL.[29]
Полиморфизмы одиночных нуклеотидов в ACTG1 были связаны с винкристин токсичность, которая является частью стандартной схемы лечения для детей острый лимфобластный лейкоз. Нейротоксичность чаще встречается у пациентов, которые ACTG1 Gly 310Ала носители мутации, предполагая, что это может играть роль в исходах пациентов от винкристин лечение.[30]
Взаимодействия
ACTG1 был показан взаимодействовать с:
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000184009 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000062825 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Entrez Gene: ACTG1 актин, гамма 1".
- ^ «Последовательность белка для человеческого ACTG1 (Uniprot ID: P63261)». Атлас кардиоорганических белков (COPaKB). Архивировано из оригинал 21 июля 2015 г.. Получено 18 июля 2015.
- ^ Рубинштейн PA (июль 1990 г.). «Функциональное значение множества изоформ актина». BioEssays. 12 (7): 309–15. Дои:10.1002 / bies.950120702. PMID 2203335. S2CID 2163289.
- ^ Крейг С.В., Пардо СП (1983). «Гамма-актин, спектрин и белки промежуточных филаментов совместно локализуются с винкулином на костамерах, сайтах прикрепления миофибрилл к сарколемме». Подвижность клеток. 3 (5–6): 449–62. Дои:10.1002 / см. 970030513. PMID 6420066.
- ^ Пардо СП, Силичиано Д.Д., Крейг С.В. (февраль 1983 г.). «Винкулин-содержащая кортикальная решетка в скелетных мышцах: элементы поперечной решетки (« костамеры ») отмечают места прикрепления между миофибриллами и сарколеммой». Труды Национальной академии наук Соединенных Штатов Америки. 80 (4): 1008–12. Bibcode:1983ПНАС ... 80.1008П. Дои:10.1073 / pnas.80.4.1008. ЧВК 393517. PMID 6405378.
- ^ Дановски Б.А., Иманака-Йошида К., Сангер Дж. М., Сангер Дж. В. (сентябрь 1992 г.). «Костамеры - это места передачи силы на субстрат кардиомиоцитов взрослых крыс». Журнал клеточной биологии. 118 (6): 1411–20. Дои:10.1083 / jcb.118.6.1411. ЧВК 2289604. PMID 1522115.
- ^ Кларк К.А., Макэлхинни А.С., Беккерл М.С., Грегорио С.К. (2002). «Цитоархитектура поперечно-полосатых мышц: сложная сеть форм и функций». Ежегодный обзор клеточной биологии и биологии развития. 18: 637–706. Дои:10.1146 / annurev.cellbio.18.012502.105840. PMID 12142273.
- ^ Ки А.Дж., Ганнинг П.В., Hardeman EC (2009). «Разнообразные роли актинового цитоскелета в поперечно-полосатых мышцах». Журнал исследований мышц и подвижности клеток. 30 (5–6): 187–97. Дои:10.1007 / s10974-009-9193-х. PMID 19997772. S2CID 6632615.
- ^ а б Рыбакова И.Н., Патель Дж. Р., Эрвасти Дж. М. (сентябрь 2000 г.). «Дистрофиновый комплекс образует механически прочную связь между сарколеммой и костамерным актином». Журнал клеточной биологии. 150 (5): 1209–14. Дои:10.1083 / jcb.150.5.1209. ЧВК 2175263. PMID 10974007.
- ^ Эрвасти JM (апрель 2003 г.). «Костамеры: ахиллесова пята геркулесовой мышцы». Журнал биологической химии. 278 (16): 13591–4. Дои:10.1074 / jbc.R200021200. PMID 12556452.
- ^ а б Наката Т., Нишина Ю., Йорифудзи Х. (август 2001 г.). «Цитоплазматический гамма-актин как белок Z-диска». Сообщения о биохимических и биофизических исследованиях. 286 (1): 156–63. Дои:10.1006 / bbrc.2001.5353. PMID 11485322.
- ^ Паппонен Х., Кайсто Т., Лейнонен С., Каакинен М., Метсикко К. (январь 2009 г.). «Доказательства гамма-актина как компонента Z диска в скелетных миофибриллах». Экспериментальные исследования клеток. 315 (2): 218–25. Дои:10.1016 / j.yexcr.2008.10.021. PMID 19013151.
- ^ Влахович Н., Ки А.Дж., Ван дер Поэль С., Чайник Э., Эрнандес-Девиес Д., Лукас С., Линч Г.С., Партон Р.Г., Ганнинг П.В., Хардеман Э.С. (январь 2009 г.). «Цитоскелетный тропомиозин Tm5NM1 необходим для нормальной связи возбуждения и сокращения в скелетных мышцах». Молекулярная биология клетки. 20 (1): 400–9. Дои:10.1091 / mbc.E08-06-0616. ЧВК 2613127. PMID 19005216.
- ^ Ллойд С.М., Берендсе М., Ллойд Д.Г., Шевцов Г., Grounds MD (июль 2004 г.). «Новая роль немышечного гамма-актина в сборке саркомеров скелетных мышц». Экспериментальные исследования клеток. 297 (1): 82–96. Дои:10.1016 / j.yexcr.2004.02.012. PMID 15194427.
- ^ Шварц Р. Дж., Ротблюм К. Н. (июль 1981 г.). «Переключение генов в миогенезе: дифференциальная экспрессия мультигенного семейства куриного актина». Биохимия. 20 (14): 4122–9. Дои:10.1021 / bi00517a027. PMID 7284314.
- ^ Шани М., Зевин-Сонкин Д., Саксель О., Кармон И., Каткофф Д., Нудель Ю., Яффе Д. (сентябрь 1981 г.). «Корреляция между синтезом актина скелетных мышц, тяжелой цепи миозина и легкой цепью миозина и накоплением соответствующих последовательностей мРНК во время миогенеза». Биология развития. 86 (2): 483–92. Дои:10.1016/0012-1606(81)90206-2. PMID 7286410.
- ^ фон Аркс П., Бантл С., Солдати Т., Перриар Дж.С. (декабрь 1995 г.). «Доминирующее негативное влияние цитоплазматических изопротеидов актина на цитоархитектуру и функцию кардиомиоцитов». Журнал клеточной биологии. 131 (6, п. 2): 1759–73. Дои:10.1083 / jcb.131.6.1759. ЧВК 2120671. PMID 8557743.
- ^ Hanft LM, Bogan DJ, Mayer U, Kaufman SJ, Kornegay JN, Ervasti JM (июль 2007 г.). «Экспрессия цитоплазматического гамма-актина в различных животных моделях мышечной дистрофии». Нервно-мышечные расстройства. 17 (7): 569–74. Дои:10.1016 / j.nmd.2007.03.004. ЧВК 1993539. PMID 17475492.
- ^ Ки А.Дж., Шевцов Г., Наир-Шалликер В., Робинсон К.С., Врховски Б., Годдуси М., Цю М.Р., Лин Дж.Дж., Вайнбергер Р., Ганнинг П.В., Хардеман Э.С. (август 2004 г.). «Сортировка немышечного тропомиозина в новый цитоскелетный компартмент в скелетных мышцах приводит к мышечной дистрофии». Журнал клеточной биологии. 166 (5): 685–96. Дои:10.1083 / jcb.200406181. ЧВК 2172434. PMID 15337777.
- ^ Зоннеманн К.Дж., Фитцсимонс Д.П., Патель-младший, Лю Й., Шнайдер М.Ф., Мосс Р.Л., Эрвасти Дж.М. (сентябрь 2006 г.). «Цитоплазматический гамма-актин не требуется для развития скелетных мышц, но его отсутствие приводит к прогрессирующей миопатии». Клетка развития. 11 (3): 387–97. Дои:10.1016 / j.devcel.2006.07.001. PMID 16950128.
- ^ ван Вейк Э., Кригер Э., Кемперман М. Х., Де Линхеер Е. М., Хюйген П. Л., Кремерс С. В., Кремерс Ф. П., Кремер Х. (декабрь 2003 г.). «Мутация в гене гамма-актина 1 (ACTG1) вызывает аутосомно-доминантную потерю слуха (DFNA20 / 26)». Журнал медицинской генетики. 40 (12): 879–84. Дои:10.1136 / jmg.40.12.879. ЧВК 1735337. PMID 14684684.
- ^ Park G, Gim J, Kim AR, Han KH, Kim HS, Oh SH, Park T, Park WY, Choi BY (18 марта 2013 г.). «Многофазный анализ данных секвенирования всего экзома выявил новую мутацию ACTG1 в семье с несиндромной потерей слуха». BMC Genomics. 14: 191. Дои:10.1186/1471-2164-14-191. ЧВК 3608096. PMID 23506231.
- ^ Ривьер Дж. Б., ван Бон Б. В., Хойшен А., Холманских СС, О'Роак Б. Дж., Гилиссен С., Гийсен С., Салливан С. Т., Кристиан С. Л., Абдул-Рахман О. А., Аткин Дж. Ф., Чассен Н., Друин-Гарро В., Фрай А. Э., Фринс JP, Gripp KW, Kempers M, Kleefstra T, Mancini GM, Nowaczyk MJ, van Ravenswaaij-Arts CM, Roscioli T, Marble M, Rosenfeld JA, Siu VM, de Vries BB, Shendure J, Verloes A, Veltman JA, Brunner HG , Росс ME, Pilz DT, Dobyns WB (апрель 2012 г.). «Мутации de novo в генах актина ACTB и ACTG1 вызывают синдром Барайцера-Винтера». Природа Генетика. 44 (4): 440–4, S1–2. Дои:10.1038 / ng.1091. ЧВК 3677859. PMID 22366783.
- ^ Ди Донато Н., Рамп А, Кениг Р., Дер Калоустиан В. М., Халяль Ф, Зоннтаг К., Краузе С., Хакманн К., Хан Дж., Шрок Е., Верлоес А. (февраль 2014 г.). «Тяжелые формы синдрома Барайцера-Винтера вызваны мутациями ACTB, а не мутациями ACTG1». Европейский журнал генетики человека. 22 (2): 179–83. Дои:10.1038 / ejhg.2013.130. ЧВК 3895648. PMID 23756437.
- ^ Бачу К., Томпсон К.Дж., Мужо Дж. Л., Брукс Б. Р., Веллер Дж. В. (24 сентября 2012 г.). «Метод LO-BaFL и анализ экспрессии микрочипов ALS». BMC Bioinformatics. 13: 244. Дои:10.1186/1471-2105-13-244. ЧВК 3526454. PMID 23006766.
- ^ Ceppi F, Langlois-Pelletier C, Gagné V, Rousseau J, Ciolino C, De Lorenzo S, Kevin KM, Cijov D, Sallan SE, Silverman LB, Neuberg D, Kutok JL, Sinnett D, Laverdière C, Krajinovic M (июнь 2014 г.) ). «Полиморфизмы пути винкристина и ответ на лечение у детей с острым лимфобластным лейкозом в детском возрасте». Фармакогеномика. 15 (8): 1105–16. Дои:10.2217 / стр. 14.68. ЧВК 4443746. PMID 25084203.
- ^ Hubberstey A, Yu G, Loewith R, Lakusta C, Young D (июнь 1996 г.). «CAP млекопитающих взаимодействует с CAP, CAP2 и актином». Журнал клеточной биохимии. 61 (3): 459–66. Дои:10.1002 / (SICI) 1097-4644 (19960601) 61: 3 <459 :: AID-JCB13> 3.0.CO; 2-E. PMID 8761950.
- ^ Герцог М., ван Хейеноорт С., Дидри Д., Годье М., Кутан Дж., Гигант Б., Дидело Дж., Прит Т., Кносов М., Гиттет Е., Карлье М. «Бета-тимозин / домен WH2; структурная основа для переключения от ингибирования к стимулированию сборки актина». Клетка. 117 (5): 611–23. Дои:10.1016 / S0092-8674 (04) 00403-9. PMID 15163409. S2CID 8628287.
- ^ Ван Тройс М., Девитт Д., Геталс М., Карлье М.Ф., Вандекеркхов Дж., Ампе С. (январь 1996 г.). «Сайт связывания актина тимозина бета 4, картированный с помощью мутационного анализа». Журнал EMBO. 15 (2): 201–10. Дои:10.1002 / j.1460-2075.1996.tb00350.x. ЧВК 449934. PMID 8617195.
- ^ Хидзиката Т., Накамура А., Исокава К., Имамура М., Юаса К., Исикава Р., Кохама К., Такеда С., Йорифудзи Х. (июнь 2008 г.). «Плектин 1 связывает промежуточные филаменты с костамерной сарколеммой через бета-синемин, альфа-дистробревин и актин». Журнал клеточной науки. 121 (Pt 12): 2062–74. Дои:10.1242 / jcs.021634. PMID 18505798.
внешняя ссылка
- Человек ACTG1 расположение генома и ACTG1 страница сведений о генах в Браузер генома UCSC.
дальнейшее чтение
- Snásel J, Pichová I (1997). «Расщепление белков клетки-хозяина протеазой ВИЧ-1». Folia Biologica. 42 (5): 227–30. Дои:10.1007 / BF02818986. PMID 8997639. S2CID 7617882.
- Родригес Дель Кастильо А., Витале М.Л., Трифаро Дж. М. (ноябрь 1992 г.). «Ca2 + и pH определяют взаимодействие сциндерина хромаффинных клеток с фосфатидилсерином и фосфатидилинозитол-4,5, -бифосфатом и его клеточное распределение во время стимуляции никотиновых рецепторов и активации протеинкиназы C». Журнал клеточной биологии. 119 (4): 797–810. Дои:10.1083 / jcb.119.4.797. ЧВК 2289683. PMID 1331119.
- Адамс Л.Д., Томасселли А.Г., Роббинс П., Мосс Б., Хейнриксон Р.Л. (февраль 1992 г.). «Протеаза ВИЧ-1 расщепляет актин во время острой инфекции Т-лимфоцитов человека». Исследования СПИДа и ретровирусы человека. 8 (2): 291–5. Дои:10.1089 / помощь.1992.8.291. PMID 1540415.
- Доусон С.Дж., Белый Лос-Анджелес (май 1992 г.). «Лечение эндокардита Haemophilus aphrophilus ципрофлоксацином». Журнал инфекции. 24 (3): 317–20. Дои:10.1016 / S0163-4453 (05) 80037-4. PMID 1602151.
- Томасселли А.Г., Хуэй Дж.О., Адамс Л., Чосей Дж., Лоури Д., Гринберг Б., Йем А., Дейбель М.Р., Цюрхер-Нили Х., Хейнриксон Р.Л. (август 1991). «Актин, тропонин С, белок-предшественник амилоида Альцгеймера и про-интерлейкин 1 бета в качестве субстратов протеазы вируса иммунодефицита человека». Журнал биологической химии. 266 (22): 14548–53. PMID 1907279.
- Шуман Р.Л., Кессельмиер С., Мотес Е., Хенер Б., Трауб П. (январь 1991 г.). «Невирусные клеточные субстраты для протеазы вируса иммунодефицита человека типа 1». Письма FEBS. 278 (2): 199–203. Дои:10.1016 / 0014-5793 (91) 80116-К. PMID 1991513. S2CID 37002682.
- Эрба Х.П., Эдди Р., Шоу Т., Кедес Л., Ганнинг П. (апрель 1988 г.). «Структура, расположение хромосомы и экспрессия гена гамма-актина человека: дифференциальная эволюция, расположение и экспрессия генов бета- и гамма-актина цитоскелета». Молекулярная и клеточная биология. 8 (4): 1775–89. Дои:10.1128 / mcb.8.4.1775. ЧВК 363338. PMID 2837653.
- Vandekerckhove J, Schering B, Bärmann M, Aktories K (январь 1988 г.). «Ботулинический токсин C2, АДФ-рибозилат цитоплазматического бета / гамма-актина в аргинине 177». Журнал биологической химии. 263 (2): 696–700. PMID 3335520.
- Чоу С.К., Дэвис Р.К., Фуллер М.Л., Словин Дж. П., Вонг А., Райт Дж., Каниа С., Шакед Р., Гатти Р. А., Сальсер В. А. (май 1987 г.). «Гамма-актин: сохранение необычной 3'-нетранслируемой последовательности мРНК и аминокислотные замены, которые могут быть связаны с раком». Труды Национальной академии наук Соединенных Штатов Америки. 84 (9): 2575–9. Bibcode:1987PNAS ... 84.2575C. Дои:10.1073 / пнас.84.9.2575. ЧВК 304700. PMID 3472224.
- Хестерберг Л.К., Вебер К. (январь 1986 г.). «Выделение домена виллина, сохраняющего кальций-зависимое взаимодействие с G-актином, но лишенного активности фрагментирования F-актина». Европейский журнал биохимии / FEBS. 154 (1): 135–40. Дои:10.1111 / j.1432-1033.1986.tb09368.x. PMID 3510866.
- Эрба Х.П., Ганнинг П., Кедес Л. (июль 1986 г.). «Нуклеотидная последовательность мРНК гамма-цитоскелета актина человека: аномальная эволюция немышечных генов актина позвоночных». Исследования нуклеиновых кислот. 14 (13): 5275–94. Дои:10.1093 / nar / 14.13.5275. ЧВК 311540. PMID 3737401.
- Fuchs E, Kim KH, Hanukoglu I, Tanese N (1984). «Эволюция и сложность генов, кодирующих белки цитоскелета эпидермальных клеток человека». Актуальные проблемы дерматологии. 11: 27–44. Дои:10.1159/000408662. ISBN 978-3-8055-3752-0. PMID 6686106.
- Ганнинг П., Понте П., Окаяма Х, Энгель Дж., Блау Х., Кедес Л. (май 1983 г.). «Выделение и характеристика полноразмерных клонов кДНК для мРНК альфа-, бета- и гамма-актина человека: скелетные, но не цитоплазматические актины имеют амино-концевой цистеин, который впоследствии удаляется». Молекулярная и клеточная биология. 3 (5): 787–95. Дои:10.1128 / mcb.3.5.787. ЧВК 368601. PMID 6865942.
- Бретчер А., Вебер К. (июль 1980 г.). «Виллин - это главный белок цитоскелета микроворсинок, который связывает как G, так и F-актин кальций-зависимым образом». Клетка. 20 (3): 839–47. Дои:10.1016 / 0092-8674 (80) 90330-Х. PMID 6893424. S2CID 568395.
- Педротти Б., Коломбо Р., Ислам К. (1995). «Связанный с микротрубочками белок MAP1A представляет собой актин-связывающий и сшивающий белок». Подвижность клеток и цитоскелет. 29 (2): 110–6. Дои:10.1002 / см. 970290203. PMID 7820861.
- Папа Б, Макивер С., Сорняки А (февраль 1995 г.). «Локализация кальций-чувствительного сайта связывания мономера актина в гельсолине в сегменте 4 и идентификация сайтов связывания кальция». Биохимия. 34 (5): 1583–8. Дои:10.1021 / bi00005a014. PMID 7849017.
- Йезайтис А.Дж., Эриксон Р.В., Клотц К.Н., Боммаканти Р.К., Симсен Д.В. (ноябрь 1993 г.). «Функциональные молекулярные комплексы рецепторов хемоаттрактанта N-формила человека и актина». Журнал иммунологии. 151 (10): 5653–65. PMID 8228254.
- Хокинс М., Папа Б, Макивер С.К., Weeds AG (сентябрь 1993 г.). «Человеческий фактор деполимеризации актина опосредует pH-чувствительное разрушение актиновых филаментов». Биохимия. 32 (38): 9985–93. Дои:10.1021 / bi00089a014. PMID 8399167.
- Ю. FX, Лин С. К., Моррисон-Богорад М., Аткинсон М. А., Инь Х. Л. (январь 1993 г.). «Тимозин бета 10 и тимозин бета 4 являются белками, связывающими мономер актина». Журнал биологической химии. 268 (1): 502–9. PMID 8416954.
- Jalaguier S, Mornet D, Mesnier D, Léger JJ, Auzou G (апрель 1996 г.). «Минералокортикоидный рецептор человека взаимодействует с актином при модуляции минералокортикоидного лиганда». Письма FEBS. 384 (2): 112–6. Дои:10.1016/0014-5793(96)00295-5. PMID 8612804. S2CID 34685894.