Актин - Actin
| Актин | |||||||||
|---|---|---|---|---|---|---|---|---|---|
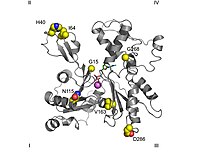
 Ленточная диаграмма G-актина. ADP связан с актином активный сайт (многоцветные палочки возле центра рисунка), а также сложный кальций дикция (зеленая сфера) выделены.[1] | |||||||||
| Идентификаторы | |||||||||
| Символ | Актин | ||||||||
| Pfam | PF00022 | ||||||||
| ИнтерПро | IPR004000 | ||||||||
| PROSITE | PDOC00340 | ||||||||
| SCOP2 | 2btf / Объем / СУПФАМ | ||||||||
| |||||||||
Актин это семья из шаровидный многофункциональный белки эта форма микрофиламенты. Он присутствует практически во всех эукариотические клетки, где он может присутствовать в концентрации более 100 мкМ; его масса примерно 42-кДа, диаметром от 4 до 7 нм.
Белок актина - это мономерный подразделение двух типов нитей в клетках: микрофиламенты, один из трех основных компонентов цитоскелет, и тонкие нити, входящие в состав сократительный аппарат в мышца клетки. Может присутствовать как бесплатный мономер называется G-актин (шаровидный) или как часть линейного полимер микрофиламент называется F-актин (нитчатые), оба из которых необходимы для таких важных клеточных функций, как мобильность и сокращение клетки в течение деление клеток.
Актин участвует во многих важных клеточных процессах, в том числе сокращение мышц, клетка подвижность, деление клеток и цитокинез, везикул и органелла движение, клеточная сигнализация, а также создание и поддержание клеточные соединения и форма ячейки. Многие из этих процессов опосредуются обширными и интимными взаимодействиями актина с клеточные мембраны.[2] У позвоночных три основных группы актина изоформы, альфа, бета, и гамма были идентифицированы. Альфа-актины, обнаруженные в мышечных тканях, являются основной составляющей сократительного аппарата. Бета- и гамма-актины сосуществуют в большинстве типов клеток как компоненты цитоскелет, и, как посредники внутренней ячейки подвижность. Считается, что разнообразный спектр структур, образованных актином, позволяющих ему выполнять такой широкий спектр функций, регулируется посредством связывания тропомиозина вдоль филаментов.[3]
Способность клетки динамически формировать микрофиламенты обеспечивает основу, которая позволяет ей быстро реконструировать себя в ответ на окружающую среду или внутренние органы организма. сигналы, например, для увеличения абсорбции клеточной мембраны или увеличения клеточная адгезия чтобы сформировать ячейку ткань. Другие ферменты или органеллы Такие как реснички могут быть прикреплены к этим лесам, чтобы контролировать деформацию внешних клеточная мембрана, который позволяет эндоцитоз и цитокинез. Он также может производить движение самостоятельно или с помощью молекулярные моторы. Таким образом, актин участвует в таких процессах, как внутриклеточный транспорт пузырьки и органеллы, а также мышечное сокращение и клеточная миграция. Поэтому он играет важную роль в эмбриогенез, заживление ран и инвазивность рак клетки. Эволюционное происхождение актина можно проследить до прокариотические клетки, которые имеют эквивалентные белки.[4] Гомологи актина прокариот и архей полимеризуются в различные спиральные или линейные филаменты, состоящие из одной или нескольких цепей. Однако внутрицепочечные контакты и сайты связывания нуклеотидов сохраняются у прокариот и архей.[5] Наконец, актин играет важную роль в контроле экспрессия гена.
Большое количество болезни и болезни вызваны мутации в аллели из гены которые регулируют производство актина или связанных с ним белков. Производство актина также является ключом к процессу инфекционное заболевание некоторыми патогенный микроорганизмы. Мутации в различных генах, регулирующих производство актина у людей, могут вызывать мышечные заболевания, вариации в размере и функциях сердце а также глухота. Состав цитоскелета также связан с патогенностью внутриклеточного бактерии и вирусы, особенно в процессах, связанных с уклонением от действий иммунная система.[6]
Открытие и раннее расследование

Актин был впервые обнаружен экспериментально в 1887 г. W.D. Halliburton, который извлек из мышц белок, который «коагулировал» препараты миозин что он назвал «миозин-фермент».[7] Однако компания Halliburton не смогла уточнить свои открытия, и открытие актина приписывают Бруно Ференц Штрауб, молодой биохимик работает в Альберт Сент-Дьёрдьи лаборатория в Институте медицинской химии Сегедский университет, Венгрия.
После открытия Илона Банга & Szent-Györdi в 1941 г., что коагуляция происходит только при некоторых экстрактах мизозина и полностью меняется при добавлении АТФ,[8] Штрауб идентифицировал и очищал актин из тех препаратов миозина, которые действительно коагулировали. Основываясь на оригинальном методе извлечения Банги, он разработал новую технику для извлечение мышечный белок, который позволил ему выделить значительное количество относительно чистый actin, опубликованный в 1942 г.[9] Метод Штрауба по сути тот же, что и в лаборатории сегодня. Поскольку белок Штрауба был необходим для активации коагуляции миозина, его окрестили актин.[8][10] Понимая, что препараты коагулирующего миозина Банги также содержат актин, Сент-Дьерди назвал смесь обоих белков актомиозин.[11]
Военные действия Вторая Мировая Война означало, что Сент-Дьёрджи не смог опубликовать работу своей лаборатории в Западный научные журналы. Таким образом, Актин стал хорошо известен на Западе только в 1945 году, когда их статья была опубликована в качестве дополнения к Acta Physiologica Scandinavica.[12] Штрауб продолжал работать над актином и в 1950 году сообщил, что актин содержит связанный АТФ[13] и что во время полимеризация белка в микрофиламенты, то нуклеотид является гидролизованный к ADP и неорганические фосфат (которые остаются связанными с микрофиламентом). Штрауб предположил, что преобразование АТФ-связанного актина в АДФ-связанный актин играет роль в мышечном сокращении. На самом деле это верно только в гладкая мышца, и не поддерживался экспериментально до 2001 года.[13][14]
В аминокислотное секвенирование актина был завершен M. Elzinga с сотрудниками в 1973 г.[15] В Кристальная структура G-актина была решена в 1990 году Kabsch и соавторами.[16] В том же году Холмс и его коллеги предложили модель F-актина после экспериментов с использованием совместной кристаллизации с различными белками.[17] Процедура совместной кристаллизации с различными белками использовалась неоднократно в течение следующих лет, пока в 2001 году изолированный белок не кристаллизовался вместе с АДФ. Однако до сих пор нет рентгеновской структуры F-актина с высоким разрешением. Кристаллизация F-актина стала возможной благодаря использованию родамин конъюгат, который препятствует полимеризации, блокируя аминокислоту cys-374.[1] Кристин Ориол-Аудит умерла в том же году, когда актин был впервые кристаллизован, но она была исследователем, который в 1977 году впервые кристаллизовал актин в отсутствие актин-связывающих белков (ABP). Однако полученные кристаллы были слишком маленькими для доступных технологий того времени.[18]
Хотя в настоящее время не существует модели нитевидной формы актина с высоким разрешением, в 2008 году команда Савайи смогла создать более точную модель ее структуры на основе нескольких кристаллов актина. димеры которые связывают в разных местах.[19] Впоследствии эта модель была усовершенствована Савайей и Лоренцем. Другие подходы, такие как использование криоэлектронная микроскопия и синхротронное излучение недавно позволили увеличить разрешение и лучше понять природу взаимодействий и конформационных изменений, участвующих в формировании актиновых филаментов.[20][21][22]
Структура
Актина аминокислотная последовательность один из самых высоких консервированный белков, поскольку он мало изменился в течение эволюция, отличающиеся не более чем на 20% по разновидность столь же разнообразный, как водоросли и люди.[23] Поэтому считается, что оптимизированный структура.[4] У него есть две отличительные особенности: это фермент так медленно гидролизует АТФ, «универсальная энергетическая валюта» биологических процессов. Однако для сохранения структурной целостности требуется АТФ. Его эффективная структура состоит из практически уникального складывание процесс. Кроме того, он может выполнять больше взаимодействия чем любой другой белок, что позволяет ему выполнять более широкий спектр функций, чем другие белки, практически на всех уровнях клеточной жизни.[4] Миозин является примером белка, который связывается с актином. Другой пример Виллин, которые могут сплетать актин в пучки или разрезать нити в зависимости от концентрации кальций катионы в окружающей среде.[24]
Актин - один из самых распространенных белков в эукариоты, где он находится по всей цитоплазме.[24] Фактически, в мышечные волокна он составляет 20% от общего клеточного белка по весу и от 1% до 5% в других клетках. Однако существует не только один тип актина; в гены этот код для актина определяется как генная семья (семейство, которое в растениях содержит более 60 элементов, включая гены и псевдогены а в человеке более 30 элементов).[4][25] Это означает, что генетическая информация каждого человека содержит инструкции, которые генерируют варианты актина (называемые изоформы ), которые обладают несколько другими функциями. Это, в свою очередь, означает, что эукариотические организмы выражать различные гены, дающие начало: α-актину, который находится в сократительных структурах; β-актин, обнаруженный на расширяющейся границе клеток, которые используют выступ своих клеточных структур как средство передвижения; и γ-актин, который находится в филаментах стрессовые волокна.[26] В дополнение к сходству, которое существует между изоформами организма, существует также эволюционное сохранение в структуре и функциях даже между организмами, содержащимися в разных эукариотических домены. В бактерии актин гомолог MreB был идентифицирован белок, способный полимеризоваться в микрофиламенты;[4][21] И в археи гомолог Ta0583 даже больше похож на эукариотические актины.[27]
Клеточный актин имеет две формы: мономерный. глобулы называется G-актин и полимерный филаменты, называемые F-актином (то есть филаменты, состоящие из многих мономеров G-актина). F-актин также можно описать как микрофиламент. Две параллельные нити F-актина должны повернуться на 166 градусов, чтобы правильно ложиться друг на друга. Это создает двойную спиральную структуру микрофиламентов цитоскелета. Микрофиламенты имеют размер примерно 7 нм диаметром со спиралью, повторяющейся через каждые 37 нм. Каждая молекула актина связана с молекулой аденозинтрифосфат (ATP) или аденозиндифосфат (ADP), который связан с Mg2+ катион. Наиболее часто встречающиеся формы актина по сравнению со всеми возможными комбинациями - это АТФ-G-актин и АДФ-F-актин.[28][29]
Джи-Актин
Растровый электронный микроскоп изображения показывают, что G-актин имеет глобулярную структуру; тем не мение, Рентгеновская кристаллография показывает, что каждая из этих глобул состоит из двух долей, разделенных щелью. Эта структура представляет собой «складку АТФазы», которая является центром ферментативный катализ связывающий АТФ и Mg2+ и гидролизует первый до АДФ плюс фосфат. Эта складка является консервативным структурным мотивом, который также встречается в других белках, которые взаимодействуют с трифосфатом. нуклеотиды Такие как гексокиназа (фермент, используемый в энергии метаболизм ) или в Hsp70 белки (семейство белков, играющих важную роль в сворачивании белков).[30] G-актин функционален только тогда, когда он содержит АДФ или АТФ в своей щели, но форма, связанная с АТФ, преобладает в клетках, когда актин присутствует в свободном состоянии.[28]

В Рентгеновская кристаллография модель актина, созданная Кабшем из поперечно-полосатая мышечная ткань из кролики является наиболее часто используемым в структурных исследованиях, поскольку он был первым очищенный. G-актин, кристаллизованный Кабшем, имеет размер примерно 67 x 40 x 37 Å по размеру, имеет молекулярная масса из 41785 Да и предполагаемый изоэлектрическая точка из 4.8. Его результирующий заряд в pH = 7 равно -7.[15][31]
- Первичная структура
Эльзинга и его коллеги первыми определили полную пептидная последовательность для этого типа актина в 1973 г., а более поздние работы того же автора добавили дополнительные детали к модели. Он содержит 374 аминокислота остатки. Его N-конец очень кислый и начинается с ацетилированный аспартат в своей аминогруппе. Пока его C-конец является щелочной и состоит из фенилаланин предшествует цистеин, имеющий определенную степень функционального значения. Обе крайности находятся в непосредственной близости внутри I-поддомена. Аномальный Nτ-метилгистидин находится в позиции 73.[31]
- Третичная структура - домены
Третичная структура образована двумя домены известное как большое и малое, которые разделены щелью, расположенной вокруг места соединения с АТФ -ADP +пя. Ниже находится более глубокая выемка, называемая «канавкой». в родное государство, несмотря на их названия, оба имеют сопоставимую глубину.[15]
Обычное соглашение в топологический Исследования означает, что белок показан с самым большим доменом слева и самым маленьким доменом с правой стороны. В этом положении меньший домен, в свою очередь, делится на два: субдомен I (нижнее положение, остатки 1–32, 70–144 и 338–374) и субдомен II (верхнее положение, остатки 33–69). Более крупный домен также делится на два: субдомен III (нижний, остатки 145–180 и 270–337) и субдомен IV (верхний, остатки 181–269). Открытые области субдоменов I и III называются «зазубренными» концами, тогда как открытые области доменов II и IV называются «заостренными» концами. Эта номенклатура относится к тому факту, что из-за небольшой массы субдомена Актин II полярен, важность этого будет обсуждаться ниже при обсуждении динамики сборки.Некоторые авторы называют субдомены Ia, Ib, IIa и IIb соответственно.[32]
- Другие важные сооружения
Наиболее заметная сверхвторичная структура - это пятицепочечная бета-лист который состоит из β-меандра и блока β-α-β по часовой стрелке. Он присутствует в обоих доменах, что позволяет предположить, что белок возник в результате дупликации гена.[16]
- В аденозиновый нуклеотид сайт связывания находится между двумя бета шпилька -образные структуры, относящиеся к I и III доменам. Вовлеченные остатки представляют собой Asp11-Lys18 и Asp154-His161 соответственно.
- В двухвалентный катион сайт связывания расположен чуть ниже, чем для аденозинового нуклеотида. В естественных условиях чаще всего формируется Mg2+ или же Ca2+ пока in vitro он образован хелатирующей структурой, состоящей из Lys18 и два кислород от α- и β- нуклеотидовфосфаты. Этот кальций координируется с шестью молекулами воды, которые удерживаются аминокислотами. Asp11, Asp154 и Gln137. Они образуют комплекс с нуклеотидом, который ограничивает движения так называемой «шарнирной» области, расположенной между остатками 137 и 144. Это поддерживает нативную форму белка до его удаления. денатурирует мономер актина. Эта область также важна, потому что она определяет, находится ли расщелина белка в «открытой» или «закрытой» конформации.[1][32]
- Весьма вероятно, что есть как минимум три других центра с меньшим близость (промежуточный) и еще другие с низким сродством к двухвалентным катионам. Было высказано предположение, что эти центры могут играть роль в полимеризации актина, действуя на стадии активации.[32]
- В субдомене 2 есть структура, которая называется «D-петля», потому что она связана с ДНКаза I, он расположен между Его40 и Gly48 остатки. Он имеет вид неупорядоченного элемента в большинстве кристаллов, но он выглядит как β-лист, когда он находится в комплексе с ДНКазой I. Было высказано предположение, что ключевым событием полимеризации, вероятно, является распространение конформационных изменений из центр связи с нуклеотидом с этим доменом, который изменяется от петли к спирали.[1] Однако эта гипотеза была опровергнута другими исследованиями.[33]
F-Актин

Классическое описание F-актина утверждает, что он имеет нитевидную структуру, которую можно рассматривать как одноцепочечную. левовращающий спираль с поворотом на 166 ° вокруг винтовой оси и осевым перемещением 27,5 Å, или одноцепочечный правовращающий спираль с шагом кроссовера 350–380 Å, причем каждый актин окружен еще четырьмя.[34] Симметрия полимера актина при 2,17 субъединицах на оборот спирали несовместима с образованием кристаллы, что возможно только при симметрии ровно 2, 3, 4 или 6 субъединиц на ход. Следовательно, модели должны быть построены, чтобы объяснить эти аномалии, используя данные из электронная микроскопия, криоэлектронная микроскопия, кристаллизация димеров в различных положениях и дифракция рентгеновских лучей.[21][22] Следует отметить, что говорить о «структуре» такой динамичной молекулы, как актиновый филамент, некорректно. На самом деле мы говорим о различных структурных состояниях, в них измерение осевой трансляции остается постоянным на уровне 27,5 Å, в то время как данные о вращении субъединицы демонстрируют значительную изменчивость с обычно наблюдаемыми смещениями до 10% от ее оптимального положения. Некоторые белки, такие как кофилин кажется, увеличивают угол поворота, но опять же это можно интерпретировать как установление различных структурных состояний. Это может быть важно в процессе полимеризации.[35]
Меньшее согласие наблюдается в отношении измерений радиуса витка и толщины волокна: в то время как первые модели приписывали длину 25 Å, текущие данные дифракции рентгеновских лучей, подтвержденные криоэлектронной микроскопией, предполагают длину 23,7 Å. Эти исследования показали точные точки контакта между мономерами. Некоторые из них состоят из звеньев одной и той же цепи между «зазубренным» концом одного мономера и «заостренным» концом следующего. В то время как мономеры в соседних цепях образуют боковой контакт через выступы субдомена IV, причем наиболее важными выступами являются выступы, образованные С-концом и гидрофобной связью, образованной тремя телами, включающими остатки 39–42, 201–203 и 286. Это Модель предполагает, что филамент образован мономерами в виде «листового» образования, в котором субдомены вращаются вокруг себя, эта форма также обнаруживается в бактериальном гомологе актина. MreB.[21]
Считается, что полимер F-актина имеет структурную полярность из-за того, что все субъединицы микрофиламента указывают на один и тот же конец. Это приводит к соглашению об именах: конец, который содержит субъединицу актина, у которой открыт сайт связывания АТФ, называется «(-) концом», в то время как противоположный конец, где расщелина направлена на другой соседний мономер, называется « (+) конец ".[26] Термины «заостренный» и «зазубренный», относящиеся к двум концам микрофиламентов, происходят от их внешнего вида под просвечивающая электронная микроскопия когда образцы исследуются в соответствии с техникой подготовки, называемой «декорирование». Этот метод состоит из добавления миозин Фрагменты S1 к ткани, которая была зафиксирована дубильная кислота. Этот миозин образует полярные связи с мономерами актина, создавая конфигурацию, которая выглядит как стрелы с оперением пера вдоль его стержня, где стержень - актин, а оперение - миозин. Следуя этой логике, конец микрофиламента, на котором нет выступающего миозина, называется острием стрелки (- конец), а другой конец - зазубренным концом (+ конец).[36]Фрагмент S1 состоит из доменов головы и шеи миозин II. В физиологических условиях G-актин ( мономер форма) превращается в F-актин ( полимер form) посредством АТФ, где роль АТФ существенна.[37]
Спиральная нить F-актина, обнаруженная в мышцах, также содержит тропомиозин молекула, которая представляет собой 40 нанометр длинный белок, который обернут вокруг спирали F-актина.[22] Во время фазы покоя тропомиозин покрывает активные участки актина, так что взаимодействие актин-миозин не может иметь место и вызывать сокращение мышц. Есть и другие белковые молекулы, связанные с тропомиозиновой нитью, это тропонины которые имеют три полимера: тропонин I, тропонин Т, и тропонин С.[38]
Складной
Актин может самопроизвольно приобретать большую часть своего третичная структура.[40] Однако то, как он приобретает полностью функциональная форма из его недавно синтезированный нативная форма является особенной и почти уникальной в химии белков. Причиной этого особого пути может быть необходимость избежать присутствия неправильно свернутых мономеров актина, которые могут быть токсичными, поскольку могут действовать как неэффективные терминаторы полимеризации. Тем не менее, это ключ к установлению стабильности цитоскелета, и, кроме того, это важный процесс для координации клеточный цикл.[41][42]
CCT требуется для обеспечения правильного складывания. CCT - это шаперонин группы II, большой белковый комплекс, который помогает в сворачивании других белков. CCT состоит из двойного кольца из восьми различных субъединиц (гетерооктамерных) и отличается от шаперонинов группы I, таких как GroEL, который содержится в эубактериях и эукариотических органеллах, поскольку не требует, чтобы ко-шаперон действовал как крышка над центральным каталитический полость. Субстраты связываются с CCT через определенные домены. Первоначально считалось, что он связывается только с актином и тубулин хотя недавно иммунопреципитация исследования показали, что он взаимодействует с большим количеством полипептиды, которые, возможно, функционируют как субстраты. Он действует через АТФ-зависимые конформационные изменения, которые иногда требуют нескольких раундов высвобождения и катализа для завершения реакции.[43]
Чтобы успешно завершить сворачивание, и актин, и тубулин должны взаимодействовать с другим белком, называемым префолдин, который представляет собой гетерогексамерный комплекс (образованный шестью отдельными субъединицами) во взаимодействии, которое настолько специфично, что молекулы имеют совместный[нужна цитата ]. Актин объединяется с префолдином, пока он еще формируется, когда его количество составляет примерно 145 аминокислоты длинные, особенно на N-терминале.[44]
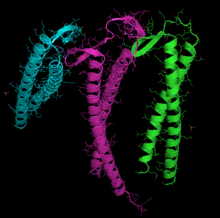
Для актина или тубулина используются разные субъединицы распознавания, хотя есть некоторые совпадения. В актине субъединицы, которые связываются с префолдином, вероятно, представляют собой PFD3 и PFD4, которые связываются в двух местах: одно между остатками 60–79 и другое между остатками 170–198. Актин распознается, загружается и доставляется к цитозольному шаперонину (CCT) в открытой конформации внутренним концом «щупалец» префолдина (см. Изображение и примечание).[40] Контакт при доставке актина настолько краток, что не образуется третичный комплекс, немедленно высвобождая префолдин.[39]

Затем CCT вызывает последовательное сворачивание актина, образуя связи с его субъединицами, а не просто заключая его в свою полость.[45] Вот почему он обладает специфическими участками узнавания в апикальном β-домене. Первый этап сворачивания состоит из распознавания остатков 245–249. Затем другие детерминанты устанавливают контакт.[46] И актин, и тубулин связываются с CCT в открытых конформациях в отсутствие АТФ. В случае актина две субъединицы связываются во время каждого конформационного изменения, тогда как в случае тубулина связывание происходит с четырьмя субъединицами. Актин имеет специфические связывающие последовательности, которые взаимодействуют с субъединицами δ и β-CCT или с δ-CCT и ε-CCT. После связывания AMP-PNP с CCT субстраты перемещаются в полости шаперонина. Также кажется, что в случае актина Белок CAP необходим как возможный кофактор в конечных состояниях фолдинга актина.[42]
Точный способ, которым регулируется этот процесс, до сих пор полностью не изучен, но известно, что белок PhLP3 (белок, похожий на фосдуцин ) подавляет его активность за счет образования третичного комплекса.[43]
Каталитический механизм АТФазы
Актин - это АТФаза, что означает, что это фермент который гидролизует АТФ. Эта группа ферментов отличается медленной скоростью реакции. Известно, что эта АТФаза «активна», то есть ее скорость увеличивается примерно в 40 000 раз, когда актин образует часть филамента.[35] Контрольное значение для этой скорости гидролиза в идеальных условиях составляет около 0,3. s−1. Тогда Pя остается связанным с актином рядом с АДФ в течение долгого времени, пока он совместно не высвобождается из внутренней части филамента.[47][48]
Точные молекулярные детали каталитического механизма до сих пор полностью не изучены. Хотя по этому вопросу ведется много споров, очевидно, что для гидролиза АТФ требуется «закрытая» конформация, и считается, что остатки, которые участвуют в процессе, перемещаются на соответствующее расстояние.[35] В глютаминовая кислота Glu137 является одним из ключевых остатков, который расположен в субдомене 1. Его функция заключается в связывании молекулы воды, которая производит нуклеофильная атака на γ-фосфат АТФ связь, в то время как нуклеотид прочно связан с субдоменами 3 и 4. Медленность каталитического процесса обусловлена большим расстоянием и перекосом положения молекулы воды по отношению к реагенту. Весьма вероятно, что конформационные изменения, вызываемые вращением доменов между формами G и F актина, перемещают Glu137 ближе, обеспечивая его гидролиз. Эта модель предполагает, что полимеризация и функция АТФазы будут разделены сразу.[21][22] Преобразование «открытое» в «закрытое» между формами G и F и его влияние на относительное движение нескольких ключевых остатков и образование водяных проводов были охарактеризованы в молекулярная динамика и QM / MM симуляции.[49][50]
Генетика

Актин был одним из наиболее консервативных белков на протяжении всей эволюции, поскольку он взаимодействует с большим количеством других белков. Он имеет последовательность 80,2% сохранение на ген уровень между Homo sapiens и Saccharomyces cerevisiae (разновидность дрожжей) и 95% сохранения первичная структура белкового продукта.[4]
Хотя большинство дрожжи имеют только один ген актина, выше эукариоты, в целом, выражать несколько изоформы актина, кодируемого семейством родственных генов. Млекопитающие иметь по крайней мере шесть изоформ актина, кодируемых отдельными генами,[51] которые делятся на три класса (альфа, бета, и гамма) согласно их изоэлектрические точки. В целом, альфа-актины обнаруживаются в мышцах (α-скелет, α-гладкая аорта, α-сердечная), тогда как бета- и гамма-изоформы заметны в немышечных клетках (β-цитоплазматические, γ1-цитоплазматические, γ2-кишечные гладкие) . Хотя аминокислотные последовательности и in vitro свойства изоформ очень похожи, эти изоформы не могут полностью заменять друг друга in vivo.[52]
Типичный ген актина состоит примерно из 100 нуклеотидов. 5 'UTR, 1200-нуклеотид переведено область и 200-нуклеотид 3 'UTR. Большинство генов актина прерваны интроны, до шести интронов в любом из 19 хорошо охарактеризованных мест. Высокая сохранность семейства делает актин предпочтительной моделью для исследований, сравнивающих интронно-раннюю и интрон-позднюю модели эволюции интрона.
Все несферические прокариоты похоже, обладают генами, такими как MreB, которые кодируют гомологи актина; эти гены необходимы для сохранения формы клетки. В плазмида -производный ген ParM кодирует актин-подобный белок, полимеризованная форма которого динамически нестабильный, и, по-видимому, разделяет плазмиду ДНК в свои дочерние клетки во время клеточного деления по механизму, аналогичному тому, который используется микротрубочками в эукариотических митоз.[53]Актин содержится как в гладкой, так и в шероховатой эндоплазматической сети.
Динамика сборки
Нуклеация и полимеризация

Факторы зародышеобразования необходимы для стимуляции полимеризации актина. Одним из таких зародышевых факторов является Комплекс Арп2 / 3, который имитирует димер G-актина, чтобы стимулировать нуклеацию (или образование первого тримера) мономерного G-актина. В Комплекс Арп2 / 3 связывается с актиновыми филаментами под углом 70 градусов с образованием новых актиновых ответвлений от существующих актиновых филаментов. Arp2 / 3-опосредованная нуклеация необходима для направленной миграции клеток.[54] Кроме того, актиновые филаменты сами связывают АТФ, и гидролиз этого АТФ стимулирует дестабилизацию полимера.
Рост актиновых филаментов может регулироваться тимозин и профилин. Тимозин связывается с G-актином для буферизации процесса полимеризации, тогда как профилин связывается с G-актином для обмена ADP за АТФ, способствуя присоединению мономера к зазубринам плюс конец филаментов F-актина.
F-актин является одновременно сильный и динамичный. в отличие от других полимеры, Такие как ДНК, составные элементы которого связаны между собой ковалентные связи, мономеры актиновых филаментов собраны более слабыми связями.[55] Боковые связи с соседними мономерами разрешают эту аномалию, которая теоретически должна ослабить структуру, поскольку они могут быть разрушены тепловым перемешиванием. Кроме того, слабые связи дают то преимущество, что концы волокон могут легко высвобождать или включать мономеры. Это означает, что волокна могут быстро перестраиваться и изменять клеточную структуру в ответ на раздражитель окружающей среды. Которая вместе с биохимический Механизм, с помощью которого это происходит, известен как «динамика сборки».[6]
- В пробирке исследования
Проведены исследования накопления и потери субъединиц микрофиламентами. in vitro (то есть в лаборатории, а не в клеточных системах), поскольку полимеризация образующегося актина дает тот же F-актин, что и продуцируемый in vivo. В in vivo Процесс контролируется множеством белков, чтобы заставить его реагировать на клеточные потребности, что затрудняет соблюдение его основных условий.[56]
В пробирке производство происходит последовательно: во-первых, это «фаза активации», когда связывание и обмен двухвалентных катионов происходит в определенных местах на G-актине, который связан с АТФ. Это вызывает конформационное изменение, иногда называемое мономером G * -актина или F-актина, поскольку оно очень похоже на единицы, расположенные на филаменте.[32] Это подготавливает его к «фазе зародышеобразования», в которой G-актин дает начало небольшим нестабильным фрагментам F-актина, которые способны полимеризоваться. Первоначально образуются нестабильные димеры и тримеры. «Фаза удлинения» начинается, когда имеется достаточно большое количество этих коротких полимеров. На этом этапе филамент формируется и быстро растет за счет обратимого добавления новых мономеров в обоих крайних случаях.[57] Наконец, стационарное равновесие достигается, когда мономеры G-актина обмениваются на обоих концах микрофиламента без какого-либо изменения его общей длины.[24] На этой последней фазе «критическая концентрация Cc"определяется как соотношение между константой сборки и константа диссоциации для G-актина, где динамика добавления и удаления димеров и тримеров не приводит к изменению длины микрофиламента. Под in vitro условия Cc составляет 0,1 мкМ,[58] это означает, что при более высоких значениях происходит полимеризация, а при более низких - деполимеризация.[59]
- Роль гидролиза АТФ
Как указано выше, хотя актин гидролизует АТФ, все указывает на то, что АТФ не требуется для сборки актина, учитывая, что, с одной стороны, гидролиз в основном происходит внутри филамента, а с другой стороны, АДФ может также вызвать полимеризацию. Это ставит вопрос о том, какие термодинамически неблагоприятный процесс требует таких огромных затрат энергия. Цикл актина, который связывает гидролиз АТФ с полимеризацией актина, состоит из предпочтительного добавления мономеров G-актин-АТФ к зазубренному концу филамента и одновременной разборки мономеров F-актин-АДФ на заостренном конце, где впоследствии находится АДФ. превратился в АТФ, тем самым замкнув цикл. Этот аспект образования актиновых филаментов известен как «беговая дорожка».
АТФ относительно быстро гидролизуется сразу после добавления мономера G-актина к филаменту. Есть две гипотезы относительно того, как это происходит; в стохастический, что предполагает, что гидролиз происходит случайным образом, и на него некоторым образом влияют соседние молекулы; и векторный, который предполагает, что гидролиз происходит только рядом с другими молекулами, АТФ которых уже был гидролизован. В любом случае полученное Pя не выпускается; осталось какое-то время нековалентно связаны с АДФ актина. Таким образом, в филаменте есть три вида актина: АТФ-актин, АДФ + Ф.я-Актин и АДФ-актин.[47][60] Количество каждого из этих видов, присутствующих в филаменте, зависит от его длины и состояния: когда начинается удлинение, филамент имеет примерно равное количество мономеров актина, связанных с АТФ и АДФ + Ф.я и небольшое количество АДФ-актина на (-) конце. Когда достигается стационарное состояние, ситуация меняется на противоположную: ADP присутствует вдоль большей части нити, и только область, ближайшая к (+) концу, содержит ADP + Pя и с АТФ, присутствующим только на кончике.[61]
Если мы сравним филаменты, которые содержат только АДФ-актин, с филаментами, содержащими АТФ, в первом случае критические константы одинаковы на обоих концах, а Cc для двух других нуклеотидов отличается: На (+) конце Cc+= 0,1 мкМ, а на (-) конце Cc−= 0,8 мкМ, что приводит к следующим ситуациям:[26]
- Для концентраций G-актин-АТФ менее Cc+ не происходит удлинения нити.
- Для концентраций G-актин-АТФ менее Cc− но больше, чем Cc+ удлинение происходит на (+) конце.
- Для концентраций G-актин-АТФ, превышающих Cc− микрофиламент разрастается с обоих концов.
Таким образом, можно сделать вывод, что энергия, произведенная при гидролизе, используется для создания истинного «стационарного состояния», то есть потока, вместо простого равновесия, которое является динамическим, полярным и прикрепленным к нити. Это оправдывает затраты энергии, так как способствует важным биологическим функциям.[47] Кроме того, конфигурация различных типов мономеров определяется связывающими актин белками, которые также контролируют этот динамизм, как будет описано в следующем разделе.
Формирование микроволокон при беговой дорожке оказалось нетипичным в стереоцилии. В этом случае контроль размера структуры полностью апикальный и каким-то образом контролируется экспрессией генов, то есть общим количеством белкового мономера, синтезируемого в любой данный момент.[62]
Связанные белки
Актиновый цитоскелет in vivo не состоит исключительно из актина, для его образования, продолжения и функции требуются другие белки. Эти белки называются актин-связывающие белки (ABP), и они участвуют в полимеризации актина, деполимеризации, стабильности, организации в пучки или сети, фрагментации и разрушении.[24] Разнообразие этих белков таково, что актин считается белком, который принимает участие в наибольшем количестве белок-белковые взаимодействия.[64] Например, существуют секвестрирующие G-актин элементы, которые препятствуют его включению в микрофиламенты. Есть также белки, которые стимулируют его полимеризацию или усложняют синтезирующие сети.[26]
- Тимозин β-4 представляет собой белок 5 кДа, который может связываться с G-актин-АТФ в соотношении 1: 1 стехиометрия; Это означает, что одна единица тимозина β-4 связывается с одной единицей G-актина. Его роль состоит в том, чтобы препятствовать включению мономеров в растущий полимер.[65]
- Профилин, это цитозольный белок с молекулярной массой 15 кДа, который также связывается с G-актин-АТФ или -АДФ со стехиометрией 1: 1, но он выполняет другую функцию, так как способствует замене нуклеотидов АДФ на АТФ. Он также участвует в других клеточных функциях, таких как связывание пролин повторения в других белках или липидах, которые действуют как вторичные посланники.[66][67]

Другие белки, которые связываются с актином, регулируют длину микрофиламентов, разрезая их, что дает начало новым активным концам для полимеризации. Например, если двухконечную микрофиламент разрезать дважды, получится три новых микрофиламента с шестью концами. Эта новая ситуация способствует динамике сборки и разборки. Наиболее заметными из этих белков являются гельсолин и кофилин. Эти белки сначала достигают разреза, связываясь с мономером актина, находящимся в полимере, а затем изменяют мономер актина. конформация оставаясь привязанным к вновь сгенерированному (+) концу. Это препятствует добавлению или обмену новых субъединиц G-актина. Деполимеризация поощряется, поскольку (-) концы не связаны ни с какой другой молекулой.[70]
Другие белки, которые связываются с актином, покрывают концы F-актина, чтобы стабилизировать их, но они не могут их разрушить. Примеры этого типа белка: CapZ, который связывает (+) концы в зависимости от уровней клетки Ca2+ /кальмодулин. Эти уровни зависят от внутренних и внешних сигналов клетки и участвуют в регуляции ее биологических функций).[71] Другой пример тропомодулин (который привязывается к (-) концу). Тропомодулин в основном стабилизирует F-актин, присутствующий в миофибриллы присутствует в мышца саркомеры, которые представляют собой конструкции, отличающиеся большой стабильностью.[72]

В Комплекс Арп2 / 3 широко встречается во всех эукариотический организмы.[74] Он состоит из семи подразделений, некоторые из которых обладают топология это явно связано с их биологической функцией: две субъединицы, ARP2 и ARP3, имеют структуру, аналогичную структуре мономеров актина. Эта гомология позволяет обеим единицам действовать как агенты зародышеобразования при полимеризации G-актина и F-актина. Этот комплекс также требуется в более сложных процессах, таких как создание дендритный структур, а также в анастомоз (повторное соединение двух ранее соединенных ветвящихся структур, например, в кровеносных сосудах).[75]
Химические ингибиторы

Есть ряд токсины которые мешают динамике актина, предотвращая его полимеризацию (латрункулин и цитохалазин D ) или стабилизируя его (фаллоидин ):
- Латрункулин - это токсин, производимый губки. Он связывается с G-актином, предотвращая его связывание с микрофиламентами.[76]
- Цитокалазин D, представляет собой алкалоид произведено грибы, который связывается с (+) концом F-актина, предотвращая добавление новых мономеров.[77] Цитокалазин D нарушает динамику актина, активируя белок. p53 у животных.[78]
- Фаллоидин - это токсин, выделенный из грибов смертельной шапочки. Мухомор фаллоидный. Он связывается с поверхностью раздела между соседними мономерами актина в полимере F-актина, предотвращая его деполимеризацию.[77]
Функции и расположение
Актин образует филаменты (F-актин или микрофиламенты ) являются важными элементами эукариотической цитоскелет, способный претерпевать очень быструю полимеризацию и динамику деполимеризации. В большинстве клеток актиновые филаменты образуют крупномасштабные сети, которые необходимы для многих ключевых функций клеток:[79]
- Различные типы актиновых сетей (состоящие из актиновых нитей) обеспечивают механическую поддержку клеткам и обеспечивают маршруты транспортировки через цитоплазму, чтобы способствовать передаче сигнала.
- Быстрая сборка и разборка актиновой сети позволяет клеткам мигрировать (Миграция клеток ).
- В многоклеточный мышца клетки, чтобы быть эшафотом, на котором миозин белки генерируют силу для поддержки сокращения мышц.
- В немышечных клетках быть дорожкой для грузовых транспортных миозинов (нетрадиционных миозинов), таких как миозин V и VI. Нетрадиционные миозины используют гидролиз АТФ для транспортировки грузов, таких как пузырьки и органеллы - направленно, намного быстрее, чем диффузия. Миозин V идет к зазубренному концу актиновых волокон, а миозин VI идет к заостренному концу. Большинство актиновых филаментов расположены зазубренным концом в направлении клеточной мембраны, а заостренным концом - внутрь клетки. Такое расположение позволяет миозину V быть эффективным двигателем для экспорта грузов, а миозину VI - эффективным двигателем для импорта.
Белок актин обнаружен как в цитоплазма и ядро клетки.[80] Его расположение регулируется клеточной мембраной. преобразование сигнала пути, которые интегрируют стимулы, которые получает клетка, стимулируя в ответ реструктуризацию актиновых сетей. В Диктиостелиум, фосфолипаза D было обнаружено, что он вмешивается в инозитолфосфат пути.[81] Актиновые филаменты особенно стабильны и обильны мышечные волокна. В рамках саркомер (основная морфологическая и физиологическая единица мышечных волокон) актин присутствует как в I, так и в A полосах; миозин также присутствует в последнем.[82]
Цитоскелет

Микрофиламенты участвуют в движении всех подвижных клеток, в том числе немышечных типов,[83][84] и препараты, нарушающие организацию F-актина (например, цитохалазины ) влияют на активность этих клеток. Актин составляет 2% от общего количества белков в гепатоциты, 10% в фибробласты, 15% в амебы и до 50–80% в активированных тромбоциты.[85] Существует ряд различных типов актина с немного разными структурами и функциями. Это означает, что α-актин находится исключительно в мышечные волокна, а типы β и γ обнаруживаются в других клетках. Кроме того, поскольку последние типы имеют высокую текучесть кадров, большинство из них находится за пределами постоянных построек. Это означает, что микрофиламенты, обнаруженные в клетках, отличных от мышечных, представлены в трех формах:[86]
- Сети из микрофиламентов - Клетки животных обычно имеют клеточную кору под клеточная мембрана содержащая большое количество микрофиламентов, что исключает наличие органеллы. Эта сеть связана с многочисленными рецепторные клетки который реле сигналов за пределы клетки.
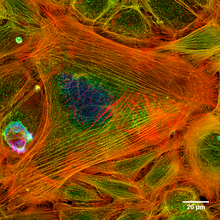
- Пучки микрофиламентов - Эти чрезвычайно длинные микрофиламенты расположены в сетях и в сочетании с сократительными белками, такими как немышечные миозин, они участвуют в перемещении веществ на внутриклеточном уровне.
- Периодические кольца актина - Недавно было обнаружено, что периодическая структура, состоящая из равномерно расположенных колец актина, специфически существует в аксоны (нет дендриты ).[87] В этой структуре кольца актина вместе с спектрин тетрамеры, связывающие соседние кольца актина, образуют сплоченный цитоскелет который поддерживает мембрану аксона. Периодичность структуры также может регулировать ионные каналы натрия в аксонах.
Дрожжи
Цитоскелет актина является ключом к процессам эндоцитоз, цитокинез, определение полярность ячейки и морфогенез в дрожжи. Помимо опоры на актин, в эти процессы вовлечены 20 или 30 ассоциированных белков, которые все имеют высокую степень эволюционной консервативности, наряду со многими сигнальными молекулами. Вместе эти элементы обеспечивают пространственно и временно модулированную сборку, которая определяет реакцию клетки как на внутренние, так и на внешние раздражители.[88]
Дрожжи содержат три основных элемента, связанных с актином: пластыри, кабели и кольца, которые, несмотря на то, что не присутствуют в течение длительного времени, находятся в состоянии динамического равновесия из-за непрерывной полимеризации и деполимеризации. Они обладают рядом дополнительных белков, включая ADF / кофилин, который имеет молекулярную массу 16 кДа и кодируется одним геном, называемым COF1; Aip1, кофактор кофилина, который способствует разборке микрофиламентов; Srv2 / CAP, регулятор процесса, связанный с аденилатциклаза белки; профилин с молекулярной массой приблизительно 14 кДа, родственный / связанный с мономерами актина; и твинфилин, белок 40 кДа, участвующий в организации пятен.[88]
Растения
Растение геном исследования показали существование изовариантов белков в семействе генов актина. В Arabidopsis thaliana, а двудольные используется как модельный организм, существует десять типов актина, девять типов α-тубулинов, шесть β-тубулинов, шесть профилинов и десятки миозинов. Это разнообразие объясняется эволюционной необходимостью обладать вариантами, немного различающимися по своему временному и пространственному выражению.[4] Большинство этих белков совместно экспрессировались в ткань проанализированы. Актиновые сети распределены по цитоплазме культивируемых клеток. in vitro. Вокруг ядра сосредоточена сеть, которая соединена спицами с клеточной корой, эта сеть очень динамична, с непрерывной полимеризацией и деполимеризацией.[89]
Несмотря на то, что большинство растительных клеток имеют клеточная стенка Это определяет их морфологию и препятствует их движению, их микрофиламенты могут генерировать достаточную силу для достижения ряда клеточных активностей, таких как цитоплазматические токи, генерируемые микрофиламентами и миозином. Актин также участвует в движении органелл и клеточном морфогенезе, в котором участвуют деление клеток а также удлинение и дифференциация клетки.[91]
Наиболее заметные белки, связанные с актиновым цитоскелетом растений, включают:[91] Виллин, который принадлежит к тому же семейству, что и гельсолин / северин и способен разрезать микрофиламенты и связывать мономеры актина в присутствии катионов кальция; фимбрин, который способен распознавать и объединять мономеры актина и который участвует в образовании сетей (посредством процесса регуляции, отличного от такового у животных и дрожжей);[92] Форминс, которые способны действовать как зародышеобразователь полимеризации F-актина; миозин, типичный молекулярный мотор, специфичный для эукариот, который Arabidopsis thaliana кодируется 17 генами двух различных классов; CHUP1, который может связывать актин и участвует в пространственном распределении хлоропласты в камере; KAM1 / MUR3, определяющие морфологию аппарат Гольджи а также состав ксилоглюканы в клеточной стенке; NtWLIM1, который способствует появлению актиновых клеточных структур; и ERD10, который участвует в ассоциации органелл внутри мембраны и микрофиламентов, которые, по-видимому, играют роль в реакции организма на стресс.
Ядерный актин
Ядерный актин был впервые замечен и описан в 1977 году Кларком и Мерриамом.[93] Авторы описывают белок, присутствующий в ядерной фракции, полученный из Xenopus laevis ооциты, которые имеют те же особенности, что и актин скелетных мышц. С того времени появилось множество научных отчетов о структуре и функциях актина в ядре (см. Обзор: Hofmann 2009.[94]) Контролируемый уровень актина в ядре, его взаимодействие с актин-связывающими белками (ABP) и присутствие различных изоформ позволяет актину играть важную роль во многих важных ядерных процессах.
Транспорт актина через ядерную мембрану
Последовательность актина не содержит сигнала ядерной локализации. Небольшой размер актина (около 43 кДа) позволяет ему проникать в ядро путем пассивной диффузии.[95] Однако актин довольно быстро перемещается между цитоплазмой и ядром, что указывает на наличие активного транспорта. Импорту актина в ядро (вероятно, в комплексе с cofilin) способствует импортный белок importin 9.[96]
Низкий уровень актина в ядре кажется очень важным, потому что актин имеет два сигнала экспорта из ядра (NES) в своей последовательности. Микроинъектированный актин быстро выводится из ядра в цитоплазму. Актин экспортируется как минимум двумя способами: через экспорт 1 (EXP1) и экспорт 6 (Опыт6).[97][98]
Конкретные модификации, такие как SUMOylation, позволяют удерживать ядерный актин. Было продемонстрировано, что мутация, предотвращающая SUMOylation, вызывает быстрый экспорт бета-актина из ядра.[99]
На основе экспериментальных результатов можно предложить общий механизм ядерного транспорта актина:[99][100]
- В цитоплазме кофилин связывает мономеры АДФ-актина. Этот комплекс активно импортируется в ядро.
- Более высокая концентрация АТФ в ядре (по сравнению с цитоплазмой) способствует обмену АДФ на АТФ в комплексе актин-кофилин. Это ослабляет силу связывания этих двух белков.
- Комплекс кофилин-актин окончательно диссоциирует после фосфорилирования кофилина ядерной киназой LIM.
- Актин СУМОилирован и в этой форме сохраняется внутри ядра.
- Актин может образовывать комплексы с профилином и покидать ядро через экспортин 6.
Организация ядерного актина
Ядерный актин существует в основном в виде мономера, но также может образовывать динамические олигомеры и короткие полимеры.[101][102][103] Организация ядерного актина варьируется в разных типах клеток. Например, в Xenopus В ооцитах (с более высоким уровнем ядерного актина по сравнению с соматическими клетками) актин образует филаменты, которые стабилизируют архитектуру ядра. Эти нити можно наблюдать под микроскопом благодаря окрашиванию фаллоидином, конъюгированным с флуорофором.[93][95]
Однако в ядрах соматических клеток актиновые филаменты нельзя наблюдать с помощью этой техники.[104] Анализ ингибирования ДНКазы I, пока единственный тест, позволяющий количественно определять полимеризованный актин непосредственно в биологических образцах, показал, что эндогенный ядерный актин действительно существует в основном в мономерной форме.[103]
Точно контролируемый уровень актина в ядре клетки, более низкий, чем в цитоплазме, предотвращает образование филаментов. Полимеризация также снижается из-за ограниченного доступа к мономерам актина, которые связаны в комплексы с ABP, в основном с кофилином.[100]
Изоформы актина в ядре клетки
Изоформам актина уделяется мало внимания; однако было показано, что в ядре клетки присутствуют разные изоформы актина. Изоформы актина, несмотря на высокое сходство последовательностей, обладают разными биохимическими свойствами, такими как кинетика полимеризации и деполимеризации.[105] Также они показывают различную локализацию и функции.
Уровень изоформ актина как в цитоплазме, так и в ядре может изменяться, например, в ответ на стимуляцию роста клеток или остановку пролиферации и транскрипционной активности.[106]
Исследования ядерного актина обычно сосредоточены на бета-изоформе.[107][108][109][110] Однако использование антител, направленных против различных изоформ актина, позволяет идентифицировать не только цитоплазматический бета в ядре клетки, но также:
- гамма-актин в ядрах клеток меланомы человека,[103]
- альфа-актин скелетных мышц в ядрах миобластов мыши,[111]
- цитоплазматический гамма-актин, а также альфа-актин гладких мышц в ядре фибробласта эмбриональной мыши[112]
Присутствие различных изоформ актина может существенно влиять на его функцию в ядерных процессах, особенно потому, что уровень отдельных изоформ можно контролировать независимо.[103]
Ядерные функции актина
Функции актина в ядре связаны с его способностью к полимеризации и взаимодействию с различными АД и структурными элементами ядра. Ядерный актин участвует в:
- Архитектура ядра - Взаимодействие актина с альфа II-спектрином и другими белками важно для поддержания правильной формы ядра.[113][114]
- Транскрипция - Актин участвует в реорганизации хроматина,[80][107][115][116] инициация транскрипции и взаимодействие с транскрипционным комплексом.[117] Актин участвует в регуляции структуры хроматина,[118][119][120] взаимодействуя с РНК-полимеразой I,[110] II[108] и III.[109] В транскрипции Pol I актин и миозин (MYO1C, который связывает ДНК) действуют как молекулярный мотор. Для транскрипции Pol II β-актин необходим для образования преинициативного комплекса. Pol III содержит β-актин в качестве субъединицы. Актин также может быть компонентом комплексов ремоделирования хроматина, а также частиц пре-мРНП (то есть предшественником информационная РНК связаны с белками) и участвует в ядерный экспорт РНК и белков.[121]
- Регуляция активности генов - Актин связывается с регуляторными областями разных типов генов.[122][123][124][125] Способность актина регулировать активность генов используется в методе молекулярного репрограммирования, который позволяет дифференцированным клеткам возвращаться в их эмбриональное состояние.[124][126]
- Транслокация активированного фрагмента хромосомы из-под мембраны в эухроматин, где начинается транскрипция. Это движение требует взаимодействия актина и миозина.[127][128]
- Интеграция различных клеточных компартментов. Актин - это молекула, которая объединяет пути передачи цитоплазматических и ядерных сигналов.[129] Примером может служить активация транскрипции в ответ на стимуляцию клеток сывороткой. in vitro.[130][131][132]
- Иммунная реакция - Ядерный актин полимеризуется на Рецептор Т-клеток стимуляция и требуется для экспрессии цитокинов и выработки антител in vivo.[133]
Благодаря своей способности претерпевать конформационные изменения и взаимодействовать со многими белками, актин действует как регулятор образования и активности белковых комплексов, таких как транскрипционный комплекс.[117]
Мышечное сокращение
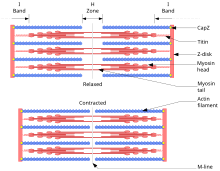
Очертание мышечного сокращения
В мышечных клетках актомиозин миофибриллы составляют большую часть цитоплазматического материала. Эти миофибриллы состоят из тонкие нити актина (обычно около 7 нм в диаметре) и толстые нити моторного белка миозин (обычно диаметром около 15 нм).[134] Эти миофибриллы используют энергию, полученную из АТФ для создания движений клеток, таких как сокращение мышц.[134] Используя гидролиз АТФ для получения энергии, миозиновые головки проходят цикл, в течение которого они прикрепляются к тонким волокнам, создают напряжение, а затем, в зависимости от нагрузки, выполняют силовой удар, который заставляет тонкие волокна скользить мимо, укорачивая мышцу.
В сократительных пучках связывающий актин белок альфа-актинин разделяет каждую тонкую нить на ≈35 нм. Это увеличение расстояния позволяет толстым нитям вставляться между ними и взаимодействовать, обеспечивая деформацию или сжатие. При деформации один конец миозина связан с плазматическая мембрана, а другой конец «идет» к положительному концу актиновой нити. Это придает мембране форму, отличную от формы клеточная кора. Для сокращения молекула миозина обычно связана с двумя отдельными филаментами, и оба конца одновременно «идут» к плюсовому концу своей филамента, сдвигая филаменты актина ближе друг к другу. Это приводит к укорачиванию или сокращению актинового пучка (но не филамента). Этот механизм отвечает за сокращение мышц и цитокинез, деление одной клетки на две.
Роль актина в сокращении мышц
Спиральная нить F-актина, обнаруженная в мышцах, также содержит тропомиозин молекула, 40-нанометр белок, который обернут вокруг спирали F-актина. Во время фазы покоя тропомиозин покрывает активные участки актина, так что взаимодействие актин-миозин не может происходить и вызывать мышечное сокращение (взаимодействие вызывает движение между двумя белками, которое, поскольку оно повторяется много раз, вызывает сокращение) . С тропомиозиновой нитью связаны и другие белковые молекулы, в том числе тропонины которые имеют три полимера: тропонин I, тропонин Т, и тропонин С.[38] Регуляторная функция тропомиозина зависит от его взаимодействия с тропонином в присутствии Ca2+ ионы.[135]
И актин, и миозин участвуют в мышца сокращение и расслабление, и они составляют 90% мышечного белка.[136] Общий процесс инициируется внешним сигналом, обычно через потенциал действия стимуляция мышцы, которая содержит специализированные клетки, внутренняя часть которых богата актиновыми и миозиновыми нитями. Цикл сокращения-расслабления состоит из следующих этапов:[82]
- Деполяризация сарколемма и передача потенциала действия через Т-канальцы.
- Открытие саркоплазматический ретикулум С Ca2+ каналы.
- Увеличить в цитозольный Ca2+ концентрации и взаимодействие этих катионов с тропонином, вызывающее конформационное изменение его структура. Это, в свою очередь, изменяет структуру тропомиозина, который покрывает активный центр актина, позволяя формировать перекрестные связи миозин-актин (последние представлены в виде тонких нитей).[38]
- Движение миозиновых головок по тонким филаментам может происходить либо с участием АТФ, либо независимо от АТФ. Первый механизм, опосредованный АТФаза активность в головках миозина вызывает движение актиновых нитей к Z-диск.
- Ca2+ захват саркоплазматической сети, вызывая новое конформационное изменение тропомиозина, которое ингибирует взаимодействие актин-миозин.[136]
Другие биологические процессы
Традиционный образ функции актина связывает его с поддержанием цитоскелета и, следовательно, с организацией и движением органелл, а также с определением формы клетки.[86] Однако актин играет более широкую роль в физиологии эукариотических клеток, в дополнение к аналогичным функциям в прокариоты.
- Цитокинез. Деление клеток в клетках животных и дрожжах обычно включает разделение родительской клетки на две дочерние клетки за счет сужения центральной окружности. Этот процесс включает сужающееся кольцо, состоящее из актина, миозина и α-актинин.[137] В делящихся дрожжах Schizosaccharomyces pombe, актин активно образуется в сжимающем кольце с участием Arp3, то формин Cdc12, профилин, и Оса вместе с предварительно сформированными микрофиламентами. После того, как кольцо построено, конструкция поддерживается путем непрерывной сборки и разборки, чему способствует Arp2 / 3 комплекс и формины, является ключом к одному из центральных процессов цитокинеза.[138] Совокупность сократительного кольца, шпиндельный аппарат, микротрубочки, а плотный периферический материал называется «телом Флеминга» или «промежуточным телом».[86]
- Апоптоз. В течение запрограммированная гибель клеток Семейство протеаз ICE / ced-3 (одна из протеаз-конвертеров интерлейкина-1) расщепляет актин на два фрагмента in vivo; один из фрагментов имеет вес 15 кДа, а другой - 31 кДа. Это представляет собой один из механизмов, участвующих в разрушении жизнеспособности клеток, составляющих основу апоптоза.[139] Протеаза Calpain также было показано, что он участвует в этом типе разрушения клеток;[140] так же, как было показано, что использование ингибиторов кальпаина снижает протеолиз актина и деградацию ДНК (еще один из характерных элементов апоптоза).[141] С другой стороны, стресс -индуцированный запуск апоптоза вызывает реорганизацию актинового цитоскелета (которая также включает его полимеризацию), в результате чего возникают структуры, называемые стрессовые волокна; это активируется MAP киназа путь.[142]

- Клеточная адгезия и разработка. Адгезия между клетками - это характеристика многоклеточные организмы что позволяет ткань специализации и, следовательно, увеличивает сложность клетки. Адгезия клетки эпителий включает актиновый цитоскелет в каждой из соединенных клеток, а также кадгерины действуя как внеклеточные элементы с связью между ними, опосредованной катенины.[143] Вмешательство в динамику актина имеет последствия для развития организма, на самом деле актин является настолько важным элементом, что системы избыточных гены доступны. Например, если α-актинин или же гелеобразование ген фактора был удален в Диктиостелиум особи не показывают аномальных фенотип возможно из-за того, что каждый из белков может выполнять функцию другого. Однако развитие двойные мутации это влияет на отсутствие обоих типов генов.[144]
- Экспрессия гена модуляция. Состояние полимеризации актина влияет на характер экспрессия гена. В 1997 году было обнаружено, что опосредованная цитокалазином D деполимеризация в Клетки Шванна вызывает определенный паттерн экспрессии генов, участвующих в миелинизация этого типа нервная клетка.[145] Было показано, что F-актин изменяет транскриптом на некоторых стадиях жизни одноклеточных организмов, таких как гриб грибковые микроорганизмы албиканс.[146] Кроме того, белки, подобные актину, играют регулирующую роль во время сперматогенез в мышей[147] а у дрожжей актин-подобные белки, как полагают, играют роль в регуляции экспрессия гена.[148] Фактически, актин способен действовать как инициатор транскрипции, когда он реагирует с типом ядерного миозина, который взаимодействует с РНК-полимеразы и другие ферменты, участвующие в процессе транскрипции.[80]
- Стереоцилии динамика. На поверхности некоторых клеток образуются тонкие, заполненные узором выросты, которые имеют механосенсорный функция. Например, этот тип органелл присутствует в Орган Корти, который находится в ухо. Основная характеристика этих конструкций - возможность изменения их длины.[149] Молекулярная архитектура стереоцилий включает в себя паракристаллический актиновое ядро находится в динамическом равновесии с мономерами, присутствующими в соседнем цитозоле. Миозины типа VI и VIIa присутствуют по всему ядру, тогда как миозин XVa присутствует в его конечностях в количествах, которые пропорциональны длине стереоцилий.[150]
- Внутренний хиральность. Актомиозиновые сети участвуют в создании внутренней хиральности в индивидуальных клетках.[151] Клетки, выросшие на хиральных поверхностях, могут демонстрировать направленное смещение влево / вправо, которое зависит от актомиозина.[152][153]
Молекулярная патология
Большая часть чего-либо млекопитающие обладают шестью разными актинами гены. Из них два кода для цитоскелет (ACTB и ACTG1 ), а остальные четыре участвуют в скелетно-поперечно-полосатая мышца (ACTA1 ), гладкая мышечная ткань (ACTA2 ), кишечный мышцы (ACTG2 ) и сердечная мышца (ACTC1 ). Актин цитоскелета участвует в патогенный механизмы многих инфекционные агенты, включая ВИЧ. Подавляющее большинство мутации которые влияют на актин, представляют собой точечные мутации, которые имеют доминирующий эффект, за исключением шести мутаций, вовлеченных в немалиновая миопатия. Это связано с тем, что во многих случаях мутант мономера актина действует как «кэп», предотвращая удлинение F-актина.[32]
Патология, связанная с ACTA1
ACTA1 ген, который кодирует α-изоформа актина, который преобладает в организме человека скелетно-поперечно-полосатые мышцы, хотя он также выражен в сердечной мышце и в щитовидная железа.[154] Его Последовательность ДНК состоит из семи экзоны которые производят пять известных стенограммы.[155] Большинство из них состоят из точечных мутаций, вызывающих замену аминокислоты. Мутации во многих случаях связаны с фенотип это определяет серьезность и течение недуга.[32][155]
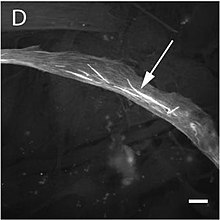
Мутация изменяет структуру и функцию скелетных мышц, производя одну из трех форм: миопатия: тип 3 немалиновая миопатия, врожденная миопатия с избытком тонких миофиламентов (См) и врожденная миопатия с диспропорцией типа волокон (CMFTD). Также были обнаружены мутации, которые производят основные миопатии.[157] Хотя их фенотипы схожи, в дополнение к типичной немалиновой миопатии некоторые специалисты выделяют другой тип миопатии, называемый актинической немалиновой миопатией. В первом случае вместо обычных палочек образуются сгустки актина. Важно отметить, что пациент может показать более одного из этих фенотипы в биопсия.[158] Самый распространенный симптомы имеют типичную морфологию лица (миопатические фации ), мышечная слабость, задержка двигательного развития и затрудненное дыхание. Течение болезни, ее тяжесть и возраст, в котором она проявляется, являются вариабельными, также обнаруживаются частично совпадающие формы миопатии. Симптомом немалиновой миопатии является то, что немалиновые стержни появляются в разных местах мышечных волокон 1 типа. Эти стержни не-патогномоничный структуры, которые по составу аналогичны Z-дискам, найденным в саркомер.[159]
В патогенез Эта миопатия очень разнообразна. Многие мутации происходят в области вдавливания актина рядом с его нуклеотид сайты связывания, тогда как другие встречаются в Домене 2 или в областях, где происходит взаимодействие со связанными белками. Это каким-то образом объясняет большое разнообразие сгустков, которые образуются в этих случаях, таких как немалин, внутриядерные тела или тела зебры.[32] Изменения актина складывание возникают при немалиновой миопатии, а также изменения в ее агрегации, а также изменения в выражение других ассоциированных белков. В некоторых вариантах, где обнаруживаются внутриядерные тела, изменения складчатости маскируют сигнал экспорта белка ядра так что накопление мутированной формы актина происходит в ядро клетки.[160] С другой стороны, мутации в ACTA1 которые вызывают CFTDM, оказывают большее влияние на саркомерную функцию, чем на его структуру.[161] Недавние исследования попытались понять этот очевидный парадокс, который предполагает, что нет четкой корреляции между количеством стержней и мышечной слабостью. Похоже, что некоторые мутации могут вызывать большее апоптоз показатель в мышечных волокнах II типа.[41]
В гладких мышцах
Есть две изоформы, которые кодируют актины в гладкая мышечная ткань:
ACTG2 коды для самой большой изоформы актина, которая имеет девять экзоны, один из которых, расположенный на конце 5 ', не переведено.[162] Это γ-актин, который экспрессируется в гладкой кишке. Мутаций этого гена, соответствующих патологиям, не обнаружено, хотя микрочипы показали, что этот белок чаще экспрессируется в случаях, устойчивых к химиотерапия с помощью цисплатин.[163]
ACTA2 кодирует α-актин, расположенный в гладких мышцах, а также в гладких мышцах сосудов. Было отмечено, что мутация MYH11 может быть причиной не менее 14% наследственных аневризмы грудной аорты особенно Тип 6. Это происходит потому, что мутировавший вариант производит неправильную филаментарную сборку и снижает способность к сокращению гладких мышц сосудов. Деградация аортальная среда было зарегистрировано у этих людей с областями дезорганизации и гиперплазия а также стеноз аорты vasa vasorum.[164] Число болезней, в которые вовлечен этот ген, увеличивается. Это было связано с Болезнь Моямоя и вполне вероятно, что определенные мутации в гетерозиготном состоянии могут вызывать предрасположенность ко многим сосудистым патологиям, таким как аневризма грудной аорты и ишемическая болезнь сердца.[165] Α-актин, обнаруженный в гладких мышцах, также является интересным маркером для оценки прогресса печени. цирроз.[166]
В сердечной мышце
В ACTC1 ген кодирует изоформу α-актина, присутствующую в сердечной мышце. Впервые он был секвенирован Хамадой и сотрудниками в 1982 году, когда было обнаружено, что он прерывается пятью интронами.[167] Это был первый из шести генов, в которых были обнаружены аллели, вовлеченные в патологические процессы.[168]
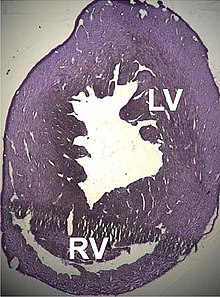
Описан ряд структурных нарушений, связанных с точечными мутациями этого гена, которые вызывают сбои в работе сердца, например, тип 1R. дилатационная кардиомиопатия и Тип 11 гипертрофическая кардиомиопатия. Определенные недостатки межпредсердная перегородка были описаны недавно, что также может быть связано с этими мутациями.[170][171]
Были изучены два случая дилатационной кардиомиопатии с заменой высококонсервативной кардиомиопатии. аминокислоты принадлежащий к белковые домены которые связывают и перемежаются с Z диски. Это привело к теории о том, что расширение вызвано дефектом передачи сократительная сила в миоциты.[34][168]
Мутации в ACTC1 ответственны как минимум за 5% гипертрофических кардиомиопатий.[172] Также было обнаружено наличие ряда точечных мутаций:[173]
- Мутация E101K: изменение чистого заряда и образование слабой электростатической связи в сайте связывания актомиозина.
- P166A: зона взаимодействия между мономерами актина.
- A333P: зона взаимодействия актин-миозин.
Патогенез, по-видимому, включает компенсаторный механизм: мутировавшие белки действуют как токсины с доминирующим действием, снижая способность сердца к договор вызывая ненормальное механическое поведение, такое, что гипертрофия, которая обычно откладывается, является следствием нормальной реакции сердечной мышцы на стресс.[174]
Недавние исследования обнаружили мутации ACTC1, которые вовлечены в два других патологических процесса: инфантильный идиопатический рестриктивная кардиомиопатия,[175] и несжатие миокарда левого желудочка.[176]
В цитоплазматических актинах
ACTB очень сложный локус. Номер псевдогены существуют, которые распределены по геном, а его последовательность содержит шесть экзонов, которые могут вызывать до 21 различных транскрипций посредством альтернативное сращивание, которые известны как β-актины. В соответствии с этой сложностью, ее продукты также можно найти во многих местах, и они являются частью широкого спектра процессов (цитоскелет, NuA4 гистон -ацилтрансферазный комплекс, ядро клетки ) и, кроме того, они связаны с механизмами большого количества патологических процессов (карциномы, несовершеннолетний дистония, механизмы заражения, нервная система пороки развития и опухолевые инвазии, среди прочего).[177] Была открыта новая форма актина, каппа-актин, которая, по-видимому, заменяет β-актин в процессах, связанных с опухоли.[178]

К настоящему времени обнаружены три патологических процесса, вызванных прямым изменением последовательности генов:
- Гемангиоперицитома с t (7; 12) (p22; q13) -транслокациями - редкое заболевание, при котором транслокационная мутация вызывает слияние ACTB ген над GLI1 в Хромосома 12.[180]
- Ювенильное начало дистония редкий дегенеративное заболевание что влияет на Центральная нервная система; в частности, это влияет на области неокортекс и таламус, где стержневидный эозинофильный образуются включения. Пострадавшие представляют собой фенотип с деформациями по срединной линии, сенсорные потеря слуха и дистония. Это вызвано точечной мутацией, в которой аминокислота триптофан заменяет аргинин в позиции 183. Это изменяет взаимодействие актина с ADF /кофилин система, регулирующая динамику нервная клетка формирование цитоскелета.[181]
- Также была обнаружена доминантная точечная мутация, которая вызывает нейтрофильный гранулоцит дисфункция и повторяющиеся инфекции. Похоже, что мутация изменяет домен, ответственный за связывание между профилин и другие регуляторные белки. Сродство актина к профилину у этого аллеля значительно снижено.[182]
В ACTG1 локус кодирует цитозольный белок γ-актина, который отвечает за формирование цитоскелета. микрофиламенты. Он содержит шесть экзоны, дав начало 22 различным мРНК, которые производят четыре полных изоформы форма выражения которого, вероятно, зависит от типа ткань они находятся в. Также есть два разных Промоторы ДНК.[183] Было отмечено, что последовательности, транслируемые из этого локуса и из локуса β-актина, очень похожи на предсказанные, что указывает на общую предковую последовательность, которая подверглась дупликации и генетической конверсии.[184]
С точки зрения патологии, это было связано с такими процессами, как амилоидоз, пигментный ретинит, механизмы заражения, почка заболевания, а также различные виды врожденной тугоухости.[183]
Было обнаружено, что шесть аутосомно-доминантных точечных мутаций в последовательности вызывают различные типы потери слуха, в частности нейросенсорную тугоухость, связанную с локусом DFNA 20/26. Кажется, что они влияют на стереоцилии реснитчатых клеток внутреннего уха Орган Корти. β-актин является наиболее распространенным белком в тканях человека, но его не так много в реснитчатых клетках, что объясняет локализацию патологии. С другой стороны, похоже, что большинство этих мутаций затрагивают области, участвующие в связывании с другими белками, особенно с актомиозином.[32] Некоторые эксперименты предполагают, что патологический механизм этого типа потери слуха связан с тем, что F-актин в мутациях более чувствителен к кофилину, чем обычно.[185]
Однако, хотя нет никаких данных о каких-либо случаях, известно, что γ-актин также экспрессируется в скелетных мышцах, и хотя он присутствует в небольших количествах, модельные организмы показали, что его отсутствие может вызвать миопатии.[186]
Другие патологические механизмы
Некоторые инфекционные агенты используют актин, особенно цитоплазматический актин, в своем жизненный цикл. Две основные формы присутствуют в бактерии:
- Listeria monocytogenes, некоторые виды Риккетсия, Шигелла флекснери и другие внутриклеточные микробы ускользают от фагоцитарный вакуоли, покрывая себя капсулой из актиновых нитей. L. monocytogenes и S. flexneri оба образуют хвост в форме «кометного хвоста», который придает им подвижность. У каждого вида есть небольшие различия в механизме молекулярной полимеризации их «кометных хвостов». Наблюдались разные скорости смещения, например, с Листерия и Шигелла оказался самым быстрым.[187] Многие эксперименты продемонстрировали этот механизм. in vitro. Это указывает на то, что бактерии не используют миозиноподобный белковый мотор, и похоже, что их движение достигается за счет давления, оказываемого полимеризацией, которая происходит рядом с клеточной стенкой микроорганизма. Бактерии ранее были окружены ABP от хозяина, и как минимум покрытие содержит Комплекс Арп2 / 3, Ena / VASP белки, кофилин, буферный белок и промоторы нуклеации, такие как винкулин сложный. Благодаря этим движениям они образуют выступы, которые достигают соседних клеток, заражая и их, так что иммунная система бороться с инфекцией можно только через клеточный иммунитет. Движение может быть вызвано изменением кривой и расщеплением волокон.[188] Другие виды, такие как Mycobacterium marinum и Burkholderia pseudomallei, также способны к локальной полимеризации клеточного актина, чтобы способствовать их перемещению посредством механизма, который сосредоточен на комплексе Arp2 / 3. Кроме того, вакцина вирус Вакцина также использует элементы актинового цитоскелета для своего распространения.[189]
- Синегнойная палочка способен образовывать защитный биопленка чтобы избежать организм хозяина Защиты, особенно белые кровяные клетки и антибиотики. Биопленка построена с использованием ДНК и актиновые нити из организма-хозяина.[190]
В дополнение к ранее приведенному примеру, полимеризация актина стимулируется на начальных этапах интернализации некоторых вирусов, в частности ВИЧ, например, путем инактивации комплекса кофилина.[191]
Роль, которую актин играет в процессе инвазии раковых клеток, до сих пор не определена.[192]
Эволюция
Эукариотический цитоскелет организмов среди всех таксономические группы имеют компоненты, аналогичные актину и тубулину. Например, белок, кодируемый ACTG2 ген у человека полностью эквивалентен гомологи присутствует у крыс и мышей, даже если нуклеотид уровень сходства снижается до 92%.[162] Однако есть существенные отличия от эквивалентов у прокариот (FtsZ и MreB ), где сходство между нуклеотидными последовательностями составляет от 40 до 50% среди разных бактерии и археи разновидность. Некоторые авторы предполагают, что предковый белок, который дал начало модельному эукариотическому актину, напоминает белки, присутствующие в современных бактериальных цитоскелетах.[4][193]

Некоторые авторы указывают, что поведение актина, тубулина и гистон, белок, участвующий в стабилизации и регуляции ДНК, схожи по своей способности связывать нуклеотиды и по своей способности использовать преимущества Броуновское движение. Также было высказано предположение, что все они имеют общего предка.[194] Следовательно, эволюционный Эти процессы привели к диверсификации предковых белков в разновидности, присутствующие сегодня, сохраняя, среди прочего, актины как эффективные молекулы, которые были способны решать важные наследственные биологические процессы, такие как эндоцитоз.[195]
Эквиваленты в бактериях
В бактериальный цитоскелет может быть не таким сложным, как в эукариоты; однако он содержит белки, которые очень похожи на мономеры и полимеры актина. Бактериальный белок MreB полимеризуется в тонкие неспиральные филаменты и иногда в спиральные структуры, подобные F-актину.[21][196] Более того, его кристаллическая структура очень похожа на структуру G-актина (с точки зрения его трехмерной конформации), есть даже сходства между протофиламентами MreB и F-актином. Бактериальный цитоскелет также содержит FtsZ белки, похожие на тубулин.[197]
Таким образом, бактерии обладают цитоскелетом с элементами, гомологичными актину (например, MreB, AlfA, ParM, FtsA, и MamK), хотя аминокислотная последовательность этих белков отличается от таковой в клетках животных. Однако такие белки обладают высокой степенью структурный сходство с эукариотическим актином. Высокодинамичные микрофиламенты, образованные агрегацией MreB и ParM, необходимы для жизнеспособности клеток и участвуют в морфогенезе клеток, хромосома сегрегация и полярность клеток. ParM является гомологом актина, который кодируется в плазмида и он участвует в регуляции плазмидной ДНК.[4][198] ParM из разных бактериальных плазмид могут образовывать удивительно разнообразные спиральные структуры, состоящие из двух[199][200] или четыре[201] цепей для поддержания точного наследования плазмид.
Приложения
Актин используется в научных и технологических лабораториях как дорожка для молекулярные моторы например, миозин (в мышечной ткани или вне ее) и как необходимый компонент для функционирования клеток. Его также можно использовать как диагностический инструмент, так как некоторые его аномальные варианты связаны с появлением конкретных патологий.
- Нанотехнологии. Актин-миозиновые системы действуют как молекулярные двигатели, которые позволяют транспортировать везикулы и органеллы по цитоплазме. Возможно, что актин может быть применен к нанотехнологии поскольку его динамические способности использовались в ряде экспериментов, в том числе в бесклеточных системах. Основная идея состоит в том, чтобы использовать микрофиламенты в качестве направляющих для молекулярных моторов, которые могут переносить заданную нагрузку. То есть актин может использоваться для определения цепи, по которой груз может транспортироваться более или менее контролируемым и направленным образом. С точки зрения общих приложений, его можно использовать для направленного транспорта молекул для осаждения в определенных местах, что позволит осуществлять контролируемую сборку наноструктур.[202] Эти атрибуты могут быть применены к лабораторным процессам, таким как лаборатория на кристалле, в механике нанокомпонентов и в нанотрансформаторах, которые преобразуют механическую энергию в электрическую.[203]
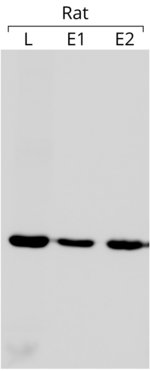
- Актин используется в качестве внутреннего контроля в вестерн-блоты чтобы убедиться, что равные количества белка были загружены на каждую полосу геля. В примере блоттинга, показанном слева, в каждую лунку загружали 75 мкг общего белка. Блот реагировал с антителом против β-актина (другие подробности блоттинга см. В ссылке [204])
Использование актина в качестве внутреннего контроля основано на предположении, что его экспрессия практически постоянна и не зависит от условий эксперимента. Сравнивая экспрессию интересующего гена с экспрессией актина, можно получить относительную величину, которую можно сравнивать в разных экспериментах,[205] всякий раз, когда выражение последнего постоянно. Стоит отметить, что актин не всегда обладает желаемой стабильностью. экспрессия гена.[206]
- Здоровье. Немного аллели актина вызывают заболевания; по этой причине были разработаны методы их обнаружения. Кроме того, актин может использоваться в качестве косвенного маркера хирургической патологии: можно использовать вариации в характере его распределения в ткани как маркер инвазии в неоплазия, васкулит, и другие условия.[207] Кроме того, из-за тесной связи актина с аппаратом мышечного сокращения его уровни в скелетных мышцах снижаются, когда эти ткани атрофия, поэтому его можно использовать в качестве маркера этого физиологического процесса.[208]
- Пищевые технологии. Можно определить качество некоторых обработанных пищевых продуктов, например колбасы, путем определения количества актина, присутствующего в мясе. Традиционно использовался метод, основанный на обнаружении 3-метилгистидин в гидролизованный образцы этих продуктов, поскольку это соединение присутствует в тяжелой цепи актина и F-миозина (оба являются основными компонентами мышц). Образование этого соединения во плоти происходит от метилирование из гистидин остатки присутствуют в обоих белках.[209][210]
Гены
Гены человека, кодирующие белки актина, включают:
Смотрите также
- Ремоделирование актина - влияние на структуру и форму клеток
- Актин-связывающий белок
- Активное вещество
- Arp2 / 3
- Филоподии
- FtsZ
- Промежуточная нить
- Ламеллиподиум
- Моторный белок - преобразует химическую энергию в механическую работу
- MreB - один из гомологов актина у бактерий
- Нейрон
- Фаллотоксин
Рекомендации
- ^ а б c d е PDB: 1J6Z; Otterbein LR, Graceffa P, Dominguez R (июль 2001 г.). «Кристаллическая структура несложного актина в состоянии АДФ». Наука. 293 (5530): 708–711. Дои:10.1126 / science.1059700. PMID 11474115. S2CID 12030018.
- ^ Доэрти Г.Дж., МакМахон ХТ (2008). «Посредничество, модуляция и последствия взаимодействий мембрана-цитоскелет». Ежегодный обзор биофизики. 37 (1): 65–95. Дои:10.1146 / annurev.biophys.37.032807.125912. PMID 18573073. S2CID 17352662.
- ^ Виндин Х., Ганнинг П. (август 2013 г.). «Цитоскелетные тропомиозины: хореографы функционального разнообразия актиновых филаментов». Журнал исследований мышц и подвижности клеток. 34 (3–4): 261–274. Дои:10.1007 / s10974-013-9355-8. ЧВК 3843815. PMID 23904035.
- ^ а б c d е ж грамм час я Gunning PW, Ghoshdastider U, Whitaker S, Popp D, Robinson RC (июнь 2015 г.). «Эволюция композиционно и функционально различных актиновых филаментов». Журнал клеточной науки. 128 (11): 2009–2019. Дои:10.1242 / jcs.165563. PMID 25788699.
- ^ Ghoshdastider U, Jiang S, Popp D, Robinson RC (июль 2015 г.). «В поисках первозданной актиновой нити». Труды Национальной академии наук Соединенных Штатов Америки. 112 (30): 9150–9151. Дои:10.1073 / pnas.1511568112. ЧВК 4522752. PMID 26178194.
- ^ а б Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2002). «Глава 16: Цитоскелет». Молекулярная биология клетки. Нью-Йорк: Наука Гарланд. С. 907–982. ISBN 978-0-8153-3218-3.
- ^ Halliburton WD (август 1887 г.). "О мышечной плазме". Журнал физиологии. 8 (3–4): 133–202. Дои:10.1113 / jphysiol.1887.sp000252. ЧВК 1485127. PMID 16991477.
- ^ а б Банга, Илона (1942). Сент-Дьёрдьи, Альберт (ред.). «Приготовление и свойства миозина А и В.» Исследования Института медицинской химии Университета Сегеда. 1941-1942 гг.. я: 5–15.
- ^ Штрауб, Бруно Ф. (1942). Сент-Дьёрдьи, Альберт (ред.). «Актин». Исследования Института медицинской химии Университета Сегеда. 1942 г.. II: 3–15.
- ^ Бугьи, Бета; Келлермайер, Миклош (март 2020 г.). «Открытие актина:« видеть то, что видели все остальные, и думать о том, о чем никто не думал ».'". Журнал исследований мышц и подвижности клеток. 41 (1): 3–9. Дои:10.1007 / s10974-019-09515-z. ЧВК 7109165. PMID 31093826.
- ^ Сент-Дьёрдьи, Альберт (1942). Сент-Дьёрдьи, Альберт (ред.). «Обсуждение». Исследования Института медицинской химии Университета Сегеда. 1941-1942 гг.. я: 67–71.
- ^ Сент-Дьердь А (1945). «Исследования на мышцах». Acta Physiol Скандинав. 9 (Прил.): 25.
- ^ а б Штрауб Ф. Б., Фойер Г. (1989). «Аденозинтрифосфат. Функциональная группа актина. 1950». Biochimica et Biophysica Acta. 1000: 180–195. Дои:10.1016/0006-3002(50)90052-7. PMID 2673365.
- ^ Барани М., Бэррон Дж. Т., Гу Л., Барани К. (декабрь 2001 г.). «Обмен актинового нуклеотида в неповрежденной гладкой мышце артерии». Журнал биологической химии. 276 (51): 48398–48403. Дои:10.1074 / jbc.M106227200. PMID 11602582.
- ^ а б c Эльзинга М., Коллинза Дж. Х., Кюля В. М., Адельштейна Р. С. (сентябрь 1973 г.). «Полная аминокислотная последовательность актина скелетных мышц кролика». Труды Национальной академии наук Соединенных Штатов Америки. 70 (9): 2687–2691. Bibcode:1973PNAS ... 70.2687E. Дои:10.1073 / пнас.70.9.2687. ЧВК 427084. PMID 4517681.
- ^ а б Kabsch W, Mannherz HG, Suck D, Pai EF, Holmes KC (сентябрь 1990 г.). «Атомная структура комплекса актин: ДНКаза I». Природа. 347 (6288): 37–44. Bibcode:1990Натура.347 ... 37K. Дои:10.1038 / 347037a0. PMID 2395459. S2CID 925337.
- ^ а б Холмс К.С., Попп Д., Гебхард В., Кабш В. (сентябрь 1990 г.). «Атомная модель актинового филамента». Природа. 347 (6288): 44–49. Bibcode:1990Натура 347 ... 44H. Дои:10.1038 / 347044a0. PMID 2395461. S2CID 4317981.
- ^ Ориол С., Даборд С., Лэндон Ф. (январь 1977 г.). «Кристаллизация нативного актина поперечно-полосатых мышц». Письма FEBS. 73 (1): 89–91. Дои:10.1016/0014-5793(77)80022-7. PMID 320040. S2CID 5142918.
- ^ Савая М.Р., Кудряшов Д.С., Пашков И., Адисетийо Х., Рейслер Э., Йейтс Т.О. (апрель 2008 г.). «Множественные кристаллические структуры димеров актина и их значение для взаимодействия в актиновом филаменте». Acta Crystallographica Раздел D. 64 (Pt 4): 454–465. Дои:10.1107 / S0907444908003351. ЧВК 2631129. PMID 18391412.
- ^ Нарита А., Такеда С., Ямасита А., Маеда Й (ноябрь 2006 г.). «Структурная основа покрытия актиновых филаментов на зазубренном конце: исследование с помощью криоэлектронной микроскопии». Журнал EMBO. 25 (23): 5626–5633. Дои:10.1038 / sj.emboj.7601395. ЧВК 1679762. PMID 17110933.
- ^ а б c d е ж Ода Т., Иваса М., Айхара Т., Маеда Ю., Нарита А. (январь 2009 г.). «Природа перехода от глобулярного к фиброзному актину». Природа. 457 (7228): 441–445. Bibcode:2009Натура.457..441O. Дои:10.1038 / природа07685. PMID 19158791. S2CID 4317892.
- ^ а б c d фон дер Экен Дж., Мюллер М., Леман В., Манштейн Д. Д., Пенчек П. А., Раунсер С. (май 2015 г.). «Структура комплекса F-актин-тропомиозин». Природа. 519 (7541): 114–117. Bibcode:2015Натура.519..114V. Дои:10.1038 / природа14033. ЧВК 4477711. PMID 25470062.
- ^ Ханукоглу И., Танезе Н., Фукс Э. (февраль 1983 г.). «Комплементарная последовательность ДНК цитоплазматического актина человека. Межвидовая дивергенция 3'-некодирующих областей». Журнал молекулярной биологии. 163 (4): 673–678. Дои:10.1016/0022-2836(83)90117-1. PMID 6842590.
- ^ а б c d Biología celular (на испанском). Elsevier España. 2002. с. 132. ISBN 978-84-458-1105-4.
- ^ Понте П., Ганнинг П., Блау Х, Кедес Л. (октябрь 1983 г.). «Гены актина человека являются единственной копией для альфа-скелетного и альфа-сердечного актина, но многокопийными для генов бета- и гамма-цитоскелета: 3 'нетранслируемые области являются изотип-специфичными, но сохраняются в процессе эволюции». Молекулярная и клеточная биология. 3 (10): 1783–1791. Дои:10.1128 / MCB.3.10.1783. ЧВК 370040. PMID 6646124.
- ^ а б c d Скотт М.П., Лодиш Х.Ф., Берк А, Кайзер С, Кригер М, Бретчер А, Плоег Х, Амон А (2012). Молекулярная клеточная биология. Сан-Франциско: В. Х. Фриман. ISBN 978-1-4292-3413-9.
- ^ Hara F, Yamashiro K, Nemoto N, Ohta Y, Yokobori S, Yasunaga T, Hisanaga S, Yamagishi A (март 2007 г.). «Гомолог актина архея Thermoplasma acidophilum, который сохраняет древние характеристики эукариотического актина». Журнал бактериологии. 189 (5): 2039–2045. Дои:10.1128 / JB.01454-06. ЧВК 1855749. PMID 17189356.
- ^ а б Graceffa P, Dominguez R (сентябрь 2003 г.). «Кристаллическая структура мономерного актина в состоянии АТФ. Структурные основы нуклеотид-зависимой динамики актина». Журнал биологической химии. 278 (36): 34172–34180. Дои:10.1074 / jbc.M303689200. PMID 12813032.
- ^ Рейслер Э (февраль 1993 г.). «Молекулярная структура и функция актина». Текущее мнение в области клеточной биологии. 5 (1): 41–47. Дои:10.1016 / S0955-0674 (05) 80006-7. PMID 8448029.
- ^ "cd00012: ACTIN". Сохраненная база данных домена. Национальный центр биотехнологической информации США (NCBI). В архиве из оригинала от 05.12.2017.
- ^ а б Коллинз Дж. Х., Эльзинга М. (август 1975 г.). «Первичная структура актина из скелетных мышц кролика. Завершение и анализ аминокислотной последовательности». Журнал биологической химии. 250 (15): 5915–5920. PMID 1150665.
- ^ а б c d е ж грамм час Dos Remedios CG, Chhabra D (2008). Актин-связывающие белки и болезнь. Springer. ISBN 978-0-387-71747-0.
- ^ Рулд М.А., Ван Кью, Джоэл ПБ, Лоуи С., Трибус К.М. (октябрь 2006 г.). «Кристаллические структуры экспрессированного неполимеризуемого мономерного актина в состояниях АДФ и АТФ». Журнал биологической химии. 281 (42): 31909–31919. Дои:10.1074 / jbc.M601973200. PMID 16920713.
- ^ а б Девлин TM (2006). Биокимика. Барселона: Реверте. ISBN 978-84-291-7208-9.
- ^ а б c Reisler E, Egelman EH (декабрь 2007 г.). «Структура и функции актина: чего мы до сих пор не понимаем». Журнал биологической химии. 282 (50): 36133–36137. Дои:10.1074 / jbc.R700030200. PMID 17965017.
- ^ Бегг Д.А., Родевальд Р., Ребхун Л.И. (декабрь 1978 г.). «Визуализация полярности актиновых филаментов в тонких срезах. Доказательства однородной полярности связанных с мембраной филаментов». Журнал клеточной биологии. 79 (3): 846–852. Дои:10.1083 / jcb.79.3.846. ЧВК 2110270. PMID 569662.
- ^ Дженезер Ф (1981). Гистологи. Мунксгаард. п. 105. ISBN 978-87-16-08418-7.
- ^ а б c Холл Дж. Э., Гайтон AC (2006). Учебник медицинской физиологии. Сент-Луис, Миссури: Elsevier Saunders. п.76. ISBN 978-0-7216-0240-0.
- ^ а б Саймонс СТ, Стаес А., Роммелер Х, Ампе С., Льюис С.А., Коуэн, штат Нью-Джерси (февраль 2004 г.). «Избирательный вклад эукариотических субъединиц префолдина в связывание актина и тубулина». Журнал биологической химии. 279 (6): 4196–4203. Дои:10.1074 / jbc.M306053200. PMID 14634002.
- ^ а б Мартин-Бенито Дж., Боскович Дж., Гомес-Пуэртас П., Карраскоса Дж. Л., Саймонс К. Т., Льюис С. А., Бартолини Ф., Коуэн Н. Дж., Валпуэста Дж. М. (декабрь 2002 г.). «Структура эукариотического префолдина и его комплексов с развернутым актином и цитозольным шаперонином CCT». Журнал EMBO. 21 (23): 6377–6386. Дои:10.1093 / emboj / cdf640. ЧВК 136944. PMID 12456645.
- ^ а б Vandamme D, Lambert E, Waterschoot D, Cognard C, Vandekerckhove J, Ampe C, Constantin B, Rommelaere H (июль 2009 г.). «Мутанты альфа-актина немалиновой миопатии скелетных мышц вызывают гибель клеток культивируемых мышечных клеток». Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1793 (7): 1259–1271. Дои:10.1016 / j.bbamcr.2009.04.004. PMID 19393268.
- ^ а б Брэкли К.И., Грэнтэм Дж. (Январь 2009 г.). «Активность шаперонина, содержащего TCP-1 (CCT): влияние на развитие клеточного цикла и организацию цитоскелета». Клеточный стресс и шапероны. 14 (1): 23–31. Дои:10.1007 / s12192-008-0057-х. ЧВК 2673901. PMID 18595008.
- ^ а б Stirling PC, Cuéllar J, Alfaro GA, El Khadali F, Beh CT, Valpuesta JM, Melki R, Leroux MR (март 2006 г.). «PhLP3 модулирует CCT-опосредованное сворачивание актина и тубулина посредством тройных комплексов с субстратами». Журнал биологической химии. 281 (11): 7012–7021. Дои:10.1074 / jbc.M513235200. PMID 16415341.
- ^ Хансен WJ, Коуэн NJ, Велч WJ (апрель 1999). «Комплексы префолдин-растущая цепь в сворачивании белков цитоскелета». Журнал клеточной биологии. 145 (2): 265–277. Дои:10.1083 / jcb.145.2.265. ЧВК 2133115. PMID 10209023.
- ^ Мартин-Бенито Дж., Грэнтэм Дж., Боскович Дж., Брэкли К.И., Карраскоса Дж. Л., Уиллисон К. Р., Вальпуэста Дж. М. (март 2007 г.). «Межкольцевое расположение цитозольного шаперонина CCT». Отчеты EMBO. 8 (3): 252–257. Дои:10.1038 / sj.embor.7400894. ЧВК 1808031. PMID 17304242.
- ^ Neirynck K, Waterschoot D, Vandekerckhove J, Ampe C, Rommelaere H (январь 2006 г.). «Актин взаимодействует с CCT через дискретные сайты связывания: модель перехода связывания-высвобождения для CCT-опосредованного сворачивания актина». Журнал молекулярной биологии. 355 (1): 124–138. Дои:10.1016 / j.jmb.2005.10.051. PMID 16300788.
- ^ а б c Вавилонис Д., Ян К., О'Шонесси Б. (июнь 2005 г.). «Кинетика полимеризации актина, структура кэпа и флуктуации». Труды Национальной академии наук Соединенных Штатов Америки. 102 (24): 8543–8548. arXiv:q-bio / 0404004. Bibcode:2005ПНАС..102.8543В. Дои:10.1073 / pnas.0501435102. ЧВК 1150824. PMID 15939882.
- ^ Каткар Х. Х., Давтян А., Дурумерик А. Е., Хоки Г. М., Шрамм А., Энрике М., Вот Г. А. (сентябрь 2018 г.). «Понимание кооперативного характера гидролиза АТФ в актиновых филаментах». Биофизический журнал. 115 (8): 1589–1602. Bibcode:2018BpJ ... 115,1589K. Дои:10.1016 / j.bpj.2018.08.034. ЧВК 6260209. PMID 30249402.
- ^ McCullagh M, Saunders MG, Voth GA (сентябрь 2014 г.). «Раскрытие тайны гидролиза АТФ в актиновых филаментах». Журнал Американского химического общества. 136 (37): 13053–13058. Дои:10.1021 / ja507169f. ЧВК 4183606. PMID 25181471.
- ^ Saunders MG, Voth GA (октябрь 2011 г.). «Молекулы воды в нуклеотидсвязывающей щели актина: влияние на конформацию субъединицы и последствия для гидролиза АТФ». Журнал молекулярной биологии. 413 (1): 279–291. Дои:10.1016 / j.jmb.2011.07.068. PMID 21856312.
- ^ Vandekerckhove J, Weber K (декабрь 1978 г.). «По крайней мере, шесть различных актинов экспрессируются у высшего млекопитающего: анализ, основанный на аминокислотной последовательности аминоконцевого триптического пептида». Журнал молекулярной биологии. 126 (4): 783–802. Дои:10.1016/0022-2836(78)90020-7. PMID 745245.
- ^ Хайтлина С.Ю. (2001). Функциональная специфичность изоформ актина. Международный обзор цитологии. 202. С. 35–98. Дои:10.1016 / S0074-7696 (01) 02003-4. ISBN 9780123646064. PMID 11061563.
- ^ Гарнер ЕС, Кэмпбелл К.С., Вейбель Д.В., Маллинс Р.Д. (март 2007 г.). «Восстановление расщепления ДНК, вызванное сборкой прокариотического гомолога актина». Наука. 315 (5816): 1270–1274. Bibcode:2007Научный ... 315.1270G. Дои:10.1126 / science.1138527. ЧВК 2851738. PMID 17332412.
- ^ Суранени, Правин; Фогельсон, Бен; Рубинштейн, Борис; Ногера, Филипп; Фолькманн, Нильс; Ханейн, Дорит; Могильнер, Алекс; Ли, Ронг (2015). «Механизм выступа передней кромки в отсутствие комплекса Arp2 / 3». Молекулярная биология клетки. 26 (5): 901–912. Дои:10.1091 / mbc.E14-07-1250. ЧВК 4342026. PMID 25568333.
- ^ Альбертс, Брюс; Джонсон, Александр; Льюис, Джулиан; Рафф, Мартин; Робертс, Кейт; Уолтер, Питер, ред. (2002). «Самосборка и динамическая структура филаментов цитоскелета». Молекулярная биология клетки (4-е изд.). Наука о гирляндах. ISBN 978-0-8153-3218-3.
- ^ Кавамура, Масару; Маруяма, Кощак (март 1970 г.). "Электронно-микроскопическая длина частиц F-актина, полимеризованного in vitro". Журнал биохимии. 67 (3): 437–457. Дои:10.1093 / oxfordjournals.jbchem.a129267. PMID 5463781.
- ^ Хаусман Р. Э., Купер Г. М. (2007). «Глава 12: Цитоскелет и движение клеток». Клетка: молекулярный подход. Вашингтон, округ Колумбия:, Сандерленд, Массачусетс: ASM Press, Sinauer Associates. ISBN 978-0-87893-219-1.
- ^ Биндшадлер М., Осборн Э.А., Дьюи С.Ф., МакГрат Д.Л. (май 2004 г.). «Механистическая модель цикла актина». Биофизический журнал. 86 (5): 2720–2739. Bibcode:2004BpJ .... 86.2720B. Дои:10.1016 / S0006-3495 (04) 74326-X. ЧВК 1304143. PMID 15111391.
- ^ Киршнер М.В. (июль 1980 г.). «Влияние беговой дорожки на стабильность и полярность полимеров актина и тубулина in vivo». Журнал клеточной биологии. 86 (1): 330–334. Дои:10.1083 / jcb.86.1.330. ЧВК 2110666. PMID 6893454.
- ^ Годси Х., Каземи М.Т. (июнь 2011 г.). «Эластичные свойства актиновых сборок в различных состояниях связывания нуклеотидов». Клетка. Мол. Bioeng. 5 (1): 1–13. Дои:10.1007 / s12195-011-0181-z. S2CID 83973622.
- ^ Плоппер Г., Левин Б., Кассимерис Л. (2007). Клетки. Бостон: Джонс и Бартлетт Издательство. п.378. ISBN 978-0-7637-3905-8.
гидролизная полимеризация актина.
- ^ Чжан Д.С., Пьяцца В., Перрин Б.Дж., Рзадзинская А.К., Початек Дж. К., Ван М., Проссер Х. М., Эрвасти Дж. М., Кори Д. П., Лечен С. П. (январь 2012 г.). «Масс-спектрометрия с мультиизотопной визуализацией выявляет медленный оборот белка в стереоцилиях волосковых клеток». Природа. 481 (7382): 520–524. Bibcode:2012Натура.481..520Z. Дои:10.1038 / природа10745. ЧВК 3267870. PMID 22246323.
- ^ PDB: 2БТФ; Schutt CE, Myslik JC, Rozycki MD, Goonesekere NC, Lindberg U (октябрь 1993 г.). «Структура кристаллического профилин-бета-актина». Природа. 365 (6449): 810–816. Bibcode:1993Натура.365..810С. Дои:10.1038 / 365810a0. PMID 8413665. S2CID 4359724.
- ^ Домингес Р. (ноябрь 2004 г.). «Актин-связывающие белки - объединяющая гипотеза». Тенденции в биохимических науках. 29 (11): 572–578. Дои:10.1016 / j.tibs.2004.09.004. PMID 15501675.
- ^ Goldschmidt-Clermont PJ, Furman MI, Wachsstock D, Safer D, Nachmias VT, Pollard TD (сентябрь 1992 г.). «Контроль обмена нуклеотидов актина с помощью тимозина бета 4 и профилина. Потенциальный механизм регуляции полимеризации актина в клетках». Молекулярная биология клетки. 3 (9): 1015–1024. Дои:10.1091 / mbc.3.9.1015. ЧВК 275662. PMID 1330091.
- ^ Витке В., Подтелейников А.В., Ди Нардо А., Сазерленд Д.Д., Гурняк С.Б., Дотти С., Манн М. (февраль 1998 г.). «В мозге мышей профилин I и профилин II связаны с регуляторами пути эндоцитов и сборки актина». Журнал EMBO. 17 (4): 967–976. Дои:10.1093 / emboj / 17.4.967. ЧВК 1170446. PMID 9463375.
- ^ Карлссон Л., Нистрем Л. Е., Сундквист И., Марки Ф., Линдберг Ю. (сентябрь 1977 г.). «Полимеризуемость актина зависит от профилина, низкомолекулярного белка в немышечных клетках». Журнал молекулярной биологии. 115 (3): 465–483. Дои:10.1016/0022-2836(77)90166-8. PMID 563468.
- ^ Kiselar JG, Janmey PA, Almo SC, Chance MR (апрель 2003 г.). «Визуализация Са2 + -зависимой активации гельсолина с помощью синхротронного следа». Труды Национальной академии наук Соединенных Штатов Америки. 100 (7): 3942–3947. Bibcode:2003ПНАС..100.3942К. Дои:10.1073 / pnas.0736004100. ЧВК 153027. PMID 12655044.
- ^ Ghoshdastider U, Popp D, Burtnick LD, Robinson RC (ноябрь 2013 г.). «Расширяющееся суперсемейство белков домена гомологии гельсолина». Цитоскелет. 70 (11): 775–795. Дои:10.1002 / см 21149. PMID 24155256. S2CID 205643538.
- ^ Southwick FS (июнь 2000 г.). «Гельсолин и АДФ / кофилин усиливают динамику актина подвижных клеток». Труды Национальной академии наук Соединенных Штатов Америки. 97 (13): 6936–6938. Bibcode:2000PNAS ... 97.6936S. Дои:10.1073 / pnas.97.13.6936. ЧВК 34364. PMID 10860951.
- ^ Колдуэлл Дж. Э., Хейсс С. Г., Мермолл В., Купер Дж. А. (октябрь 1989 г.). «Влияние CapZ, белка, покрывающего актин мышц, на полимеризацию актина». Биохимия. 28 (21): 8506–8514. Дои:10.1021 / bi00447a036. PMID 2557904.
- ^ Вебер А., Пеннис С.Р., Бэбкок Г.Г., Фаулер В.М. (декабрь 1994 г.). «Тропомодулин закрывает заостренные концы актиновых нитей». Журнал клеточной биологии. 127 (6 Pt 1): 1627–1635. Дои:10.1083 / jcb.127.6.1627. ЧВК 2120308. PMID 7798317.
- ^ Робинсон Р.К., Турбедски К., Кайзер Д.А., Маршан Дж. Б., Хиггс Н. Н., Чо С., Поллард Т. Д. (ноябрь 2001 г.). «Кристаллическая структура комплекса Arp2 / 3». Наука. 294 (5547): 1679–1684. Bibcode:2001Научный ... 294.1679R. Дои:10.1126 / science.1066333. PMID 11721045. S2CID 18088124.
- ^ Маллинз Р.Д., Поллард Т.Д. (апрель 1999 г.). «Строение и функции комплекса Арп2 / 3». Текущее мнение в структурной биологии. 9 (2): 244–249. Дои:10.1016 / S0959-440X (99) 80034-7. PMID 10322212.
- ^ Machesky LM, Gould KL (февраль 1999 г.). «Комплекс Арп2 / 3: многофункциональный организатор актина». Текущее мнение в области клеточной биологии. 11 (1): 117–121. Дои:10.1016 / S0955-0674 (99) 80014-3. PMID 10047519.
- ^ Мортон В.М., Эйскоу К.Р., Маклафлин П.Дж. (июнь 2000 г.). «Латрункулин изменяет границу раздела актин-мономерная субъединица, чтобы предотвратить полимеризацию». Природа клеточной биологии. 2 (6): 376–378. Дои:10.1038/35014075. HDL:1842/757. PMID 10854330. S2CID 1803612.
- ^ а б Купер Дж. А. (октябрь 1987 г.). «Влияние цитохалазина и фаллоидина на актин». Журнал клеточной биологии. 105 (4): 1473–1478. Дои:10.1083 / jcb.105.4.1473. ЧВК 2114638. PMID 3312229.
- ^ Рубцова С.Н., Кондратов Р.В., Копнин ПБ, Чумаков П.М., Копнин Б.П., Васильев Ю.М. (июль 1998 г.). «Нарушение микрофиламентов актина цитохалазином D приводит к активации р53». Письма FEBS. 430 (3): 353–357. Дои:10.1016 / S0014-5793 (98) 00692-9. PMID 9688570. S2CID 38044707.
- ^ Huber, F .; Schnauß, J .; Rönicke, S .; Rauch, P .; Müller, K .; Fütterer, C .; Кас, Дж. (Январь 2013 г.). «Возникающая сложность цитоскелета: от единичных нитей до ткани». Успехи в физике. 62 (1): 1–112. Bibcode:2013AdPhy..62 .... 1H. Дои:10.1080/00018732.2013.771509. ЧВК 3985726. PMID 24748680.
- ^ а б c Grummt I (апрель 2006 г.). «Актин и миозин как факторы транскрипции». Текущее мнение в области генетики и развития. 16 (2): 191–196. Дои:10.1016 / j.gde.2006.02.001. PMID 16495046.
- ^ Zouwail S, Pettitt TR, Dove SK, Chibalina MV, Powner DJ, Haynes L, Wakelam MJ, Insall RH (июль 2005 г.). «Активность фосфолипазы D важна для локализации актина и актиновой подвижности у Dictyostelium». Биохимический журнал. 389 (Pt 1): 207–214. Дои:10.1042 / BJ20050085. ЧВК 1184553. PMID 15769249.
- ^ а б Eckert R, Randall D, Burggren WW, French K (2002). Физиология животных Эккерта: механизмы и адаптации. Нью-Йорк: W.H. Фриман и CO. ISBN 978-0-7167-3863-3.
- ^ Theriot, Julie A .; Митчисон, Тимоти Дж. (Июль 1991 г.). «Динамика актиновых микрофиламентов в двигательных клетках». Природа. 352 (6331): 126–131. Bibcode:1991Натура.352..126Т. Дои:10.1038 / 352126a0. PMID 2067574. S2CID 3062637.
- ^ Ли, Джульетта; Исихара, Акира; Theriot, Julie A .; Джейкобсон, Кен (март 1993). «Принципы передвижения клеток простой формы». Природа. 362 (6416): 167–171. Bibcode:1993Натура 362..167л. Дои:10.1038 / 362167a0. PMID 8450887. S2CID 4366904.
- ^ Тромбоцитопения (испанское издание) (2-е изд.). Elsevier Espana. 2001. с. 25. ISBN 978-84-8174-595-5.
- ^ а б c Паниагуа Р., Нисталь М., Сесма П., Альварес-Урия М., Фрайле Б., Анадон Р., Хосе Саес Ф. (2002). Citología e histología Vegetal y animal (на испанском). McGraw-Hill Interamericana de España, S.A.U. ISBN 978-84-486-0436-3.
- ^ Сюй К., Чжун Г, Чжуан Х (январь 2013 г.). «Актин, спектрин и ассоциированные белки образуют периодическую структуру цитоскелета в аксонах». Наука. 339 (6118): 452–456. Bibcode:2013Наука ... 339..452X. Дои:10.1126 / наука.1232251. ЧВК 3815867. PMID 23239625.
- ^ а б Мозли Дж. Б., Гуд Б. Л. (сентябрь 2006 г.). «Актиновый цитоскелет дрожжей: от клеточной функции к биохимическому механизму». Обзоры микробиологии и молекулярной биологии. 70 (3): 605–645. Дои:10.1128 / MMBR.00013-06. ЧВК 1594590. PMID 16959963.
- ^ Meagher RB, McKinney EC, Kandasamy MK (июнь 1999 г.). «Изовариантная динамика расширяет и буферизует ответы сложных систем: разнообразного семейства генов актина растений». Растительная клетка. 11 (6): 995–1006. Дои:10.1105 / tpc.11.6.995. ЧВК 1464670. PMID 10368172.
- ^ PDB 1unc; Vermeulen W, Vanhaesebrouck P, Van Troys M, Verschueren M, Fant F, Goethals M, Ampe C, Martins JC, Borremans FA (май 2004 г.). «Структуры раствора С-концевых субдоменов головного мозга ворсин и адвиллина человека, оценка требований связывания F-актина головного мозга». Белковая наука. 13 (5): 1276–1287. Дои:10.1110 / пс 03518104. ЧВК 2286768. PMID 15096633.
- ^ а б Хигаки Т., Сано Т., Хаседзава С. (декабрь 2007 г.). «Актиновая микрофиламентная динамика и белки, связывающие актин на стороне растений». Текущее мнение в области биологии растений. 10 (6): 549–556. Дои:10.1016 / j.pbi.2007.08.012. PMID 17936064.
- ^ Ковар Д.Р., Стайгер С.Дж., Уивер Е.А., Маккарди Д.В. (декабрь 2000 г.). «AtFim1 представляет собой белок, сшивающий актиновые филаменты из Arabidopsis thaliana». Журнал растений. 24 (5): 625–636. Дои:10.1046 / j.1365-313x.2000.00907.x. PMID 11123801.
- ^ а б Clark TG, Merriam RW (декабрь 1977 г.). «Диффузионные и связанные ядра актина ооцитов Xenopus laevis». Клетка. 12 (4): 883–891. Дои:10.1016/0092-8674(77)90152-0. PMID 563771. S2CID 34708250.
- ^ Хофманн WA (2009-01-01). Клеточная и молекулярная биология ядерного актина. Международный обзор клеточной и молекулярной биологии. 273. С. 219–263. Дои:10.1016 / S1937-6448 (08) 01806-6. ISBN 9780123748041. PMID 19215906.
- ^ а б Bohnsack MT, Stüven T, Kuhn C, Cordes VC, Görlich D (март 2006 г.). «Избирательный блок ядерного экспорта актина стабилизирует гигантские ядра ооцитов Xenopus». Природа клеточной биологии. 8 (3): 257–263. Дои:10.1038 / ncb1357. HDL:11858 / 00-001M-0000-0012-E6EB-9. PMID 16489345. S2CID 16529470.
- ^ Dopie J, Skarp KP, Rajakylä EK, Tanhuanpää K, Vartiainen MK (февраль 2012 г.). «Активное поддержание ядерного актина импортином 9 поддерживает транскрипцию». Труды Национальной академии наук Соединенных Штатов Америки. 109 (9): E544–552. Дои:10.1073 / pnas.1118880109. ЧВК 3295300. PMID 22323606.
- ^ Вада А., Фукуда М., Мисима М., Нисида Е. (март 1998 г.). «Ядерный экспорт актина: новый механизм, регулирующий субклеточную локализацию основного цитоскелетного белка». Журнал EMBO. 17 (6): 1635–1641. Дои:10.1093 / emboj / 17.6.1635. ЧВК 1170511. PMID 9501085.
- ^ Stüven T, Hartmann E, Görlich D (ноябрь 2003 г.). «Экспортин 6: новый ядерный экспортный рецептор, специфичный для комплексов профилин.актин». Журнал EMBO. 22 (21): 5928–5940. Дои:10.1093 / emboj / cdg565. ЧВК 275422. PMID 14592989.
- ^ а б Hofmann WA, Arduini A, Nicol SM, Camacho CJ, Lessard JL, Fuller-Pace FV, de Lanerolle P (июль 2009 г.). «СУМОилирование ядерного актина». Журнал клеточной биологии. 186 (2): 193–200. Дои:10.1083 / jcb.200905016. ЧВК 2717643. PMID 19635839.
- ^ а б Chhabra D, dos Remedios CG (сентябрь 2005 г.). «Кофилин, актин и их комплекс, наблюдаемые in vivo с использованием резонансного переноса энергии флуоресценции». Биофизический журнал. 89 (3): 1902–1908. Bibcode:2005BpJ .... 89.1902C. Дои:10.1529 / biophysj.105.062083. ЧВК 1366693. PMID 15994898.
- ^ Макдональд Д., Карреро Дж., Андрин К., де Врис Дж., Хендзель М.Дж. (февраль 2006 г.). «Нуклеоплазматический бета-актин существует в динамическом равновесии между низкоподвижными полимерными видами и быстро диффундирующими популяциями». Журнал клеточной биологии. 172 (4): 541–552. Дои:10.1083 / jcb.200507101. ЧВК 2063674. PMID 16476775.
- ^ Jockusch BM, Schoenenberger CA, Stetefeld J, Aebi U (август 2006 г.). «Отслеживание различных форм ядерного актина». Тенденции в клеточной биологии. 16 (8): 391–396. Дои:10.1016 / j.tcb.2006.06.006. PMID 16828286.
- ^ а б c d Migocka-Patrzałek M, Makowiecka A, Nowak D, Mazur AJ, Hofmann WA, Malicka-Błaszkiewicz M (ноябрь 2015 г.). «β- и γ-актины в ядре клеток меланомы человека A375». Гистохимия и клеточная биология. 144 (5): 417–428. Дои:10.1007 / s00418-015-1349-8. ЧВК 4628621. PMID 26239425.
- ^ Педерсон Т., Эби Ю. (2002-12-01). «Актин в ядре: в какой форме и для чего?». Журнал структурной биологии. 140 (1–3): 3–9. Дои:10.1016 / с1047-8477 (02) 00528-2. PMID 12490148.
- ^ Bergeron SE, Zhu M, Thiem SM, Friderici KH, Rubenstein PA (май 2010 г.). «Различия в ион-зависимой полимеризации между бета- и гамма-немышечными изоформами актина млекопитающих». Журнал биологической химии. 285 (21): 16087–16095. Дои:10.1074 / jbc.M110.110130. ЧВК 2871477. PMID 20308063.
- ^ Спенсер В.А. (сентябрь 2011 г.). «Ядерный актин: ключевой игрок во взаимодействии межклеточного матрикса и ядра». Коммуникативная и интегративная биология. 4 (5): 511–512. Дои:10.4161 / cib.16256. ЧВК 3204115. PMID 22046450.
- ^ а б Чжао К., Ван В., Рандо О.Дж., Сюэ Ю., Свидерек К., Куо А., Крэбтри Г.Р. (ноябрь 1998 г.). «Быстрое и фосфоинозитол-зависимое связывание SWI / SNF-подобного комплекса BAF с хроматином после передачи сигналов рецептора Т-лимфоцитов». Клетка. 95 (5): 625–636. Дои:10.1016 / s0092-8674 (00) 81633-5. PMID 9845365. S2CID 3184211.
- ^ а б Hofmann WA, Stojiljkovic L, Fuchsova B, Vargas GM, Mavrommatis E, Philimonenko V, Kysela K, Goodrich JA, Lessard JL, Hope TJ, Hozak P, de Lanerolle P (ноябрь 2004 г.). «Актин является частью пре-инициаторных комплексов и необходим для транскрипции РНК-полимеразой II». Природа клеточной биологии. 6 (11): 1094–1101. Дои:10.1038 / ncb1182. PMID 15502823. S2CID 23909479.
- ^ а б Ху П., Ву С., Эрнандес Н. (декабрь 2004 г.). «Роль бета-актина в транскрипции РНК-полимеразы III». Гены и развитие. 18 (24): 3010–3015. Дои:10.1101 / gad.1250804. ЧВК 535912. PMID 15574586.
- ^ а б Филимоненко В.В., Чжао Дж., Ибен С., Дингова Х., Кисела К., Кале М., Зентграф Х., Хофманн В.А., де Ланероль П., Хозак П., Груммт I. (декабрь 2004 г.). «Ядерный актин и миозин I необходимы для транскрипции РНК-полимеразы I. Природа клеточной биологии. 6 (12): 1165–1172. Дои:10.1038 / ncb1190. PMID 15558034. S2CID 6633625.
- ^ Маральди Н.М., Латтанци Дж., Мармироли С., Скварцони С., Манзоли Ф.А. (01.01.2004). «Новые роли ламинов, белков ядерной оболочки и актина в ядре». Достижения в регуляции ферментов. 44: 155–172. Дои:10.1016 / j.advenzreg.2003.11.005. PMID 15581488.
- ^ Tondeleir D, Lambrechts A, Müller M, Jonckheere V, Doll T, Vandamme D, Bakkali K, Waterschoot D, Lemaistre M, Debeir O, Decaestecker C, Hinz B, Staes A, Timmerman E, Colaert N, Gevaert K, Vandekerckhove J , Ampe C (август 2012 г.). «Клетки, лишенные β-актина, генетически перепрограммированы и поддерживают условную миграционную способность». Молекулярная и клеточная протеомика. 11 (8): 255–271. Дои:10.1074 / mcp.M111.015099. ЧВК 3412960. PMID 22448045.
- ^ Холаска Дж. М., Ковальски А. К., Уилсон К. Л. (сентябрь 2004 г.). «Эмерин закрывает заостренный конец актиновых нитей: свидетельство наличия актиновой корковой сети на внутренней ядерной мембране». PLOS Биология. 2 (9): E231. Дои:10.1371 / journal.pbio.0020231. ЧВК 509406. PMID 15328537.
- ^ Пакельварц М., Макнелли Э.М. (01.01.2011). «Мышечная дистрофия Эмери – Дрейфуса». Мышечные дистрофии. Справочник по клинической неврологии. 101. С. 155–166. Дои:10.1016 / B978-0-08-045031-5.00012-8. ISBN 9780080450315. PMID 21496632.
- ^ Фарранц А.К. (июнь 2008 г.). «Ремоделирование хроматина и организация актина». Письма FEBS. 582 (14): 2041–2050. Дои:10.1016 / j.febslet.2008.04.032. PMID 18442483. S2CID 23147656.
- ^ Шёлиндер М., Бьорк П., Седерберг Э., Сабри Н., Фаррант А. К., Visa N (август 2005 г.). «Растущая пре-мРНК рекрутирует актин и факторы, модифицирующие хроматин, в транскрипционно активные гены». Гены и развитие. 19 (16): 1871–1884. Дои:10.1101 / gad.339405. ЧВК 1186187. PMID 16103215.
- ^ а б Percipalle P, Visa N (март 2006 г.). «Молекулярные функции ядерного актина в транскрипции». Журнал клеточной биологии. 172 (7): 967–971. Дои:10.1083 / jcb.200512083. ЧВК 2063754. PMID 16549500.
- ^ Федорова Е., Цинк Д. (ноябрь 2008 г.). «Ядерная архитектура и генная регуляция». Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1783 (11): 2174–2184. Дои:10.1016 / j.bbamcr.2008.07.018. PMID 18718493.
- ^ Скарп К.П., Вартиайнен М.К. (август 2010 г.). «Актин на ДНК - древние и динамичные отношения». Цитоскелет. 67 (8): 487–495. Дои:10.1002 / см. 20464. PMID 20593452. S2CID 37763449.
- ^ Олав И.А., Рек-Петерсон С.Л., Крэбтри Г.Р. (01.01.2002). «Ядерный актин и родственные актину белки в ремоделировании хроматина». Ежегодный обзор биохимии. 71: 755–781. Дои:10.1146 / annurev.biochem.71.110601.135507. PMID 12045110.
- ^ Чжэн Б., Хань М., Бернье М., Вэнь Дж. К. (май 2009 г.). «Ядерный актин и актин-связывающие белки в регуляции транскрипции и экспрессии генов». Журнал FEBS. 276 (10): 2669–2685. Дои:10.1111 / j.1742-4658.2009.06986.x. ЧВК 2978034. PMID 19459931.
- ^ Феррай К., Наум-Онгания Г., Лонгобарди Е., Палаццоло М., Дисанза А., Диас В. М., Криппа М. П., Сцита Г., Блази Ф (август 2009 г.). «Индукция транскрипции HoxB ретиноевой кислотой требует полимеризации актина». Молекулярная биология клетки. 20 (15): 3543–3551. Дои:10.1091 / mbc.E09-02-0114. ЧВК 2719572. PMID 19477923.
- ^ Xu YZ, Thuraisingam T, Morais DA, Rola-Pleszczynski M, Radzioch D (март 2010 г.). «Ядерная транслокация бета-актина участвует в регуляции транскрипции во время дифференцировки макрофагов клеток HL-60». Молекулярная биология клетки. 21 (5): 811–820. Дои:10.1091 / mbc.E09-06-0534. ЧВК 2828967. PMID 20053683.
- ^ а б Миямото К., Паске В., Жюльен Дж., Гурдон Дж. Б. (май 2011 г.). «Ядерная полимеризация актина необходима для транскрипционного репрограммирования Oct4 ооцитами». Гены и развитие. 25 (9): 946–958. Дои:10.1101 / gad.615211. ЧВК 3084028. PMID 21536734.
- ^ Хуанг В., Гислетти С., Сайджо К., Ганди М., Ауади М., Теш Г.Дж., Чжан Д.X., Яо Дж., Член парламента Чехии, Гуд Б.Л., Розенфельд М.Г., Glass CK (февраль 2011 г.). «Коронин 2A опосредует актин-зависимую дерепрессию генов воспалительной реакции». Природа. 470 (7334): 414–418. Bibcode:2011Натура.470..414H. Дои:10.1038 / природа09703. ЧВК 3464905. PMID 21331046.
- ^ Миямото К., Гурдон Дж. Б. (сентябрь 2011 г.). «Ядерный актин и активация транскрипции». Коммуникативная и интегративная биология. 4 (5): 582–583. Дои:10.4161 / cib.16491. ЧВК 3204135. PMID 22046469.
- ^ Chuang CH, Carpenter AE, Fuchsova B, Johnson T., de Lanerolle P, Belmont AS (апрель 2006 г.). «Дальнее направленное движение интерфазного участка хромосомы». Текущая биология. 16 (8): 825–831. Дои:10.1016 / j.cub.2006.03.059. PMID 16631592. S2CID 1191289.
- ^ Hofmann WA, Vargas GM, Ramchandran R, Stojiljkovic L, Goodrich JA, de Lanerolle P (ноябрь 2006 г.). «Ядерный миозин I необходим для образования первой фосфодиэфирной связи во время инициации транскрипции РНК-полимеразой II». Журнал клеточной биохимии. 99 (4): 1001–1009. Дои:10.1002 / jcb.21035. PMID 16960872. S2CID 39237955.
- ^ Олсон Э. Н., Нордхайм А (май 2010 г.). «Связывание динамики актина и транскрипции генов для управления подвижными функциями клеток». Обзоры природы Молекулярная клеточная биология. 11 (5): 353–365. Дои:10.1038 / nrm2890. ЧВК 3073350. PMID 20414257.
- ^ Miralles F, Posern G, Zaromytidou AI, Treisman R (май 2003 г.). «Динамика актина регулирует активность SRF, регулируя его коактиватор MAL». Клетка. 113 (3): 329–342. CiteSeerX 10.1.1.327.7451. Дои:10.1016 / s0092-8674 (03) 00278-2. PMID 12732141. S2CID 17209744.
- ^ Вартиайнен МК (июнь 2008 г.). «Динамика ядерного актина - от формы к функции». Письма FEBS. 582 (14): 2033–2040. Дои:10.1016 / j.febslet.2008.04.010. PMID 18423404. S2CID 35474838.
- ^ Knöll B (июнь 2010 г.). «Актин-опосредованная экспрессия гена в нейронах: связь MRTF-SRF». Биологическая химия. 391 (6): 591–597. Дои:10.1515 / BC.2010.061. PMID 20370316. S2CID 36373214.
- ^ Tsopoulidis N, Kaw S, Laketa V, Kutscheidt S, Baarlink C, Stolp B, Grosse R, Fackler OT (январь 2019 г.). «Формирование ядерной актиновой сети, инициируемое Т-клеточным рецептором, управляет эффекторными функциями CD4 + Т-клеток». Sci Immunol. 4 (31): eaav1987. Дои:10.1126 / sciimmunol.aav1987. PMID 30610013.
- ^ а б Купер, Джеффри М. (2000). «Актин, миозин и движение клеток». Клетка (2-е изд.). Sinauer Associates. ISBN 978-0-87893-106-4.
- ^ de Luna AB, Staff VV, López-Sendón J, Attie F, Ezquerra EA (2003). Cardiología clínica. Elsevier España. ISBN 978-84-458-1179-5.
- ^ а б Dominiczak MH, Baynes J (2005). Bioquimica Medica: при получении консультации для студентов (Испанский ред.). Elsevier Espana. ISBN 978-84-8174-866-6.
- ^ Фудзивара К., Портер М.Э., Поллард Т.Д. (октябрь 1978 г.). «Локализация альфа-актинина в борозде дробления при цитокинезе». Журнал клеточной биологии. 79 (1): 268–275. Дои:10.1083 / jcb.79.1.268. ЧВК 2110217. PMID 359574.
- ^ Пелхэм Р.Дж., Чанг Ф. (сентябрь 2002 г.). «Динамика актина в сократительном кольце во время цитокинеза у делящихся дрожжей». Природа. 419 (6902): 82–86. Bibcode:2002Натура.419 ... 82П. Дои:10.1038 / природа00999. PMID 12214236. S2CID 4389564.
- ^ Машима Т., Наито М., Ногучи К., Миллер Д.К., Николсон Д.В., Цуруо Т. (март 1997 г.). «Расщепление актина СРР-32 / апопаином во время развития апоптоза». Онкоген. 14 (9): 1007–1012. Дои:10.1038 / sj.onc.1200919. PMID 9070648.
- ^ Ван К.К. (январь 2000 г.). «Кальпаин и каспасе: можете ли вы отличить?». Тенденции в неврологии. 23 (1): 20–26. Дои:10.1016 / S0166-2236 (99) 01479-4. PMID 10631785. S2CID 17571984.
- ^ Вилла PG, Хензель В.Дж., Сенсенбреннер М., Хендерсон С.Е., Петтманн Б. (март 1998 г.). «Ингибиторы кальпаина, но не ингибиторы каспаз, предотвращают протеолиз актина и фрагментацию ДНК во время апоптоза». Журнал клеточной науки. 111 (Пт 6): 713–722. PMID 9472000.
- ^ Хуот Дж., Хоул Ф., Руссо С., Дешеснес Р.Г., Шах Г.М., Ландри Дж. (Ноябрь 1998 г.). «SAPK2 / p38-зависимая реорганизация F-актина регулирует ранние мембранные пузыри во время стресс-индуцированного апоптоза». Журнал клеточной биологии. 143 (5): 1361–1373. Дои:10.1083 / jcb.143.5.1361. ЧВК 2133090. PMID 9832563.
- ^ Адамс К.Л., Нельсон В.Дж., Смит С.Дж. (декабрь 1996 г.). «Количественный анализ реорганизации кадгерин-катенин-актин при развитии клеточно-клеточной адгезии». Журнал клеточной биологии. 135 (6, часть 2): 1899–1911. Дои:10.1083 / jcb.135.6.1899. ЧВК 2133977. PMID 8991100.
- ^ Витке В., Шлейхер М., Ноегель А.А. (январь 1992 г.). «Избыточность в системе микрофиламентов: аномальное развитие клеток Dictyostelium, лишенных двух сшивающих белков F-актина». Клетка. 68 (1): 53–62. Дои:10.1016 / 0092-8674 (92) 90205-Q. PMID 1732064. S2CID 37569656.
- ^ Фернандес-Валле С., Горман Д., Гомес А.М., Бунге МБ (январь 1997 г.). «Актин играет роль как в изменениях формы клеток, так и в экспрессии генов, связанных с миелинизацией шванновских клеток». Журнал неврологии. 17 (1): 241–250. Дои:10.1523 / JNEUROSCI.17-01-00241.1997. ЧВК 6793673. PMID 8987752.
- ^ Волыняк MJ, Sundstrom P (октябрь 2007 г.). «Роль динамики цитоскелета актина в активации пути циклического АМФ и экспрессии гена HWP1 у Candida albicans». Эукариотическая клетка. 6 (10): 1824–1840. Дои:10.1128 / EC.00188-07. ЧВК 2043390. PMID 17715368.
- ^ Танака Х., Игучи Н., Эгидио де Карвалью К., Тадокоро Й., Йомогида К., Нишимуне Й. (август 2003 г.). «Новые актин-подобные белки T-ACTIN 1 и T-ACTIN 2 по-разному экспрессируются в цитоплазме и ядре гаплоидных зародышевых клеток мыши». Биология размножения. 69 (2): 475–482. Дои:10.1095 / биолрепрод.103.015867. PMID 12672658.
- ^ Цзян Ю.В., Стиллман ди-джей (март 1996 г.). «Эпигенетические эффекты на транскрипцию дрожжей, вызванные мутациями в связанном с актином белке, присутствующем в ядре». Гены и развитие. 10 (5): 604–619. Дои:10.1101 / gad.10.5.604. PMID 8598290.
- ^ Усадьба У, Качар Б (декабрь 2008 г.). «Динамическая регуляция длины сенсорных стереоцилий». Семинары по клеточной биологии и биологии развития. 19 (6): 502–510. Дои:10.1016 / j.semcdb.2008.07.006. ЧВК 2650238. PMID 18692583.
- ^ Рзадзинская А.К., Шнайдер М.Э., Дэвис К., Риордан Г.П., Качар Б. (март 2004 г.). «Молекулярная беговая дорожка актина и миозины поддерживают функциональную архитектуру стереоцилий и самообновление». Журнал клеточной биологии. 164 (6): 887–897. Дои:10.1083 / jcb.200310055. ЧВК 2172292. PMID 15024034.
- ^ Сюй Дж., Ван Кеймеулен А., Вакида Н.М., Карлтон П., Бернс М.В., Борн Х.Р. (май 2007 г.). «Полярность показывает внутреннюю хиральность клетки». Труды Национальной академии наук Соединенных Штатов Америки. 104 (22): 9296–9300. Bibcode:2007PNAS..104.9296X. Дои:10.1073 / pnas.0703153104. ЧВК 1890488. PMID 17517645.
- ^ Тамада А., Кавасе С., Мураками Ф., Камигучи Х. (февраль 2010 г.). «Автономное правостороннее вращение филоподий конуса роста приводит в движение нейриты». Журнал клеточной биологии. 188 (3): 429–441. Дои:10.1083 / jcb.200906043. ЧВК 2819689. PMID 20123994.
- ^ Ван Л.К., Рональдсон К., Парк М., Тейлор Дж., Чжан Й., Гимбл Дж. М., Вунджак-Новакович Дж. (Июль 2011 г.). «Клетки млекопитающих с микропроцессором демонстрируют фенотип-специфичную лево-правую асимметрию». Труды Национальной академии наук Соединенных Штатов Америки. 108 (30): 12295–12300. Bibcode:2011PNAS..10812295W. Дои:10.1073 / pnas.1103834108. ЧВК 3145729. PMID 21709270.
- ^ Су А.И., Уилтшир Т., Баталов С., Лапп Х., Чинг К.А., Блок D, Чжан Дж., Соден Р., Хаякава М., Крейман Г., Кук М.П., Уокер Дж. Р., Хогенеш Дж. Б. (апрель 2004 г.). "Атлас генов транскриптомов, кодирующих белки человека и мыши". Труды Национальной академии наук Соединенных Штатов Америки. 101 (16): 6062–6067. Bibcode:2004ПНАС..101.6062С. Дои:10.1073 / pnas.0400782101. ЧВК 395923. PMID 15075390.
- ^ а б "ACTS_HUMAN". P68133. Консорциум UniProt. В архиве из оригинала от 05.11.2012. Получено 2013-01-21.
- ^ а б Купание FS, Rommelaere H, Machesky LM (2007). «Фенотипы связанных с миопатией мутантов актина в дифференцированных мышечных трубках C2C12». BMC Cell Biology. 8 (1): 2. Дои:10.1186/1471-2121-8-2. ЧВК 1779783. PMID 17227580.
- ^ Kaindl AM, Rüschendorf F, Krause S, Goebel HH, Koehler K, Becker C, Pongratz D, Müller-Höcker J, Nürnberg P, Stoltenburg-Didinger G, Lochmüller H, Huebner A (ноябрь 2004 г.). «Миссенс-мутации ACTA1 вызывают доминантную врожденную миопатию с ядрами». Журнал медицинской генетики. 41 (11): 842–848. Дои:10.1136 / jmg.2004.020271. ЧВК 1735626. PMID 15520409.
- ^ Sparrow JC, Nowak KJ, Durling HJ, Beggs AH, Wallgren-Pettersson C, Romero N, Nonaka I, Laing NG (сентябрь 2003 г.). «Заболевание мышц, вызванное мутациями в гене альфа-актина скелетных мышц (ACTA1)». Нервно-мышечные расстройства. 13 (7–8): 519–531. Дои:10.1016 / S0960-8966 (03) 00101-9. PMID 12921789. S2CID 20716.
- ^ Норт К., Райан М. М. (2002). «Немалиновая миопатия». В Pagon RA, Bird TD, Dolan CR, Stephens K, Adam MP (ред.). GeneReviews [Интернет]. Сиэтл (Вашингтон): Вашингтонский университет, Сиэтл. В архиве из оригинала от 18.01.2017.
- ^ Ильковски Б., Новак К.Дж., Домазетовска А., Максвелл А.Л., Клемент С., Дэвис К.Э., Лейнг Н.Г., Норт К.Н., Купер СТ (август 2004 г.). «Доказательства доминантно-негативного эффекта при немалиновой миопатии ACTA1, вызванного аномальной укладкой, агрегацией и измененной полимеризацией мутантных изоформ актина». Молекулярная генетика человека. 13 (16): 1727–1743. Дои:10,1093 / hmg / ddh185. PMID 15198992.
- ^ Кларк Н.Ф., Ильковски Б., Купер С., Валова В.А., Робинсон П.Дж., Нонака И., Фенг Дж.Дж., Марстон С., Норт К. (июнь 2007 г.). «Патогенез ACTA1-связанной врожденной диспропорции типа волокон». Анналы неврологии. 61 (6): 552–561. Дои:10.1002 / ana.21112. PMID 17387733. S2CID 11746835.
- ^ а б Miwa T, Manabe Y, Kurokawa K, Kamada S, Kanda N, Bruns G, Ueyama H, Kakunaga T. (июнь 1991 г.). «Структура, расположение хромосом и экспрессия гена гамма-актина гладких мышц человека (кишечного типа): эволюция шести генов актина человека». Молекулярная и клеточная биология. 11 (6): 3296–3306. Дои:10.1128 / mcb.11.6.3296. ЧВК 360182. PMID 1710027.
- ^ Уотсон МБ, Линд М.Дж., Смит Л., Дрю П.Дж., Коуквелл Л. (2007). «Анализ экспрессии микроматрицы выявляет гены, связанные с устойчивостью к цисплатину in vitro в модели клеточной линии». Acta Oncologica. 46 (5): 651–658. Дои:10.1080/02841860601156157. PMID 17562441. S2CID 7163200.
- ^ Гуо, округ Колумбия, Панну Х, Тран-Фадулу В., Папке С.Л., Ю РК, Авидан Н., Буржуа С., Эстрера А.Л., Сафи Х.Дж., Спаркс Е, Амор Д., Адес Л., МакКоннелл В., Уиллоуби К.Э., Абуэло Д., Виллинг М., Льюис Р.А., Ким Д.Х., Шерер С., Тунг П.П., Ан С., Буя Л.М., Раман С.С., Шете С.С., Милевич Д.М. (декабрь 2007 г.). «Мутации в альфа-актине гладких мышц (ACTA2) приводят к аневризмам и расслоениям грудной аорты». Природа Генетика. 39 (12): 1488–1493. Дои:10,1038 / нг.2007,6. PMID 17994018. S2CID 62785801.
- ^ Guo DC, Papke CL, Tran-Fadulu V, Regalado ES, Avidan N, Johnson RJ, Kim DH, Pannu H, Willing MC, Sparks E, Pyeritz RE, Singh MN, Dalman RL, Grotta JC, Marian AJ, Boerwinkle EA, Frazier LQ, LeMaire SA, Coselli JS, Estrera AL, Safi HJ, Veeraraghavan S, Muzny DM, Wheeler DA, Willerson JT, Yu RK, Shete SS, Scherer SE, Raman CS, Buja LM, Milewicz DM (май 2009 г.). «Мутации в альфа-актине гладких мышц (ACTA2) вызывают ишемическую болезнь сердца, инсульт и болезнь Моямоя, наряду с заболеванием грудной аорты». Американский журнал генетики человека. 84 (5): 617–627. Дои:10.1016 / j.ajhg.2009.04.007. ЧВК 2680995. PMID 19409525.
- ^ Акполат Н., Яхси С., Годекмердан А., Ялниз М., Демирбаг К. (сентябрь 2005 г.). «Значение альфа-SMA в оценке тяжести фиброза печени при инфекции гепатита B и развитии цирроза: гистопатологическое и иммуногистохимическое исследование». Гистопатология. 47 (3): 276–280. Дои:10.1111 / j.1365-2559.2005.02226.x. PMID 16115228. S2CID 23800095.
- ^ Хамада Х., Петрино М.Г., Какунага Т. (октябрь 1982 г.). «Молекулярная структура и эволюционное происхождение гена актина сердечной мышцы человека». Труды Национальной академии наук Соединенных Штатов Америки. 79 (19): 5901–5905. Bibcode:1982PNAS ... 79.5901H. Дои:10.1073 / пнас.79.19.5901. ЧВК 347018. PMID 6310553.
- ^ а б Olson TM, Michels VV, Thibodeau SN, Tai YS, Keating MT (май 1998 г.). «Мутации актина при дилатационной кардиомиопатии, наследственной форме сердечной недостаточности». Наука. 280 (5364): 750–752. Bibcode:1998Sci ... 280..750O. Дои:10.1126 / science.280.5364.750. PMID 9563954. S2CID 26971894.
- ^ Ся XG, Чжоу Х., Сампер Э., Мелов С., Сюй З. (янв 2006). «Pol II-экспрессируемая кшРНК подавляет экспрессию гена Sod2 и вызывает фенотип нокаута гена у мышей». PLOS Genetics. 2 (1): e10. Дои:10.1371 / journal.pgen.0020010. ЧВК 1358942. PMID 16450009.
- ^ Онлайн-менделевское наследование в человеке (OMIM): Актин, альфа, сердечная мышца; ACTC1 - 102540
- ^ Матссон Х., Исон Дж., Буквалтер С.С., Клар Дж., Густавссон П., Суннегард Дж., Энелл Х, Йонзон А., Виккула М., Гутьеррес I, Гранадос-Риверон Дж., Поуп М., Бу'лок Ф, Кокс Дж., Робинсон Т. Э., Песня F, Brook DJ, Marston S, Trybus KM, Dahl N (январь 2008 г.). «Мутации альфа-сердечного актина вызывают дефекты межпредсердной перегородки». Молекулярная генетика человека. 17 (2): 256–265. Дои:10,1093 / hmg / ddm302. PMID 17947298.
- ^ Кабаева, Жылдыз (11 ноября 2002 г.). Генетический анализ при гипертрофической кардиомиопатии (Тезис). Дои:10.18452/14800.
- ^ Olson TM, Doan TP, Kishimoto NY, Whitby FG, Ackerman MJ, Fananapazir L (сентябрь 2000 г.). «Унаследованные и de novo мутации в гене сердечного актина вызывают гипертрофическую кардиомиопатию». Журнал молекулярной и клеточной кардиологии. 32 (9): 1687–1694. Дои:10.1006 / jmcc.2000.1204. PMID 10966831.
- ^ Рамирес, Карлос Дарио; Падрон, Рауль (2004). "Кардиомиопатия гипертрофическая знакомая: гены, mutaciones y modelos animales. Revisión" [Семейная гипертрофическая кардиомиопатия: гены, мутации и животные модели. Обзор]. Investigación Clínica (на испанском). 45 (1): 69–100.
- ^ Каски Дж. П., Сиррис П., Берч М., Томе-Эстебан М. Т., Фентон М., Кристиансен М., Андерсен П. С., Себир Н., Эшворт М., Динфилд Дж. Э., Маккенна В. Дж., Эллиотт П. М. (ноябрь 2008 г.). «Идиопатическая рестриктивная кардиомиопатия у детей вызвана мутациями в генах сердечного саркомера». Сердце. 94 (11): 1478–1484. Дои:10.1136 / час.2007.134684. PMID 18467357. S2CID 44257334.
- ^ Пиготт Т.Дж., Джефферсон Д. (1991). «Идиопатический паралич общего малоберцового нерва - обзор тринадцати случаев». Британский журнал нейрохирургии. 5 (1): 7–11. Дои:10.3109/02688699108998440. PMID 1850600.
- ^ «Ген: ACTB». AceView. Национальный центр биотехнологической информации США (NCBI). В архиве из оригинала 18.06.2013. Получено 2013-01-21.
- ^ Chang KW, Yang PY, Lai HY, Yeh TS, Chen TC, Yeh CT (сентябрь 2006 г.). «Идентификация новой изоформы актина при гепатоцеллюлярной карциноме». Гепатологические исследования. 36 (1): 33–39. Дои:10.1016 / j.hepres.2006.05.003. PMID 16824795.
- ^ Уильямс К.Л., Рахимтула М., Меаров К.М. (2005). «Hsp27 и рост аксонов во взрослых сенсорных нейронах in vitro». BMC Neuroscience. 6 (1): 24. Дои:10.1186/1471-2202-6-24. ЧВК 1087488. PMID 15819993.
- ^ «Опухоли мягких тканей: перицитома с t (7; 12)». Атлас генетики и цитогенетики в онкологии и гематологии. Университетская клиника Пуатье. В архиве из оригинала 30.12.2008. Получено 2013-01-21.
- ^ Procaccio V, Salazar G, Ono S, Styers ML, Gearing M, Davila A, Jimenez R, Juncos J, Gutekunst CA, Meroni G, Fontanella B, Sontag E, Sontag JM, Faundez V, Wainer BH (июнь 2006 г.). «Мутация бета-актина, которая изменяет динамику деполимеризации, связана с аутосомно-доминантными пороками развития, глухотой и дистонией». Американский журнал генетики человека. 78 (6): 947–960. Дои:10.1086/504271. ЧВК 1474101. PMID 16685646.
- ^ Нунои Х., Ямадзаки Т., Цучия Х., Като С., Малек Х.Л., Мацуда И., Канегасаки С. (июль 1999 г.). «Гетерозиготная мутация бета-актина, связанная с дисфункцией нейтрофилов и рецидивирующей инфекцией». Труды Национальной академии наук Соединенных Штатов Америки. 96 (15): 8693–8698. Bibcode:1999PNAS ... 96.8693N. Дои:10.1073 / пнас.96.15.8693. ЧВК 17578. PMID 10411937.
- ^ а б «Ген: ACTG1». AceView. Национальный центр биотехнологической информации США (NCBI). В архиве из оригинала 18.06.2013. Получено 2013-01-21.
- ^ Эрба Х.П., Ганнинг П., Кедес Л. (июль 1986 г.). «Нуклеотидная последовательность мРНК гамма-цитоскелета актина человека: аномальная эволюция немышечных генов актина позвоночных». Исследования нуклеиновых кислот. 14 (13): 5275–5294. Дои:10.1093 / nar / 14.13.5275. ЧВК 311540. PMID 3737401.
- ^ Брайан К.Е., Рубинштейн П.А. (июль 2009 г.). «Аллель-специфические эффекты мутаций гамма-актина глухоты человека (DFNA20 / 26) на взаимодействие актин / кофилин». Журнал биологической химии. 284 (27): 18260–18269. Дои:10.1074 / jbc.M109.015818. ЧВК 2709362. PMID 19419963.
- ^ Зоннеманн К.Дж., Фитцсимонс Д.П., Патель-младший, Лю Й., Шнайдер М.Ф., Мосс Р.Л., Эрвасти Дж.М. (сентябрь 2006 г.). «Цитоплазматический гамма-актин не требуется для развития скелетных мышц, но его отсутствие приводит к прогрессирующей миопатии». Клетка развития. 11 (3): 387–397. Дои:10.1016 / j.devcel.2006.07.001. PMID 16950128.
- ^ Gouin, E .; Gantelet, H .; Egile, C .; Lasa, I .; Ohayon, H .; Вильерс, В .; Gounon, P .; Sansonetti, P.J .; Коссарт, П. (1 июня 1999 г.). «Сравнительное исследование актиновой подвижности патогенных бактерий Listeria monocytogenes, Shigella flexneri и Rickettsia conorii». Журнал клеточной науки. 112 (11): 1697–1708. PMID 10318762.
- ^ Lambrechts A, Gevaert K, Cossart P, Vandekerckhove J, Van Troys M (май 2008 г.). "Кометные хвосты Listeria: действующий механизм подвижности на основе актина". Тенденции в клеточной биологии. 18 (5): 220–227. Дои:10.1016 / j.tcb.2008.03.001. PMID 18396046.
- ^ Гуин Э., Велч, доктор медицины, Коссарт П. (февраль 2005 г.). «Актиновая подвижность внутриклеточных патогенов». Текущее мнение в микробиологии. 8 (1): 35–45. Дои:10.1016 / j.mib.2004.12.013. PMID 15694855.
- ^ Parks QM, Young RL, Poch KR, Malcolm KC, Vasil ML, Nick JA (апрель 2009 г.). «Повышение нейтрофилов в развитии биопленки Pseudomonas aeruginosa: человеческий F-актин и ДНК в качестве мишеней для терапии». Журнал медицинской микробиологии. 58 (Pt 4): 492–502. Дои:10.1099 / jmm.0.005728-0. ЧВК 2677169. PMID 19273646.
- ^ Лю Ю., Белкина Н.В., Шоу С. (2009). «ВИЧ-инфекция Т-клеток: входящий и выходной актин». Научная сигнализация. 2 (66): pe23. Дои:10.1126 / scisignal.266pe23. PMID 19366992. S2CID 30259258.
- ^ Machesky LM, Tang HR (июль 2009 г.). «Актиновые протрузии: промоторы или ингибиторы инвазии рака?». Раковая клетка. 16 (1): 5–7. Дои:10.1016 / j.ccr.2009.06.009. PMID 19573806.
- ^ Эриксон HP (июль 2007 г.). «Эволюция цитоскелета». BioEssays. 29 (7): 668–677. Дои:10.1002 / bies.20601. ЧВК 2630885. PMID 17563102.
- ^ Гардинер Дж., Макги П., Общий Р., Марк Дж. (2008). «Являются ли гистоны, тубулин и актин производными от общего предкового белка?». Протоплазма. 233 (1–2): 1–5. Дои:10.1007 / s00709-008-0305-z. PMID 18615236. S2CID 21765920.
- ^ Галлетта Б.Дж., Купер Д.А. (февраль 2009 г.). «Актин и эндоцитоз: механизмы и филогения». Текущее мнение в области клеточной биологии. 21 (1): 20–27. Дои:10.1016 / j.ceb.2009.01.006. ЧВК 2670849. PMID 19186047.
- ^ Попп Д., Нарита А., Маэда К., Фудзисава Т., Гошдастидер Ю., Иваса М., Маеда Й., Робинсон Р.С. (май 2010 г.). «Структура, организация и динамика волокон в листах MreB». Журнал биологической химии. 285 (21): 15858–15865. Дои:10.1074 / jbc.M109.095901. ЧВК 2871453. PMID 20223832.
- ^ ван ден Энт Ф, Амос Л.А., Лёве Дж. (сентябрь 2001 г.). «Прокариотическое происхождение актинового цитоскелета». Природа. 413 (6851): 39–44. Bibcode:2001 Натур.413 ... 39 В. Дои:10.1038/35092500. PMID 11544518. S2CID 4427828.
- ^ Карбаллидо-Лопес Р. (декабрь 2006 г.). «Бактериальный актиноподобный цитоскелет». Обзоры микробиологии и молекулярной биологии. 70 (4): 888–909. Дои:10.1128 / MMBR.00014-06. ЧВК 1698507. PMID 17158703.
- ^ Попп Д., Сюй В., Нарита А., Брзоска А.Дж., Скуррей Р.А., Ферт Н., Гошдастидер Ю., Гошдастидер Ю., Маеда Ю., Робинсон Р.С., Шумахер М.А. (март 2010 г.). «Структура и динамика филаментов актин-подобного белка ParM pSK41: значение для сегрегации плазмидной ДНК». Журнал биологической химии. 285 (13): 10130–10140. Дои:10.1074 / jbc.M109.071613. ЧВК 2843175. PMID 20106979.
- ^ Попп Д., Нарита А., Гошдастидер У., Маеда К., Маэда Й, Ода Т., Фудзисава Т., Ониши Х., Ито К., Робинсон Р.К. (апрель 2010 г.). «Полимерные структуры и динамические свойства бактериального актина AlfA». Журнал молекулярной биологии. 397 (4): 1031–1041. Дои:10.1016 / j.jmb.2010.02.010. PMID 20156449.
- ^ Попп Д., Нарита А., Ли Л. Дж., Гошдастидер Ю., Сюэ Б., Сринивасан Р., Баласубраманиан М.К., Танака Т., Робинсон Р.К. (июнь 2012 г.). «Новая актиноподобная структура филаментов из Clostridium tetani». Журнал биологической химии. 287 (25): 21121–21129. Дои:10.1074 / jbc.M112.341016. ЧВК 3375535. PMID 22514279.
- ^ Хесс Х, Клемменс Дж, Цин Д., Ховард Дж, Фогель V (2001). «Управляемые светом молекулярные челноки, сделанные из моторных белков, переносящие грузы на инженерных поверхностях». Нано буквы. 1 (5): 235–239. Bibcode:2001NanoL ... 1..235H. Дои:10.1021 / nl015521e.
- ^ Манссон А., Сундберг М., Банк Р., Балаз М., Николлс И.А., Омлинг П., Тегенфельдт Дж. О., Тагеруд С., Монтелиус Л. (2005). «Молекулярные двигатели на основе актина для грузовых перевозок в нанотехнологиях - возможности и проблемы». IEEE Transactions по расширенной упаковке. 28 (4): 547–555. Дои:10.1109 / TADVP.2005.858309. S2CID 33608087.
- ^ Шарма С., Ханукоглу I (2019). «Картирование участков локализации эпителиального натриевого канала (ENaC) и CFTR в сегментах придатка яичка млекопитающих». Журнал молекулярной гистологии. 50 (2): 141–154. Дои:10.1007 / s10735-019-09813-3. PMID 30659401. S2CID 58026884.
- ^ Вандесомпеле Дж., Де Претер К., Паттин Ф., Поппе Б., Ван Рой Н., Де Паепе А., Спелеман Ф. (июнь 2002 г.). «Точная нормализация количественных данных ОТ-ПЦР в реальном времени путем геометрического усреднения нескольких генов внутреннего контроля». Геномная биология. 3 (7): ИССЛЕДОВАНИЕ0034. Дои:10.1186 / gb-2002-3-7-research0034. ЧВК 126239. PMID 12184808.
- ^ Селви С., Томпсон Э. У., Маттей К., Ли Р. А., Ирвинг М. Г., Гриффитс Л. Р. (октябрь 2001 г.). «Бета-актин - неподходящий внутренний контроль для ОТ-ПЦР». Молекулярные и клеточные зонды. 15 (5): 307–311. Дои:10.1006 / mcpr.2001.0376. PMID 11735303.
- ^ Мукаи К., Шоллмейер СП, Розай Дж. (Январь 1981 г.). «Иммуногистохимическая локализация актина: применение в хирургической патологии». Американский журнал хирургической патологии. 5 (1): 91–97. Дои:10.1097/00000478-198101000-00013. PMID 7018275.
- ^ Хаддад Ф., Рой Р.Р., Чжун Х., Эджертон В.Р., Болдуин К.М. (август 2003 г.). «Атрофические реакции на мышечную неактивность. II. Молекулярные маркеры белкового дефицита». Журнал прикладной физиологии. 95 (2): 791–802. Дои:10.1152 / japplphysiol.01113.2002. PMID 12716877. S2CID 8268572.
- ^ Hocquette JF, Lehnert S, Barendse W, Cassar-Malek I, Picard B (2006). «Современные достижения в протеомном анализе и его использовании для определения качества мяса птицы». Журнал World's Poultry Science Journal. 62 (1): 123–130. Дои:10.1079 / WPS200589. S2CID 86189373.
- ^ Нолле Л. (2004). «Методы и инструменты прикладного анализа пищевых продуктов». Справочник по анализу пищевых продуктов. 3 (2-е изд.). Нью-Йорк, Нью-Йорк: Марсель Деккер. С. 1741–2226. ISBN 978-0-8247-5039-8.
внешняя ссылка
- Методы окрашивания актином (окрашивание живых и фиксированных клеток)
- Ресурс Eukaryotic Linear Motif класс мотива LIG_Actin_RPEL_3
- Ресурс Eukaryotic Linear Motif класс мотива LIG_Actin_WH2_1
- Ресурс Eukaryotic Linear Motif класс мотива LIG_Actin_WH2_2
- Трехмерные макромолекулярные структуры актиновых филаментов из EM Data Bank (EMDB)