Аксон - Axon
| Аксон | |
|---|---|
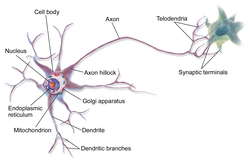 Аксон многополярного нейрона | |
| Идентификаторы | |
| MeSH | D001369 |
| Анатомическая терминология | |
An аксон (от греч. ἄξων áxōn, ось), или нервное волокно (или же нерв волокно: видеть орфографические различия ), представляет собой длинный тонкий выступ нервной клетки, или нейрон, у позвоночных, который обычно проводит электрические импульсы, известные как потенциалы действия подальше от тело нервной клетки. Функция аксона - передавать информацию различным нейронам, мышцам и железам. В определенных сенсорные нейроны (псевдоуниполярные нейроны ), например аксоны прикосновения и тепла, аксоны называются афферентные нервные волокна и электрический импульс проходит по ним от периферия к телу клетки и от тела клетки к спинному мозгу по другой ветви того же аксона. Дисфункция аксонов является причиной многих наследственных и приобретенных неврологических расстройств, которые могут поражать как периферические, так и центральные нейроны. Нервные волокна классифицированный на три типа - нервные волокна группы А, нервные волокна группы B, и нервные волокна группы C. Группы A и B являются миелинизированный, и группа C немиелинизированы. Эти группы включают как сенсорные волокна, так и двигательные волокна. Другая классификация группирует только сенсорные волокна как Тип I, Тип II, Тип III и Тип IV.
Аксон - это один из двух типов цитоплазматический выступы из тела клетки нейрона; другой тип - это дендрит. Аксоны отличаются от дендритов несколькими особенностями, включая форму (дендриты часто сужаются, в то время как аксоны обычно имеют постоянный радиус), длину (дендриты ограничены небольшой областью вокруг тела клетки, в то время как аксоны могут быть намного длиннее) и функцию (дендриты получают сигналы, тогда как аксоны передают их). Некоторые типы нейронов не имеют аксона и передают сигналы от своих дендритов. У некоторых видов аксоны могут исходить из дендритов, известных как дендриты, несущие аксоны.[1] Ни у одного нейрона никогда не бывает более одного аксона; однако у беспозвоночных, таких как насекомые или пиявки, аксон иногда состоит из нескольких областей, которые функционируют более или менее независимо друг от друга.[2]
Аксоны покрыты мембраной, известной как аксолемма; цитоплазма аксона называется аксоплазма. Большинство аксонов разветвляются, в некоторых случаях очень обильно. Концевые ветви аксона называются телодендрия. Распухший конец телодендрона известен как терминал аксона который присоединяется к дендрону или телу клетки другого нейрона, образуя синаптическое соединение. Аксоны контактируют с другими клетками - обычно с другими нейронами, но иногда с клетками мышц или желез - в соединениях, называемых синапсы. В некоторых случаях аксон одного нейрона может образовывать синапс с дендритами того же нейрона, что приводит к autapse. В синапсе мембрана аксона близко примыкает к мембране клетки-мишени, а специальные молекулярные структуры служат для передачи электрических или электрохимических сигналов через промежуток. Некоторые синаптические соединения появляются вдоль аксона по мере его расширения - они называются мимоходом («попутно») синапсов и может быть сотнями или даже тысячами вдоль одного аксона.[3] Другие синапсы выглядят как терминалы на концах аксональных ветвей.
Отдельный аксон со всеми его ветвями, взятыми вместе, может иннервировать несколько частей мозга и генерируют тысячи синаптических окончаний. Связка аксонов делает нервный тракт в Центральная нервная система,[4] и пучок в периферическая нервная система. В плацентарные млекопитающие самый большой белое вещество тракт в головном мозге мозолистое тело, образованный примерно из 200 миллионов аксонов в человеческий мозг.[4]
Анатомия
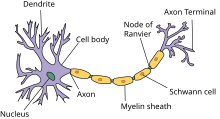

Аксоны - это основные линии передачи нервная система, и как пучки они образуют нервы. Некоторые аксоны могут достигать одного метра и более, а другие - всего лишь один миллиметр. Самые длинные аксоны в человеческом теле - аксоны седалищный нерв, которые идут от основания спинной мозг к большому пальцу каждой стопы. Диаметр аксонов также варьируется. Большинство отдельных аксонов микроскопические в диаметре (обычно около одного микрометр (мкм) в поперечнике). Самые большие аксоны млекопитающих могут достигать в диаметре до 20 мкм. В гигантский аксон кальмара, который специализируется на очень быстром проведении сигналов, близок к 1 миллиметр в диаметре, размером с грифель карандаша. Количество аксональных телодендрий (разветвленных структур на конце аксона) также может отличаться от одного нервного волокна к другому. Аксоны в Центральная нервная система (ЦНС) обычно показывают несколько телодендрий с множеством синаптических конечных точек. Для сравнения: гранулярная клетка мозжечка аксон характеризуется одним Т-образным узлом ветви, от которого два параллельные волокна продлевать. Продуманное ветвление позволяет одновременно передавать сообщения большому количеству целевых нейронов в одной области мозга.
Есть два типа аксонов в нервная система: миелинизированный и немиелинизированный аксоны.[5] Миелин представляет собой слой изолирующего жирового вещества, который образован двумя типами глиальные клетки Клетки Шванна и олигодендроциты. в периферическая нервная система Шванновские клетки образуют миелиновую оболочку миелинизированного аксона. в Центральная нервная система олигодендроциты образуют изолирующий миелин. Вдоль миелинизированных нервных волокон пробелы в миелиновой оболочке, известные как узлы Ранвье происходят через равные промежутки времени. Миелинизация обеспечивает особенно быстрый режим распространения электрических импульсов, называемый скачкообразное проведение.
Миелинизированные аксоны из корковые нейроны образуют основную часть нервной ткани, называемой белое вещество в мозгу. Миелин придает белому цвету ткань в отличие от серое вещество коры головного мозга, содержащей тела нейрональных клеток. Аналогичное расположение можно увидеть на мозжечок. Связки миелинизированных аксонов составляют нервные пути в ЦНС. Там, где эти тракты пересекают среднюю линию мозга и соединяют противоположные области, они называются комиссур. Самый крупный из них - мозолистое тело что соединяет два полушария головного мозга, а это около 20 миллионов аксонов.[4]
Видно, что структура нейрона состоит из двух отдельных функциональных областей или компартментов - тела клетки вместе с дендритами в качестве одной области и аксональной области в качестве другой.
Аксональная область
Аксональная область или компартмент включает бугорок аксона, начальный сегмент, остальную часть аксона и телодендрии аксона, а также терминалы аксона. Он также включает миелиновую оболочку. В Тела Nissl которые продуцируют нейрональные белки, отсутствуют в аксональной области.[3] Белки, необходимые для роста аксона и удаления отходов жизнедеятельности, нуждаются в транспортном каркасе. Этот аксональный транспорт обеспечивается в аксоплазме за счет расположения микротрубочки и промежуточные нити известный как нейрофиламенты.
Аксонный бугорок

В аксональный бугорок это область, образованная клеточным телом нейрона по мере того, как она расширяется, чтобы стать аксоном. Он предшествует начальному сегменту. Полученные потенциалы действия, которые подведены в нейроне передаются на бугорок аксона для генерации потенциала действия из начального сегмента.
Начальный сегмент
В аксональный начальный сегмент (AIS) представляет собой структурно и функционально отдельный микродомен аксона.[6][7] Одна из функций начального сегмента - отделить основную часть аксона от остальной части нейрона; другая функция - помочь инициировать потенциалы действия.[8] Обе эти функции поддерживают нейрон полярность ячейки, в котором дендриты (а в некоторых случаях сома ) нейрона получают входные сигналы в базальной области, а в апикальной области аксон нейрона обеспечивает выходные сигналы.[9]
Начальный сегмент аксона немиелинизирован и содержит специализированный комплекс белков. Его длина составляет примерно от 20 до 60 мкм, и он функционирует как место инициации потенциала действия.[10][11] Как положение на аксоне, так и длина AIS могут изменяться, показывая степень пластичности, которая может точно настроить вывод нейронов.[10][12] Более длинный AIS связан с большей возбудимостью.[12] Пластичность также проявляется в способности AIS изменять свое распределение и поддерживать активность нейронных схем на постоянном уровне.[13]
AIS узкоспециализирована для быстрого проведения нервные импульсы. Это достигается за счет высокой концентрации напряжение-управляемые натриевые каналы в начальном сегменте, где возникает потенциал действия.[13] Ионные каналы сопровождаются большим количеством молекулы клеточной адгезии и каркасные белки, которые прикрепляют их к цитоскелету.[10] Взаимодействие с Анкирин Г важны, так как это главный организатор в САИ.[10]
Аксональный транспорт
В аксоплазма эквивалентен цитоплазма в клетка. Микротрубочки образуются в аксоплазме на бугорке аксона. Они расположены по длине аксона в перекрывающихся участках и все направлены в одном направлении - к окончанию аксона.[14] Об этом говорят положительные окончания микротрубочек. Такое перекрывающееся расположение обеспечивает маршруты транспортировки различных материалов из тела клетки.[14] Исследования аксоплазмы показали движение многочисленных пузырьков всех размеров, которые можно увидеть вдоль цитоскелетных филаментов - микротрубочек и нейрофиламенты, в обоих направлениях между аксоном и его окончаниями и телом клетки.
Исходящий антероградный транспорт из тела клетки по аксону переносит митохондрии и мембранные белки, необходимые для роста, к концу аксона. Входящий ретроградный транспорт переносит отходы клетки от терминала аксона к телу клетки.[15] Исходящие и входящие треки используют разные наборы моторные белки.[14] Исходящий транспорт обеспечивает кинезин, а входящий обратный трафик обеспечивается динеин. Динеин направлен на минус-конец.[15] Существует множество форм моторных белков кинезина и динеина, и считается, что каждая из них несет свой груз.[14] Исследования транспорта в аксоне привели к названию кинезина.[14]
Миелинизация


В нервной системе аксоны могут быть миелинизированный, или немиелинизированные. Это обеспечение изолирующего слоя, называемого миелиновой оболочкой. Миелиновая мембрана уникальна своим относительно высоким соотношением липидов к белку.[16]
В периферической нервной системе аксоны миелинизируются глиальные клетки известный как Клетки Шванна. В центральной нервной системе миелиновую оболочку представляют глиальные клетки другого типа, олигодендроцит. Клетки Шванна миелинизируют единственный аксон. Олигодендроцит может миелинизировать до 50 аксонов.[17]
Состав миелина у этих двух типов разный. В ЦНС основным белком миелина является протеолипидный белок, а в ПНС это основной белок миелина.
Узлы Ранвье
Узлы Ранвье (также известен как щели миелиновой оболочки) - короткие немиелинизированные сегменты миелинизированный аксон, которые находятся периодически вкраплениями между сегментами миелиновой оболочки. Следовательно, в точке узла Ранвье аксон уменьшается в диаметре.[18] Эти узлы являются областями, где могут быть созданы потенциалы действия. В скачкообразное проведение электрические токи, возникающие в каждом узле Ранвье, передаются с небольшим затуханием к следующему узлу в линии, где они остаются достаточно сильными, чтобы генерировать другой потенциал действия. Таким образом, в миелинизированном аксоне потенциалы действия эффективно «прыгают» от узла к узлу, минуя миелинизированные участки между ними, в результате чего скорость распространения намного выше, чем может выдержать даже самый быстрый немиелинизированный аксон.
Терминалы Axon
Аксон может делиться на множество ветвей, называемых телодендриями (греч. Конец дерева). В конце каждого телодендрон является аксонный терминал (также называемый синаптическим бутоном или терминальным бутоном). Терминалы Axon содержат синаптические везикулы которые хранят нейротрансмиттер для выпуска в синапс. Это делает возможными множественные синаптические связи с другими нейронами. Иногда аксон нейрона может синапсировать с дендритами того же нейрона, когда он известен как autapse.
Потенциалы действия
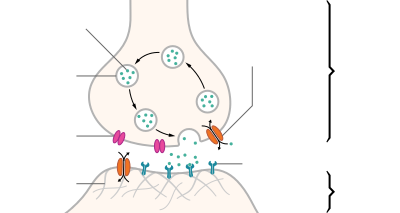
| Структура типового химический синапс |
|---|
Большинство аксонов несут сигналы в виде потенциалы действия, которые представляют собой дискретные электрохимические импульсы, которые быстро проходят по аксону, начиная с тела клетки и заканчивая в точках, где аксон производит синаптический контакт с клетками-мишенями. Определяющей характеристикой потенциала действия является то, что он действует по принципу «все или ничего» - каждый потенциал действия, который генерирует аксон, по существу имеет одинаковый размер и форму. Эта характеристика «все или ничего» позволяет передавать потенциалы действия от одного конца длинного аксона к другому без какого-либо уменьшения размера. Однако есть некоторые типы нейронов с короткими аксонами, которые несут ступенчатые электрохимические сигналы переменной амплитуды.
Когда потенциал действия достигает пресинаптического терминала, он активирует процесс синаптической передачи. Первый шаг - это быстрое открытие каналов для ионов кальция в мембране аксона, позволяя ионам кальция проходить внутрь через мембрану. Возникающее в результате повышение концентрации внутриклеточного кальция вызывает синаптические везикулы (крошечные контейнеры, окруженные липидной мембраной), заполненные нейротрансмиттер химикат, чтобы сливаться с мембраной аксона и выводить их содержимое во внеклеточное пространство. Нейромедиатор высвобождается из пресинаптического нерва через экзоцитоз. Затем химический нейротрансмиттер диффундирует к рецепторам, расположенным на мембране клетки-мишени. Нейромедиатор связывается с этими рецепторами и активирует их. В зависимости от типа активируемых рецепторов действие на клетку-мишень может заключаться в возбуждении клетки-мишени, ее подавлении или каким-либо образом изменяющем ее метаболизм. Вся эта последовательность событий часто происходит менее чем за тысячную долю секунды. После этого внутри пресинаптического терминала новый набор везикул перемещается в положение рядом с мембраной, готовых к высвобождению при достижении следующего потенциала действия. Потенциал действия - это последний электрический шаг в интеграции синаптических сообщений в масштабе нейрона.[5]

(B) Средняя и стандартная ошибка времени прохождения пика для интернейронов пирамидных клеток и предполагаемых аксонов;
(C) График разброса отношения сигнал / шум для отдельных единиц от времени пика для аксонов, пирамидных клеток (PYR) и интернейронов (INT).
Внеклеточные записи потенциал действия распространение в аксонах было продемонстрировано у свободно перемещающихся животных. В то время как внеклеточные соматические потенциалы действия использовались для изучения клеточной активности у свободно перемещающихся животных, таких как разместить клетки, аксональная активность в обоих белый и серое вещество также могут быть записаны. Внеклеточные записи распространения потенциала действия аксона отличаются от соматических потенциалов действия по трем причинам: 1. Сигнал имеет более короткую продолжительность пика и спада (~ 150 мкс), чем у пирамидных клеток (~ 500 мкс) или интернейронов (~ 250 мкс). 2. Изменение напряжения трехфазное. 3. Активность, записанная на тетроде, видна только на одном из четырех проводов записи. В записях от свободно движущихся крыс аксональные сигналы были изолированы в трактах белого вещества, включая альвеус и мозолистое тело, а также серое вещество гиппокампа.[19]
Фактически, поколение потенциалы действия in vivo носит последовательный характер, и эти последовательные всплески составляют цифровые коды в нейроны. Хотя предыдущие исследования указывают на аксональное происхождение одиночного спайка, вызванного кратковременными импульсами, физиологические сигналы in vivo запускают инициирование последовательных спайков в телах клеток нейронов.[20][21]
В дополнение к распространению потенциалов действия к окончанию аксона, аксон способен усиливать потенциалы действия, что гарантирует безопасное распространение последовательных потенциалов действия к окончанию аксона. Что касается молекулярных механизмов, напряжение-управляемые натриевые каналы в аксонах обладают нижними порог и короче период отражения в ответ на кратковременные импульсы.[22]
Развитие и рост
Разработка
Развитие аксона к его цели - один из шести основных этапов в общей развитие нервной системы.[23] Исследования проведены на культивированных гиппокамп нейроны предполагают, что нейроны изначально производят несколько невриты которые эквивалентны, но только одному из этих нейритов суждено стать аксоном.[24] Неясно, предшествует ли спецификация аксона удлинению аксона или наоборот,[25] хотя недавние свидетельства указывают на последнее. Если разрезать не полностью развитый аксон, полярность может измениться, и другие нейриты потенциально могут стать аксоном. Это изменение полярности происходит только в том случае, если аксон сокращен как минимум на 10 мкм короче, чем другие нейриты. После того, как разрез будет сделан, самый длинный нейрит станет будущим аксоном, а все остальные нейриты, включая исходный аксон, превратятся в дендриты.[26] Воздействие внешней силы на нейрит, заставляющее его удлиниться, превращает его в аксон.[27] Тем не менее, развитие аксонов достигается за счет сложного взаимодействия между внеклеточной передачей сигналов, внутриклеточной передачей сигналов и цитоскелет динамика.
Внеклеточная передача сигналов
Внеклеточные сигналы, распространяющиеся через внеклеточный матрикс окружающие нейроны играют важную роль в развитии аксонов.[28] Эти сигнальные молекулы включают белки, нейротрофические факторы, внеклеточный матрикс и молекулы адгезии. Нетрин (также известный как UNC-6) секретируемый белок, участвующий в образовании аксонов. Когда UNC-5 рецептор нетрина мутирован, несколько нейритов нерегулярно проецируются из нейронов, и, наконец, один аксон выходит вперед.[29][30][31][32] Нейротрофические факторы - фактор роста нервов (NGF), нейротрофический фактор головного мозга (BDNF) и нейротрофин-3 (NTF3) также участвуют в развитии аксонов и связываются с Рецепторы Trk.[33]
В ганглиозид -превращающий фермент ганглиозид плазматической мембраны сиалидаза (PMGS), который участвует в активации TrkA на кончике нейтритов, требуется для удлинения аксонов. PMGS асимметрично распределяется по кончику нейрита, которому суждено стать будущим аксоном.[34]
Внутриклеточная передача сигналов
Во время развития аксонов активность PI3K увеличивается на конце предназначенного аксона. Нарушение активности PI3K тормозит развитие аксонов. Активация PI3K приводит к образованию фосфатидилинозит (3,4,5) -трисфосфат (PtdIns), которые могут вызывать значительное удлинение нейрита, превращая его в аксон. Таким образом, чрезмерное проявление фосфатазы что дефосфорилирование PtdIns приводит к нарушению поляризации.[28]
Цитоскелетная динамика
Неврит с самым низким актин содержимое филамента станет аксоном. Концентрация PGMS и f-актин содержание обратно коррелировано; когда PGMS становится обогащенным на кончике нейрита, содержание в нем f-актина существенно снижается.[34] Кроме того, воздействие препаратов, деполимеризующих актин, и токсина B (который инактивирует Rho-сигнализация ) вызывает образование множественных аксонов. Следовательно, разрыв актиновой сети в конусе роста будет способствовать превращению ее нейрита в аксон.[35]
Рост

Растущие аксоны перемещаются в окружающей среде через конус роста, который находится на кончике аксона. Конус роста имеет широкое пластинчатое расширение, называемое ламеллиподиум которые содержат выступы, называемые филоподия. Филоподии - это механизм, с помощью которого весь процесс прикрепляется к поверхностям и исследует окружающую среду. Актин играет важную роль в мобильности этой системы. Среды с высоким уровнем молекулы клеточной адгезии (CAM) создают идеальную среду для роста аксонов. Похоже, что это обеспечивает «липкую» поверхность для роста аксонов. Примеры CAM, специфичных для нейронных систем, включают: N-CAM, ТЕГ-1 - аксональный гликопротеин —[36]-и МАГ, все из которых являются частью иммуноглобулин надсемейство. Другой набор молекул называется внеклеточный матрикс -молекулы адгезии также обеспечивают липкий субстрат для роста аксонов. Примеры этих молекул включают ламинин, фибронектин, тенасцин, и перлекан. Некоторые из них поверхностно связаны с клетками и, таким образом, действуют как аттрактанты или репелленты ближнего действия. Другие являются диффундирующими лигандами и, следовательно, могут иметь эффекты длительного действия.
Ячейки называются клетки-указатели помочь в руководство роста аксонов нейронов. Эти клетки, которые помогают управление аксоном, как правило, другие нейроны, которые иногда незрелые. Когда аксон завершит свой рост в месте его соединения с мишенью, диаметр аксона может увеличиться до пяти раз, в зависимости от скорость проведения требуется.[37]
В ходе исследований также было обнаружено, что если аксоны нейрона были повреждены, то до тех пор, пока сома (тело клетки нейрон ) не повреждается, аксоны регенерируют и восстанавливают синаптические связи с нейронами с помощью клетки-указатели. Это также называется нейрорегенерация.[38]
Ного-А это тип компонента, ингибирующего рост нейритов, который присутствует в миелиновых мембранах центральной нервной системы (обнаружен в аксоне). Он играет решающую роль в ограничении регенерации аксонов в центральной нервной системе взрослых млекопитающих. В недавних исследованиях, если Nogo-A заблокирован и нейтрализован, можно вызвать регенерацию аксонов на большом расстоянии, что приводит к усилению функционального восстановления у крыс и спинного мозга мыши. Этого еще предстоит сделать на людях.[39] Недавнее исследование также показало, что макрофаги активируется специфическим воспалительным путем, активируемым Дектин-1 рецепторы способны способствовать восстановлению аксонов, однако также вызывают нейротоксичность в нейроне.[40]
Регулировка длины
Аксоны в значительной степени различаются по длине от нескольких микрометров до метров у некоторых животных. Это подчеркивает, что должен существовать механизм регулирования длины клетки, позволяющий нейронам ощущать длину своих аксонов и соответственно контролировать их рост. Было обнаружено, что моторные белки играют важную роль в регулировании длины аксонов.[41] Основываясь на этом наблюдении, исследователи разработали четкую модель роста аксонов, описывающую, как моторные белки могут влиять на длину аксона на молекулярном уровне.[42][43][44][45] Эти исследования предполагают, что моторные белки переносят сигнальные молекулы от сомы к конусу роста и наоборот, концентрация которых колеблется во времени с частотой, зависящей от длины.
Классификация
Аксоны нейронов человека периферическая нервная система могут быть классифицированы по их физическим характеристикам и свойствам проводимости сигнала. Известно, что аксоны имеют разную толщину (от 0,1 до 20 мкм).[3] и считалось, что эти различия связаны со скоростью, с которой потенциал действия может перемещаться по аксону - его скорость проводимости. Эрлангер и Гассер доказали эту гипотезу и идентифицировали несколько типов нервных волокон, установив связь между диаметром аксона и его скорость нервной проводимости. Они опубликовали свои открытия в 1941 году, дав первую классификацию аксонов.
Аксоны подразделяются на две системы. Первый, введенный Эрлангером и Гассером, сгруппировал волокна в три основные группы, используя буквы A, B и C. группа А, группа B, и группа C включают оба сенсорных волокна (афференты ) и двигательные волокна (эфференты ). Первая группа A была разделена на альфа, бета, гамма и дельта волокна - Aα, Aβ, Aγ и Aδ. Моторные нейроны различных моторных волокон были нижние двигательные нейроны – альфа двигательный нейрон, бета мотонейрон, и гамма мотонейрон с нервными волокнами Aα, Aβ и Aγ соответственно.
Позже другие исследователи обнаружили две группы волокон Aa, которые были сенсорными волокнами. Затем они были введены в систему, которая включала только сенсорные волокна (хотя некоторые из них были смешанными нервами, а также двигательными волокнами). Эта система называет сенсорные группы Типами и использует римские цифры: Тип Ia, Тип Ib, Тип II, Тип III и Тип IV.
Мотор
Нижние двигательные нейроны имеют два вида волокон:
| Тип | Эрлангер-Гассер Классификация | Диаметр (мкм) | Миелин | Проведение скорость (м / с) | Связанный мышечные волокна |
|---|---|---|---|---|---|
| α | Aα | 13-20 | да | 80–120 | Экстрафузионные мышечные волокна |
| β | Aβ | ||||
| γ | Aγ | 5-8 | да | 4–24[46][47] | Внутрифузионные мышечные волокна |
Сенсорный
Разные Рецепторы чувств иннервируют разные типы нервных волокон. Проприоцепторы иннервируются сенсорными волокнами типа Ia, Ib и II, механорецепторы сенсорными волокнами II и III типов и ноцицепторы и терморецепторы сенсорными волокнами III и IV типа.
| Тип | Эрлангер-Гассер Классификация | Диаметр (мкм) | Миелин | Проведение скорость (м / с) | Связанный Рецепторы чувств | Проприоцепторы | Механоцепторы | Ноцицепторы и терморецепторы |
|---|---|---|---|---|---|---|---|---|
| Я | Aα | 13-20 | да | 80–120 | Первичные рецепторы мышечное веретено (аннулоспиральное окончание) | ✔ | ||
| Ib | Aα | 13-20 | да | 80–120 | Орган сухожилия Гольджи | |||
| II | Aβ | 6-12 | да | 33–75 | Вторичные рецепторы мышечное веретено (окончание цветочно-спрей). Все кожные механорецепторы | ✔ | ||
| III | Aδ | 1-5 | Тонкий | 3–30 | Свободные нервные окончания прикосновения и давления Ноцицепторы из боковой спиноталамический тракт Холодный терморецепторы | ✔ | ||
| IV | C | 0.2-1.5 | Нет | 0.5-2.0 | Ноцицепторы из передний спиноталамический тракт Рецепторы тепла |
Автономный
В автономная нервная система имеет два вида периферических волокон:
| Тип | Эрлангер-Гассер Классификация | Диаметр (мкм) | Миелин[48] | Проведение скорость (м / с) |
|---|---|---|---|---|
| преганглионарные волокна | B | 1–5 | да | 3–15 |
| постганглионарные волокна | C | 0.2–1.5 | Нет | 0.5–2.0 |
Клиническое значение
В порядке степени тяжести повреждение нерва можно описать как неврапраксия, аксонотмезис, или же невротмезис.Сотрясение считается легкой формой диффузное повреждение аксонов.[49] Аксональное повреждение также может вызвать центральный хроматолиз. Нарушение функции аксонов нервной системы является одной из основных причин многих наследственных заболеваний. неврологические расстройства которые влияют как на периферические, так и на центральные нейроны.[5]
Когда аксон раздавлен, активный процесс дегенерация аксонов происходит в части аксона, наиболее удаленной от тела клетки. Эта дегенерация происходит быстро после травмы, когда часть аксона блокируется мембранами и разрушается макрофагами. Это известно как Валлеровское вырождение.[50] Отмирание аксона также может иметь место при многих нейродегенеративных заболеваниях, особенно при нарушении транспорта аксонов, это известно как дегенерация, подобная валлеровской.[51] Исследования показывают, что дегенерация происходит в результате действия аксонального белка. NMNAT2, будучи не в состоянии достичь всего аксона.[52]
Демиелинизация аксонов вызывает множество неврологических симптомов, обнаруженных при заболевании рассеянный склероз.
Дисмиелинизация это аномальное образование миелиновой оболочки. Это связано с несколькими лейкодистрофии, а также в шизофрения.[53][54][55]
Суровый травматическое повреждение мозга может привести к обширным поражениям нервных путей, повреждая аксоны в состоянии, известном как диффузное повреждение аксонов. Это может привести к стойкое вегетативное состояние.[56] Это было показано в исследованиях на крыса такое повреждение аксонов в результате единичного легкого черепно-мозгового повреждения может оставить восприимчивость к дальнейшему повреждению после повторных легких черепно-мозговых травм.[57]
А нервный проводник является искусственным средством направления роста аксонов, чтобы нейрорегенерация, и является одним из многих методов лечения, используемых для различных видов повреждение нерва.
История
Немецкий анатом Отто Фридрих Карл Дайтерс обычно приписывают открытие аксона, отличив его от дендритов.[5] Швейцарский Рюдольф Альберт фон Кёлликер и немецкий Роберт Ремак были первыми, кто идентифицировал и охарактеризовал начальный сегмент аксона. Келликер назвал аксон в 1896 году.[58] Луи-Антуан Ранвье был первым, кто описал бреши или узлы, обнаруженные на аксонах, и за этот вклад эти аксональные особенности теперь обычно называют узлы Ранвье. Сантьяго Рамон-и-Кахаль, испанский анатом, предположил, что аксоны были выходными компонентами нейронов, описывая их функции.[5] Джозеф Эрлангер и Герберт Гассер ранее разработали систему классификации периферических нервных волокон,[59] на основе скорости аксональной проводимости, миелинизация, размер волокна и т. д. Алан Ходжкин и Эндрю Хаксли также использовали гигантский аксон кальмара (1939), а к 1952 году они получили полное количественное описание ионной основы потенциал действия, что привело к формулировке Модель Ходжкина – Хаксли. Ходжкин и Хаксли были награждены совместно Нобелевская премия для этой работы в 1963 году. Формулы, описывающие аксональную проводимость, были распространены на позвоночных в уравнениях Франкенхойзера-Хаксли. Понимание биохимической основы распространения потенциала действия продвинулось дальше и включает много деталей об отдельных ионные каналы.
Другие животные
Аксоны в беспозвоночные были широко изучены. В Прибрежный кальмар, часто используется как модельный организм имеет самый длинный из известных аксонов.[60] В Гигантский кальмар имеет самый большой аксон известен. Его размер варьируется от половины (обычно) до одного миллиметра в диаметре и используется для управления его реактивный двигатель система. Самая быстрая зарегистрированная скорость проводимости 210 м / с обнаружена в заключенных в оболочку аксонах некоторых пелагических Креветки Penaeid[61] и обычный диапазон составляет от 90 до 200 м / с.[62] (ср 100–120 м / с для аксона самого быстрого миелинизированного позвоночного.)
В других случаях, как показали исследования на крысах, аксон происходит от дендрита; такие аксоны, как говорят, имеют «дендритное происхождение». Некоторые аксоны с дендритным происхождением аналогичным образом имеют «проксимальный» начальный сегмент, который начинается непосредственно в источнике аксона, в то время как другие имеют «дистальный» начальный сегмент, заметно отделенный от источника аксона.[63] У многих видов некоторые из нейронов имеют аксоны, которые исходят из дендрита, а не из тела клетки, и они известны как дендриты, несущие аксоны.[1] Во многих случаях аксон берет свое начало от бугорка аксона на соме; такие аксоны, как говорят, имеют «соматическое происхождение». Некоторые аксоны соматического происхождения имеют «проксимальный» начальный сегмент, прилегающий к бугорку аксона, в то время как другие имеют «дистальный» начальный сегмент, отделенный от сомы протяженным бугорком аксона.[63]
Смотрите также
- Электрофизиология
- Ганглионарное возвышение
- Гигантская аксональная нейропатия
- Нейрональная трассировка
- Пионерский аксон
Рекомендации
- ^ а б Triarhou LC (2014). «Аксоны, исходящие из дендритов: филогенетические последствия с оттенками Кахаля». Границы нейроанатомии. 8: 133. Дои:10.3389 / fnana.2014.00133. ЧВК 4235383. PMID 25477788.
- ^ Яу К.В. (декабрь 1976 г.). «Рецептивные поля, геометрия и проводящий блок сенсорных нейронов центральной нервной системы пиявки». Журнал физиологии. 263 (3): 513–38. Дои:10.1113 / jphysiol.1976.sp011643. ЧВК 1307715. PMID 1018277.
- ^ а б c Сквайр, Ларри (2013). Фундаментальная нейробиология (4-е изд.). Амстердам: Elsevier / Academic Press. С. 61–65. ISBN 978-0-12-385-870-2.
- ^ а б c Людерс Э., Томпсон П.М., Тога А.В. (август 2010 г.). «Развитие мозолистого тела в мозгу здорового человека». Журнал неврологии. 30 (33): 10985–90. Дои:10.1523 / JNEUROSCI.5122-09.2010. ЧВК 3197828. PMID 20720105.
- ^ а б c d е Дебанн Д., Кампанак Е., Бяловас А., Карлье Е., Алькарас Г. (апрель 2011 г.). «Аксонная физиология» (PDF). Физиологические обзоры. 91 (2): 555–602. Дои:10.1152 / Physrev.00048.2009. PMID 21527732. S2CID 13916255.
- ^ Нельсон А.Д., Дженкинс П.М. (2017). «Аксональные мембраны и их домены: сборка и функция начального сегмента аксона и узла Ранвье». Границы клеточной неврологии. 11: 136. Дои:10.3389 / fncel.2017.00136. ЧВК 5422562. PMID 28536506.
- ^ Летерье С., Клерк Н., Руэда-Борони Ф, Монтерсино А., Дарджент Б., Кастетс Ф (2017). «Мембранные партнеры Ankyrin G стимулируют создание и поддержание начального сегмента Axon». Границы клеточной неврологии. 11: 6. Дои:10.3389 / fncel.2017.00006. ЧВК 5266712. PMID 28184187.
- ^ Летерье С (февраль 2018 г.). "Начальный сегмент аксона: обновленная точка зрения". Журнал неврологии. 38 (9): 2135–2145. Дои:10.1523 / jneurosci.1922-17.2018. ЧВК 6596274. PMID 29378864.
- ^ Расбанд М.Н. (август 2010 г.). «Начальный сегмент аксона и поддержание полярности нейронов». Обзоры природы. Неврология. 11 (8): 552–62. Дои:10.1038 / nrn2852. PMID 20631711. S2CID 23996233.
- ^ а б c d Джонс С.Л., Свиткина Т.М. (2016). "Цитоскелет начального сегмента аксона: архитектура, развитие и роль в полярности нейронов". Нейронная пластичность. 2016: 6808293. Дои:10.1155/2016/6808293. ЧВК 4967436. PMID 27493806.
- ^ Кларк Б.Д., Голдберг Е.М., Руди Б. (декабрь 2009 г.). «Электрогенная настройка начального сегмента аксона». Нейробиолог. 15 (6): 651–68. Дои:10.1177/1073858409341973. ЧВК 2951114. PMID 20007821.
- ^ а б Ямада Р., Куба Х (2016). «Структурная и функциональная пластичность в начальном сегменте аксона». Границы клеточной неврологии. 10: 250. Дои:10.3389 / fncel.2016.00250. ЧВК 5078684. PMID 27826229.
- ^ а б Сусуки К., Куба Х (март 2016 г.). «Активно-зависимая регуляция возбудимых аксональных доменов». Журнал физиологических наук. 66 (2): 99–104. Дои:10.1007 / s12576-015-0413-4. PMID 26464228. S2CID 18862030.
- ^ а б c d е Альбертс Б. (2004). Essential Cell Biology: введение в молекулярную биологию клетки (2-е изд.). Нью-Йорк: Гарленд. стр.584–587. ISBN 978-0-8153-3481-1.
- ^ а б Альбертс Б. (2002). Молекулярная биология клетки (4-е изд.). Нью-Йорк: Гарленд. С. 979–981. ISBN 978-0-8153-4072-0.
- ^ Озген, Н; Барон, W; Hoekstra, D; Кахья, Н. (сентябрь 2016 г.). «Динамика олигодендроглиальной мембраны в связи с биогенезом миелина». Клеточные и молекулярные науки о жизни. 73 (17): 3291–310. Дои:10.1007 / s00018-016-2228-8. ЧВК 4967101. PMID 27141942.
- ^ Сэдлер, Т. (2010). Медицинская эмбриология Лангмана (11-е изд.). Филадельфия: Липпинкотт Уильям и Уилкинс. п.300. ISBN 978-0-7817-9069-7.
- ^ Гесс А., Янг Дж. З. (ноябрь 1952 г.). «Узлы Ранвье». Труды Лондонского королевского общества. Серия B, Биологические науки. Серия Б. 140 (900): 301–20. Bibcode:1952RSPSB.140..301H. Дои:10.1098 / rspb.1952.0063. JSTOR 82721. PMID 13003931. S2CID 11963512.
- ^ Роббинс А.А., Фокс С.Е., Холмс Г.Л., Скотт Р.К., Барри Дж. М. (ноябрь 2013 г.). «Кратковременные сигналы, записанные внеклеточно у свободно движущихся крыс, представляют активность аксонов». Границы в нейронных цепях. 7 (181): 181. Дои:10.3389 / fncir.2013.00181. ЧВК 3831546. PMID 24348338.
- ^ Rongjing Ge, Hao Qian и Jin-Hui Wang * (2011) Molecular Brain 4 (19), 1 ~ 11
- ^ Rongjing Ge, Hao Qian, Na Chen и Jin-Hui Wang * (2014) Molecular Brain 7 (26): 1-16
- ^ Чен Н, Ю Дж, Цянь Х, Ге Р, Ван Дж Х (июль 2010 г.). «Аксоны усиливают соматические неполные спайки до однородных амплитуд в пирамидных нейронах коры головного мозга мышей». PLOS ONE. 5 (7): e11868. Bibcode:2010PLoSO ... 511868C. Дои:10.1371 / journal.pone.0011868. ЧВК 2912328. PMID 20686619.
- ^ Вольперт, Льюис (2015). Принципы развития (5-е изд.). С. 520–524. ISBN 978-0-19-967814-3.
- ^ Флетчер Т.Л., Банкир Г.А. (декабрь 1989 г.). «Установление полярности нейронами гиппокампа: взаимосвязь между стадией развития клетки in situ и ее последующим развитием в культуре». Биология развития. 136 (2): 446–54. Дои:10.1016/0012-1606(89)90269-8. PMID 2583372.
- ^ Цзян Х., Рао Й. (май 2005 г.). «Формирование аксона: судьба против роста». Природа Неврология. 8 (5): 544–6. Дои:10.1038 / nn0505-544. PMID 15856056. S2CID 27728967.
- ^ Гослин К., Банкир Г. (апрель 1989 г.). «Экспериментальные наблюдения за развитием полярности нейронов гиппокампа в культуре». Журнал клеточной биологии. 108 (4): 1507–16. Дои:10.1083 / jcb.108.4.1507. ЧВК 2115496. PMID 2925793.
- ^ Lamoureux P, Ruthel G, Buxbaum RE, Heidemann SR (ноябрь 2002 г.). «Механическое напряжение может определять судьбу аксонов в нейронах гиппокампа». Журнал клеточной биологии. 159 (3): 499–508. Дои:10.1083 / jcb.200207174. ЧВК 2173080. PMID 12417580.
- ^ а б Аримура Н., Кайбути К. (март 2007 г.). «Полярность нейронов: от внеклеточных сигналов к внутриклеточным механизмам». Обзоры природы. Неврология. 8 (3): 194–205. Дои:10.1038 / номер 2056. PMID 17311006. S2CID 15556921.
- ^ Нейроглия и пионерные нейроны express UNC-6 для предоставления глобальных и локальных сетевых сигналов для управления миграциями в C. elegans
- ^ Серафини Т., Кеннеди Т.Э., Галко М.Дж., Мирзаян С., Джессел Т.М., Тесье-Лавин М. (август 1994 г.). «Нетрины определяют семейство белков, способствующих отрастанию аксонов, гомологичных C. elegans UNC-6». Клетка. 78 (3): 409–24. Дои:10.1016/0092-8674(94)90420-0. PMID 8062384. S2CID 22666205.
- ^ Хонг К., Хинк Л., Нишияма М., Пу М.М., Тесье-Лавин М., Штейн Э. (июнь 1999 г.). «Управляемая лигандом ассоциация между цитоплазматическими доменами рецепторов семейства UNC5 и DCC превращает индуцированное нетрином притяжение конуса роста в отталкивание». Клетка. 97 (7): 927–41. Дои:10.1016 / S0092-8674 (00) 80804-1. PMID 10399920. S2CID 18043414.
- ^ Hedgecock EM, Culotti JG, Hall DH (январь 1990 г.). «Гены unc-5, unc-6 и unc-40 управляют периферической миграцией первичных аксонов и мезодермальных клеток по эпидермису C. elegans». Нейрон. 4 (1): 61–85. Дои:10.1016 / 0896-6273 (90) 90444-К. PMID 2310575. S2CID 23974242.
- ^ Хуанг Э.Дж., Райхардт Л.Ф. (2003). «Рецепторы Trk: роли в передаче сигнала нейронов». Ежегодный обзор биохимии. 72: 609–42. Дои:10.1146 / annurev.biochem.72.121801.161629. PMID 12676795. S2CID 10217268.
- ^ а б Да Силва Дж. С., Хасегава Т., Мияги Т., Дотти К. Г., Абад-Родригес Дж. (Май 2005 г.). «Активность асимметричной мембранной ганглиозидной сиалидазы определяет судьбу аксонов». Природа Неврология. 8 (5): 606–15. Дои:10.1038 / nn1442. PMID 15834419. S2CID 25227765.
- ^ Брадке Ф., Дотти К.Г. (март 1999 г.). «Роль локальной нестабильности актина в формировании аксонов». Наука. 283 (5409): 1931–4. Bibcode:1999Научный ... 283.1931B. Дои:10.1126 / science.283.5409.1931. PMID 10082468.
- ^ Ферли А.Дж., Мортон С.Б., Манало Д., Карагогеос Д., Додд Дж., Джессел Т.М. (апрель 1990 г.). «Аксональный гликопротеин TAG-1 является членом суперсемейства иммуноглобулинов с активностью, способствующей росту нейритов». Клетка. 61 (1): 157–70. Дои:10.1016/0092-8674(90)90223-2. PMID 2317872. S2CID 28813676.
- ^ Альбертс, Брюс (2015). Молекулярная биология клетки (Шестое изд.). п. 947. ISBN 9780815344643.
- ^ Куник Д., Дион С., Одзаки Т., Левин Л.А., Константино С. (2011). «Лазерная пересечение одного аксона для исследований повреждения и регенерации аксонов с высоким содержанием аксонов». PLOS ONE. 6 (11): e26832. Bibcode:2011PLoSO ... 626832K. Дои:10.1371 / journal.pone.0026832. ЧВК 3206876. PMID 22073205.
- ^ Schwab ME (февраль 2004 г.). «Регенерация ног и аксонов». Текущее мнение в нейробиологии. 14 (1): 118–24. Дои:10.1016 / j.conb.2004.01.004. PMID 15018947. S2CID 9672315.
- ^ Гензель Дж. К., Накамура С., Гуан З., ван Ройен Н., Анкени Д. П., Попович П. Г. (март 2009 г.). «Макрофаги способствуют регенерации аксонов с одновременной нейротоксичностью». Журнал неврологии. 29 (12): 3956–68. Дои:10.1523 / JNEUROSCI.3992-08.2009. ЧВК 2693768. PMID 19321792.
- ^ Майерс К.А., Баас П.В. (сентябрь 2007 г.). «Кинезин-5 регулирует рост аксона, действуя как тормоз на его массив микротрубочек». Журнал клеточной биологии. 178 (6): 1081–91. Дои:10.1083 / jcb.200702074. ЧВК 2064629. PMID 17846176.
- ^ Ришал И., Кам Н., Перри Р. Б., Шиндер В., Фишер Е. М., Скьяво Г., Файнзильбер М. (июнь 2012 г.). «Механизм с приводом от двигателя для измерения длины клетки». Отчеты по ячейкам. 1 (6): 608–16. Дои:10.1016 / j.celrep.2012.05.013. ЧВК 3389498. PMID 22773964.
- ^ Карамчед Б.Р., Бресслофф ПК (май 2015 г.). «Модель отсроченной обратной связи для измерения длины аксонов». Биофизический журнал. 108 (9): 2408–19. Bibcode:2015BpJ ... 108.2408K. Дои:10.1016 / j.bpj.2015.03.055. ЧВК 4423051. PMID 25954897.
- ^ Бресслов П.С., Карамчед Б.Р. (2015). «Механизм частотно-зависимого декодирования для определения длины аксона». Границы клеточной неврологии. 9: 281. Дои:10.3389 / fncel.2015.00281. ЧВК 4508512. PMID 26257607.
- ^ Фольц Ф., Веттманн Л., Мориджи Г., Круз К. (май 2019 г.). «Звук роста аксона». Физический обзор E. 99 (5–1): 050401. arXiv:1807.04799. Bibcode:2019PhRvE..99e0401F. Дои:10.1103 / PhysRevE.99.050401. PMID 31212501.
- ^ Эндрю Б.Л., часть Нью-Джерси (апрель 1972 г.). «Свойства быстрых и медленных двигательных единиц в мышцах задних конечностей и хвоста крысы». Ежеквартальный журнал экспериментальной физиологии и когнитивных медицинских наук. 57 (2): 213–25. Дои:10.1113 / expphysiol.1972.sp002151. PMID 4482075.
- ^ Рассел Нью-Джерси (январь 1980 г.). «Скорость аксональной проводимости изменяется после тенотомии мышц или деафферентации во время развития у крысы». Журнал физиологии. 298: 347–60. Дои:10.1113 / jphysiol.1980.sp013085. ЧВК 1279120. PMID 7359413.
- ^ Покок Г., Ричардс С.Д. и др. (2004). Физиология человека (2-е изд.). Нью-Йорк: Издательство Оксфордского университета. С. 187–189. ISBN 978-0-19-858527-5.
- ^ Dawodu ST (16 августа 2017 г.). «Травматическая травма головного мозга (ЧМТ) - определение, эпидемиология, патофизиология». Medscape. В архиве с оригинала 12 июня 2018 г.. Получено 14 июля 2018.
- ^ Травма и валлеровская дегенерация В архиве 2 мая 2006 г. Wayback Machine, Калифорнийский университет в Сан-Франциско
- ^ Coleman MP, Freeman MR (1 июня 2010 г.). "Валлеровское вырождение, мир (а) и сущность". Ежегодный обзор нейробиологии. 33 (1): 245–67. Дои:10.1146 / annurev-neuro-060909-153248. ЧВК 5223592. PMID 20345246.
- ^ Джилли Дж., Член парламента Коулмана (январь 2010 г.). «Эндогенный Nmnat2 является важным фактором выживания для поддержания здоровья аксонов». PLOS Биология. 8 (1): e1000300. Дои:10.1371 / journal.pbio.1000300. ЧВК 2811159. PMID 20126265.
- ^ Кремер-Альберс Е.М., Гериг-Бургер К., Тиле С., Троттер Дж., Наве К.А. (ноябрь 2006 г.). «Нарушенные взаимодействия мутантного протеолипидного белка / DM20 с холестерином и липидными рафтами в олигодендроглии: последствия для дисмиелинизации при спастической параплегии». Журнал неврологии. 26 (45): 11743–52. Дои:10.1523 / JNEUROSCI.3581-06.2006. ЧВК 6674790. PMID 17093095.
- ^ Маталон Р., Михалс-Маталон К., Сурендран С., Тайринг С.К. (2006). «Болезнь Канавана: исследования на нокаутной мыши». N-ацетиласпартат. Adv. Exp. Med. Биол. Успехи экспериментальной медицины и биологии. 576. С. 77–93, обсуждение 361–3. Дои:10.1007/0-387-30172-0_6. ISBN 978-0-387-30171-6. PMID 16802706. S2CID 44405442.
- ^ Ткачев Д., Миммак М.Л., Хаффакер С.Дж., Райан М., Bahn S (август 2007 г.). «Дальнейшие доказательства изменения биосинтеза миелина и глутаматергической дисфункции при шизофрении». Международный журнал нейропсихофармакологии. 10 (4): 557–63. Дои:10.1017 / S1461145706007334. PMID 17291371.
- ^ «Травма головного мозга, травматическая». Медциклопедия. GE. Архивировано из оригинал 26 мая 2011 г.
- ^ Райт Д.К., Брэди Р.Д., Камнакш А., Трезизе Дж., Сан М., Макдональд С.Дж. и др. (Октябрь 2019 г.). «Повторные легкие черепно-мозговые травмы вызывают стойкие изменения белков плазмы и биомаркеров магнитно-резонансной томографии у крыс». Научные отчеты. 9 (1): 14626. Дои:10.1038 / с41598-019-51267-ш. ЧВК 6787341. PMID 31602002.
- ^ Палец S (1994). Истоки нейробиологии: история исследований функций мозга. Издательство Оксфордского университета. п. 47. ISBN 9780195146943. OCLC 27151391.
Келликер дал название аксону в 1896 году.
- ^ Грант G (декабрь 2006 г.). «Нобелевские премии 1932 и 1944 годов по физиологии и медицине: награды за новаторские исследования в области нейрофизиологии». Журнал истории неврологии. 15 (4): 341–57. Дои:10.1080/09647040600638981. PMID 16997762. S2CID 37676544.
- ^ Хелье, Дженнифер Л. (16 декабря 2014 г.). Мозг, нервная система и их болезни [3 тома]. ABC-CLIO. ISBN 9781610693387. В архиве из оригинала 14 марта 2018 г.
- ^ Хсу К., Теракава С. (июль 1996 г.). «Фенестрация в миелиновой оболочке нервных волокон креветки: новый узел возбуждения для скачкообразной проводимости». Журнал нейробиологии. 30 (3): 397–409. Дои:10.1002 / (SICI) 1097-4695 (199607) 30: 3 <397 :: AID-NEU8> 3.0.CO; 2- #. PMID 8807532.
- ^ Зальцер Дж. Л., Залц Б. (октябрь 2016 г.). «Миелинизация». Текущая биология. 26 (20): R971 – R975. Дои:10.1016 / j.cub.2016.07.074. PMID 27780071.
- ^ а б Хёффлин Ф., Джек А., Ридель С., Мак-Бухер Дж., Роос Дж., Корчелли С. и др. (2017). «Неоднородность начального сегмента аксона в интернейронах и пирамидных клетках зрительной коры грызунов». Границы клеточной неврологии. 11: 332. Дои:10.3389 / fncel.2017.00332. ЧВК 5684645. PMID 29170630.
внешняя ссылка
- Гистологическое изображение: 3_09 в Центре медицинских наук Университета Оклахомы - «Слайд 3 Спинной мозг "