Семейство Rho GTPases - Rho family of GTPases
В Семейство Rho GTPases представляет собой семейство небольших (~ 21 кДа) сигнальных G белки, и является подсемейством Рас надсемейство. Члены Ро GTPase семья, как было показано, регулирует многие аспекты внутриклеточного актин динамику и обнаружены во всех царствах эукариот, включая дрожжи и некоторые растения. Детально изучены три члена семьи: Cdc42, Rac1, и RhoA. Все белки G являются «молекулярными переключателями», а белки Rho играют роль в органелла разработка, цитоскелет динамика, движение клеток и другие общие клеточные функции.[1][2][3][4][5]
История
Идентификация семейства Rho GTPases началась в середине 1980-х годов. Первым идентифицированным членом Rho был RhoA, случайно выделенный в 1985 году из-за низкой строгости. кДНК скрининг.[6] Следующими были идентифицированы Rac1 и Rac2, в 1989 г.[7] за ним последовал Cdc42 в 1990 году.[8] Восемь дополнительных представителей Rho у млекопитающих были идентифицированы в ходе биологических исследований до конца 1990-х годов, что стало поворотным моментом в биологии, когда доступность полных геномных последовательностей позволила полностью идентифицировать семейства генов. Все клетки эукариот содержат Rho GTPase (от 6 у дрожжей до 20 у млекопитающих). Таким образом, у млекопитающих семейство Rho состоит из 20 членов, распределенных в 8 подсемейств: Rho, Rnd, RhoD / F, RhoH, Rac, Cdc42, RhoU / V и RhoBTB.[1]
Еще в 1990 г. Патерсон и др. началось выражая активированный белок Rho в Швейцарские фибробласты 3T3.[9]
К середине 1990-х годов было обнаружено, что белки Rho влияют на формирование клеточных выступов («отростков») в фибробластах. В обзорной статье 1998 года Алан Холл собрал доказательства, показывающие, что не только фибробласты образуют процессы при активации Rho, но и практически все эукариотические клетки.[10]
В обзорной статье 2006 г., опубликованной Bement et al. исследовали значение пространственных зон активации Rho.[11]
Категоризация
Семейство Rho GTPases принадлежит к Рас надсемейство белков, которых у млекопитающих насчитывается более 150 разновидностей. Белки Rho иногда обозначают некоторых членов семейства Rho (RhoA, RhoB, и RhoC ), а иногда относится ко всем членам семьи. Эта статья о семье в целом.
У млекопитающих семейство Rho состоит из 20 членов.[1] Почти во всех исследованиях участвуют три наиболее распространенных члена семейства Rho: Cdc42, Rac1 и RhoA.
| Член семьи Ро | Действие на актиновые филаменты |
|---|---|
| Cdc42 | влияет филоподии |
| Rac1 | влияет ламеллиподии |
| RhoA | влияет стрессовые волокна |
Эти 20 представителей млекопитающих подразделяются на подсемейство Rac (Rac1, Rac2, Rac3 и RhoG), подсемейство Cdc42 (Cdc42, TC10 / RhoQ, TCL / RhoJ), семейство RhoUV (RhoV / Chp и RhoU / Wrch-1 /). , Подсемейство RhoA (RhoA, RhoB и RhoC), подсемейство Rnd (Rnd1 / Rho6, Rnd2 / RhoN и Rnd3 / RhoE), подсемейство RhoD (RhoD и RhoF / Rif), RhoBTB (RhoBTBH1 & 2) и Rho.[1]
| Подкласс | Цитоскелетный эффект | Члены семьи Ро |
|---|---|---|
| Подкласс cdc42 | филоподии | Cdc42 |
| RhoQ (TC10) | ||
| RhoJ (TCL) | ||
| Подкласс RhoUV | филоподии и ламеллиподии | RhoU (Wrch) |
| RhoV (Гл.) | ||
| Rac | ламеллиподии | Rac1 |
| Rac2 | ||
| Rac3 | ||
| RhoG | ||
| RhoBTB | стабильность белка | RhoBTB1 |
| RhoBTB2 | ||
| RhoBTB3 | ||
| RhoH | Рас-агонист? | RhoH |
| Ро (подкласс) | ↑стрессовые волокна и ↑очаговые спайки | RhoA |
| RhoB | ||
| RhoC | ||
| Rnd | ↓стрессовые волокна и ↓очаговые спайки | Rnd1 |
| Rnd2 | ||
| Rnd3 (RhoE) | ||
| RhoF | Транспорт везикул, филоподии | RhoD |
| RhoF (Риф) |
Регуляторы
Были идентифицированы три основных класса регуляторов передачи сигналов Rho-белка: фактор обмена гуаниновых нуклеотидов (GEF), Белки, активирующие ГТФазу (GAP) и ингибиторы диссоциации гуаниновых нуклеотидов (GDI).[12] GEF активируют белки Rho, катализируя обмен GDP на GTP. GAP контролируют способность GTPase гидролизовать GTP к ВВП, контролируя естественную скорость движения от активного строения к неактивному. Белки GDI образуют большой комплекс с белком Rho, помогая предотвратить диффузию внутри мембраны и в цитозоль и, таким образом, действуя как якорь и позволяя жесткий пространственный контроль активации Rho.[12] У человека 82 GEF (71 Dbl-подобный [13] и 11 DOCK-подобных [14]) положительно контролируют активность членов Rho, тогда как 66 белков GAP контролируют ее отрицательно.[15]
Недавняя работа раскрыла важные дополнительные механизмы регулирования: микроРНК регулируют посттранскрипционный процессинг мРНК, кодирующих Rho GTPase; пальмитоилирование и ядерное нацеливание влияют на внутриклеточное распределение; посттрансляционное фосфорилирование, трансглютаминирование и AMPилирование модулируют передачу сигналов Rho GTPase; и убиквитинирование контролирует стабильность и оборот белка Rho GTPase. Эти способы регуляции увеличивают сложность сигнальной сети Rho GTPase и обеспечивают точный пространственно-временной контроль отдельных Rho GTPases.[16]
Эффекторы
Каждый белок Rho влияет на многочисленные нижестоящие белки, каждый из которых играет роль в различных клеточных процессах. Было обнаружено более 60 мишеней трех распространенных Rho GTPases.[17] Две молекулы, которые непосредственно стимулируют полимеризацию актина, - это белки Arp2 / 3 и родственные Diaphanous формины.[18]
| GTPase | Эффектор[2][18] |
|---|---|
| RhoA | Cit, Cnksr1, Диаф1, Диаф2, DgkQ, FlnA, KcnA2, Ktn1, Rtkn1, Rtkn2, Rhpn1, Rhpn2, Itpr1, PlcG1, ПИ-5-п5К, Pld1, Pkn1, Pkn2, Рок1, Рок2, PrkcA, Ппп1р12А |
| Rac1 | Sra1, IRSp53, PAK1, PAK2, PAK3 |
| Cdc42 | Белок синдрома Вискотта-Олдрича, N-WASP, IRSp53, Dia2, Dia3, ROCK1, ROCK2, PAK4 |
Функции
Белки Rho / Rac участвуют в большом количестве клеточных функций, таких как полярность клеток, везикулярный транспорт, клеточный цикл и транскриптомная динамика.[2]
Морфология
Клетки животных образуют множество разных форм в зависимости от их функции и расположения в организме. Белки Rho помогают клеткам регулировать изменения формы на протяжении их жизненного цикла. Прежде чем клетки смогут пройти ключевые процессы, такие как почкование, митоз или передвижение, они должны иметь некоторый способ полярность ячейки.
Один из примеров роли Rho GTPases в полярности клеток можно увидеть в хорошо изученных дрожжевых клетках. Прежде, чем клетка сможет отпочковаться, Cdc42 используется для определения области клеточной мембраны, которая начнет выпирать в новую клетку. Когда Cdc42 удаляется из клетки, наросты все еще образуются, но неорганизованно.[17]
Одним из наиболее очевидных изменений морфологии клеток, контролируемых белками Rho, является образование ламеллиподии и филоподии, проецируя отростки, похожие на «пальцы» или «ступни», часто приводящие в движение клетки шишки по поверхностям. Практически все эукариотические клетки образуют такие отростки при активации Rho.[10] Фибробласты такие как швейцарские клетки 3T3 часто используются для изучения этих явлений.
Методы обучения
Многое из того, что известно об изменениях клеточной морфологии и влиянии белков Rho, связано с созданием конститутивно активной мутированной формы белка. Мутация ключевой аминокислоты может изменить конформацию всего белка, заставляя его постоянно принимать конформацию, которая напоминает состояние, связанное с GTP.[9] Этот белок не может быть инактивирован обычным образом посредством гидролиза GTP, и поэтому он «застревает». Когда активированный таким образом белок Rho экспрессируется в клетках 3T3, возникают морфологические изменения, такие как сокращения и образование филоподий.[9]
Поскольку белки Rho G-белки и связаны с плазматической мембраной, их расположение можно легко контролировать. В каждой ситуации, будь то заживление ран, цитокинез, или же подающий надежды можно отобразить и идентифицировать место активации Rho. Например, если в сферической ячейке сделать круглое отверстие, Cdc42 и другие активные Rhos наблюдаются в наибольшей концентрации по окружности круговой травмы.[11] Один из методов поддержания пространственных зон активации - это закрепление на актиновом цитоскелете, предотвращающее диффузию мембраносвязанного белка из области, где он больше всего необходим.[11] Другой метод поддержания - образование большого комплекса, который устойчив к диффузии и более жестко связан с мембраной, чем сам Rho.[11]
Морфогенез дендритных шипов
Морфогенез дендритные шипы имеет решающее значение для индукции долгосрочное потенцирование (ДП).[19][20] Морфология позвоночника зависит от состояния актин либо в глобулярной (G-актин), либо в нитчатой (F-актин) форме. Роль семейства Rho GTPases и его эффекты в стабильности актин и моторика позвоночника[21] имеет важное значение для памяти. Если дендритный позвоночник является основной единицей хранения информации, то способность позвоночника самопроизвольно расширяться и втягиваться должна быть ограничена. В противном случае информация может быть потеряна. Семейство Rho GTPases вносит значительный вклад в процесс, который стимулирует полимеризацию актина, что, в свою очередь, увеличивает размер и форму позвоночника.[22] Большие шипы более стабильны, чем маленькие, и могут быть устойчивы к модификации за счет дополнительной синаптической активности.[23] Поскольку изменения формы и размера дендритных шипов коррелируют с силой возбуждающих синаптических связей и сильно зависят от ремоделирования лежащего в основе актинового цитоскелета,[24] специфические механизмы регуляции актина и, следовательно, семейство Rho GTPases, являются неотъемлемой частью образования, созревания и пластичность дендритных шипов, обучения и памяти.
Путь RhoA
Одна из основных Rho GTPases, участвующих в морфогенезе позвоночника, - это RhoA, белок, который также модулирует регуляцию и время деления клеток. В контексте активности нейронов RhoA активируется следующим образом: как только кальций попадает в клетку через Рецепторы NMDA, это привязано к кальмодулин и активирует CaMKII, что приводит к активации RhoA.[22] Активация белка RhoA активирует ROCK, киназу RhoA, что приводит к стимуляции LIM киназа, что, в свою очередь, подавляет белок кофилин. Функция кофилина заключается в реорганизации актинового цитоскелета клетки; а именно, он деполимеризует актиновые сегменты и, таким образом, подавляет рост конусов роста и восстановление аксонов.[25]
Исследование, проведенное Murakoshi et al. в 2011 вовлечены Rho GTPases RhoA и Cdc42 в морфогенез дендритных шипов. Обе ГТФазы быстро активировались в отдельных дендритных шипах пирамидные нейроны в области СА1 крысы гиппокамп во время структурной пластичности, вызванной длительными стимуляторами потенцирования. Одновременная активация RhoA и Cdc42 приводила к временному увеличению роста позвоночника до 300% в течение пяти минут, которое переходило в более мелкий, но устойчивый рост в течение тридцати минут.[22] Активация RhoA распространялась вокруг позвоночника, подвергающегося стимуляции, и было определено, что RhoA необходим для переходной фазы и, скорее всего, для устойчивой фазы роста позвоночника.
Путь cdc42
Cdc42 участвует во многих различных функциях, включая рост дендритов, ветвление и стабильность ветвей.[26] Приток кальция в клетку через рецепторы NMDA связывается с кальмодулином и активирует Са2 + / кальмодулин-зависимые протеинкиназы II (CaMKII). В свою очередь, CaMKII активируется, и это активирует Cdc42, после чего передача сигналов обратной связи не происходит выше по течению от кальция и CaMKII. Если он помечен зеленым флуоресцентным белком, усиленным мономером, можно увидеть, что активация Cdc42 ограничивается только стимулированным шипом дендрита. Это связано с тем, что молекула постоянно активируется во время пластичности и сразу же деактивируется после диффузии из позвоночника. Несмотря на свою компартментализованную активность, Cdc42 все еще подвижен вне стимулированного позвоночника, как и RhoA. Cdc42 активирует PAK, протеинкиназу, которая специфически фосфорилирует и, следовательно, инактивирует ADF / кофилин.[27] Инактивация кофилина приводит к усилению полимеризации актина и увеличению объема позвоночника. Активация Cdc42 необходима для устойчивого увеличения объема позвоночника.
Наблюдаемые изменения структурной пластичности

Murakoshi, Wang и Yasuda (2011) исследовали эффекты активации Rho GTPase на структурную пластичность отдельных дендритных шипов, выясняя различия между переходной и устойчивой фазами.[22]
Переходные изменения структурной пластичности
Применение низкочастотной последовательности двухфотонного освобождения каркаса глутамата в единственном дендритном шипе может вызвать быструю активацию как RhoA, так и Cdc42. В течение следующих двух минут объем стимулированного позвоночника может увеличиться до 300 процентов от первоначального размера. Однако это изменение морфологии позвоночника носит временный характер; объем позвоночника уменьшается через пять минут. Введение трансферазы C3, ингибитора Rho, или глицил-H1152, ингибитора Rock, ингибирует временное расширение позвоночника, указывая на то, что для этого процесса каким-то образом требуется активация пути Rho-Rock.[22]
Устойчивые изменения структурной пластичности
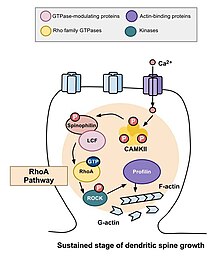
После того, как происходят переходные изменения, описанные выше, объем позвоночника уменьшается, пока не увеличится на 70–80 процентов от исходного объема. Это устойчивое изменение структурной пластичности продлится около тридцати минут. Еще раз, введение трансферазы C3 и Glycyl-H1152 подавляло этот рост, предполагая, что путь Rho-Rock необходим для более стойкого увеличения объема позвоночника. Кроме того, введение Cdc42-связывающего домена Wasp или ингибитора, нацеленного на активацию Pak1-3 (IPA3), снижает этот устойчивый рост в объеме, демонстрируя, что путь Cdc42-Pak также необходим для этого роста в объеме спинного мозга. Это важно, потому что устойчивые изменения структурной пластичности могут обеспечить механизм кодирования, сохранения и восстановления воспоминаний. Сделанные наблюдения могут предполагать, что Rho GTPases необходимы для этих процессов.[22]
Движение
Помимо образования ламеллиподий и филоподий, внутриклеточная концентрация и перекрестная связь между различными белками Rho управляют растяжениями и сокращениями, которые вызывают клеточное перемещение. Сакумура и др. предложили модель, основанную на дифференциальных уравнениях, которая помогает объяснить активность белков Rho и их связь с движением. Эта модель включает три белка: Cdc42, RhoA и Rac. Cdc42, как полагают, стимулирует удлинение филоподий и блокирует деполимеризацию актина. Считалось, что RhoA стимулирует ретракцию актина. Rac лечили, чтобы стимулировать распространение ламеллиподий, но блокировать деполимеризацию актина. Эти три белка, хотя и значительно упрощены, охватывают ключевые этапы клеточного передвижения. С помощью различных математических методов были найдены решения дифференциальных уравнений, описывающих различные области активности на основе внутриклеточной активности. В заключение в статье показано, что модель предсказывает наличие нескольких пороговых концентраций, которые вызывают интересное влияние на активность клетки. Ниже определенной концентрации активность очень мала, не вызывая разгибания рук и ног клетки. Выше определенной концентрации белок Rho вызывает синусоидальные колебания, похожие на растяжения и сокращения ламеллиподий и филоподий. По сути, эта модель предсказывает, что увеличение внутриклеточной концентрации этих трех ключевых активных белков Rho вызывает противофазную активность клетки, что приводит к расширению и сокращению, которые также не совпадают по фазе.[28]
Лечение раны
Одним из примеров поведения, которое модулируется белками Rho GTPase, является заживление ран. Раны заживают по-разному у молодых и взрослых цыплят. У молодых цыплят раны заживают путем сжатия, как за шнурок, который затягивают, чтобы закрыть мешок. У цыплят старшего возраста клетки ползают по ране посредством передвижения. Образование актина, необходимое для закрытия ран у молодых цыплят, контролируется белками Rho GTPase, поскольку после инъекции бактериального экзофермента, используемого для блокирования активности rho и rac, полимеры актина не образуются, и, таким образом, заживление полностью не происходит.[29]
Полярность ячейки
Исследования фибробластов указывают на положительную обратную связь между активностью Cdc42 и оттоком H + изоформой 1 обменника Na-H (NHE1) на переднем крае мигрирующих клеток. NHE1-опосредованный отток H + необходим для катализируемого гуанин-нуклеотидным обменным фактором (GEF) связывания GTP с Cdc42, что предполагает механизм регуляции полярности этой небольшой GTPase в мигрирующих клетках.[30]
Фагоцитоз
Еще одно клеточное поведение, на которое влияют rho-белки, - фагоцитоз. Как и в случае с большинством других типов модуляции клеточных мембран, фагоцитозу требуется актиновый цитоскелет, чтобы поглощать другие элементы. Актиновые филаменты контролируют образование фагоцитарной чашки, и активные Rac1 и Cdc42 участвуют в этом сигнальном каскаде.[31]
Митоз
Еще одним важным аспектом клеточного поведения, который, как считается, включает передачу сигналов rho-белка, является митоз. Хотя в течение многих лет считалось, что активность rho GTPase ограничивается полимеризацией актина и, следовательно, цитокинез, который происходит после митоза, появились новые доказательства, которые показывают некоторую активность в формировании микротрубочек и самом процессе митоза. Эта тема все еще обсуждается, и есть доказательства как за, так и против важности rho в митозе.[32]
Приложения
Регенерация нервной системы
Из-за их влияния на клеточную подвижность и форму, белки Rho стали явной целью при изучении шишки эта форма во время аксональный генерация и регенерация нервной системы. Белки Rho могут быть потенциальной мишенью для доставки в повреждения спинного мозга после травматического повреждения. После повреждения спинного мозга внеклеточное пространство становится препятствием для естественных усилий нейронов по регенерации.
Эти естественные усилия включают формирование конуса роста на проксимальном конце поврежденного аксона. Вновь сформированные конусы роста впоследствии пытаются «ползти» по поражению. Они чувствительны к химическим сигналам внеклеточной среды. Один из многих тормозящих сигналов включает: хондроитинсульфат протеогликаны (CSPG). Нейроны, растущие в культуре, становятся более способными пересекать области субстрата, покрытые CSPG, после экспрессии конститутивно активных Cdc42 или Rac1[33] или проявление доминантно-отрицательной формы (ингибирование) RhoA[нужна цитата ]. Частично это происходит из-за экзогенных белков Rho, управляющих движением клеток, несмотря на внеклеточные сигналы, способствующие апоптозу и коллапсу конуса роста. Таким образом, внутриклеточная модуляция белков Rho представляет интерес для исследований, направленных на регенерацию спинного мозга.
Умственная отсталость
Дисфункция белков Rho также причастна к умственная отсталость. Умственная отсталость в некоторых случаях связана с пороками развития дендритные шипы, которые образуют постсинаптические связи между нейроны. Деформированные дендритные шипы могут быть результатом модуляции передачи сигналов rho-белка. После клонирования различных генов, участвующих в Х-связанный умственная отсталость, были идентифицированы три гена, которые влияют на передачу сигналов Rho, включая олигофренин-1 (белок GAP, который стимулирует активность GTPase Rac1, Cdc42 и RhoA), PAK3 (участвующий в эффектах Rac и Cdc42 на актиновый цитоскелет) и αPIX (GEF, который помогает активировать Rac1 и Cdc42).[34] Из-за эффекта передачи сигналов Rho на актиновый цитоскелет, генетические нарушения rho-белка могут объяснять нерегулярную морфологию нейрональных дендритов, наблюдаемую в некоторых случаях умственной отсталости.
Рак
После обнаружения этого Рас белки мутируют в 30% случаев рака человека, предполагалось, что мутировавшие белки Rho также могут участвовать в репродукции рака.[12] Однако по состоянию на август 2007 г. онкогенных мутаций в белках Rho обнаружено не было, и только одна была обнаружена генетически измененной.[12] Чтобы объяснить роль путей Rho без мутаций, исследователи теперь обратились к регуляторам активности rho и уровням экспрессии белков Rho.
Один из способов объяснить измененную передачу сигналов в отсутствие мутации - увеличение экспрессии. Сверхэкспрессия RhoA, RhoB, RhoC, Rac1, Rac2, Rac3, RhoE, RhoG, RhoH и Cdc42 была показана при нескольких типах рака.[12] Это повышенное присутствие такого количества сигнальных молекул означает, что эти белки способствуют клеточным функциям, которые становятся чрезмерно активными в раковых клетках.
Вторая цель для объяснения роли белков Rho в развитии рака - это их регуляторные белки. Белки Rho очень жестко контролируются множеством источников, и было идентифицировано более 60 активаторов и 70 инактиваторов.[17] Было показано, что множественные GAP, GDI и GEF подвергаются сверхэкспрессии, подавлению или мутации при различных типах рака.[12] После изменения восходящего сигнала активность его нижестоящих мишеней, то есть белков Rho, изменится в активности.
Ellenbroek et al. описал ряд различных эффектов активации Rho в раковых клетках. Во-первых, при инициации опухолевой модификации активность Rho может подавлять апоптоз и, следовательно, способствуют искусственному долголетию клеток. После подавления естественного апоптоза можно наблюдать аномальный рост опухоли через потерю полярности, в которой белки Rho играют неотъемлемую роль. Затем растущая масса может вторгаться через ее нормальные границы через изменение адгезионных белков, потенциально вызываемых белками Rho.[12] Наконец, после ингибирования апоптоза, полярности клеток и молекул адгезии, раковая масса может свободно подвергаться метастазировать и распространились на другие части тела.
Рекомендации
- ^ а б c d Boureux A, Vignal E, Faure S, Fort P (2007). «Эволюция семейства Rho ras-подобных GTPases у эукариот». Мол Биол Эвол. 24 (1): 203–16. Дои:10.1093 / molbev / msl145. ISSN 0021-9193. ЧВК 2665304. PMID 17035353.
- ^ а б c Bustelo XR, Sauzeau V, Berenjeno IM (2007). «GTP-связывающие белки семейства Rho / Rac: регуляция, эффекторы и функции in vivo». BioEssays. 29 (4): 356–370. Дои:10.1002 / bies.20558. ЧВК 1971132. PMID 17373658.
- ^ Ридли, Энн Дж (2015). «Передача сигналов Rho GTPase при миграции клеток». Текущее мнение в области клеточной биологии. 36: 103–112. Дои:10.1016 / j.ceb.2015.08.005. ЧВК 4728192. PMID 26363959.

- ^ Ридли, Энн Жаклин (2016). "Энн Ридли: Сеть с Rho GTPases". Тенденции в клеточной биологии. 26 (7): 465–466. Дои:10.1016 / j.tcb.2016.04.005. ISSN 0962-8924. PMID 27166090. (требуется подписка)
- ^ Хисман, Сара Дж .; Ридли, Энн Дж. (2008). «Rho GTPases млекопитающих: новое понимание их функций из исследований in vivo». Обзоры природы Молекулярная клеточная биология. 9 (9): 690–701. Дои:10.1038 / nrm2476. PMID 18719708. (требуется подписка)
- ^ Madaule P .; Аксель Р. (1985). «Новое семейство генов, связанных с ras». Клетка. 41 (1): 31–40. Дои:10.1016/0092-8674(85)90058-3. PMID 3888408.
- ^ Дидсбери Дж, Вебер Р.Ф., Бокоч Г.М., Эванс Т., Снайдерман Р. (1989). «Rac, новое семейство белков, связанных с ras, которые являются субстратами ботулотоксина». J Biol Chem. 264 (28): 16378–82. ISSN 0021-9258. PMID 2674130.
- ^ Munemitsu S, Innis M, Clark R, McCormick F, Ullrich A, Polakis P (1990). «Молекулярное клонирование и экспрессия кДНК G25K, человеческого гомолога гена клеточного цикла дрожжей CDC42». Mol Cell Biol. 10 (11): 5977–82. Дои:10.1128 / MCB.10.11.5977. ISSN 0270-7306. ЧВК 361395. PMID 2122236.
- ^ а б c Патерсон HF, Self AJ, Garrett MD, Just I, Aktories K, Hall A (1990). «Микроинъекция рекомбинантного p21 rho вызывает быстрые изменения морфологии клеток». J Cell Biol. 111 (3): 1001–7. Дои:10.1083 / jcb.111.3.1001. ЧВК 2116288. PMID 2118140.
- ^ а б Холл А. (1998). «Rho GTPases и актиновый цитоскелет». Наука. 279 (5350): 509–14. Дои:10.1126 / science.279.5350.509. PMID 9438836.
- ^ а б c d Бемент В.М., Миллер А.Л., фон Дассов Г. (2006). «Зоны активности Rho GTPase и транзиторные сократительные массивы». BioEssays. 28 (10): 983–93. Дои:10.1002 / bies.20477. ЧВК 4364130. PMID 16998826.
- ^ а б c d е ж грамм Элленбрук С., Коллард Дж. (2007). «RhoGTPases: функции и связь с раком». Clin Exp Метастаз. 24 (8): 657–72. Дои:10.1007 / s10585-007-9119-1. PMID 18000759.
- ^ Форт П., Бланги А. (2017). «Эволюционный ландшафт Dbl-подобных семейств RhoGEF: адаптация эукариотических клеток к сигналам окружающей среды». Геномная биология и эволюция. 9 (6): 1471–86. Дои:10.1093 / gbe / evx100. ЧВК 5499878. PMID 28541439.
- ^ Меллер Н., Мерло С., Гуда С. (2005). «Белки CZH: новое семейство Rho-GEF». Журнал клеточной науки. 118 (21): 4937–46. Дои:10.1242 / jcs.02671. PMID 16254241.
- ^ Амин Э., Джайсвал М., Деревенда У., Рейс К., Нури К., Кёссмайер К.Т., Аспенстрём П., Сомлио А.В., Дворский Р., Ахмадиан М.Р. (2016). «Расшифровка молекулярной и функциональной основы белков семейства RHOGAP: систематический подход к селективной инактивации белков семейства Rho». J Biol Chem. 291 (39): 20353–71. Дои:10.1074 / jbc.M116.736967. ЧВК 5034035. PMID 27481945.
- ^ Мэн Лю; И Чжэн (2012). «Регулирование Rho GTPase с помощью miRNA и ковалентных модификаций». Тенденции в клеточной биологии. 22 (7): 367–373. Дои:10.1016 / j.tcb.2012.04.004. ЧВК 3383930. PMID 22572609.
- ^ а б c Этьен-Манневиль S, зал A (2002). «Rho GTPases в клеточной биологии». Природа. 420 (6916): 629–35. Дои:10.1038 / природа01148. PMID 12478284.
- ^ а б Ридли, AJ; и другие. (2006). «Rho GTPases и динамика актина в мембранных выступах и перемещении пузырьков». Тенденции Cell Biol. 16 (10): 522–9. Дои:10.1016 / j.tcb.2006.08.006. PMID 16949823.
- ^ Ким, Чон-Хен; Лисман (1999). «Роль актиновой нити в синаптической передаче и долгосрочной потенциации». Журнал неврологии. 19 (11): 4314–4324. Дои:10.1523 / JNEUROSCI.19-11-04314.1999. PMID 10341235.
- ^ Krucker, T .; Siggins, G.R .; Халпаин, С. (23 мая 2000 г.). «Динамические актиновые филаменты необходимы для стабильной долговременной потенциации (ДП) в области СА1 гиппокампа». Труды Национальной академии наук. 97 (12): 6856–6861. Дои:10.1073 / pnas.100139797. ЧВК 18765. PMID 10823894.
- ^ Таширо, Аюму; Юсте, Рафаэль (1 июля 2004 г.). «Регуляция дендритной подвижности и стабильности позвоночника с помощью Rac1 и Rho киназы: данные о двух формах подвижности позвоночника». Молекулярная и клеточная неврология. 26 (3): 429–440. Дои:10.1016 / j.mcn.2004.04.001. PMID 15234347.
- ^ а б c d е ж Муракоши, Хидеджи; Ван, Хун; Ясуда, Рёхей (20 марта 2011 г.). «Локальная, стойкая активация Rho GTPases во время пластичности отдельных дендритных шипов». Природа. 472 (7341): 100–104. Дои:10.1038 / природа09823. ЧВК 3105377. PMID 21423166.
- ^ Касаи, Харуо; Мацудзаки, Масанори; Ногучи, Джун; Ясумацу, Нобуаки; Накахара, Хироюки (1 июля 2003 г.). «Взаимоотношения структура – стабильность – функция дендритных шипов». Тенденции в неврологии. 26 (7): 360–368. Дои:10.1016 / S0166-2236 (03) 00162-0. PMID 12850432.
- ^ Hotulainen, P .; Hoogenraad, C.C. (10 мая 2010 г.). «Актин в дендритных отростках: связь динамики с функцией». Журнал клеточной биологии. 189 (4): 619–629. Дои:10.1083 / jcb.201003008. ЧВК 2872912. PMID 20457765.
- ^ Поцелуй, C .; Li, J .; Szeles, A .; Гизатуллин, Р.З .; Кашуба В.И.; Лушникова, Т.Л .; Протопопов, А.И .; Kelve, M .; Поцелуй, H .; Холоднюк И.Д .; Irnreh, S .; Klein, G .; Забаровский, Э.Р. (1 января 1997 г.). «Отнесение генов ARHA и GPX1 к полосам хромосомы человека 3p21.3 путем гибридизации in situ и с гибридами соматических клеток». Цитогенетические и геномные исследования. 79 (3–4): 228–230. Дои:10.1159/000134729. PMID 9605859.
- ^ Скотт, Итан К .; Reuter, J .; Луо, Л. (11 апреля 2003 г.). «Малая GTPase Cdc42 необходима для множества аспектов морфогенеза дендритов». Журнал неврологии. 28 (8): 3118–3123. Дои:10.1523 / JNEUROSCI.23-08-03118.2003. ЧВК 6742332. PMID 12716918.
- ^ Калабрезе, Барбара; Wilson, M.S .; Халпаин, С. (1 февраля 2006 г.). «Развитие и регуляция дендритных синапсов позвоночника». Физиология. 21 (1): 38–47. Дои:10.1152 / Physiol.00042.2005. PMID 16443821.
- ^ Сакумура Й., Цукада Й., Ямамото Н., Исии С. (2005). «Молекулярная модель для управления аксоном, основанная на перекрестном взаимодействии между rho GTPases». Biophys J. 89 (2): 812–22. Дои:10.1529 / biophysj.104.055624. ЧВК 1366631. PMID 15923236.
- ^ Брок Дж., Мидвинтер К., Льюис Дж., Мартин П. (1996). «Заживление послеоперационной раны в зародышевом зачатке крыла цыпленка: характеристика актиновой кисетной нити и демонстрация потребности в активации Rho». J Cell Biol. 135 (4): 1097–107. Дои:10.1083 / jcb.135.4.1097. ЧВК 2133375. PMID 8922389.
- ^ Франц, Кристиан; Каридис, Анастасиос; Налбант, Перихан; Hahn, Klaus M .; Барбер, Дайан Л. (2007-11-05). «Положительная обратная связь между активностью Cdc42 и оттоком H + через обменник Na-H NHE1 для полярности мигрирующих клеток». Журнал клеточной биологии. 179 (3): 403–410. Дои:10.1083 / jcb.200704169. ISSN 0021-9525. ЧВК 2064788. PMID 17984318.
- ^ Нидерганг Ф., Шаврие П. (2005). Регуляция фагоцитоза Rho GTPases. Curr Top Microbiol Immunol. Актуальные темы микробиологии и иммунологии. 291. С. 43–60. Дои:10.1007/3-540-27511-8_4. ISBN 978-3-540-23865-2. PMID 15981459.
- ^ Нарумия С., Ясуда С. (2006). «Rho GTPases в митозе клеток животных». Curr Opin Cell Biol. 18 (2): 199–205. Дои:10.1016 / j.ceb.2006.02.002. PMID 16487696.
- ^ Джайн А., Брэди-Калнай С.М., Белламконда Р.В. (2004). «Модуляция активности Rho GTPase облегчает хондроитинсульфат протеогликан-зависимое ингибирование роста нейритов». J Neurosci Res. 77 (2): 299–307. Дои:10.1002 / jnr.20161. PMID 15211597.
- ^ Ramakers GJ. (2002). «Белки Rho, умственная отсталость и клеточные основы познания». Тенденции Neurosci. 25 (4): 191–9. Дои:10.1016 / S0166-2236 (00) 02118-4. PMID 11998687.
Несколько мутаций в белках Rho были идентифицированы при крупномасштабном секвенировании рака. Эти мутации перечислены в базе данных Каталог соматических мутаций (http://www.sanger.ac.uk/genetics/CGP/cosmic/ ). Функциональные последствия этих мутаций неизвестны.
