Dynamin - Dynamin
| Семья Dynamin | |||||||||
|---|---|---|---|---|---|---|---|---|---|
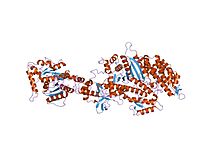 Структура безнуклеотидного моторного домена миозина II из Dictyostelium discoideum слит с доменом GTPase динамина I из Раттус норвегикус | |||||||||
| Идентификаторы | |||||||||
| Символ | Dynamin_N | ||||||||
| Pfam | PF00350 | ||||||||
| Pfam клан | CL0023 | ||||||||
| ИнтерПро | IPR001401 | ||||||||
| PROSITE | PDOC00362 | ||||||||
| |||||||||
| Dynamin центральный регион | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Структура безнуклеотидного моторного домена миозина II из Dictyostelium discoideum слит с доменом GTPase динамина I из Раттус норвегикус | |||||||||
| Идентификаторы | |||||||||
| Символ | Dynamin_M | ||||||||
| Pfam | PF01031 | ||||||||
| ИнтерПро | IPR000375 | ||||||||
| |||||||||
Dynamin это GTPase ответственный за эндоцитоз в эукариотической клетке. Динамин является частью «суперсемейства динаминов», которое включает классические динамины, динамин-подобные белки, Mx белки, OPA, митофузины, и фунты стерлингов. Члены семейства динаминов в основном участвуют в разделении вновь образованных пузырьки от мембраны одного клеточного компартмента и их нацеливания на другой компартмент и слияние с ним, как на поверхности клетки (в частности, кавеолы интернализация), а также аппарат Гольджи.[1][2][3] Члены семейства Dynamin также играют роль во многих процессах, включая разделение органеллы,[4] цитокинез и микробный возбудитель сопротивление.
Структура
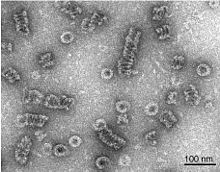
Сам Dynamin - 96 кДа фермент, и впервые был изолирован, когда исследователи пытались выделить новые микротрубочка моторы из бычьего мозга. Динамин широко изучался в контексте клатрин покрытые оболочкой пузырьки, отрастающие от клеточная мембрана.[3][6] Начиная с N-конца, Dynamin состоит из домена GTPase, соединенного со спиральным стержневым доменом через гибкую шейку, содержащую сигнальный элемент Bundle и Эффекторный домен GTPase. На противоположном конце стеблевого домена находится петля, которая связывается с мембраной. Домен гомологии плекстрина. Затем белковая цепь возвращается к домену GTPase и заканчивается Пролин богатый домен что привязано к Src области гомологии многих белков.
Функция
Во время опосредованного клатрином эндоцитоза клеточная мембрана инвагинирует, образуя почкующийся пузырек. Dynamin связывается и собирается вокруг шейки эндоцитарной везикулы, образуя спиральный полимер, расположенный так, что домены GTPase димеризуются асимметричным образом по спиральным ступеням.[7][8] Полимер сжимает нижележащую мембрану при Связывание и гидролиз GTP через конформационные изменения, происходящие из области гибкой шейки, которая изменяет общую спиральную симметрию.[8] Сужение шейки везикулы приводит к образованию состояния мембраны полуделения, что в конечном итоге приводит к разрыву мембраны.[2][6][9] Сужение может быть частично результатом скручивающей активности динамина, которая делает динамин единственным молекулярный мотор известно, что имеет скручивающую активность.[10]
Типы
У млекопитающих были идентифицированы три разных гена динамина с ключевыми различиями последовательностей в их доменах гомологии плэкстрина, что привело к различиям в распознавании липидных мембран:
- Dynamin I выражается в нейроны и нейроэндокринные клетки
- Dynamin II экспрессируется в большинстве типов клеток
- Dynamin III сильно выражен в яичко, но также присутствует в сердце, мозг, и легкое ткань.[1][6]
Последствия болезни
Мутации в Dynamin II было обнаружено, что они вызывают доминирующие промежуточные Болезнь Шарко-Мари-Тута.[11]Было высказано предположение, что вызывающие эпилептическую энцефалопатию мутации de novo в динамине вызывают дисфункцию рассечения везикул во время эндоцитоза синаптических везикул.[12]
Рекомендации
- ^ а б Хенли-младший, Цао Х., МакНивен Массачусетс (декабрь 1999 г.). «Участие динамина в биогенезе цитоплазматических везикул». Журнал FASEB. 13 Приложение 2 (9002): S243-7. Дои:10.1096 / fasebj.13.9002.S243. PMID 10619136.
- ^ а б Хиншоу, Дж. «Заявление об исследовании, Дженни Э. Хиншоу, доктор философии». Национальный институт диабета, болезней органов пищеварения и почек, лаборатория биохимии и биологии клетки. По состоянию на 19 марта 2013 г.
- ^ а б Уррутия Р., Хенли-младший, Кук Т., МакНивен Массачусетс (январь 1997 г.). «Динамины: избыточные или отдельные функции для расширяющегося семейства родственных GTPases?». Труды Национальной академии наук Соединенных Штатов Америки. 94 (2): 377–84. Дои:10.1073 / пнас.94.2.377. ЧВК 34135. PMID 9012790.
- ^ Томс С., Эрдманн Р. (октябрь 2005 г.). «Родственные динамину белки и белки Pex11 в делении и пролиферации пероксисом». Журнал FEBS. 272 (20): 5169–81. Дои:10.1111 / j.1742-4658.2005.04939.x. PMID 16218949.
- ^ Хиншоу Дж. Э., Шмид С. Л. (март 1995 г.). «Dynamin самособирается в кольца, предлагая механизм отпочкования покрытых пузырьков». Природа. 374 (6518): 190–2. Дои:10.1038 / 374190a0. PMID 7877694. S2CID 4365628.
- ^ а б c Praefcke GJ, McMahon HT (февраль 2004 г.). «Суперсемейство динаминов: универсальные мембранные трубочки и молекулы деления?». Обзоры природы Молекулярная клеточная биология. 5 (2): 133–47. Дои:10.1038 / nrm1313. PMID 15040446. S2CID 6305282. Сложить резюме – Домашняя страница Dynamin.
- ^ Сандборгер А.С., Фанг С., Хейманн Дж. А., Рэй П., Чаппи Дж. С., Хиншоу Дж. Э. (август 2014 г.). «Мутант динамина определяет сверхсуженное состояние перед делением». Отчеты по ячейкам. 8 (3): 734–42. Дои:10.1016 / j.celrep.2014.06.054. ЧВК 4142656. PMID 25088425.
- ^ а б Конг Л., Сохацкий К.А., Ван Х., Фанг С., Канагараджа Б., Кехр А.Д., Райс В.Дж., Страб М.П., Тараска Д.В., Хиншоу Д.Э. (август 2018 г.). «Крио-ЭМ динаминового полимера, собранного на липидной мембране». Природа. 560 (7717): 258–262. Дои:10.1038 / s41586-018-0378-6. ЧВК 6121775. PMID 30069048.
- ^ Маттила Дж. П., Шнырова А. В., Сундборгер А. С., Хортелано Э. Р., Фурманс М., Нойманн С., Мюллер М., Хиншоу Дж. Э., Шмид С. Л., Фролов В. А. (август 2015 г.). «Промежуточное звено полураспада связывает две механически различные стадии мембранного деления». Природа. 524 (7563): 109–113. Дои:10.1038 / природа14509. ЧВК 4529379. PMID 26123023.
- ^ Ру А., Уйхази К., Фрост А., Де Камилли П. (май 2006 г.). «GTP-зависимое скручивание динамина подразумевает сжатие и напряжение в делении мембраны». Природа. 441 (7092): 528–31. Дои:10.1038 / природа04718. PMID 16648839. S2CID 4413887.
- ^ Цюхнер С., Нуреддин М., Кеннерсон М., Верховен К., Клэйс К., Де Йонге П. и др. (Март 2005 г.). «Мутации в домене гомологии плекстрина динамина 2 вызывают доминантную промежуточную болезнь Шарко-Мари-Тута». Природа Генетика. 37 (3): 289–94. Дои:10,1038 / ng1514. PMID 15731758. S2CID 19191581.
- ^ Дхиндса Р.С., Брэдрик С.С., Яо Х, Хайнцен Е.Л., Петровски С., Крюгер Б.Дж., Джонсон М.Р., Франкель В.Н., Петру С., Бумиль Р.М., Голдштейн Д.Б. (июнь 2015 г.). «Мутации DNM1, вызывающие эпилептическую энцефалопатию, нарушают эндоцитоз синаптических везикул». Неврология. Генетика. 1 (1): e4. Дои:10.1212 / 01.NXG.0000464295.65736.da. ЧВК 4821085. PMID 27066543.
внешняя ссылка
- Dynamins в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
