ANK1 - ANK1
Анкирин 1, эритроцитарный, также известный как ANK1, это белок что у людей кодируется ANK1 ген.[5][6]
Распределение тканей
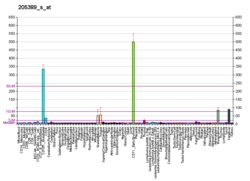
В белок кодируемый этим геном, Анкирин 1, является прототипом анкирин семья, была впервые обнаружена в эритроциты, но с тех пор также был обнаружен в мозге и мышцах.[6]
Генетика
Сложные альтернативные модели сращивание в сфере регулирования, что порождает различные изоформы анкирина 1 были описаны, однако точные функции различных изоформ не известны. Альтернатива полиаденилирование также сообщалось о мРНК эритроцитарного анкирина-1 разного размера. Усеченные мышечно-специфичные изоформы анкирина 1 в результате использования альтернативного промоутер также были идентифицированы.[6]
Связь с заболеванием
Мутации в эритроцитарном анкирине 1 были связаны примерно у половины всех пациентов с наследственным сфероцитоз.[6]
ANK1 показывает измененное метилирование и экспрессию при болезни Альцгеймера.[7][8] Исследование экспрессии генов в головном мозге после смерти показало, что ANK1 взаимодействует с интерферон-γ сигнализация.[9]
Функция
Белок ANK1 относится к анкирин семья, которая считается связующим звеном мембранные белки к основному спектрин -актин цитоскелет и играют ключевую роль в таких действиях, как клеточная подвижность, активация, пролиферация, контакт и поддержание специализированных мембранных доменов. Множественные изоформы анкирина с различным сродством к различным целевым белкам экспрессируются тканеспецифичным, регулируемым в процессе развития образом. Большинство анкиринов обычно состоят из трех структурных доменов: аминоконцевой домен, содержащий несколько анкириновых повторов; центральная область с высококонсервативным спектрин-связывающим доменом; и карбокси-концевой регуляторный домен, который наименее консервативен и подвержен вариациям.[6]
Варианты сплайсинга небольших белков ANK1 (sAnk1) контактируют с скрывать, гигантский белок, окружающий сократительный аппарат в поперечно-полосатые мышцы.[10]
Взаимодействия
ANK1 был показан взаимодействовать с Инвазия Т-клеточной лимфомы и белок 1, вызывающий метастазирование,[11] Титин,[12] RHAG[13] и OBSCN.[14]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000029534 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000031543 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Ламберт С., Ю Х, Прчал Дж. Т. и др. (Март 1990 г.). «последовательность кДНК анкирина эритроцитов человека». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 87 (5): 1730–4. Bibcode:1990PNAS ... 87.1730L. Дои:10.1073 / pnas.87.5.1730. ЧВК 53556. PMID 1689849.
- ^ а б c d е «Энтрез Ген: ANK1 анкирин 1, эритроцитарный».
- ^ De Jager, P. L .; Шривастава, G; Lunnon, K; Берджесс, Дж; Schalkwyk, L.C .; Ю, Л; Eaton, M. L .; Keenan, B.T .; Эрнст, Дж; МакКейб, К; Тан, А; Радж, Т; Реплогл, Дж; Brodeur, W; Габриэль, S; Chai, H. S .; Юнкин, К; Юнкин, С.Г .; Zou, F; Шиф, М; Epstein, C.B .; Schneider, J. A .; Bernstein, B.E .; Мейснер, А; Эртекин-Танер, Н; Чибник, Л. Б .; Келлис, М; Милл, Дж; Беннетт, Д. А. (2014). «Болезнь Альцгеймера: ранние изменения метилирования ДНК головного мозга в ANK1, BIN1, RHBDF2 и других локусах». Природа Неврология. 17 (9): 1156–63. Дои:10.1038 / номер 3786. ЧВК 4292795. PMID 25129075.
- ^ Lunnon, K; Smith, R; Hannon, E; De Jager, P. L .; Шривастава, G; Вольта, М; Троакс, С; Ас-Саррадж, S; Burrage, Дж; Макдональд, Р. Кондлифф, Д; Harries, L.W .; Кацель, П; Арутюнян, В; Каминский, З .; Иоахим, C; Пауэлл, Дж; Лавстон, S; Bennett, D.A .; Schalkwyk, L.C .; Милл, Дж (2014). «Метиломное профилирование подразумевает корковое нарушение регуляции ANK1 при болезни Альцгеймера». Природа Неврология. 17 (9): 1164–70. Дои:10.1038 / № 3782. ЧВК 4410018. PMID 25129077.
- ^ Лискович, N; Французский, L (2014). «Дифференциальная коэкспрессия между сигнальными генами α-синуклеина и IFN-γ в процессе развития и при болезни Паркинсона». PLOS ONE. 9 (12): e115029. Bibcode:2014PLoSO ... 9k5029L. Дои:10.1371 / journal.pone.0115029. ЧВК 4262449. PMID 25493648.
- ^ Борзок М.А., Катино Д.Х., Николсон Д.Д., Контроджианни-Константопулос А., Блох Р.Дж. (ноябрь 2007 г.). «Картирование сайта связывания на малом анкирине 1 для обскурина». J. Biol. Chem. 282 (44): 32384–96. Дои:10.1074 / jbc.M704089200. PMID 17720975.
- ^ Бургиньон, Луизиана; Zhu H; Shao L; Chen Y W (июль 2000 г.). «Взаимодействие анкирин-Tiam1 способствует передаче сигналов Rac1, а также инвазии и миграции метастатических клеток опухоли молочной железы». J. Cell Biol. 150 (1): 177–91. Дои:10.1083 / jcb.150.1.177. ISSN 0021-9525. ЧВК 2185563. PMID 10893266.
- ^ Контржианни-Константопулос, Айкатерини; Блох Роберт Дж (февраль 2003 г.). «Гидрофильный домен малого анкирина-1 взаимодействует с двумя N-концевыми иммуноглобулиновыми доменами тайтина». J. Biol. Chem. 278 (6): 3985–91. Дои:10.1074 / jbc.M209012200. ISSN 0021-9258. PMID 12444090.
- ^ Николас, Вирджиния; Ле Ван Ким, Кэролайн; Гане, Пьер; Биркенмайер, Конни; Картрон, Жан-Пьер; Колин, Ив; Муро-Шантелуп, Изабель (июль 2003 г.). «Rh-RhAG / анкирин-R, новый сайт взаимодействия между бислоем мембраны и скелетом эритроцитов, нарушен мутацией, ассоциированной с Rh (нуль)». J. Biol. Chem. 278 (28): 25526–33. Дои:10.1074 / jbc.M302816200. ISSN 0021-9258. PMID 12719424.
- ^ Контржианни-Константопулос, Айкатерини; Джонс Эллен М; Ван Россум Дамиан Б; Блох Роберт Дж (март 2003 г.). «Обскурин - лиганд малого анкирина 1 в скелетных мышцах». Мол. Биол. Клетка. 14 (3): 1138–48. Дои:10.1091 / mbc.E02-07-0411. ISSN 1059-1524. ЧВК 151585. PMID 12631729.
дальнейшее чтение
- Беннетт В., Бейнс А.Дж. (2001). «Спектрин и анкириновые пути: изобретения многоклеточных животных для интеграции клеток в ткани». Physiol. Rev. 81 (3): 1353–92. Дои:10.1152 / Physrev.2001.81.3.1353. PMID 11427698.
- Беннетт V (1979). «Иммунореактивные формы анкирина эритроцитов человека присутствуют в различных клетках и тканях». Природа. 281 (5732): 597–9. Bibcode:1979Натура.281..597Б. Дои:10.1038 / 281597a0. PMID 492324. S2CID 263106.
- Ламберт С., Ю Х, Прчал Дж. Т. и др. (1990). «последовательность кДНК анкирина эритроцитов человека». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 87 (5): 1730–4. Bibcode:1990PNAS ... 87.1730L. Дои:10.1073 / pnas.87.5.1730. ЧВК 53556. PMID 1689849.
- Фудзимото Т., Ли К., Мива С., Огава К. (1991). «Иммуноцитохимическая локализация фодрина и анкирина в хромаффинных клетках крупного рогатого скота in vitro».. J. Histochem. Cytochem. 39 (11): 1485–93. Дои:10.1177/39.11.1833445. PMID 1833445.
- Люкс SE, Джон К.М., Беннетт В. (1990). «Анализ кДНК анкирина эритроцитов человека указывает на повторяющуюся структуру с гомологией с белками тканевой дифференцировки и контроля клеточного цикла». Природа. 344 (6261): 36–42. Bibcode:1990Натура 344 ... 36л. Дои:10.1038 / 344036a0. PMID 2137557. S2CID 4351060.
- Дэвис LH, Беннет V (1990). «Картирование сайтов связывания анкирина эритроцитов человека для анионита и спектрина». J. Biol. Chem. 265 (18): 10589–96. PMID 2141335.
- Корсгрен C, Коэн CM (1988). «Ассоциации полосы эритроцитов человека 4.2. Связывание с анкирином и цитоплазматическим доменом полосы 3». J. Biol. Chem. 263 (21): 10212–8. PMID 2968981.
- Cianci CD, Giorgi M, Morrow JS (1988). «Фосфорилирование анкирина подавляет его кооперативное взаимодействие со спектрином и белком 3». J. Cell. Биохим. 37 (3): 301–15. Дои:10.1002 / jcb.240370305. PMID 2970468. S2CID 42349239.
- Штайнер Дж. П., Беннетт В. (1988). «Анкирин-независимые мембранные белки-связывающие сайты для спектрина мозга и эритроцитов». J. Biol. Chem. 263 (28): 14417–25. PMID 2971657.
- Харгривз WR, Гедд KN, Verkleij A, Branton D (1981). «Реассоциация анкирина с полосой 3 в мембранах эритроцитов и в липидных пузырьках». J. Biol. Chem. 255 (24): 11965–72. PMID 6449514.
- Бургиньон Л. Я., Локешвар В. Б., Чен Х, Керрик В. Г. (1994). «Индуцированная гиалуроновой кислотой передача сигнала лимфоцитов и взаимодействие рецептора НА (GP85 / CD44) с цитоскелетом». J. Immunol. 151 (12): 6634–44. PMID 7505012.
- Маруяма К., Сугано С. (1994). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Ген. 138 (1–2): 171–4. Дои:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Морганс К. В., Копито Р. Р. (1993). «Ассоциация мозгового анионита, AE3, с повторяющимся доменом анкирина». J. Cell Sci. 105. (Pt 4): 1137–42. PMID 8227202.
- Bourguignon LY, Jin H, Iida N и др. (1993). «Участие анкирина в регуляции опосредованного инозитол-1,4,5-трифосфатным рецептором внутреннего высвобождения Са2 + из запасных везикул Са2 + в клетках Т-лимфомы мышей». J. Biol. Chem. 268 (10): 7290–7. PMID 8385102.
- Эбер С.В., Гонсалес Дж.М., Люкс М.Л. и др. (1996). «Мутации анкирина-1 являются основной причиной доминантного и рецессивного наследственного сфероцитоза». Nat. Genet. 13 (2): 214–8. Дои:10.1038 / ng0696-214. PMID 8640229. S2CID 10946374.
- Ланфранчи Г., Мураро Т., Калдара Ф. и др. (1996). «Идентификация 4370 экспрессируемых тегов последовательности из библиотеки кДНК, специфичной для 3'-конца, скелетных мышц человека путем секвенирования ДНК и гибридизации с фильтром». Genome Res. 6 (1): 35–42. Дои:10.1101 / гр.6.1.35. PMID 8681137.
- дель Джудиче Е.М., Хайетт С., Бозон М. и др. (1996). «Анкирин Наполи: делеционная мутация сдвига рамки считывания de novo в экзоне 16 гена анкирина (ANK1), связанная со сфероцитозом». Br. J. Haematol. 93 (4): 828–34. Дои:10.1046 / j.1365-2141.1996.d01-1746.x. PMID 8703812. S2CID 28906962.
- Чжоу Д., Биркенмайер С.С., Уильямс М.В. и др. (1997). «Небольшие мембраносвязанные, альтернативно сплайсированные формы анкирина 1, связанные с саркоплазматическим ретикулумом скелетных мышц млекопитающих». J. Cell Biol. 136 (3): 621–31. Дои:10.1083 / jcb.136.3.621. ЧВК 2134284. PMID 9024692.
- Галлахер П.Г., Це В.Т., Скарпа А.Л. и др. (1997). «Структура и организация гена анкирина-1 человека. Основа сложности обработки пре-мРНК». J. Biol. Chem. 272 (31): 19220–8. Дои:10.1074 / jbc.272.31.19220. PMID 9235914.
- Судзуки Ю., Ёситомо-Накагава К., Маруяма К. и др. (1997). «Создание и характеристика полноразмерной библиотеки кДНК, обогащенной по 5'-концу». Ген. 200 (1–2): 149–56. Дои:10.1016 / S0378-1119 (97) 00411-3. PMID 9373149.
внешняя ссылка
- ANK1 + белок, + человеческий в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Человек ANK1 расположение генома и ANK1 страница сведений о генах в Браузер генома UCSC.
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.