Анкирин - Ankyrin
| АНК1, эритроцитарный | |||||||
|---|---|---|---|---|---|---|---|
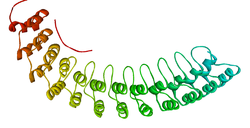 Ленточная диаграмма фрагмента мембрансвязывающего домена анкирина R.[1] | |||||||
| Идентификаторы | |||||||
| Символ | ANK1 | ||||||
| Альт. символы | AnkyrinR, Band2.1 | ||||||
| Ген NCBI | 286 | ||||||
| HGNC | 492 | ||||||
| OMIM | 182900 | ||||||
| PDB | 1N11 | ||||||
| RefSeq | NM_000037 | ||||||
| UniProt | P16157 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 8 п21.1-11.2 | ||||||
| |||||||
| Анкирин повторяется | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | Анк | ||||||||
| Pfam | PF00023 | ||||||||
| ИнтерПро | IPR002110 | ||||||||
| УМНАЯ | SM00248 | ||||||||
| PROSITE | PDOC50088 | ||||||||
| SCOP2 | 1awc / Объем / СУПФАМ | ||||||||
| |||||||||
| ANK2, нейронный | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | ANK2 | ||||||
| Альт. символы | АнкиринБ | ||||||
| Ген NCBI | 287 | ||||||
| HGNC | 493 | ||||||
| OMIM | 106410 | ||||||
| RefSeq | NM_001148 | ||||||
| UniProt | Q01484 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 4 q25-q27 | ||||||
| |||||||
| ANK3, узел Ранвье | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | ANK3 | ||||||
| Альт. символы | АнкиринГ | ||||||
| Ген NCBI | 288 | ||||||
| HGNC | 494 | ||||||
| OMIM | 600465 | ||||||
| RefSeq | NM_020987 | ||||||
| UniProt | Q12955 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 10 q21 | ||||||
| |||||||
Анкирины представляют собой семейство белков, которые опосредуют прикрепление интегральные мембранные белки к спектрин -актин в основе мембранного цитоскелета.[2] Анкирины имеют сайты связывания для бета-субъединицы спектрина и по крайней мере 12 семейств интегральных мембранных белков. Эта связь требуется для поддержания целостности плазматические мембраны и привязать конкретные ионные каналы, ионообменники и ионные транспортеры в плазматической мембране. Название происходит от греческого слова «слитый».[нужна цитата ]
Структура
Анкирины содержат четыре функциональных домены: N-концевой домен, содержащий 24 тандема Анкирин повторяет, центральный домен, который связывается с спектрин, домен смерти, который связывается с белками, участвующими в апоптоз и С-концевой регуляторный домен, который сильно варьирует между разными анкириновыми белками.[2]
Распознавание мембранных белков
24 тандемных анкириновых повтора ответственны за распознавание широкого спектра мембранных белков. Эти 24 повтора содержат 3 структурно различных сайта связывания в диапазоне от 1 до 14 повторов. Эти сайты связывания квазинезависимы друг от друга и могут использоваться в комбинации. Взаимодействия, которые сайты используют для связывания с мембранными белками, неспецифичны и состоят из водородных связей, гидрофобных взаимодействий и электростатических взаимодействий. Эти неспецифические взаимодействия придают анкирину свойство распознавать широкий спектр белков, поскольку последовательность не должна сохраняться, а только свойства аминокислоты. Квазинезависимость означает, что если сайт связывания не используется, он не окажет большого влияния на общее связывание. Эти два свойства в сочетании дают начало большому репертуару белков, которые может распознавать анкирин.
Подтипы
Анкирины кодируются тремя генами (ANK1, ANK2 и ANK3 ) у млекопитающих. Каждый ген, в свою очередь, производит несколько белков посредством альтернативное сращивание.
ANK1
В ANK1 Ген кодирует белки AnkyrinR. AnkyrinR был впервые охарактеризован в эритроцитах человека, где этот анкирин был обозначен как анкирин эритроцитов или band2.1.[3] AnkyrinR позволяет эритроцитам противостоять силам сдвига, возникающим в кровотоке. Люди с пониженным или дефектным анкирином R имеют форму гемолитическая анемия названный наследственный сфероцитоз.[4] В эритроцитах AnkyrinR связывает мембранный скелет с Cl−/ HCO3− анионообменник.[5]
Анкирин 1 связывает мембранный рецептор CD44 к инозитолтрифосфатный рецептор и цитоскелет.[6]
Было высказано предположение, что Анкирин 1 взаимодействует с КАХРП (показано с помощью выборочных раскрывающихся списков, SPR и ELISA ).[7]
ANK2

Впоследствии белки анкиринB (продукты ANK2 ген[8]) были обнаружены в мозге и мышцах. Белки AnkyrinB и AnkyrinG необходимы для поляризованного распределения многих мембранных белков, включая Na+/ К+ АТФаза, напряжение закрытого Na+ канал и Na+/ Ca2+ обменник.
ANK3
Белки AnkyrinG (продукты ANK3 ген[9]) были идентифицированы в эпителиальных клетках и нейронах. Крупномасштабный генетический анализ, проведенный в 2008 году, показывает возможность того, что ANK3 участвует в биполярное расстройство.[10][11]
Смотрите также
- DARPin (разработанный белок анкириновых повторов), сконструированный миметик антитела, основанный на структуре анкириновых повторов
Рекомендации
- ^ PDB: 1N11; Микаэли П., Томчик Д. Р., Мачиус М., Андерсон Р. Г. (декабрь 2002 г.). "Кристаллическая структура стека из 12 повторов ANK анкирина человека". Журнал EMBO. 21 (23): 6387–96. Дои:10.1093 / emboj / cdf651. ЧВК 136955. PMID 12456646.
- ^ а б Беннетт В., Бейнс А.Дж. (июль 2001 г.). «Спектрин и анкириновые пути: изобретения многоклеточных животных для интеграции клеток в ткани». Физиологические обзоры. 81 (3): 1353–92. Дои:10.1152 / Physrev.2001.81.3.1353. PMID 11427698.
- ^ Беннет В., Стенбак П.Дж. (апрель 1979 г.). «Идентификация и частичная очистка анкирина, высокоаффинного участка прикрепления к мембране спектрина эритроцитов человека». Журнал биологической химии. 254 (7): 2533–41. PMID 372182.
- ^ Lux SE, Tse WT, Menninger JC, John KM, Harris P, Shalev O, Chilcote RR, Marchesi SL, Watkins PC, Bennett V (июнь 1990 г.). «Наследственный сфероцитоз, связанный с делецией гена анкирина эритроцитов человека на 8-й хромосоме». Природа. 345 (6277): 736–9. Bibcode:1990Натура.345..736л. Дои:10.1038 / 345736a0. PMID 2141669. S2CID 4334791.
- ^ Беннет В., Стенбак П.Дж. (август 1979 г.). «Белок прикрепления к мембране для спектрина связан с полосой 3 в мембранах эритроцитов человека». Природа. 280 (5722): 468–73. Bibcode:1979Натура.280..468Б. Дои:10.1038 / 280468a0. PMID 379653. S2CID 4268702.
- ^ Синглтон, Пенсильвания, Бургиньон, ЛЮ (апрель 2004 г.). «Взаимодействие CD44 с анкирином и рецептором IP3 в липидных рафтах способствует передаче сигналов Са2 +, опосредованной гиалуронаном, что приводит к продукции оксида азота и адгезии и пролиферации эндотелиальных клеток». Экспериментальные исследования клеток. 295 (1): 102–18. Дои:10.1016 / j.yexcr.2003.12.025. PMID 15051494.
- ^ Вен Х, Го Х, Папоин Дж, Ван Дж, Коппель Р., Мохандас Н., Ан Х (январь 2014 г.). «Взаимодействие белка, богатого гистидином, богатого гистидином (KAHRP) Plasmodium falciparum, с анкирином R эритроцитов необходимо для его прикрепления к мембране эритроцитов». Biochimica et Biophysica Acta (BBA) - Биомембраны. 1838 (1 балл B): 185–92. Дои:10.1016 / j.bbamem.2013.09.014. ЧВК 4403245. PMID 24090929.
- ^ Schott JJ, Charpentier F, Peltier S, Foley P, Drouin E, Bouhour JB, Donnelly P, Vergnaud G, Bachner L, Moisan JP (ноябрь 1995 г.). «Картирование гена синдрома удлиненного интервала QT на хромосоме 4q25-27». Американский журнал генетики человека. 57 (5): 1114–22. ЧВК 1801360. PMID 7485162.
- ^ Капфхамер Д., Миллер Д.Е., Ламберт С., Беннет В., Гловер Т.В., Бурмейстер М. (май 1995 г.). «Хромосомная локализация гена ankyrinG (ANK3 / Ank3) для человеческого 10q21 и мыши 10». Геномика. 27 (1): 189–91. Дои:10.1006 / geno.1995.1023. PMID 7665168.
- ^ Феррейра М.А., О'Донован М.С., Мэн Ю.А., Джонс И.Р., Рудерфер Д.М., Джонс Л. и др. (Сентябрь 2008 г.). «Совместный анализ ассоциаций всего генома подтверждает роль ANK3 и CACNA1C в биполярном расстройстве». Природа Генетика. 40 (9): 1056–8. Дои:10,1038 / нг.209. ЧВК 2703780. PMID 18711365.
- ^ "Направление психических заболеваний: GWAS связывает ионные каналы, биполярное расстройство". Форум по исследованию шизофрении: Новости. schizophreniaforum.org. 2008-08-19. Архивировано из оригинал на 2010-12-18. Получено 2008-08-21.
внешняя ссылка
- Анкирины в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Протеопедия 1n11 Анкирин-Р
