Миозин - Myosin
Миозины (/ˈмаɪəsɪп,-oʊ-/[1][2]) площадь надсемейство из моторные белки наиболее известен своими ролями в сокращение мышц и в большом количестве других подвижность процессы в эукариоты. Они есть АТФ -зависимый и ответственный за актин моторика. Этот термин изначально использовался для описания группы похожих АТФазы найдено в клетки обоих поперечно-полосатая мышечная ткань и гладкая мышечная ткань.[3] После открытия Поллардом и Корном (1973) ферментов с миозиноподобной функцией в Acanthamoeba castellanii, глобальный диапазон дивергентного миозина гены были обнаружены повсюду в мире эукариот.
Хотя первоначально считалось, что миозин ограничен мышечными клетками (отсюда мио- (s) + -в ) нет единственного миозина; скорее это очень большое суперсемейство генов, белковые продукты которых имеют общие свойства связывания актина, АТФ гидролиз (Активность фермента АТФазы) и силовая трансдукция. Практически все эукариотические клетки содержат миозин. изоформы. Некоторые изоформы выполняют специализированные функции в определенных типах клеток (например, в мышцах), в то время как другие изоформы встречаются повсеместно. Структура и функция миозина глобально сохранены у разных видов до такой степени, что миозин II из мышц кролика будет связываться с актином из амеба.[4]
Структура и функции
Домены
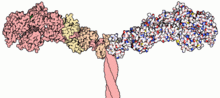
Большинство молекул миозина состоит из голова, область шеи и хвоста.
- В главный домен связывает нитевидные актин, и использует АТФ гидролиз для создания силы и «ходьбы» вдоль нити к зазубренному (+) концу (за исключением миозина VI, который движется к заостренному (-) концу).
- то область шеи действует как линкер и как плечо рычага для передачи силы, создаваемой каталитическим моторным доменом. Шейный домен также может служить сайтом связывания миозина. легкие цепи которые представляют собой отдельные белки, которые образуют часть макромолекулярного комплекса и обычно выполняют регуляторные функции.
- В хвостовая область обычно опосредует взаимодействие с молекулами груза и / или другим миозином подразделения. В некоторых случаях хвостовой домен может играть роль в регуляции двигательной активности.
Рабочий ход
Множественные молекулы миозина II создают силу в скелетная мышца через механизм рабочего хода, питаемый энергией, высвобождаемой при гидролизе АТФ.[5] Силовой удар происходит при высвобождении фосфата из молекулы миозина после гидролиза АТФ, в то время как миозин прочно связан с актином. Эффект этого высвобождения - конформационное изменение в молекуле, которая противодействует актину. Высвобождение молекулы АДФ приводит к так называемому состоянию окоченения миозина.[6] Связывание новой молекулы АТФ высвобождает миозин из актина. Гидролиз АТФ внутри миозина заставляет его снова связываться с актином, чтобы повторить цикл. Комбинированный эффект множества силовых ударов заставляет мышцу сокращаться.
Номенклатура, эволюция и генеалогическое древо

Широкое разнообразие генов миозина, обнаруженных во всех типах эукариот, было названо в соответствии с разными схемами по мере их открытия. Поэтому номенклатура может несколько сбивать с толку при попытке сравнить функции белков миозина внутри организмов и между ними.
Миозин скелетных мышц, наиболее заметный из суперсемейства миозинов из-за его обилия в мышечные волокна, был обнаружен первым. Этот белок составляет часть саркомера и образует макромолекулярные филаменты, состоящие из множества субъединиц миозина. Подобные белки миозина, образующие нити, были обнаружены в сердечной мышце, гладких мышцах и немышечных клетках. Однако, начиная с 1970-х годов, исследователи начали открывать новые гены миозина у простых эукариот.[3] кодирующие белки, которые действовали как мономеры и поэтому были названы миозинами класса I. Эти новые миозины получили общее название «нетрадиционные миозины».[7] и были обнаружены во многих тканях, кроме мышц. Эти новые члены суперсемейства были сгруппированы в соответствии с филогенетическими отношениями, полученными из сравнения аминокислотных последовательностей их головных доменов, при этом каждому классу был присвоен определенный класс. Римская цифра[8][9][10][11] (см. филогенетическое древо). Нетрадиционные миозины также имеют дивергентные хвостовые домены, предполагающие уникальные функции.[12] Разнообразный ныне массив миозинов, вероятно, произошел от предков. предшественник (см. рисунок).
Анализ аминокислотных последовательностей различных миозинов показывает большую вариабельность хвостовых доменов, но сильную консервацию последовательностей головных доменов. Предположительно, это так, что миозины могут взаимодействовать через свои хвосты с большим количеством различных грузов, в то время как цель в каждом случае - двигаться по актиновым филаментам - остается той же самой и, следовательно, требует того же механизма в двигателе. Например, человеческий геном содержит более 40 различных миозинов гены.
Эти различия в форме также определяют скорость, с которой миозины могут перемещаться по актиновым филаментам. Гидролиз АТФ и последующее высвобождение фосфат Группа вызывает «силовой удар», при котором «плечо рычага» или «шея» тяжелой цепи тянут вперед. Поскольку рабочий ход всегда перемещает плечо рычага на один и тот же угол, длина плеча рычага определяет смещение груза относительно актиновой нити. Более длинное плечо рычага заставит груз перемещаться на большее расстояние, даже если плечо рычага подвергается одинаковому угловому смещению - так же, как человек с более длинными ногами может перемещаться дальше с каждым отдельным шагом. Скорость миозинового двигателя зависит от скорости, с которой он проходит полный кинетический цикл связывания АТФ с высвобождением АДФ.
Классы миозина
Миозин I
Миозин I, повсеместно распространенный клеточный белок, функционирует как мономер и функционирует в везикул транспорт.[13] Он имеет размер шага 10 нм и считается ответственным за адаптационную реакцию стереоцилий во внутреннем ухе.[14]
Миозин II

Миозин II (также известный как обычный миозин) - это тип миозина, ответственный за производство сокращение мышц в мышечные клетки в большинстве типов клеток животных. Он также обнаружен в немышечных клетках сократительных пучков, называемых стрессовые волокна.[15]
- Миозин II содержит два тяжелые цепи, каждая около 2000 аминокислоты длины, которые составляют головную и хвостовую области. Каждая из этих тяжелых цепей содержит N-концевой главный домен, в то время как C-терминал хвосты берут на себя спиральная катушка морфологии, удерживая две тяжелые цепи вместе (представьте себе двух змей, обвивающих друг друга, как в кадуцей ). Таким образом, миозин II имеет две головки. Промежуточный шея домен - это область, образующая угол между головой и хвостом.[16] В гладкой мускулатуре единственный ген (MYH11[17]) кодирует тяжелые цепи миозина II, но варианты стыковки этого гена приводят к четырем различным изоформам.[16]
- Он также содержит 4 легкие цепи миозина (MLC), в результате получается 2 на голову, весом 20 (MLC20) и 17 (MLC17) кДа.[16] Они связывают тяжелые цепи в области «шеи» между головой и хвостом.
- MLC20 также известен как регуляторная легкая цепь и активно участвует в сокращение мышц.[16]
- MLC17 также известен как основная легкая цепь.[16] Его точная функция неясна, но считается, что он способствует структурной стабильности миозиновой головки вместе с MLC.20.[16] Два варианта MLC17 (MLC17а / б) существуют в результате альтернативное сращивание в MLC17 ген.[16]
В мышечных клетках длинный спиральная катушка хвосты отдельных молекул миозина соединяются вместе, образуя толстые волокна саркомер. Выделяющие силу домены головки выступают со стороны толстой нити, готовые пройти вдоль соседних тонких нитей на основе актина в ответ на соответствующие химические сигналы.
Миозин III
Миозин III - плохо изученный член семейства миозинов. Было изучено in vivo в глазах Дрозофила, где считается, что он играет роль в фототрансдукция.[18] Человек гомолог ген миозина III, MYO3A, был обнаружен через Проект "Геном человека" и выражается в сетчатка и улитка.[19]
Миозин IV
Миозин IV имеет единственный мотив IQ и хвост, в котором отсутствует какая-либо последовательность, образующая спиральную спираль. Он имеет гомологию, аналогичную хвостовым доменам миозина VII и XV.[20]
Миозин V

Миозин V - это нетрадиционный миозиновый мотор, который является процессивным в виде димера и имеет размер шага 36 нм.[21] Он перемещается (проходит) вдоль актиновых филаментов, двигаясь к зазубренному концу (+ концу) филаментов. Миозин V участвует в транспортировке грузов (например, РНК, везикул, органелл, митохондрий) от центра клетки к периферии, но, кроме того, было показано, что он действует как динамическая связка, удерживая везикулы и органеллы в богатых актином периферия клеток.[22][23] Недавнее исследование восстановления одной молекулы in vitro по сборке актиновых филаментов предполагает, что Myosin V перемещается дальше на вновь собираемом (богатый ADP-Pi) F-актине, в то время как длина процессивного пробега короче на более старом (богатом ADP) F-actin.[24]
Миозин VI

Миозин VI - это нетрадиционный миозиновый мотор, который в основном является процессивным как димер, но также действует как непроцессивный мономер. Он движется по актиновым филаментам, двигаясь к заостренному концу (-концу) филаментов.[26] Считается, что миозин VI переносит эндоцитарный везикулы в клетку.[27]
Миозин VII
Миозин VII - нетрадиционный миозин с двумя FERM домены в хвостовой части. Он имеет удлиненное плечо рычага, состоящее из пяти IQ-мотивов, связывающих кальмодулин, за которыми следует одна альфа-спираль (SAH).[28] Миозин VII необходим для фагоцитоз в Dictyostelium discoideum, сперматогенез в C. elegans и стереоцилии образование у мышей и рыбок данио.[29]
Миозин VIII
Миозин VIII - это миозин, специфичный для растений, связанный с делением клеток;[30] в частности, он участвует в регулировании потока цитоплазмы между клетками.[31] и в локализации пузырьков на фрагмопласт.[32]
Миозин IX
Миозин IX - группа одноголовых моторных белков. Впервые было показано, что он направлен на минус,[33] но более позднее исследование показало, что оно направлено на плюс.[34] Механизм движения этого миозина плохо изучен.
Миозин X
Миозин X - это нетрадиционный миозиновый двигатель, который функционирует как димер. Считается, что димеризация миозина X антипараллельна.[35] У других миозинов такое поведение не наблюдалось. В клетках млекопитающих двигатель локализован в филоподии. Миозин X движется к зазубренным концам нитей. Некоторые исследования показывают, что он преимущественно движется по пучкам актина, а не по отдельным нитям.[36] Это первый миозиновый двигатель, демонстрирующий такое поведение.
Миозин XI
Миозин XI управляет движением органелл, таких как пластиды и митохондрии в клетках растений.[37] Он отвечает за направленное светом движение хлоропласты в зависимости от интенсивности света и образования стромулы соединение разных пластид. Миозин XI также играет ключевую роль в росте кончиков полярных корней и необходим для правильного корни волос удлинение.[38] Специфический миозин XI, обнаруженный в Nicotiana tabacum было обнаружено, что это самый быстрый из известных процессивов молекулярный мотор, перемещаясь со скоростью 7 мкм / с с шагом 35 нм вдоль актин нить.[39]
Миозин XII
Миозин XIII
Миозин XIV
Эта группа миозина была обнаружена в Apicomplexa тип.[40] Миозины локализуются на плазматических мембранах внутриклеточного паразиты и затем может участвовать в процессе клеточной инвазии.[41]
Этот миозин также содержится в мерцательных простейших. Tetrahymena thermaphila. Известные функции включают транспортировку фагосом к ядру и нарушение регулируемого в процессе развития элиминации макронуклеуса во время конъюгации.
Миозин XV
Миозин XV необходим для развития основной структуры актина неподвижных стереоцилии расположен во внутреннем ухе. Считается, что он действует как мономер.
Миозин XVI
Миозин XVII
Миозин XVIII
MYO18A Ген на хромосоме 17q11.2, который кодирует основанные на актине моторные молекулы с АТФазной активностью, которые могут участвовать в поддержании каркаса стромальных клеток, необходимого для поддержания межклеточного контакта.
Гены у человека
Обратите внимание, что не все эти гены активны.
- Класс I: MYO1A, MYO1B, MYO1C, MYO1D, MYO1E, MYO1F, MYO1G, MYO1H
- Класс II: MYH1, MYH2, MYH3, MYH4, MYH6, MYH7, MYH7B, MYH8, MYH9, MYH10, MYH11, MYH13, MYH14, MYH15, MYH16
- Класс III: MYO3A, MYO3B
- Класс V: MYO5A, MYO5B, MYO5C
- Класс VI: MYO6
- Класс VII: MYO7A, MYO7B
- Класс IX: MYO9A, MYO9B
- Класс X: MYO10
- Класс XV: MYO15A
- Класс XVIII: MYO18A, MYO18B
Легкие цепи миозина различны и обладают собственными свойствами. Они не считаются «миозинами», но являются компонентами макромолекулярных комплексов, составляющих функциональные ферменты миозина.
Парамиозин
Парамиозин большой, 93-115 кДа мышца белок который был описан в ряде разнообразных беспозвоночный тип.[42] Считается, что толстые нити беспозвоночных состоят из внутреннего парамиозинового ядра, окруженного миозином. Миозин взаимодействует с актин, что приводит к сокращению волокон.[43] Парамиозин встречается у многих различных видов беспозвоночных, например, у Брахиоподы, Sipunculidea, Нематода, Аннелида, Моллюска, Арахнида, и Насекомое.[42] Парамиозин отвечает за механизм «захвата», который обеспечивает устойчивое сокращение мышц с очень небольшими затратами энергии, так что моллюск могут оставаться закрытыми в течение длительного времени.
Смотрите также
Рекомендации
- ^ «Миозин». Словарь Merriam-Webster.
- ^ "myosin - определение слова myosin на английском языке из Оксфордского словаря". OxfordDictionaries.com. Получено 2016-01-20.
- ^ а б Поллард Т.Д., Корн Э.Д. (июль 1973 г.). «Миозин Acanthamoeba. I. Выделение из Acanthamoeba castellanii фермента, аналогичного мышечному миозину». Журнал биологической химии. 248 (13): 4682–90. PMID 4268863. В архиве из оригинала от 06.01.2016.
- ^ Мак-Магон, Т. А. 1984. Мышцы, рефлексы и движения. 1-е издание. Издательство Принстонского университета. ISBN 978-0-691-02376-2
- ^ Тыска MJ, Warshaw DM (январь 2002 г.). «Силовой удар миозина». Подвижность клеток и цитоскелет. 51 (1): 1–15. Дои:10.1002 / см.10014. PMID 11810692.
- ^ фон дер Экен Дж., Хейсслер С. М., Патан-Чхатбар С., Манштейн Д. Д., Раунсер С. (июнь 2016 г.). «Крио-ЭМ структура цитоплазматического актомиозинового комплекса человека при почти атомном разрешении». Природа. 534 (7609): 724–8. Bibcode:2016Натура.534..724E. Дои:10.1038 / природа18295. PMID 27324845. S2CID 4472407.
- ^ Cheney RE, Mooseker MS (февраль 1992 г.). «Нетрадиционные миозины». Текущее мнение в области клеточной биологии. 4 (1): 27–35. Дои:10.1016 / 0955-0674 (92) 90055-H. PMID 1558751.
- ^ Чейни Р.Э., Райли М.А., Мусекер М.С. (1993). «Филогенетический анализ надсемейства миозинов». Подвижность клеток и цитоскелет. 24 (4): 215–23. Дои:10.1002 / см. 970240402. PMID 8477454.
- ^ Гудсон HV (1994). «Молекулярная эволюция суперсемейства миозинов: применение филогенетических методов к вопросам клеточной биологии». Серия Общества общих физиологов. 49: 141–57. PMID 7939893.
- ^ Ходж Т., Коп MJ (октябрь 2000 г.). «Генеалогическое древо миозинов». Журнал клеточной науки. 113 Pt 19 (19): 3353–4. PMID 10984423.
- ^ Берг Дж. С., Пауэлл BC, Чейни Р. Э. (апрель 2001 г.). «Тысячелетняя перепись миозина». Молекулярная биология клетки. 12 (4): 780–94. Дои:10.1091 / mbc.12.4.780. ЧВК 32266. PMID 11294886.
- ^ Оливер Т. Н., Берг Дж. С., Чейни Р. Э. (октябрь 1999 г.). «Хвосты нетрадиционных миозинов». Клеточные и молекулярные науки о жизни. 56 (3–4): 243–57. Дои:10.1007 / с000180050426. PMID 11212352. S2CID 23407921.
- ^ Macive S (4 июня 2003 г.). «Миозин I». Архивировано из оригинал 2 июня 2007 г.. Получено 2007-05-23.
- ^ Баттерс К., Артур С.П., Лин А., Портер Дж., Дживз М.А., Миллиган Р.А., Моллой Дж. Э., Колуччио Л. М. (апрель 2004 г.). «Myo1c разработан для адаптации во внутреннем ухе». Журнал EMBO. 23 (7): 1433–40. Дои:10.1038 / sj.emboj.7600169. ЧВК 391074. PMID 15014434.
- ^ Висенте-Мансанарес М., Ма Х, Адельштейн Р.С., Хорвиц А.Р. (ноябрь 2009 г.). «Немышечный миозин II занимает центральное место в адгезии и миграции клеток». Обзоры природы. Молекулярная клеточная биология. 10 (11): 778–90. Дои:10.1038 / nrm2786. ЧВК 2834236. PMID 19851336.
- ^ а б c d е ж грамм Агилар Х.Н., Митчелл Б.Ф. (2010). «Физиологические пути и молекулярные механизмы, регулирующие сократимость матки». Обновление репродукции человека. 16 (6): 725–44. Дои:10.1093 / humupd / dmq016. PMID 20551073.
- ^ Мацуока Р., Ёсида М.С., Фурутани Ю., Имамура С., Канда Н., Янагисава М., Масаки Т., Такао А. (апрель 1993 г.). «Ген тяжелой цепи миозина гладких мышц человека, картированный в хромосомной области 16q12». Американский журнал медицинской генетики. 46 (1): 61–7. Дои:10.1002 / ajmg.1320460110. PMID 7684189.
- ^ «Архивная копия». В архиве из оригинала от 07.07.2009. Получено 2015-12-16.CS1 maint: заархивированная копия как заголовок (ссылка на сайт)
- ^ EntrezGene 53904
- ^ Продавцы JR (март 2000 г.). «Миозины: разнообразное надсемейство». Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1496 (1): 3–22. Дои:10.1016 / S0167-4889 (00) 00005-7. PMID 10722873.
- ^ Mehta AD, Rock RS, Rief M, Spudich JA, Mooseker MS, Cheney RE (август 1999). «Миозин-V - это процессивный мотор на основе актина». Природа. 400 (6744): 590–3. Bibcode:1999Натура 400..590М. Дои:10.1038/23072. PMID 10448864. S2CID 204995058.
- ^ Lecuona E, Minin A, Trejo HE, Chen J, Comellas AP, Sun H, Grillo D, Nekrasova OE, Welch LC, Szleifer I, Gelfand VI, Sznajder JI (ноябрь 2009 г.). «Миозин-Va ограничивает перенос везикул, содержащих Na + / K + -АТФазу, в альвеолярные эпителиальные клетки». Журнал клеточной науки. 122 (Пт 21): 3915–22. Дои:10.1242 / jcs.046953. ЧВК 2773192. PMID 19808891.
- ^ Хаммер Дж. А., Селлерс Дж. Р. (декабрь 2011 г.). «Пешком на работу: роль миозинов класса V как транспортеров грузов». Обзоры природы. Молекулярная клеточная биология. 13 (1): 13–26. Дои:10.1038 / nrm3248. PMID 22146746. S2CID 11853457.
- ^ Циммерманн Д., Сантос А., Ковар Д. Р., Rock RS (август 2015 г.). «Возраст актина регулирует длину пробега миозина-5 и миозина-6». Текущая биология. 25 (15): 2057–62. Дои:10.1016 / j.cub.2015.06.033. ЧВК 4556227. PMID 26190073.
- ^ Ménétrey J, Llinas P, Mukherjea M, Sweeney HL, Houdusse A (октябрь 2007 г.). «Структурная основа большого удара миозина VI». Клетка. 131 (2): 300–8. Дои:10.1016 / j.cell.2007.08.027. PMID 17956731. S2CID 14102005.
- ^ Басс Ф, Кендрик-Джонс Дж (апрель 2008 г.). «Как клеточные функции миозина VI регулируются внутри клетки?». Сообщения о биохимических и биофизических исследованиях. 369 (1): 165–75. Дои:10.1016 / j.bbrc.2007.11.150. ЧВК 2635068. PMID 18068125.
- ^ Басс Ф, Спудич Дж, Кендрик-Джонс Дж (2004). «Миозин VI: клеточные функции и двигательные свойства». Ежегодный обзор клеточной биологии и биологии развития. 20: 649–76. Дои:10.1146 / annurev.cellbio.20.012103.094243. ЧВК 1693462. PMID 15473855.
- ^ Ли Дж, Чен И, Дэн И, Унарта И.К., Лу Кью, Хуанг Х, Чжан М. (апрель 2017 г.). «Ca2 + -индуцированное изменение жесткости мотива IQ миозина VIIa - одиночное удлинение рычага α-спирали». Структура. 25 (4): 579–591.e4. Дои:10.1016 / j.str.2017.02.002. PMID 28262393.
- ^ Schliwa M, ed. (2003). Молекулярные двигатели. Wiley-VCH. С. 516, 518. ISBN 978-3-527-30594-0.
- ^ Редди А.С., День И.С. (2001). «Анализ миозинов, закодированных в недавно завершенной последовательности генома Arabidopsis thaliana». Геномная биология. 2 (7): ИССЛЕДОВАНИЕ0024. Дои:10.1186 / gb-2001-2-7-research0024. ЧВК 55321. PMID 11516337.
- ^ Балуска Ф., Цврчкова Ф., Кендрик-Джонс Дж., Фолькманн Д. (май 2001 г.). «Поглотить плазмодесмы как ворота для разгрузки флоэмы. Миозин VIII и кальретикулин как молекулярные детерминанты силы поглощения?». Физиология растений. 126 (1): 39–46. Дои:10.1104 / стр.126.1.39. ЧВК 1540107. PMID 11351069.
- ^ Райхельт С., Найт А.Е., Ходж Т.П., Балуска Ф., Самадж Дж., Фолькманн Д., Кендрик-Джонс Дж. (Сентябрь 1999 г.). «Характеристика нетрадиционного миозина VIII в растительных клетках и его локализация на постцитокинетической клеточной стенке». Журнал растений. 19 (5): 555–67. Дои:10.1046 / j.1365-313X.1999.00553.x. PMID 10504577.
- ^ Иноуэ А., Сайто Дж., Икебе Р., Икебе М. (апрель 2002 г.). «Миозин IXb представляет собой процессивный мотор с одной головкой, направленным на минус-конец». Природа клеточной биологии. 4 (4): 302–6. Дои:10.1038 / ncb774. PMID 11901422. S2CID 12158370.
- ^ О'Коннелл CB, Mooseker MS (февраль 2003 г.). «Нативный Myosin-IXb - это мотор, направленный на плюс, а не на минус». Природа клеточной биологии. 5 (2): 171–2. Дои:10.1038 / ncb924. PMID 12563277. S2CID 687308.
- ^ Лу Цюй, Е Ф, Вэй З, Вэнь З, Чжан М. (октябрь 2012 г.). «Антипараллельная спиральная спиральная димеризация миозина X». Труды Национальной академии наук Соединенных Штатов Америки. 109 (43): 17388–93. Дои:10.1073 / pnas.1208642109. ЧВК 3491486. PMID 23012428.
- ^ Ропарс В., Янг З., Изабет Т., Блан Ф., Чжоу К., Лин Т., Лю X, Хисье П., Самазан Ф., Амигуес Б., Ян Э.Д., Пак Х., Пилипенко О., Чеккини М., Синделар CV, Суини Х.Л., Худусс А. (Сентябрь 2016 г.). «Мотор миозина X оптимизирован для движения пучков актина». Nature Communications. 7: 12456. Bibcode:2016НатКо ... 712456R. Дои:10.1038 / ncomms12456. ЧВК 5025751. PMID 27580874.
- ^ Sattarzadeh A, Krahmer J, Germain AD, Hanson MR (ноябрь 2009 г.). «Хвостовой домен миозина XI, гомологичный дрожжевому миозиновому вакуоль-связывающему домену, взаимодействует с пластидами и стромулами у Nicotiana benthamiana». Молекулярный завод. 2 (6): 1351–8. Дои:10.1093 / mp / ssp094. PMID 19995734.
- ^ Перемыслов В.В., Прохневский А.И., Ависар Д, Доля В.В. (март 2008 г.). «Два миозина класса XI участвуют в перемещении органелл и развитии корневых волосков у Arabidopsis». Физиология растений. 146 (3): 1109–16. Дои:10.1104 / pp.107.113654. ЧВК 2259062. PMID 18178669.
- ^ Томинага М., Кодзима Х., Йокота Е., Ории Х., Накамори Р., Катаяма Е. и др. (Март 2003 г.). «Миозин XI высшего растения движется по актину с высокой скоростью с шагом 35 нм». Журнал EMBO. 22 (6): 1263–72. Дои:10.1093 / emboj / cdg130. ЧВК 151065. PMID 12628919.
- ^ Delbac F, Sänger A, Neuhaus EM, Stratmann R, Ajioka JW, Toursel C, Herm-Götz A, Tomavo S, Soldati T, Soldati D (ноябрь 2001 г.). «Миозины Toxoplasma gondii B / C: один ген, два хвоста, две локализации и роль в делении паразита». Журнал клеточной биологии. 155 (4): 613–23. Дои:10.1083 / jcb.200012116. ЧВК 2198869. PMID 11706051.
- ^ Hettmann C, Herm A, Geiter A, Frank B, Schwarz E, Soldati T, Soldati D (апрель 2000 г.). «Двухосновный мотив в хвосте апикомплексного миозина класса XIV является важным детерминантом локализации плазматической мембраны». Молекулярная биология клетки. 11 (4): 1385–400. Дои:10.1091 / mbc.11.4.1385. ЧВК 14854. PMID 10749937.
- ^ а б Винкельман Л (1976). «Сравнительные исследования парамиозинов». Сравнительная биохимия и физиология B. 55 (3): 391–7. Дои:10.1016/0305-0491(76)90310-2. PMID 987889.
- ^ Twarog BM (октябрь 1976 г.). «Аспекты функции гладкой мускулатуры в мышцах моллюска». Физиологические обзоры. 56 (4): 829–38. Дои:10.1152 / Physrev.1976.56.4.829. PMID 185635.
дальнейшее чтение
- Гэвин Р.Х. (2001). «Миозины у протистов». Обзор клеточной биологии. Международный обзор цитологии. 206. С. 97–134. Дои:10.1016 / S0074-7696 (01) 06020-X. ISBN 978-0-12-364610-1. PMID 11407764.
- Мусекер М.С., Чейни Р.Э. (1995). «Нетрадиционные миозины». Ежегодный обзор клеточной биологии и биологии развития. 11: 633–75. Дои:10.1146 / annurev.cb.11.110195.003221. PMID 8689571.
- Продавцы JR (март 2000 г.). «Миозины: разнообразное надсемейство». Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1496 (1): 3–22. Дои:10.1016 / S0167-4889 (00) 00005-7. PMID 10722873.
- Soldati T, Geissler H, Schwarz EC (1999). «Сколько достаточно? Изучение репертуара миозина на модельном эукариоте Dictyostelium discoideum». Биохимия клетки и биофизика. 30 (3): 389–411. Дои:10.1007 / BF02738121. PMID 10403058. S2CID 13319819.
- Молекулярная биология клетки. Альбертс, Джонсон, Льюис, Рафф, Робертс и Уолтер. 4-е издание. 949–952.
Дополнительные изображения

Фаза 1
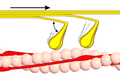
Фаза 2
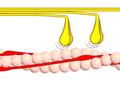
Фаза 3
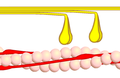
Фаза 4
внешняя ссылка
- MBInfo - Изоформы миозина
- MBInfo - Миозин Powerstroke
- Миозин видео Видео движущегося моторного белка миозина.
- Миозины в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Домашняя страница Myosin
- http://cellimages.ascb.org/cdm4/item_viewer.php?CISOROOT=/p4041coll12&CISOPTR=101&CISOBOX=1&REC=2[мертвая ссылка ] Анимация движущегося моторного белка миозина
- ЕС 3.6.4.1
- Трехмерные макромолекулярные структуры миозина из банка данных EM (EMDB)




