CDC42 - CDC42
Гомолог белка 42 контроля клеточного деления, также известный как Cdc42, это белок участвует в регулировании клеточный цикл. Первоначально он был идентифицирован в С. cerevisiae (дрожжи) как посредник деление клеток, и теперь известно, что он влияет на множество сигнальных событий и клеточных процессов в различных организмах от дрожжей до млекопитающих.
Функция
Human Cdc42 - небольшой GTPase из Семья Ро, который регулирует сигнальные пути, контролирующие различные клеточные функции, включая клеточные морфология, миграция клеток, эндоцитоз и прогрессирование клеточного цикла.[3] Rho GTPases играют центральную роль в динамической сборке и перестройке цитоскелета актина, которые являются основой клеточной адгезии и миграции. Активированный Cdc42 активируется, вызывая конформационные изменения[4] в р21-активированных киназах PAK1 и PAK2, которые, в свою очередь, инициируют реорганизацию актина и регулируют клеточную адгезию, миграцию и инвазию.[5]
Структура
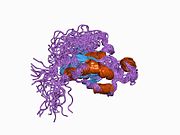
Cdc42 - это гомодимер с цепями A и B.[6] Его общая длина составляет 191 аминокислоту, а его теоретический вес составляет 21,33 кДа.[6] Его домены последовательности включают P-петлю, содержащую нуклеозидтрифосфатгидролазу, и небольшой домен GTP-связывающего белка.[6]
Cdc42 циклически переключается между активным состоянием, связанным с GTP, и неактивным состоянием, связанным с GDP. Этот процесс регулируется факторами обмена гуаниновых нуклеотидов (GEF), которые способствуют обмену связанного GDP на свободный GTP, белками, активирующими GTPase (GAP), которые увеличивают активность гидролиза GTP, и ингибиторами диссоциации GDP, которые ингибируют диссоциацию нуклеотида от GTPase.[7]
Роль в раке
Недавно было показано, что Cdc42 активно способствует прогрессированию рака. Несколько исследований установили основу для этого и выдвинули гипотезу о лежащих в основе механизмах.
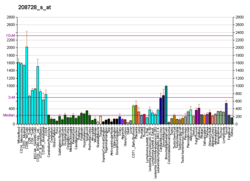
Cdc42 сверхэкспрессируется при немелкоклеточном раке легкого, колоректальной аденокарциноме, меланоме, раке груди и раке яичек.[8] Повышенные уровни белка коррелировали с отрицательной выживаемостью пациентов. Также было показано, что Cdc42 необходим как для прогрессирования фазы G1-S, так и для митоза, и он также модулирует факторы транскрипции SRF, STAT3 и NFkB.[8] Было высказано предположение, что нацеливание на Cdc42 в сочетании с химиотерапией может быть эффективной стратегией лечения рака.
В одном исследовании, посвященном роли Cdc42 в развитии рака шейки матки, иммуногистохимия был использован для обнаружения экспрессии Cdc42 в трех типах тканей: нормальных тканях шейки матки, цервикальная интраэпителиальная неоплазия (CIN) I или ниже, CIN II или выше, а также ткани рака шейки матки.[9] Экспрессия Cdc42 постепенно увеличивалась, показывая значительную разницу, и была значительно выше в HeLa клетки, чем в обычных клетках. Миграционная способность клеток HeLa, трансфицированных Cdc42, была выше, чем у нетрансфицированных клеток.[9] Было высказано предположение, что избыточная экспрессия Cdc42 может способствовать филоподия образование в клетках HeLa. Сверхэкспрессия Cdc42 значительно улучшила способность клеток рака шейки матки к миграции, возможно, из-за улучшения псевдоподия формирование.[9]
Другое исследование показало, что Cdc42 управляет процессом инициирования метастатический опухоль в новой ткани, способствуя экспрессии β1 интегрин рецептор адгезии, который, как известно, участвует в метастазировании.[10] Уровни интегрина β1 были снижены в Cdc42-дефицитных клетках. интегрин β1 важен для адгезии к внеклеточный матрикс, и также может быть важным для начального прикрепления к эндотелиальным клеткам. Подавление интегрина β1 ингибирует миграцию раковых клеток, тогда как сверхэкспрессия интегрина в клетках с дефицитом Cdc42 восстанавливает эндотелиальный вторжение.[10] Cdc42 стимулировал экспрессию интегрина β1 путем активации фактора транскрипции, называемого SRF. Постоянно активная форма фактора транскрипции также способна восстанавливать вставку эндотелия в раковые клетки, лишенные Cdc42.
Нормальные раковые клетки и раковые клетки с дефицитом Cdc42 также сравнивали in vivo. Когда оба типа клеток вводили в вены хвоста мыши, контрольные клетки больше распределялись по эндотелию сосудов в течение нескольких минут, предполагая, что Cdc42 способствует миграции клеток.[10] Через шесть недель в контрольных клетках образовалось больше метастазов, чем в клетках с дефицитом Cdc42. Проникающие раковые клетки выпускают выступы, которые достигают между соседними эндотелиальными клетками, чтобы контактировать с подлежащей базальной мембраной. Затем раковые клетки распространяются на этот внеклеточный матрикс, так что эндотелиальные клетки втягиваются и позволяют захватчикам вставать между собой.[10] В отсутствие Cdc42 раковые клетки не могли распространяться по базальной мембране, а клетки с дефицитом Cdc42 демонстрировали сниженную адгезию к покровным стеклам, покрытым внеклеточным матриксом.[10] Cdc42, следовательно, способствует прикреплению раковых клеток как к эндотелиальным клеткам, так и к базовой базальной мембране во время трансэндотелиальной миграции.
Низкомолекулярный ингибитор AZA197 был использован для ингибирования Cdc42 при лечении мутантного рака прямой кишки по KRAS.[11] Получены доказательства того, что ингибирование Cdc42 обработкой AZA197 подавляет пролиферативные и сигнальные пути выживания посредством передачи сигналов PAK1-ERK и снижает миграцию и инвазию клеток рака толстой кишки.[11] У мышей системная обработка AZA197 in vivo уменьшала рост первичной опухоли и увеличивала выживаемость.[11] Терапия, нацеленная на сигнальные пути Rho GTPase Cdc42, может быть эффективной для лечения пациентов с распространенным раком толстой кишки, сверхэкспрессирующим Cdc42, и особенно пациентов с заболеванием с мутантным KRAS.
Взаимодействия
CDC42 был показан взаимодействовать с:
- ARHGAP1,[12][13][14][15]
- ARHGDIA,[16][17]
- BAIAP2,[18][19][20]
- BNIP2,[14][21][22]
- BNIPL,[23]
- CDC42EP2,[24][25]
- CDC42EP3,[24][26]
- ERRFI1,[27]
- GDI1,[28]
- IQGAP1,[15][29][30][31][32]
- IQGAP2,[33]
- ITSN1,[34][35]
- MAP3K10,[12]
- MAP3K11,[12][36]
- PAK1,[15][37]
- PAK2,[15][38][39]
- PAK4.[16][39][40]
- PAK7,[40][41]
- PARD6A,[42][43][44]
- PARD6B,[42][43][45]
- Фосфолипаза D1,[46]
- RICS[47][48][49]
- TRIP10,[50][51]
- WASL,[52][53]
- Белок синдрома Вискотта-Олдрича,[51][54][55][56]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000070831 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Кадир М.И., Парвин А., Али М. (октябрь 2015 г.). «Cdc42: роль в управлении раком». Химическая биология и дизайн лекарств. 86 (4): 432–9. Дои:10.1111 / cbdd.12556. PMID 25777055.
- ^ Епископ А.Л., зал А (июнь 2000 г.). «Rho GTPases и их эффекторные белки». Биохимический журнал. 348 (2): 241–255. Дои:10.1042 / bj3480241. ЧВК 1221060. PMID 10816416.
- ^ Guo Y, Kenney SR, Muller CY, Adams S, Rutledge T, Romero E, Murray-Krezan C, Prekeris R, Sklar LA, Hudson LG, Wandinger-Ness A (октябрь 2015 г.). «R-кеторолак нацелен на Cdc42 и Rac1 и изменяет поведение раковых клеток яичников, критическое для инвазии и метастазирования». Молекулярная терапия рака. 14 (10): 2215–27. Дои:10.1158 / 1535-7163.MCT-15-0419. ЧВК 4596774. PMID 26206334.
- ^ а б c "Обзор структуры PDB 1a4r". Банк данных о белках в Европе. EMBL-EBI. Получено 2016-04-22.
- ^ «CDC42 (цикл клеточного деления 42 (GTP-связывающий белок, 25 кДа))». atlasgeneticsoncology.org. Получено 2016-04-22.
- ^ а б Стенгель К., Чжэн Ю. (сентябрь 2011 г.). «Cdc42 в онкогенной трансформации, инвазии и онкогенезе». Сотовая связь. 23 (9): 1415–23. Дои:10.1016 / j.cellsig.2011.04.001. ЧВК 3115433. PMID 21515363.
- ^ а б c Е Х, Чжан И, Гэн Л., Ли З (февраль 2015 г.). «Экспрессия Cdc42 при раке шейки матки и его влияние на инвазию и миграцию опухоли шейки матки». Международный журнал онкологии. 46 (2): 757–63. Дои:10.3892 / ijo.2014.2748. PMID 25394485.
- ^ а б c d е Уилсон Дж. М., Менхаус П., Гастин Б. В. (май 1987 г.). «Объем и исход операции аортокоронарного шунтирования». JAMA. 257 (18): 2434–5. Дои:10.1001 / jama.1987.03390180052010. PMID 3494856.
- ^ а б c Зинс К., Гунавардхана С., Лукас Т., Авраам Д., Ахаринеджад С. (01.01.2013). «Нацеливание на Cdc42 с помощью низкомолекулярного лекарственного средства AZA197 подавляет рост первичного рака толстой кишки и продлевает выживаемость в доклинической модели ксенотрансплантата мышей путем подавления активности PAK1». Журнал трансляционной медицины. 11: 295. Дои:10.1186/1479-5876-11-295. ЧВК 4222769. PMID 24279335.
- ^ а б c Нагата К., Пульс А., Футтер С., Аспенстром П., Шефер Е., Наката Т., Хирокава Н., зал A (январь 1998 г.). «MAP-киназа-киназа-киназа MLK2 совместно локализуется с активированным JNK вдоль микротрубочек и ассоциируется с моторным KIF3 суперсемейства кинезинов». Журнал EMBO. 17 (1): 149–58. Дои:10.1093 / emboj / 17.1.149. ЧВК 1170366. PMID 9427749.
- ^ Ли Р, Чжан Б., Чжэн И (декабрь 1997 г.). «Структурные детерминанты, необходимые для взаимодействия между Rho GTPase и активирующим GTPase доменом p190». Журнал биологической химии. 272 (52): 32830–5. Дои:10.1074 / jbc.272.52.32830. PMID 9407060.
- ^ а б Низкая BC, Лим Ю.П., Лим Дж., Вонг Е.С., Гай Г.Р. (ноябрь 1999 г.). «Фосфорилирование тирозина Bcl-2-ассоциированного белка BNIP-2 рецептором-1 фактора роста фибробластов предотвращает его связывание с Cdc42GAP и Cdc42». Журнал биологической химии. 274 (46): 33123–30. Дои:10.1074 / jbc.274.46.33123. PMID 10551883.
- ^ а б c d Чжан Б., Чернофф Дж., Чжэн Ю. (апрель 1998 г.). «Взаимодействие Rac1 с белками, активирующими GTPase, и предполагаемыми эффекторами. Сравнение с Cdc42 и RhoA». Журнал биологической химии. 273 (15): 8776–82. Дои:10.1074 / jbc.273.15.8776. PMID 9535855.
- ^ а б Юинг Р.М., Чу П., Элизма Ф, Ли Х, Тейлор П., Клими С., Макбрум-Цераевски Л., Робинсон, доктор медицины, О'Коннор Л., Ли М., Тейлор Р., Дхарси М., Хо Й, Хейлбут А., Мур Л., Чжан S, Орнатски O, Бухман YV, Ethier M, Sheng Y, Vasilescu J, Abu-Farha M, Lambert JP, Duewel HS, Stewart II, Kuehl B, Hogue K, Colwill K, Gladwish K, Muskat B, Kinach R, Adams С.Л., Моран М.Ф., Морин Г.Б., Топалоглоу Т., Фигейз Д. (2007). «Крупномасштабное картирование белок-белковых взаимодействий человека с помощью масс-спектрометрии». Молекулярная системная биология. 3 (1): 89. Дои:10.1038 / msb4100134. ЧВК 1847948. PMID 17353931.
- ^ Горвел Дж. П., Чанг Т. С., Боретто Дж., Адзума Т., Шаврие П. (январь 1998 г.). «Отличительные свойства D4 / LyGDI по сравнению с RhoGDI: фосфорилирование и селективность rho GTPase». Письма FEBS. 422 (2): 269–73. Дои:10.1016 / S0014-5793 (98) 00020-9. PMID 9490022.
- ^ Soltau M, Richter D, Kreienkamp HJ (декабрь 2002 г.). «Субстрат рецептора инсулина IRSp53 связывает постсинаптический стержень 1 с небольшим G-белком cdc42». Молекулярная и клеточная нейронауки. 21 (4): 575–83. Дои:10.1006 / mcne.2002.1201. PMID 12504591.
- ^ Krugmann S, Jordens I, Gevaert K, Driessens M, Vandekerckhove J, Hall A (октябрь 2001 г.). «Cdc42 индуцирует филоподии, способствуя образованию комплекса IRSp53: Mena». Текущая биология. 11 (21): 1645–55. Дои:10.1016 / S0960-9822 (01) 00506-1. PMID 11696321.
- ^ Мики Х., Ямагути Х., Суэцугу С., Такенава Т. (декабрь 2000 г.). «IRSp53 является важным промежуточным звеном между Rac и WAVE в регуляции взъерошенности мембран». Природа. 408 (6813): 732–5. Дои:10.1038/35047107. PMID 11130076.
- ^ Low BC, Seow KT, Guy GR (май 2000 г.). «Доказательства нового домена Cdc42GAP на карбоксильном конце BNIP-2». Журнал биологической химии. 275 (19): 14415–22. Дои:10.1074 / jbc.275.19.14415. PMID 10799524.
- ^ Low BC, Seow KT, Guy GR (декабрь 2000 г.). «Домен гомологии BNIP-2 и Cdc42GAP BNIP-2 опосредует его гомофильную ассоциацию и гетерофильное взаимодействие с Cdc42GAP». Журнал биологической химии. 275 (48): 37742–51. Дои:10.1074 / jbc.M004897200. PMID 10954711.
- ^ Цинь В., Ху Дж., Го М., Сюй Дж., Ли Дж., Яо Дж., Чжоу Х, Цзян Х., Чжан П., Шэнь Л., Ван Д., Гу Дж. (Август 2003 г.). «BNIPL-2, новый гомолог BNIP-2, взаимодействует с Bcl-2 и Cdc42GAP при апоптозе». Сообщения о биохимических и биофизических исследованиях. 308 (2): 379–85. Дои:10.1016 / S0006-291X (03) 01387-1. PMID 12901880.
- ^ а б Джоберти Г., Перлунгер Р. Р., Макара И. Г. (октябрь 1999 г.). «Борги, новое семейство белков, взаимодействующих с ГТФазой Cdc42 и TC10». Молекулярная и клеточная биология. 19 (10): 6585–97. Дои:10.1128 / MCB.19.10.6585. ЧВК 84628. PMID 10490598.
- ^ Хирш Д.С., Пироне Д.М., Бурбело П.Д. (январь 2001 г.). «Новое семейство эффекторных белков Cdc42, CEP, функционирует в фибробластах и изменениях формы эпителиальных клеток». Журнал биологической химии. 276 (2): 875–83. Дои:10.1074 / jbc.M007039200. PMID 11035016.
- ^ Альбертс А.С., Букен Н., Джонстон Л.Х., Трейсман Р. (апрель 1998 г.). «Анализ RhoA-связывающих белков выявляет домен взаимодействия, законсервированный в бета-субъединицах гетеротримерного G-белка и регуляторном белке дрожжевого ответа Skn7». Журнал биологической химии. 273 (15): 8616–22. Дои:10.1074 / jbc.273.15.8616. PMID 9535835.
- ^ Маккинье А., Куинн Д.А., Чен А., Cadilla CL, Force T, Bonventre JV, Kyriakis JM (июнь 2000 г.). «Ген 33 / Mig-6, транскрипционно индуцируемый адаптерный белок, который связывает GTP-Cdc42 и активирует SAPK / JNK. Потенциальный маркер-транскрипт для хронических патологических состояний, таких как диабетическая нефропатия. Возможная роль в ответе на стойкий стресс». Журнал биологической химии. 275 (23): 17838–47. Дои:10.1074 / jbc.M909735199. ЧВК 3668664. PMID 10749885.
- ^ Гибсон Р.М., Уилсон-Делфосс А.Л. (октябрь 2001 г.). «RhoGDI-дефектный по связыванию мутант Cdc42Hs нацеливается на мембраны и активирует образование филоподий, но не участвует в цикле с цитозолем клеток млекопитающих». Биохимический журнал. 359 (Pt 2): 285–94. Дои:10.1042/0264-6021:3590285. ЧВК 1222146. PMID 11583574.
- ^ Курода С., Фуката М., Кобаяси К., Накафуку М., Номура Н., Ивамацу А., Кайбути К. (сентябрь 1996 г.). «Идентификация IQGAP как предполагаемой цели для малых GTPases, Cdc42 и Rac1». Журнал биологической химии. 271 (38): 23363–7. Дои:10.1074 / jbc.271.38.23363. PMID 8798539.
- ^ Фуката М., Ватанабе Т., Норитаке Дж., Накагава М., Ямага М., Курода С., Мацуура Ю., Ивамацу А., Перес Ф, Кайбути К. (июнь 2002 г.). «Rac1 и Cdc42 захватывают микротрубочки через IQGAP1 и CLIP-170». Клетка. 109 (7): 873–85. Дои:10.1016 / S0092-8674 (02) 00800-0. PMID 12110184.
- ^ Харт MJ, Callow MG, Соуза Б., Полакис П. (июнь 1996 г.). «IQGAP1, кальмодулин-связывающий белок с доменом, связанным с rasGAP, является потенциальным эффектором для cdc42Hs». Журнал EMBO. 15 (12): 2997–3005. Дои:10.1002 / j.1460-2075.1996.tb00663.x. ЧВК 450241. PMID 8670801.
- ^ Joyal JL, Annan RS, Ho YD, Huddleston ME, Carr SA, Hart MJ, Sacks DB (июнь 1997 г.). «Кальмодулин модулирует взаимодействие между IQGAP1 и Cdc42. Идентификация IQGAP1 с помощью тандемной масс-спектрометрии с наноэлектрораспылением». Журнал биологической химии. 272 (24): 15419–25. Дои:10.1074 / jbc.272.24.15419. PMID 9182573.
- ^ Брилл С., Ли С., Лайман К.В., Черч Д.М., Васмут Дж. Дж., Вайсбах Л., Бернардс А., Снайдерс А. Дж. (Сентябрь 1996 г.). «Связанный с белком человека, активирующий ГТФазу Ras, IQGAP2 содержит потенциальный актин-связывающий домен и взаимодействует с кальмодулином и GTPases семейства Rho». Молекулярная и клеточная биология. 16 (9): 4869–78. Дои:10.1128 / mcb.16.9.4869. ЧВК 231489. PMID 8756646.
- ^ Хуссейн Н.К., Дженна С., Глогауэр М., Куинн С.К., Васиак С., Гиппони М., Антонаракис С.Е., Кей Б.К., Стоссель Т.П., Ламарш-Вейн Н., Макферсон П.С. (октябрь 2001 г.). «Эндоцитарный белок интерсектин-1 регулирует сборку актина через Cdc42 и N-WASP». Природа клеточной биологии. 3 (10): 927–32. Дои:10.1038 / ncb1001-927. PMID 11584276.
- ^ Снайдер Дж. Т., Уортилейк Д. К., Россман К. Л., Беттс Л., Прюитт В. М., Сидеровски Д. П., Дер С. Дж., Сондек Дж. (Июнь 2002 г.). «Структурная основа для избирательной активации Rho GTPases факторами обмена Dbl». Структурная биология природы. 9 (6): 468–75. Дои:10.1038 / nsb796. PMID 12006984.
- ^ Бёк BC, Vacratsis PO, Qamirani E, Gallo KA (май 2000 г.). «Cdc42-индуцированная активация киназы смешанного происхождения SPRK in vivo. Потребность в интерактивном связывающем мотиве Cdc42 / Rac и изменения в фосфорилировании». Журнал биологической химии. 275 (19): 14231–41. Дои:10.1074 / jbc.275.19.14231. PMID 10799501.
- ^ Сео М.Л., Нг Ч., Йонг Дж., Лим Л., Люнг Т. (март 2003 г.). «ArhGAP15, новый человеческий белок RacGAP со свойством связывания GTPase». Письма FEBS. 539 (1–3): 131–7. Дои:10.1016 / S0014-5793 (03) 00213-8. PMID 12650940.
- ^ Стивенс В.К., Вранкен В., Гудро Н., Сян Х., Сюй П, Ни Ф (май 1999 г.). «Конформация интерактивного связывающего пептида Cdc42 / Rac в комплексе с Cdc42 и анализ интерфейса связывания». Биохимия. 38 (19): 5968–75. Дои:10.1021 / bi990426u. PMID 10320322.
- ^ а б Abo A, Qu J, Cammarano MS, Dan C, Fritsch A, Baud V, Belisle B, Minden A (ноябрь 1998 г.). «PAK4, новый эффектор для Cdc42Hs, участвует в реорганизации актинового цитоскелета и в образовании филоподий». Журнал EMBO. 17 (22): 6527–40. Дои:10.1093 / emboj / 17.22.6527. ЧВК 1171000. PMID 9822598.
- ^ а б Дэн К., Нат Н., Либерто М., Минден А. (январь 2002 г.). «PAK5, новая специфическая для мозга киназа, способствует разрастанию нейритов в клетках N1E-115». Молекулярная и клеточная биология. 22 (2): 567–77. Дои:10.1128 / MCB.22.2.567-577.2002. ЧВК 139731. PMID 11756552.
- ^ Панди А., Дан I, Кристиансен Т.З., Ватанабе Н.М., Волдби Дж., Кадзикава Э., Хосрави-Фар Р., Благоев Б., Манн М. (май 2002 г.). «Клонирование и характеристика PAK5, нового члена подсемейства p21-активируемой киназы-II млекопитающих, который преимущественно экспрессируется в головном мозге». Онкоген. 21 (24): 3939–48. Дои:10.1038 / sj.onc.1205478. PMID 12032833.
- ^ а б Джоберти Г., Петерсен С., Гао Л., Макара И.Г. (август 2000 г.). «Белок клеточной полярности Par6 связывает Par3 и атипичную протеинкиназу C с Cdc42». Природа клеточной биологии. 2 (8): 531–9. Дои:10.1038/35019573. PMID 10934474.
- ^ а б Нода Й, Такея Р., Оно С., Наито С., Ито Т., Сумимото Х. (февраль 2001 г.). «Человеческие гомологи белка PAR6 клеточной полярности Caenorhabditis elegans в качестве адаптера, который связывает малые GTPases Rac и Cdc42 с атипичной протеинкиназой C». Гены в клетки. 6 (2): 107–19. Дои:10.1046 / j.1365-2443.2001.00404.x. PMID 11260256.
- ^ Цю Р., Або А, Стивен Мартин Дж. (Июнь 2000 г.). «Человеческий гомолог детерминанты полярности C. elegans Par-6 связывает Rac и Cdc42 с передачей сигналов PKCzeta и трансформацией клеток». Текущая биология. 10 (12): 697–707. Дои:10.1016 / S0960-9822 (00) 00535-2. PMID 10873802.
- ^ Neudauer CL, Joberty G, Macara IG (январь 2001 г.). «PIST: новый партнер связывания PDZ / домена спиральной спирали для GTPase TC10 семейства rho». Сообщения о биохимических и биофизических исследованиях. 280 (2): 541–7. Дои:10.1006 / bbrc.2000.4160. PMID 11162552.
- ^ Уокер SJ, Wu WJ, Cerione RA, Brown HA (май 2000 г.). «Активация фосфолипазы D1 с помощью Cdc42 требует области вставки Rho». Журнал биологической химии. 275 (21): 15665–8. Дои:10.1074 / jbc.M000076200. PMID 10747870.
- ^ Накадзава Т., Ватабэ А.М., Тэдзука Т., Ёсида Ю., Ёкояма К., Умемори Х., Иноуэ А., Окабе С., Манабе Т., Ямамото Т. (июль 2003 г.). «p250GAP, новый мозг, обогащенный GTPase-активирующим белком для GTPases семейства Rho, участвует в передаче сигналов рецептора N-метил-d-аспартата». Молекулярная биология клетки. 14 (7): 2921–34. Дои:10.1091 / mbc.E02-09-0623. ЧВК 165687. PMID 12857875.
- ^ Чжао Ц., Ма Х., Босси-Ветцель Э., Липтон С.А., Чжан Ц., Фэн Г.С. (сентябрь 2003 г.). «GC-GAP, белок, активирующий ГТФазу семейства Rho, который взаимодействует с сигнальными адаптерами Gab1 и Gab2». Журнал биологической химии. 278 (36): 34641–53. Дои:10.1074 / jbc.M304594200. PMID 12819203.
- ^ Накамура Т., Комия М., Сон К., Хиросэ Э, Гото Н., Мори Х, Охта Й, Мори Н. (декабрь 2002 г.). «Grit, белок, активирующий GTPase для семейства Rho, регулирует расширение нейритов посредством ассоциации с рецептором TrkA и адапторными молекулами N-Shc и CrkL / Crk». Молекулярная и клеточная биология. 22 (24): 8721–34. Дои:10.1128 / MCB.22.24.8721-8734.2002. ЧВК 139861. PMID 12446789.
- ^ Аспенстрём П. (июль 1997 г.). «Целевой белок Cdc42, гомологичный некиназному домену FER, может играть потенциальную роль в регуляции актинового цитоскелета». Текущая биология. 7 (7): 479–87. Дои:10.1016 / S0960-9822 (06) 00219-3. PMID 9210375.
- ^ а б Тиан Л., Нельсон Д.Л., Стюарт Д.М. (март 2000 г.). «Cdc42-взаимодействующий белок 4 опосредует связывание белка синдрома Вискотта-Олдрича с микротрубочками». Журнал биологической химии. 275 (11): 7854–61. Дои:10.1074 / jbc.275.11.7854. PMID 10713100.
- ^ Карлье М.Ф., Ниош П., Брутин-Л'Эрмит I, Бужемаа Р., Ле Кленш С., Эжиль С., Гарбай С., Дюкрюа А., Сансонетти П., Панталони Д. (июль 2000 г.). «GRB2 связывает передачу сигналов со сборкой актина, усиливая взаимодействие нейрального белка синдрома Вискотта-Олдрича (N-WASp) с комплексом актин-родственного белка (ARP2 / 3)». Журнал биологической химии. 275 (29): 21946–52. Дои:10.1074 / jbc.M000687200. PMID 10781580.
- ^ Мики Х, Сасаки Т, Такай Й, Такенава Т (январь 1998 г.). «Индукция образования филоподия с помощью WASP-родственного актин-деполимеризирующего белка N-WASP». Природа. 391 (6662): 93–6. Дои:10.1038/34208. PMID 9422512.
- ^ Ким А.С., Какалис Л.Т., Абдул-Манан Н., Лю Г.А., Розен М.К. (март 2000 г.). «Аутоингибирование и механизмы активации белка синдрома Вискотта-Олдрича». Природа. 404 (6774): 151–8. Дои:10.1038/35004513. PMID 10724160.
- ^ Коллури Р., Толиас К.Ф., Карпентер С.Л., Розен Ф.С., Кирххаузен Т. (май 1996 г.). «Прямое взаимодействие белка синдрома Вискотта-Олдрича с GTPase Cdc42». Труды Национальной академии наук Соединенных Штатов Америки. 93 (11): 5615–8. Дои:10.1073 / пнас.93.11.5615. ЧВК 39296. PMID 8643625.
- ^ Саймонс М., Дерри Дж.М., Карлак Б., Цзян С., Лемахье В., Маккормик Ф., Франк У., Або А (март 1996 г.). «Белок синдрома Вискотта-Олдрича, новый эффектор для GTPase CDC42Hs, участвует в полимеризации актина». Клетка. 84 (5): 723–34. Дои:10.1016 / S0092-8674 (00) 81050-8. PMID 8625410.
внешняя ссылка
- cdc42 + GTP-связывание + белок в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- CDC42 Информация со ссылками в Шлюз миграции ячеек
- Человек CDC42 расположение генома и CDC42 страница сведений о гене в Браузер генома UCSC.