Сетчатка - Retina - Wikipedia
Эта статья требует внимания специалиста в области медицины. (Май 2018) |
| Сетчатка | |
|---|---|
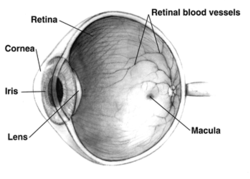 Правильно человеческий глаз вид в разрезе; глаза значительно различаются у животных. | |
| Подробности | |
| Произношение | Великобритания: /ˈрɛтɪпə/, нас: /ˈрɛтənə/, пл. сетчатка /-пя/ |
| Часть | Глаз |
| Система | Визуальная система |
| Артерия | Центральная артерия сетчатки |
| Идентификаторы | |
| латинский | Сеть |
| MeSH | D012160 |
| TA98 | A15.2.04.002 |
| TA2 | 6776 |
| FMA | 58301 |
| Анатомическая терминология | |
В сетчатка (из латинский: сеть) - самый внутренний, светочувствительный слой ткани глаз из большинства позвоночные и немного моллюски. Оптика глаза создает сосредоточенный двухмерное изображение визуального мира на сетчатке глаза, которое преобразует это изображение в электрические нейронные импульсы в мозг для создания визуальное восприятие. Сетчатка выполняет функцию, аналогичную функции сетчатки. фильм или же датчик изображений в камера.
Нервная сетчатка состоит из нескольких слоев нейроны связаны между собой синапсы и поддерживается внешним слоем пигментированных эпителиальных клеток. Первичные светочувствительные клетки сетчатки - это фоторецепторные клетки, которые бывают двух типов: стержни и шишки. Жезлы работают в основном при тусклом свете и обеспечивают черно-белое изображение. Колбочки работают в хорошо освещенных условиях и отвечают за восприятие цвета, а также за высокую остроту зрения, используемую для таких задач, как чтение. Третий тип светочувствительных ячеек, светочувствительная ганглиозная клетка, важно для увлечение циркадных ритмов и рефлексивных реакций, таких как зрачковый световой рефлекс.
Свет, падающий на сетчатку, инициирует каскад химических и электрических событий, которые в конечном итоге запускают нервные импульсы, которые отправляются в различные зрительные центры мозг через волокна Зрительный нерв. Нейронные сигналы от палочек и колбочек обрабатываются другими нейронами, вывод которых принимает форму потенциалы действия в ганглиозные клетки сетчатки чей аксоны формируют зрительный нерв.[1] Несколько важных особенностей визуальное восприятие можно проследить до кодирования сетчатки глаза и обработки света.
У позвоночных эмбриональное развитие сетчатка и зрительный нерв возникают как отростки развивающегося мозга, в частности, эмбрионального промежуточный мозг; таким образом, сетчатка считается частью Центральная нервная система (ЦНС) и фактически является тканью мозга.[2][3] Это единственная часть ЦНС, которую можно визуализировать. неинвазивно.
Структура
Перевернутая сетчатка по сравнению с не перевернутой сетчаткой
Сетчатка позвоночных перевернутый в том смысле, что светочувствительные клетки находятся позади сетчатки, так что свет должен пройти через слои нейронов и капилляров, прежде чем достигнет палочек и колбочек.[4] Ганглиозные клетки, аксоны которых образуют зрительный нерв, находятся в передней части сетчатки; следовательно, зрительный нерв должен проходить через сетчатку на пути к мозгу. В этой области нет фоторецепторов, дающих начало слепая зона.[5] Напротив, в головоногие моллюски На сетчатке фоторецепторы находятся спереди, а обрабатывающие нейроны и капилляры - позади них. Благодаря этому у головоногих моллюсков нет слепого пятна.
Хотя вышележащая нервная ткань частично прозрачна, а сопутствующие глиальные клетки, как было показано, действуют как оптоволоконный кабель каналы для транспортировки фотонов непосредственно к фоторецепторам,[6][7] светорассеяние действительно происходит.[8] У некоторых позвоночных, в том числе человека, есть область центральной сетчатки, адаптированная для высокой остроты зрения. Эта область, названная центральная ямка, бессосудистая (не имеет кровеносных сосудов) и имеет минимальную нервную ткань перед фоторецепторами, что сводит к минимуму рассеяние света.[8]
У головоногих моллюсков не перевернутая сетчатка, по разрешающей способности сопоставимая с глазами многих позвоночных. Глаза кальмаров не имеют аналога у позвоночных. пигментный эпителий сетчатки (RPE). Хотя их фоторецепторы содержат белок, ретинохром, который рециркулирует сетчатку и воспроизводит одну из функций РПЭ позвоночных, можно утверждать, что фоторецепторы головоногих моллюсков не поддерживаются так же хорошо, как у позвоночных, и что, как следствие, полезный срок службы фоторецепторов в беспозвоночные намного короче позвоночных.[9] Легко заменив стебельчатые глаза (у некоторых омаров) или сетчатку (у некоторых пауков, таких как Деинопис[10]) встречается редко.
Сетчатка головоногих моллюсков не является выростом мозга, как сетчатка позвоночных. Можно утверждать, что это различие показывает, что глаза позвоночных и головоногих не являются гомологичный но развивались отдельно. С эволюционной точки зрения, более сложная структура, такая как перевернутая сетчатка, обычно может возникать как следствие двух альтернативных процессов: (а) выгодный «хороший» компромисс между конкурирующими функциональными ограничениями или (б) как исторически неадаптивный пережиток прошлого. запутанный путь эволюции и трансформации органов. Зрение - важная адаптация у высших позвоночных.
Третий взгляд на «перевернутый» глаз позвоночных состоит в том, что он сочетает в себе два преимущества: поддержание фоторецепторов, упомянутых выше, и уменьшение интенсивности света, необходимое для предотвращения ослепления фоторецепторов, которые основаны на чрезвычайно чувствительных глазах предков современные миксины (рыба, обитающая в очень глубокой темной воде).[11]
Слои сетчатки
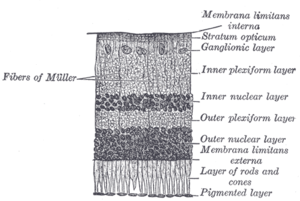



Сетчатка позвоночных состоит из десяти отдельных слоев.[13] От ближайшего к наиболее удаленному от стекловидного тела:
- Внутренняя ограничивающая мембрана - базальная мембрана, разработанная Клетки Мюллера.
- Слой нервных волокон - аксоны ганглиозная клетка тела (обратите внимание, что между этим слоем и внутренней ограничивающей мембраной существует тонкий слой ножек клеток Мюллера).
- Слой ганглиозных клеток - содержит ядра ганглиозных клеток, аксоны которых становятся волокнами зрительного нерва, а некоторые смещены амакриновые клетки.[2]
- Внутренний плексиформный слой - содержит синапс между биполярная клетка аксоны и дендриты ганглий и амакриновые клетки.[2]
- Внутренний ядерный слой - содержит ядра и окружающие клеточные тела (перикарья) амакриновые клетки, биполярные клетки, и горизонтальные ячейки.[2]
- Внешний плексиформный слой - выступы стержней и колбочки, заканчивающиеся сферулой стержня и ножкой конуса соответственно. Они образуют синапсы с дендритами биполярных клеток и горизонтальных клеток.[2] в макулярный регион, это известно как Волокнистый слой Henle.
- Внешний ядерный слой - тела палочек и колбочек.
- Внешняя ограничивающая мембрана - слой, который отделяет внутренние сегменты фоторецепторов от их клеточных ядер.
- Слой внутреннего сегмента / внешнего сегмента - внутренние сегменты и внешние сегменты стержней и конусов. Наружные сегменты содержат узкоспециализированный светочувствительный аппарат.[14][15]
- Пигментный эпителий сетчатки - однослойные кубовидные эпителиальные клетки (с выступами, не показанными на схеме). Этот слой находится ближе всего к сосудистой оболочке и обеспечивает питание и поддерживающие функции нервной сетчатки. Черный пигмент меланин в пигментном слое предотвращает отражение света по всему земному шару глазного яблока; это чрезвычайно важно для ясного зрения.[16][17][18]
Эти слои можно сгруппировать в 4 основных этапа обработки: фоторецепция; передача в биполярные клетки; передача в ганглиозные клетки, которые также содержат фоторецепторы, светочувствительные ганглиозные клетки; и передача по зрительному нерву. На каждой синаптической стадии также есть латерально соединяющиеся горизонтальный и амакриновые клетки.
В Зрительный нерв является центральным трактом многих аксонов ганглиозных клеток, соединяющихся в первую очередь с боковое коленчатое тело, визуальная релейная станция в промежуточный мозг (задняя часть переднего мозга). Он также направлен на верхний холмик, то супрахиазматическое ядро, а ядро зрительного тракта. Он проходит через другие слои, создавая диск зрительного нерва у приматов.[19]
Дополнительные структуры, не связанные напрямую со зрением, обнаруживаются в виде выростов сетчатки у некоторых групп позвоночных. В птицы, то Pecten представляет собой сосудистую структуру сложной формы, которая выступает из сетчатки в стекловидное тело; он снабжает глаза кислородом и питательными веществами, а также может улучшить зрение. Рептилии имеют похожую, но гораздо более простую структуру.[20]
У взрослых людей вся сетчатка составляет примерно 72% сферы диаметром около 22 мм. Вся сетчатка содержит около 7 миллионов колбочек и от 75 до 150 миллионов палочек. Диск зрительного нерва, часть сетчатки, которую иногда называют «слепым пятном» из-за отсутствия фоторецепторов, расположен в зрительный сосок, где волокна зрительного нерва выходят из глаза. Он выглядит как овальная белая область площадью 3 мм². Височным (в направлении висков) к этому диску является пятно, в центре которого находится ямка, яма, которая отвечает за наше острое центральное зрение, но на самом деле менее чувствительна к свету из-за отсутствия стержней. Человек и нечеловек приматы обладают одной ямкой, в отличие от некоторых видов птиц, таких как двулистные ястребы, а также собак и кошек, у которых нет ямки, но есть центральная полоса, известная как зрительная полоса.[нужна цитата ] Вокруг ямки проходит центральная сетчатка примерно на 6 мм, а затем периферическая сетчатка. Самый дальний край сетчатки определяется ora serrata. Расстояние от одного или другого до другого (или макулы), наиболее чувствительная область по горизонтали. меридиан составляет около 32 мм.[требуется разъяснение ]
На срезе толщина сетчатки не более 0,5 мм. Он состоит из трех слоев нерв камеры и два из синапсы, включая уникальные ленточный синапс. Зрительный нерв несет ганглиозная клетка аксоны в мозг и кровеносные сосуды, кровоснабжающие сетчатку. Ганглиозные клетки лежат внутри глаза, а светочувствительные клетки - за его пределами. Из-за этого противоречащего интуиции устройства свет должен сначала пройти через ганглиозные клетки и сквозь толщу сетчатки (включая ее капиллярные сосуды, не показаны), прежде чем достигнет палочек и колбочек. Свет поглощается пигментный эпителий сетчатки или сосудистая оболочка (оба непрозрачны).
В белые кровяные клетки в капилляры перед фоторецепторами можно воспринимать как крошечные яркие движущиеся точки при взгляде на синий свет. Это известно как синоптическое явление (или феномен Шерера).
Между ганглиозная клетка слой и стержни и конусы есть два слоя нейропилы где установлены синаптические контакты. Слои нейропиля - это внешний плексиформный слой и внутренний плексиформный слой. Во внешнем слое нейропиля палочки и колбочки соединяются с вертикально идущими биполярные клетки, а горизонтально ориентированные горизонтальные ячейки соединяются с ганглиозными клетками.
Центральная сетчатка преимущественно содержит колбочки, а периферическая сетчатка - преимущественно палочки. Всего насчитывается около семи миллионов колбочек и сто миллионов стержней. В центре макулы находится фовеальная ямка с узкими и длинными конусами, расположенными в форме шестиугольника. мозаика, наиболее плотные, в отличие от более толстых колбочек, расположенных более периферически в сетчатке.[21] В фовеальной ямке смещаются другие слои сетчатки перед их наращиванием вдоль фовеального склона до края ямки, или парафовеа, достигается самая толстая часть сетчатки. Макула имеет желтую пигментацию из-за скрининговых пигментов и известна как желтое пятно. Область, непосредственно окружающая фовеа, имеет самую высокую плотность палочек, сходящихся на единичные биполярные клетки. Поскольку его конусы имеют гораздо меньшую конвергенцию сигналов, ямка обеспечивает самое резкое зрение, которое только может получить глаз.[2]
Хотя стержень и конусы мозаика своего рода, передача от рецепторов к биполярам, к ганглиозные клетки не прямой. Поскольку существует около 150 миллионов рецепторов и только 1 миллион волокон зрительного нерва, должна происходить конвергенция и, следовательно, смешение сигналов. Кроме того, горизонтальное действие горизонтальный и амакриновые клетки может позволить одной области сетчатки контролировать другую (например, один стимул подавляет другой). Это торможение является ключом к уменьшению количества сообщений, отправляемых в высшие области мозга. У некоторых низших позвоночных (например, голубь ), существует «центробежный» контроль сообщений - то есть один слой может контролировать другой, или более высокие области мозга могут управлять нервными клетками сетчатки, но у приматов этого не происходит.[2]
Слои, которые можно представить с помощью оптической когерентной томографии
С помощью оптической когерентной томографии (ОКТ) в сетчатке можно идентифицировать 18 слоев. Слои и анатомическая корреляция следующие:[22][23][24]

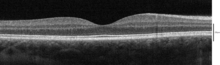

От самого внутреннего до самого внешнего, OCT идентифицирует следующие уровни:
| # | Слой OCT / Обычная этикетка | Анатомический коррелят | Отражательная способность | Специфический анатомический границы? | Дополнительный Рекомендации |
|---|---|---|---|---|---|
| 1 | Задний кортикальный слой стекловидного тела | Задний кортикальный слой стекловидного тела | Гиперотражающий | да | [23] |
| 2 | Преретинальное пространство | В глазах, где стекловидное тело полностью или частично отдельный от сетчатки это пространство, образованное между задней частью кортикального слоя стекловидного тела и внутренней ограничивающей мембраной сетчатки. | Гипоотражающий | [23] | |
| 3 | Внутренняя ограничивающая мембрана (ILM) | Образована Ячейка Мюллера концы (неясно, можно ли это наблюдать на ОКТ) | Гиперотражающий | Нет | [23] |
| Слой нервных волокон (НФЛ) | Ганглиозная клетка аксоны путешествуя к Зрительный нерв | ||||
| 4 | Слой ганглиозных клеток (GCL) | Ганглиозная клетка тела (и некоторые перемещенные амакриновые клетки ) | Гипоотражающий | [23] | |
| 5 | Внутренний плексиформный слой (IPL) | Синапсы между биполярный, амакрин и ганглиозные клетки | Гиперотражающий | [23] | |
| 6 | Внутренний ядерный слой (INL) | а) По горизонтали, биполярный и амакрин клеточные тела б) Ячейка Мюллера ядра | Гипоотражающий | [23] | |
| 7 | Внешний плексиформный слой (OPL) | Синапсы между фоторецептор, биполярный и горизонтальные ячейки | Гиперотражающий | [23] | |
| 8 | (Внутренняя половина) Слой нервных волокон Генле (HL) | Фоторецептор аксоны (косо ориентированные волокна; отсутствуют в среднепериферической или периферической сетчатке) | Гипоотражающий | Нет | [23] |
| (Внешняя половина) Внешний ядерный слой (ONL) | В фоторецептор клеточные тела | ||||
| 9 | Внешняя ограничивающая мембрана (ELM) | Сделано из zonulae adherens между Клетки Мюллера и внутренние сегменты фоторецепторов | Гиперотражающий | [23] | |
| 10 | Миоидная зона (МЗ) | Самая внутренняя часть внутренний сегмент фоторецептора (IS) содержащий:
| Гипоотражающий | Нет | [25][26] |
| 11 | Зона эллипсоида (EZ) | Самая внешняя часть внутренний сегмент фоторецептора (IS) упакован с митохондрии | Очень гиперотражающий | Нет | [22][27][25][23][28][29] |
| Соединение IS / OS или же Линия целостности фоторецепторов (PIL) | Фоторецептор соединительные реснички которые соединяют внутренний и внешний сегменты фоторецепторных клеток. | ||||
| 12 | Наружные сегменты фоторецепторов (OS) | В внешние сегменты фоторецепторов (OS) которые содержат диски, заполненные опсин, молекула, поглощающая фотоны. | Гипоотражающий | [30][23] | |
| 13 | Зона пересечения (IZ) | Вершины RPE клетки, которые охватывают часть ОС конуса. Слабо отличим от РПЭ. Ранее: "линия вершин внешнего сегмента конуса" (СТОИМОСТЬ) | Гиперотражающий | Нет | |
| 14 | RPE /Бруха сложный | RPE зона фагосом | Очень гиперотражающий | Нет | [22][23] |
| RPE зона меланосом | Гипоотражающий | ||||
| RPE зона митохондрий + стык между РПЭ и Мембрана Бруха | Очень гиперотражающий | ||||
| 15 | Хориокапилляры | Тонкий слой умеренной отражательной способности во внутренней сосудистой оболочке | Нет | [23] | |
| 16 | Слой Саттлера | Толстый слой гиперотражающих профилей круглой или овальной формы с гипорефлективными сердцевинами в средней части сосудистой оболочки. | [23] | ||
| 17 | Слой Халлера | Толстый слой овальных гиперотражающих профилей с гипорефлективными сердцевинами в наружной сосудистой оболочке | [23] | ||
| 18 | Хориоидально-склеральный переход | Зона внешней сосудистой оболочки с заметным изменением текстуры, в которой большие круглые или овальные профили примыкают к однородная область переменной отражательной способности | [23] | ||
Разработка
Развитие сетчатки начинается с образования глазных полей, опосредованных SHH и ШЕСТЬ 3 белков, с последующим развитием зрительных пузырьков, регулируемых PAX6 и LHX2 белки.[31] Роль Pax6 в развитии глаза была элегантно продемонстрирована Вальтером Герингом и его коллегами, которые показали, что эктопическая экспрессия Pax6 может приводить к формированию глаза на Дрозофила усики, крылья и ноги.[32] Зрительный пузырек дает начало трем структурам: нервной сетчатке, пигментированному эпителию сетчатки и оптическому стеблю. Нервная сетчатка содержит клетки-предшественники сетчатки (RPC), которые дают начало семи типам клеток сетчатки. Дифференциация начинается с ганглиозные клетки сетчатки и завершается производством глии Мюллера.[33] Хотя каждый тип клеток дифференцируется от RPC в последовательном порядке, существует значительное перекрытие во времени, когда дифференцируются отдельные типы клеток.[31] Признаки, которые определяют судьбу дочерней клетки RPC, кодируются множеством семейств факторов транскрипции, включая bHLH и гомеодомен факторы.[34][35]
В дополнение к определению судьбы направляющих клеток в сетчатке существуют сигналы для определения дорсально-вентральной (D-V) и назально-височной (N-T) осей. Ось D-V определяется вентрально-дорсальным градиентом VAX2, тогда как ось N-T координируется экспрессией факторов транскрипции вилки. FOXD1 и FOXG1. Внутри сетчатки формируются дополнительные градиенты.[35] Это пространственное распределение может помочь в правильном нацеливании на аксоны RGC, которые функционируют, чтобы установить ретинотопную карту.[31]
Кровоснабжение
Эта статья поднимает множество проблем. Пожалуйста помоги Улучши это или обсудите эти вопросы на страница обсуждения. (Узнайте, как и когда удалить эти сообщения-шаблоны) (Узнайте, как и когда удалить этот шаблон сообщения)
|
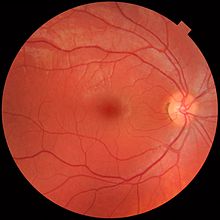
Сетчатка разделена на отдельные слои, каждый из которых содержит определенные типы клеток или клеточные компартменты.[36] которые имеют метаболизм с различными требованиями к питанию.[37] Чтобы удовлетворить эти требования, глазная артерия раздваивается и снабжает сетчатку через две различные сосудистые сети: хориоидальную сеть, которая снабжает сосудистую оболочку и внешнюю сетчатку, и сетчатую сеть, которая снабжает внутренний слой сетчатки.[38]
Механизмы кровообращения
На первый взгляд, можно подумать, что сетчатка позвоночного «неправильно спроектирована» или «плохо спроектирована»; но на самом деле сетчатка не могла бы функционировать, если бы ее не перевернули. Слой фоторецепторов должен быть встроен в пигментный эпителий сетчатки (РПЭ), который выполняет как минимум семь жизненно важных функций.[39] одним из наиболее очевидных является обеспечение кислородом и другими необходимыми питательными веществами, необходимыми для работы фоторецепторов. Эти питательные вещества включают глюкозу, жирные кислоты и сетчатку. Процесс амплификации фоторецепторов млекопитающих использует большие количества энергии для зрения в фотопических условиях (требуя меньше в скотопических условиях) и, таким образом, требует большого количества питательных веществ, поставляемых кровеносными сосудами в сосудистой оболочке, которая находится за пределами РПЭ. Хориоидея поставляет около 75% этих питательных веществ в сетчатку, а сосудистая сеть сетчатки - только 25%.[4]
Когда свет попадает на 11-цис-ретиналь (диски в палочках и колбочках), 11-цис-сетчатка превращается в полностью транс-ретиналь, что затем вызывает изменения в опсинах. Теперь внешние сегменты не регенерируют сетчатку обратно в цис-форму после того, как она была изменена светом. Вместо этого сетчатка откачивается к окружающему РПЭ, где она регенерируется и транспортируется обратно во внешние сегменты фоторецепторов. Эта функция рециркуляции RPE защищает фоторецепторы от фотоокислительного повреждения.[40][41] и позволяет фоторецепторным клеткам жить десятилетиями.
У птиц
Сетчатка птицы лишена кровеносных сосудов, возможно, для обеспечения беспрепятственного прохождения света для формирования изображений, что дает лучшее разрешение. Таким образом, считается, что сетчатка птицы питается и снабжается кислородом от специализированного органа, называемого «пектен» или Pecten Oculi, расположенный на слепой зоне или на диске зрительного нерва. Этот орган чрезвычайно богат кровеносными сосудами и, как полагают, обеспечивает питанием и кислородом сетчатку птицы путем диффузии через стекловидное тело. Пектен очень богат активностью щелочной фосфатазы и поляризованными клетками в своей мостиковой части, что соответствует его секреторной роли.[42] Пектеновые клетки заполнены темными гранулами меланина, которые, как предполагалось, сохраняют этот орган в тепле за счет поглощения паразитного света, падающего на пектен. Считается, что это увеличивает скорость метаболизма пектена, тем самым экспортируя больше питательных молекул для удовлетворения строгих энергетических потребностей сетчатки в течение длительных периодов воздействия света.[43]
Биометрическая идентификация и диагностика болезни
Известно, что бифуркации и другие физические характеристики внутренней сосудистой сети сетчатки у разных людей различаются.[44] и эти индивидуальные отклонения использовались для биометрическая идентификация и для раннего выявления начала болезни. Картирование сосудистых бифуркаций - один из основных этапов биометрической идентификации.[45] Результаты таких анализов структуры кровеносных сосудов сетчатки могут быть сопоставлены с достоверными данными.[46] сосудистых бифуркаций изображений глазного дна сетчатки, полученных из набора данных DRIVE.[47] Кроме того, были определены классы судов из набора данных DRIVE,[48] Также доступен автоматизированный метод точного извлечения этих раздвоений.[49] С возрастом видны изменения в кровообращении сетчатки[50] и подверженность загрязнению воздуха,[51] и может указывать на сердечно-сосудистые заболевания, такие как гипертония и атеросклероз.[52][53][54] Определение эквивалентной ширины артериол и венул около диска зрительного нерва также является широко используемым методом выявления сердечно-сосудистых рисков.[55]
Функция
Сетчатка преобразует оптическое изображение в нервные импульсы, начиная с шаблонного возбуждения цветочувствительных пигментов своих палочек и колбочек, фоторецепторные клетки. Возбуждение обрабатывается нейронной системой и различными частями мозга, работающими параллельно, чтобы сформировать представление о внешней среде в мозгу.
Колбочки реагируют на яркий свет и обеспечивают цветовое зрение с высоким разрешением при дневном освещении (также называемое фотопическое зрение ). Реакции стержней насыщены при дневном свете и не влияют на видение паттернов. Однако стержни действительно реагируют на тусклый свет и обеспечивают монохроматическое зрение с низким разрешением при очень низких уровнях освещения (так называемое скопическое зрение ). Освещение в большинстве офисных помещений находится между этими двумя уровнями и называется мезопическое зрение. На мезопических уровнях освещения и стержни, и колбочки активно передают информацию о структуре. Неясно, какой вклад вносит информация о стержне в видение паттернов в этих обстоятельствах.
Реакция колбочек на световые волны различной длины называется их спектральной чувствительностью. В нормальном человеческом зрении спектральная чувствительность конуса подразделяется на один из трех подтипов, часто называемых синим, зеленым и красным, но более точно известный как подтипы чувствительных к короткой, средней и длинной волнам колбочек. Отсутствие одного или нескольких подтипов колбочек приводит к тому, что у людей наблюдается дефицит цветового зрения или различные виды дальтонизм. Эти люди не слепы к предметам определенного цвета, но не могут различать цвета, которые могут различить люди с нормальным зрением. У людей есть это трехцветное зрение, в то время как у большинства других млекопитающих нет колбочек с чувствительным к красному пигментом, и поэтому у них плохое двухцветное цветовое зрение. Однако у некоторых животных есть четыре спектральных подтипа, например форель добавляет ультрафиолетовую подгруппу к коротким, средним и длинным подтипам, которые похожи на людей. Некоторые рыбы также чувствительны к поляризации света.
В фоторецепторах воздействие света гиперполяризует мембрану в виде серии постепенных сдвигов. Внешний сегмент ячейки содержит фотопигмент. Внутри клетки нормальный уровень циклический гуанозинмонофосфат (cGMP) сохраняет канал Na + открытым, и, таким образом, в состоянии покоя клетка деполяризуется. В фотон вызывает сетчатка связаны с рецепторным белком изомеризация к трансретинальный. Это заставляет рецептор активировать несколько G-белки. Это, в свою очередь, заставляет Ga-субъединицу белка активировать фосфодиэстеразу (PDE6), которая разрушает cGMP, что приводит к закрытию Na + циклические нуклеотидные ионные каналы (КПГ). Таким образом, клетка гиперполяризована. Количество выделяемого нейротрансмиттера уменьшается при ярком свете и увеличивается с понижением уровня освещенности. Настоящий фотопигмент обесцвечивается при ярком свете и заменяется только в результате химического процесса, поэтому при переходе от яркого света к темноте глазу может потребоваться до тридцати минут, чтобы достичь полной чувствительности.
При таком возбуждении светом фоторецептор посылает пропорциональный ответ синаптически к биполярные клетки которые, в свою очередь, сигнализируют ганглиозные клетки сетчатки. Фоторецепторы также сшиты горизонтальные ячейки и амакриновые клетки, которые изменяют синаптический сигнал до того, как он достигает ганглиозных клеток, при этом нервные сигналы перемешиваются и комбинируются. Из нервных клеток сетчатки только ганглиозные клетки сетчатки и несколько амакриновых клеток создают потенциалы действия.
В ганглиозных клетках сетчатки есть два типа ответа, в зависимости от рецептивное поле ячейки. Восприимчивые поля ганглиозных клеток сетчатки включают центральную, приблизительно круглую область, где свет оказывает одно влияние на активацию клетки, и кольцевое окружение, где свет имеет противоположный эффект. В ячейках ON увеличение интенсивности света в центре воспринимающего поля приводит к увеличению скорости стрельбы. В ВЫКЛЮЧЕННЫХ ячейках заставляет его уменьшаться. В линейной модели этот профиль отклика хорошо описывается разница гауссиан и является основой для обнаружение края алгоритмы. Помимо этого простого различия, ганглиозные клетки также различаются по хроматической чувствительности и типу пространственного суммирования. Клетки, демонстрирующие линейное пространственное суммирование, называются X-клетками (также называемыми парвоцеллюлярными, P или сверхмалыми ганглиозными клетками), а те, которые демонстрируют нелинейное суммирование, являются Y-клетками (также называемыми магноклеточными, M или паразольными ганглиозными клетками сетчатки), хотя соответствие между X- и Y-клетки (в сетчатке кошки) и P- и M-клетки (в сетчатке приматов) не так просты, как когда-то казалось.
При передаче зрительных сигналов в мозг зрительный путь сетчатка по вертикали делится на две части: височную (ближе к виску) и носовую (ближе к носу) половину. Аксоны из носовой половины пересекают мозг в зрительный перекрест соединиться с аксонами из височной половины другого глаза перед переходом в боковое коленчатое тело.
Хотя в сетчатке более 130 миллионов рецепторов, в зрительном нерве насчитывается всего около 1,2 миллиона волокон (аксонов). Таким образом, большая часть предварительной обработки выполняется внутри сетчатки. В ямка дает наиболее точную информацию. Несмотря на то, что они занимают около 0,01% поля зрения (менее 2 ° угол обзора ) около 10% аксонов зрительного нерва посвящены ямке. Предел разрешения фовеа составляет около 10 000 точек. Информационная емкость оценивается в 500 000 бит в секунду (подробнее о битах см. теория информации ) без цвета или около 600 000 бит в секунду, включая цвет.[56]
Пространственное кодирование

Когда сетчатка посылает в мозг нейронные импульсы, представляющие изображение, она пространственно кодирует (сжимает) эти импульсы, чтобы соответствовать ограниченной емкости зрительного нерва. Сжатие необходимо, потому что их в 100 раз больше фоторецепторные клетки чем ганглиозные клетки. Это делается "декорреляция », который осуществляется« структурами центр-окружение », которые реализуются биполярными и ганглиозными клетками.
В сетчатке есть два типа центрально-окружающих структур - на центрах и вне центра. На центрах есть положительно взвешенный центр и отрицательно взвешенный объем. Вне центров как раз наоборот. Положительный вес более известен как возбуждающий, и отрицательный вес как тормозящий.
Эти центрально-окружающие структуры не являются физически очевидными в том смысле, что их нельзя увидеть, окрашивая образцы ткани и исследуя анатомию сетчатки. Структуры центр-окружение логичны (т.е. математически абстрактны) в том смысле, что они зависят от силы связи между биполярными и ганглиозными клетками. Считается, что прочность связи между ячейками обусловлена количеством и типами ионные каналы встроен в синапсы между биполярными и ганглиозными клетками.
Структуры центр-окружение математически эквивалентны обнаружение края алгоритмы, используемые компьютерными программистами для выделения или улучшения краев цифровой фотографии. Таким образом, сетчатка выполняет операции с импульсами, представляющими изображение, для усиления краев объектов в пределах своего поля зрения. Например, на изображении собаки, кошки и машины именно края этих объектов содержат больше всего информации. Чтобы высшие функции мозга (или компьютера) извлекали и классифицировали такие объекты, как собака и кошка, сетчатка является первым шагом к разделению различных объектов в сцене.
Например, следующие матрица лежит в основе компьютера алгоритм который реализует обнаружение краев. Эта матрица является компьютерным эквивалентом структуры центр-окружение. В этом примере каждый блок (элемент) в этой матрице будет подключен к одному фоторецептору. Фоторецептор в центре - это рецептор тока, который обрабатывается. Центральный фоторецептор умножается на весовой коэффициент +1. Окружающие фоторецепторы являются «ближайшими соседями» к центру и умножаются на значение -1/8. Окончательно вычисляется сумма всех девяти этих элементов. Это суммирование повторяется для каждого фоторецептора в изображении, сдвигаясь влево до конца строки, а затем вниз до следующей строки.
| -1/8 | -1/8 | -1/8 |
| -1/8 | +1 | -1/8 |
| -1/8 | -1/8 | -1/8 |
Общая сумма этой матрицы равна нулю, если все входы от девяти фоторецепторов имеют одинаковое значение. Нулевой результат означает, что изображение было однородным (неизменным) внутри этого небольшого участка. Отрицательные или положительные суммы означают, что изображение изменялось (изменялось) в пределах этого небольшого участка из девяти фоторецепторов.
Вышеупомянутая матрица является лишь приближением к тому, что действительно происходит внутри сетчатки. Отличия заключаются в следующем:
- Приведенный выше пример называется «сбалансированным». Термин сбалансированный означает, что сумма отрицательных весов равна сумме положительных весов, так что они полностью компенсируются. Ганглиозные клетки сетчатки почти никогда не сбалансированы идеально.
- Стол имеет квадратную форму, в то время как центрально-окружающие структуры сетчатки имеют круглую форму.
- Нейроны действуют на шипованные поезда движение вниз по нервной клетке аксоны. Компьютеры работают на одном плавающая точка число, которое практически постоянно на каждом входе пиксель. (Компьютерный пиксель в основном эквивалент биологического фоторецептора.)
- Сетчатка глаза выполняет все эти вычисления параллельно, в то время как компьютер обрабатывает каждый пиксель по очереди. Сетчатка не выполняет повторных суммирований и сдвигов, как компьютер.
- Наконец, горизонтальный и амакриновые клетки играют важную роль в этом процессе, но здесь это не представлено.
Вот пример входного изображения и того, как обнаружение краев изменит его.

Как только изображение пространственно кодируется структурами центр-окружение, сигнал отправляется по зрительному нерву (через аксоны ганглиозных клеток) через зрительный перекрест в LGN (латеральное коленчатое ядро ). Точная функция LGN в настоящее время неизвестна. Затем результат LGN отправляется в заднюю часть мозга. В частности, выход LGN "излучается" в V1. первичная зрительная кора.
Упрощенный поток сигналов: фоторецепторы → биполярный → ганглион → хиазм → LGN → кора V1

Клиническое значение
Существует множество наследственных и приобретенных заболеваний или нарушений, которые могут повлиять на сетчатку. Некоторые из них включают:
- Пигментный ретинит представляет собой группу генетических заболеваний, поражающих сетчатку и вызывающих потерю ночного и периферического зрения.
- Дегенерация желтого пятна описывает группу заболеваний, характеризующихся потерей центрального зрения из-за гибели или повреждения клеток в пятно.
- Конусно-стержневая дистрофия (CORD) описывает ряд заболеваний, при которых потеря зрения вызвана ухудшением шишки и / или стержни в сетчатке.
- В разделение сетчатки сетчатка отделяется от задней части глазного яблока. Игнипунктура это устаревший метод лечения. Период, термин отслойка сетчатки используется для описания отделения нейросенсорной сетчатки от пигментный эпителий сетчатки.[57] Существует несколько современных методов лечения отслоения сетчатки: пневматическая ретинопексия, склеральная пряжка, криотерапия, лазерная фотокоагуляция и pars plana витрэктомия.
- Обе гипертония и сахарный диабет может вызвать повреждение крошечных кровеносных сосудов, снабжающих сетчатку, что приводит к гипертоническая ретинопатия и диабетическая ретинопатия.
- Ретинобластома это рак сетчатки.
- Заболевания сетчатки в собаки включают дисплазия сетчатки, прогрессирующая атрофия сетчатки, и внезапная приобретенная дегенерация сетчатки.
- Липемия сетчатки представляет собой белый цвет сетчатки, который может возникать в результате отложения липидов в дефицит липопротеинлипазы.
- Отслойка сетчатки. Нервная сетчатка иногда отделяется от пигментного эпителия. В некоторых случаях причиной такой отслойки является повреждение глазного яблока, которое позволяет жидкости или крови собираться между нервной сетчаткой и пигментным эпителием. Detachment is occasionally caused by contracture of fine collagenous fibrils in the vitreous humor, which pull areas of the retina toward the interior of the globe.[58]
- Куриная слепота : Night blindness occurs in any person with severe vitamin A deficiency. The reason for this is that without vitamin A, the amounts of retinal and rhodopsin that can be formed are severely depressed. This condition is called night blindness because the amount of light available at night is too little to permit adequate vision in vitamin A–deficient persons.[59]
Диагностика
A number of different instruments are available for the diagnosis of diseases and disorders affecting the retina. Офтальмоскопия и fundus photography have long been used to examine the retina. Недавно, адаптивная оптика has been used to image individual rods and cones in the living human retina, and a company based in Scotland has engineered technology that allows physicians to observe the complete retina without any discomfort to patients.[60]
В electroretinogram используется, чтобы неинвазивно measure the retina's electrical activity, which is affected by certain diseases. A relatively new technology, now becoming widely available, is optical coherence tomography (OCT). This non-invasive technique allows one to obtain a 3D volumetric or high resolution cross-sectional tomogram of the fine structures of the retina, with гистологический качественный. Retinal vessel analysis is a non-invasive method to examine the small arteries and veins in the retina which allows to draw conclusions about the morphology and the function of small vessels elsewhere in the human body. It has been established as a predictor of сердечно-сосудистые заболевания[61] and seems to have, according to a study published in 2019, potential in the early detection of Alzheimer's disease.[62]
Уход
Treatment depends upon the nature of the disease or disorder.
Common treatment modalities
The following are commonly modalities of management for retinal disease:
- Интравитреальный medication, such as anti-VEGF или же кортикостероид агенты
- Витреоретинальная хирургия
- Use of nutritional supplements
- Modification of systemic risk factors for retinal disease
Uncommon treatment modalities
Rare or uncommon methods of treatment for retinal disease |
|---|
Retinal gene therapy Генная терапия holds promise as a potential avenue to cure a wide range of retinal diseases. This involves using a non-infectious virus to shuttle a gene into a part of the retina. Рекомбинантный аденоассоциированный вирус (rAAV) vectors possess a number of features that render them ideally suited for retinal gene therapy, including a lack of pathogenicity, minimal immunogenicity, and the ability to transduce postmitotic cells in a stable and efficient manner.[63] rAAV vectors are increasingly utilized for their ability to mediate efficient transduction of пигментный эпителий сетчатки (RPE), фоторецепторные клетки и ганглиозные клетки сетчатки. Each cell type can be specifically targeted by choosing the appropriate combination of AAV serotype, promoter, and intraocular injection site. Several clinical trials have already reported positive results using rAAV to treat Врожденный амавроз Лебера, showing that the therapy was both safe and effective.[64][65] There were no serious adverse events, and patients in all three studies showed improvement in their visual function as measured by a number of methods. The methods used varied among the three trials, but included both functional methods such as visual acuity[65][66][67] and functional mobility[66][67][68] as well as objective measures that are less susceptible to bias, such as the pupil's ability to respond to light[64][69] and improvements on functional MRI.[70] Improvements were sustained over the long-term, with patients continuing to do well after more than 1.5 years.[64][65] The unique architecture of the retina and its relatively immune-privileged environment help this process.[71] Узкие стыки которые образуют blood retinal barrier separate the subretinal space from the blood supply, thus protecting it from microbes and most immune-mediated damage, and enhancing its potential to respond to vector-mediated therapies. The highly compartmentalized anatomy of the eye facilitates accurate delivery of therapeutic vector suspensions to specific tissues under direct visualization using microsurgical techniques.[72] In the sheltered environment of the retina, AAV vectors are able to maintain high levels of трансген expression in the retinal pigmented epithelium (RPE), photoreceptors, or ganglion cells for long periods of time after a single treatment. In addition, the eye and the visual system can be routinely and easily monitored for visual function and retinal structural changes after injections with noninvasive advanced technology, such as visual acuities, contrast sensitivity, глазное дно auto-fluorescence (FAF), dark-adapted visual thresholds, vascular diameters, pupillometry, electroretinography (ERG), multifocal ERG and optical coherence tomography (OCT).[73] This strategy is effective against a number of retinal diseases that have been studied, including neovascular diseases that are features of возрастная дегенерация желтого пятна, диабетическая ретинопатия и ретинопатия недоношенных. Since the regulation of vascularization in the mature retina involves a balance between endogenous positive факторы роста, Такие как фактор роста эндотелия сосудов (VEGF) and inhibitors of ангиогенез, such as pigment epithelium-derived factor (PEDF ), rAAV-mediated expression of PEDF, angiostatin, and the soluble VEGF receptor sFlt-1, which are all antiangiogenic proteins, have been shown to reduce aberrant vessel formation in animal models.[74] Since specific gene therapies cannot readily be used to treat a significant fraction of patients with retinal dystrophy, there is a major interest in developing a more generally applicable survival factor therapy. Нейротрофические факторы have the ability to modulate neuronal growth during development to maintain existing cells and to allow recovery of injured neuronal populations in the eye. AAV encoding neurotrophic factors such as fibroblast growth factor (FGF) family members and GDNF either protected photoreceptors from apoptosis or slowed down cell death.[74] Трансплантация органовТрансплантация of retinas has been attempted, but without much success. В Массачусетский технологический институт, The University of Southern California, RWTH Aachen University, and the Университет Нового Южного Уэльса, an "artificial retina" is under development: an implant which will bypass the photoreceptors of the retina and stimulate the attached nerve cells directly, with signals from a digital camera. |
История
In 1894, Сантьяго Рамон-и-Кахаль published the first major characterization of retinal neurons in Retina der Wirbelthiere (The Retina of Vertebrates).[75]
Джордж Уолд, Халдан Кеффер Хартлайн, и Рагнар Гранит выиграл 1967 Нобелевская премия по физиологии и медицине for their scientific research on the retina.[76]
Недавний Пенсильванский университет study calculated that the approximate пропускная способность of human retinas is 8.75 megabits per second, whereas a морская свинка 's retinal transfer rate is 875 kilobits per second.[77]
Макларен & Pearson and colleagues at Университетский колледж Лондона и Глазная больница Мурфилдс in London, in 2006, showed that фоторецепторные клетки could be transplanted successfully in the mouse retina if donor cells were at a critical developmental stage.[78] Recently Ader and colleagues in Dublin showed, using the electron microscope, that transplanted photoreceptors formed synaptic connections.[79]
В 2012, Себастьян Сунг and his laboratory at Массачусетский технологический институт запущен EyeWire, онлайн Гражданская наука game where players trace neurons in the retina.[80] The goals of the EyeWire project are to identify specific cell types within the known broad classes of retinal cells, and to map the connections between neurons in the retina, which will help to determine how vision works.[81][82]
Дополнительные изображения
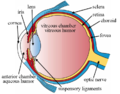
The structures of the eye labeled

Another view of the eye and the structures of the eye labeled

Illustration of image as 'seen' by the retina independent of optic nerve and striate cortex processing.
Смотрите также
- Adeno associated virus and gene therapy of the human retina
- Чарльз Шепенс – "the father of modern retinal surgery"
- Эволюция глаза
- Duplex retina
- Retinal scan
- List of xanthoma variants associated with hyperlipoproteinemia subtypes
- Родопсин
Рекомендации
- ^ J, Krause William (2005). Основы гистологии человека Краузе для студентов-медиков. Boca Raton, FL: Universal Publishers. ISBN 978-1-58112-468-2.
- ^ а б c d е ж грамм "Sensory Reception: Human Vision: Structure and function of the Human Eye" vol. 27, Encyclopædia Britannica, 1987
- ^ «Архивная копия». В архиве из оригинала 11 марта 2013 г.. Получено 11 февраля 2013.CS1 maint: заархивированная копия как заголовок (связь)
- ^ а б Kolb, Helga (1995). "Simple Anatomy of the Retina". Webvision. PMID 21413391. Получено 1 января 2018.
- ^ Kolb, Helga. "Photoreceptors". Webvision. Получено 11 января 2018.
- ^ Franze K, Grosche J, Skatchkov SN, Schinkinger S, Foja C, Schild D, Uckermann O, Travis K, Reichenbach A, Guck J (2007). "Muller cells are living optical fibers in the vertebrate retina". Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 104 (20): 8287–8292. Bibcode:2007PNAS..104.8287F. Дои:10.1073/pnas.0611180104. ЧВК 1895942. PMID 17485670.
- ^ Baker, Oliver (23 April 2010). "Focus: Eye Cells as Light Pipes". Phys. Rev. Focus. 25 (15). Дои:10.1103/physrevfocus.25.15.
- ^ а б Bringmann A, Syrbe S, Görner K, Kacza J, Francke M, Wiedemann P, Reichenbach A (2018). "The primate fovea: Structure, function and development". Prog Retin Eye Res. 66: 49–84. Дои:10.1016/j.preteyeres.2018.03.006. PMID 29609042. S2CID 5045660.
- ^ Sperling, L.; Hubbard, R. (1 February 1975). "Squid retinochrome". Журнал общей физиологии. 65 (2): 235–251. Дои:10.1085/jgp.65.2.235. ISSN 0022-1295. ЧВК 2214869. PMID 235007.
- ^ "How spiders see the world – Australian Museum". www.australian.museum. В архиве из оригинала 12 сентября 2017 г.. Получено 5 декабря 2017.
- ^ Drazen, J. C.; Yeh, J.; Friedman, J .; Condon, N. (June 2011). "Metabolism and enzyme activities of hagfish from shallow and deep water of the Pacific Ocean". Сравнительная биохимия и физиология, часть A: Молекулярная и интегративная физиология. 159 (2): 182–187. Дои:10.1016/j.cbpa.2011.02.018. PMID 21356325.
- ^ Foundations of Vision В архиве 3 декабря 2013 г. Wayback Machine, Brian A. Wandell
- ^ The Retinal Tunic. В архиве 18 May 2007 at the Wayback Machine Virginia–Maryland Regional College of Veterinary Medicine
- ^ Goldberg AF, Moritz OL, Williams DS (2016). "Molecular basis for photoreceptor outer segment architecture". Prog Retin Eye Res. 55: 52–81. Дои:10.1016/j.preteyeres.2016.05.003. ЧВК 5112118. PMID 27260426.
- ^ Arshavsky VY, Burns ME (2012). "Photoreceptor signaling: supporting vision across a wide range of light intensities". J Biol Chem. 287 (3): 1620–1626. Дои:10.1074/jbc.R111.305243. ЧВК 3265842. PMID 22074925.
- ^ Guyton and Hall Physiology. п. 612.
- ^ Sparrow JR, Hicks D, Hamel CP (2010). "The retinal pigment epithelium in health and disease". Curr Mol Med. 10 (9): 802–823. Дои:10.2174/156652410793937813. ЧВК 4120883. PMID 21091424.
- ^ Letelier J, Bovolenta P, Martínez-Morales JR (2017). "The pigmented epithelium, a bright partner against photoreceptor degeneration". J Neurogenet. 31 (4): 203–215. Дои:10.1080/01677063.2017.1395876. PMID 29113536. S2CID 1351539.
- ^ Shepherd, Gordon (2004). The Synaptic Organization of the Brain. Нью-Йорк: Издательство Оксфордского университета. стр.217 –225. ISBN 978-0-19-515956-1.
- ^ Ромер, Альфред Шервуд; Парсонс, Томас С. (1977). Тело позвоночного. Филадельфия, Пенсильвания: Holt-Saunders International. п. 465. ISBN 978-0-03-910284-5.
- ^ Guyton and Hall Physiology. п. 609.
- ^ а б c Cuenca, Nicolás; Ortuño-Lizarán, Isabel; Pinilla, Isabel (March 2018). "Cellular Characterization of OCT and Outer Retinal Bands Using Specific Immunohistochemistry Markers and Clinical Implications" (PDF). Офтальмология. 125 (3): 407–422. Дои:10.1016/j.ophtha.2017.09.016. HDL:10045/74474. PMID 29037595.
- ^ а б c d е ж грамм час я j k л м п о п q Staurenghi, Giovanni; Sadda, Srinivas; Чакраварти, Уша; Spaide, Richard F. (2014). "Proposed Lexicon for Anatomic Landmarks in Normal Posterior Segment Spectral-Domain Optical Coherence Tomography". Офтальмология. 121 (8): 1572–1578. Дои:10.1016/j.ophtha.2014.02.023. PMID 24755005.
- ^ Spectral domain optical coherence tomography in macular diseases. Meyer, Carsten H.; Saxena, Sandeep; Sadda, SriniVas R. New Delhi: Springer. 2017 г. ISBN 978-8132236108. OCLC 964379175.CS1 maint: другие (связь)
- ^ а б Hildebrand, Göran Darius; Fielder, Alistair R. (2011). Pediatric Retina. Шпрингер, Берлин, Гейдельберг. С. 39–65. Дои:10.1007/978-3-642-12041-1_2. ISBN 978-3642120404.
- ^ Turgut, Burak; University, Fırat; Medicine, School of; Ophthalmology, Department of; Elazig; Turkey (2017). "Past and Present Terminology for the Retinal and Choroidal Structures in Optical Coherence Tomography". European Ophthalmic Review. 11 (1): 59. Дои:10.17925/eor.2017.11.01.59.
- ^ "Outer Retinal Layers as Predictors of Vision Loss". Review of Ophthalmology.
- ^ "The ABCs of OCT". Обзор оптометрии.
- ^ Sherman, J (June 2009). "Photoreceptor integrity line joins the nerve fiber layer as key to clinical diagnosis". Оптометрии. 80 (6): 277–278. Дои:10.1016/j.optm.2008.12.006. PMID 19465337.
- ^ Boston, Marco A. Bonini Filho, MD, and Andre J. Witkin, MD. "Outer Retinal Layers as Predictors of Vision Loss". Получено 7 апреля 2018.
- ^ а б c Heavner, W; Pevny, L (1 December 2012). "Eye development and retinogenesis". Перспективы Колд-Спринг-Харбор в биологии. 4 (12): a008391. Дои:10.1101 / cshperspect.a008391. ЧВК 3504437. PMID 23071378.
- ^ Halder, G; Callaerts, P; Gehring, WJ (24 March 1995). «Индукция эктопических глаз путем направленной экспрессии гена безглазых у дрозофилы». Наука. 267 (5205): 1788–1792. Bibcode:1995Sci...267.1788H. Дои:10.1126/science.7892602. PMID 7892602.
- ^ Cepko, Connie (September 2014). "Intrinsically different retinal progenitor cells produce specific types of progeny". Обзоры природы Неврология. 15 (9): 615–627. Дои:10.1038/nrn3767. ISSN 1471-003X. PMID 25096185. S2CID 15038502.
- ^ Hatakeyama, J; Kageyama, R (February 2004). "Retinal cell fate determination and bHLH factors". Семинары по клеточной биологии и биологии развития. 15 (1): 83–89. Дои:10.1016/j.semcdb.2003.09.005. PMID 15036211.
- ^ а б Lo Giudice, Quentin; Leleu, Marion; La Manno, Gioele; Fabre, Pierre J. (1 September 2019). "Single-cell transcriptional logic of cell-fate specification and axon guidance in early-born retinal neurons". Разработка. 146 (17): dev178103. Дои:10.1242/dev.178103. ISSN 0950-1991. PMID 31399471.
- ^ Remington, Lee Ann (2012). Clinical anatomy and physiology of the visual system (3-е изд.). St. Louis: Elsevier/Butterworth-Heinemann. ISBN 978-1-4377-1926-0. OCLC 745905738.
- ^ Yu, DY; Yu, PK; Cringle, SJ; Kang, MH; Su, EN (May 2014). "Functional and morphological characteristics of the retinal and choroidal vasculature". Прогресс в исследованиях сетчатки и глаз. 40: 53–93. Дои:10.1016/j.preteyeres.2014.02.001. PMID 24583621. S2CID 21312546.
- ^ Kiel, Jeffrey W. Анатомия. Morgan & Claypool Life Sciences. В архиве из оригинала 5 декабря 2017 г.. Получено 17 апреля 2017.
- ^ Strauss, Olaf. "The retinal pigment epithelium". Webvision. Получено 1 января 2018.
- ^ Photobiology of the retina "Light-Induced Damage to the Retina". В архиве из оригинала от 9 августа 2012 г.. Получено 27 июля 2012.
- ^ Diagrammatic representation of disc shedding and phagosome retrieval into the pigment epithelial cell «Архивная копия». В архиве из оригинала 21 сентября 2012 г.. Получено 27 июля 2012.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Bawa S.R.; YashRoy R.C. (1972). "Effect of dark and light adaptation on the retina and pecten of chicken". Экспериментальные исследования глаз. 13 (1): 92–97. Дои:10.1016/0014-4835(72)90129-7. PMID 5060117. В архиве from the original on 9 October 2014.
- ^ Bawa, S.R.; YashRoy, R.C. (1974). "Structure and function of vulture pecten". Клетки Ткани Органы. 89 (3): 473–480. Дои:10.1159/000144308. PMID 4428954. В архиве from the original on 14 July 2015.
- ^ Sherman, T (1981). "On connecting large vessels to small – the meaning of murray law". Журнал общей физиологии. 78 (4): 431–453. Дои:10.1085/jgp.78.4.431. ЧВК 2228620. PMID 7288393.
- ^ Azzopardi G.; Petkov N. (2011). Detection of retinal vascular bifurcations by trainable V4-like filters, in Computer Analysis of Images and Patterns (CAIP), Seville (PDF). Конспект лекций по информатике. 6854. pp. 451–459. Дои:10.1007/978-3-642-23672-3_55. ISBN 978-3-642-23671-6. В архиве (PDF) из оригинала от 9 августа 2017 года.
- ^ "Retinal fundus images – Ground truth of vascular bifurcations and crossovers". Гронингенский университет. Получено 20 апреля 2018.
- ^ "DRIVE: Digital Retinal Images for Vessel Extraction". Image Sciences Institute, Утрехтский университет. Получено 20 апреля 2018.
- ^ Qureshi, T. A.; Habib, M .; Хантер, А .; Al-Diri, B. (June 2013). A manually-labeled, artery/vein classified benchmark for the DRIVE dataset. Proceedings of the 26th IEEE International Symposium on Computer-Based Medical Systems. С. 485–488. Дои:10.1109/cbms.2013.6627847. ISBN 978-1-4799-1053-3. S2CID 7705121.
- ^ Qureshi, T. A.; Хантер, А .; Al-Diri, B. (June 2014). A Bayesian Framework for the Local Configuration of Retinal Junctions. Конференция IEEE 2014 года по компьютерному зрению и распознаванию образов. pp. 3105–3110. CiteSeerX 10.1.1.1026.949. Дои:10.1109/cvpr.2014.397. ISBN 978-1-4799-5118-5. S2CID 14654500.
- ^ Adar SD, Klein R, Klein BE, Szpiro AA, Cotch MF, Wong TY, et al. (2010). "Air Pollution and the microvasculature: a crosssectional assessment of in vivo retinal images in the population based multiethnic study of atherosclerosis (MESA)". PLOS Med. 7 (11): e1000372. Дои:10.1371/journal.pmed.1000372. ЧВК 2994677. PMID 21152417.
- ^ Louwies, Tijs; Panis, Luc Int; Kicinski, Michal; Boever, Patrick De; Nawrot, Tim S. (2013). "Retinal Microvascular Responses to Short-Term Changes in Particulate Air Pollution in Healthy Adults". Перспективы гигиены окружающей среды. 121 (9): 1011–1016. Дои:10.1289/ehp.1205721. ЧВК 3764070. PMID 23777785.
- ^ Tso, Mark O.M.; Jampol, Lee M. (1982). "Pathophysiology of Hypertensive Retinopathy". Офтальмология. 89 (10): 1132–1145. Дои:10.1016/s0161-6420(82)34663-1. PMID 7155524.
- ^ Chapman, N.; Dell'omo, G.; Sartini, M. S.; Witt, N.; Hughes, A .; Thom, S.; Pedrinelli, R. (1 August 2002). "Peripheral vascular disease is associated with abnormal arteriolar diameter relationships at bifurcations in the human retina". Клиническая наука. 103 (2): 111–116. Дои:10.1042/cs1030111. ISSN 0143-5221. PMID 12149100.
- ^ Patton, N.; Aslam, T.; MacGillivray, T.; Deary, I.; Dhillon, B.; Eikelboom, R.; Yogesan, K.; Constable, I. (2006). "Retinal image analysis: Concepts, applications and potential". Прогресс в исследованиях сетчатки и глаз. 25 (1): 99–127. Дои:10.1016/j.preteyeres.2005.07.001. PMID 16154379. S2CID 7434103.
- ^ Wong TY, Knudtson MD, Klein R, Klein BE, Meuer SM, Hubbard LD (2004). "Computer assisted measurement of retinal vessel diameters in the Beaver Dam Eye Study: methodology, correlation between eyes, and effect of refractive errors". Офтальмология. 111 (6): 1183–1190. Дои:10.1016/j.ophtha.2003.09.039. PMID 15177969.
- ^ Handbook of visual display technology. Chen, Janglin., Cranton, Wayne., Fihn, Mark. (2-е изд.). Чам, Швейцария: Springer. 2016 г. ISBN 9783319143460. OCLC 962009228.CS1 maint: другие (связь)
- ^ Сетчатка (4-е изд.). Philadelphia: Elsevier/Mosby. 2006. pp. 2013–2015. ISBN 978-0-323-02598-0. OCLC 62034580.
- ^ Guyton and Hall Physiology. п. 609.
- ^ Guyton and Hall Physiology. п. 612.
- ^ Seeing into the Future Ingenia, March 2007
- ^ Seidelmann, SB; и другие. (1 ноября 2016 г.). "Retinal Vessel Calibers in Predicting Long-Term Cardiovascular Outcomes". Тираж. 134 (18): 1328–1338. Дои:10.1161/CIRCULATIONAHA.116.023425. ЧВК 5219936. PMID 27682886.
- ^ Querques, G; и другие. (11 января 2019 г.). "Functional and morphological changes of the retinal vessels in Alzheimer's disease and mild cognitive impairment". Научные отчеты. 9 (63): 63. Bibcode:2019NatSR...9...63Q. Дои:10.1038/s41598-018-37271-6. ЧВК 6329813. PMID 30635610.
- ^ Dinculescu Astra; Glushakova Lyudmyla; Seok-Hong Min; Hauswirth William W (2005). «Аденоассоциированная вирусная генная терапия заболеваний сетчатки». Генная терапия человека. 16 (6): 649–663. Дои:10.1089 / hum.2005.16.649. PMID 15960597.
- ^ а б c Cideciyan A. V .; Hauswirth W. W .; Aleman T. S .; Kaushal S .; Schwartz S. B .; Boye S. L.; Windsor E. A. M.; и другие. (2009). "Human RPE65 gene therapy for Leber congenital amaurosis: persistence of early visual improvements and safety at 1 year". Генная терапия человека. 20 (9): 999–1004. Дои:10.1089/hum.2009.086. ЧВК 2829287. PMID 19583479.
- ^ а б c Simonelli F .; Магуайр А. М .; Testa F.; Pierce E. A.; Mingozzi F .; Bennicelli J. L .; Rossi S.; и другие. (2010). "Gene therapy for Leber's congenital amaurosis is safe and effective through 1.5 years after vector administration". Молекулярная терапия. 18 (3): 643–650. Дои:10.1038/mt.2009.277. ЧВК 2839440. PMID 19953081.
- ^ а б Магуайр А. М .; Simonelli F .; Pierce E. A.; Пью Э. Н .; Mingozzi F .; Bennicelli J .; Banfi S .; и другие. (2008). «Безопасность и эффективность переноса генов при врожденном амаврозе Лебера». Медицинский журнал Новой Англии. 358 (21): 2240–2248. Дои:10.1056 / NEJMoa0802315. ЧВК 2829748. PMID 18441370.
- ^ а б Магуайр А. М .; High K. A.; Auricchio A.; Wright J. F.; Pierce E. A.; Testa F.; Mingozzi F .; и другие. (2009). "Age-dependent effects of RPE65 gene therapy for Leber's congenital amaurosis: a phase 1 dose-escalation trial". Ланцет. 374 (9701): 1597–1605. Дои:10.1016/S0140-6736(09)61836-5. ЧВК 4492302. PMID 19854499.
- ^ Bainbridge J. W. B .; Smith A. J .; Баркер С. С .; Робби С .; Хендерсон Р .; Балагган К .; Вишванатан А .; и другие. (2008). "Effect of gene therapy on visual function in Leber's congenital amaurosis" (PDF). Медицинский журнал Новой Англии. 358 (21): 2231–2239. CiteSeerX 10.1.1.574.4003. Дои:10.1056 / NEJMoa0802268. PMID 18441371. В архиве (PDF) с оригинала от 11 августа 2017 года.
- ^ Hauswirth W. W .; Aleman T. S .; Kaushal S .; Cideciyan A. V .; Schwartz S. B .; Ван Л .; Конлон Т. Дж .; и другие. (2008). «Лечение врожденного амавроза Лебера, вызванного мутациями RPE65 с помощью субретинальной инъекции вектора аденоассоциированного вирусного гена: краткосрочные результаты исследования фазы I». Генная терапия человека. 19 (10): 979–990. Дои:10.1089 / гум.2008.107. ЧВК 2940541. PMID 18774912.
- ^ Ashtari M.; Cyckowski L. L.; Monroe J. F.; Marshall K. A.; Chung D. C.; Auricchio A.; Simonelli F .; и другие. (2011). "The human visual cortex responds to gene therapy-mediated recovery of retinal function". Журнал клинических исследований. 121 (6): 2160–2168. Дои:10.1172/JCI57377. ЧВК 3104779. PMID 21606598.
- ^ Беннетт Дж. (2003). «Иммунный ответ после внутриглазной доставки рекомбинантных вирусных векторов». Генная терапия. 10 (11): 977–982. Дои:10.1038 / sj.gt.3302030. PMID 12756418.
- ^ Curace Enrico M.; Auricchio Alberto (2008). "Versatility of AAV vectors for retinal gene transfer". Исследование зрения. 48 (3): 353–359. Дои:10.1016/j.visres.2007.07.027. PMID 17923143. S2CID 9926758.
- ^ den Hollander, Anneke I.; Roepman, Ronald; Koenekoop, Robert K.; Cremers, Frans P.M. (2008). "Leber congenital amaurosis: Genes, proteins and disease mechanisms". Прогресс в исследованиях сетчатки и глаз. 27 (4): 391–419. Дои:10.1016/j.preteyeres.2008.05.003. PMID 18632300. S2CID 30202286.
- ^ а б Rolling, F. (2004). "Recombinant AAV-mediated gene transfer to the retina: gene therapy perspectives". Генная терапия. 11 (S1): S26–S32. Дои:10.1038/sj.gt.3302366. ISSN 0969-7128. PMID 15454954.
- ^ "Santiago Ramón y Cajal – Biographical". www.nobelprize.org. В архиве из оригинала от 6 октября 2015 г.. Получено 20 октября 2015.
- ^ "Nobelprize.org". nobelprize.org. В архиве с оригинала 30 июня 2017 г.. Получено 5 декабря 2017.
- ^ "Calculating the speed of sight". newscientist.com. В архиве с оригинала 31 мая 2015 г.. Получено 5 декабря 2017.
- ^ MacLaren, RE; Pearson, RA; MacNeil, A; и другие. (Ноябрь 2006 г.). "Retinal repair by transplantation of photoreceptor precursors" (PDF). Природа. 444 (7116): 203–7. Bibcode:2006Natur.444..203M. Дои:10.1038/nature05161. HDL:2027.42/62596. PMID 17093405. S2CID 4415311.
- ^ Bartsch, U.; Oriyakhel, W.; Kenna, P. F.; Linke, S.; Ричард, G .; Petrowitz, B.; Humphries, P.; Farrar, G. J.; Ader, M. (2008). "Retinal cells integrate into the outer nuclear layer and differentiate into mature photoreceptors after subretinal transplantation into adult mice". Экспериментальные исследования глаз. 86 (4): 691–700. Дои:10.1016/j.exer.2008.01.018. PMID 18329018.
- ^ "About: EyeWire". Архивировано из оригинал 13 февраля 2012 г.. Получено 26 марта 2012.
- ^ "Retina << EyeWire". Архивировано из оригинал 24 марта 2012 г.. Получено 27 марта 2012.
- ^ "EyeWire". В архиве из оригинала 24 апреля 2012 г.. Получено 27 марта 2012.
дальнейшее чтение
- S. Ramón y Cajal, Histologie du Système Nerveux de l'Homme et des Vertébrés, Maloine, Paris, 1911.
- Rodieck RW (1965). "Quantitative analysis of cat retinal ganglion cell response to visual stimuli". Видение Res. 5 (11): 583–601. Дои:10.1016/0042-6989(65)90033-7. PMID 5862581.
- Wandell, Brian A. (1995). Foundations of vision. Sunderland, Mass: Sinauer Associates. ISBN 978-0-87893-853-7.
- Wässle H, Boycott BB (1991). "Functional architecture of the mammalian retina". Physiol. Rev. 71 (2): 447–480. Дои:10.1152/physrev.1991.71.2.447. PMID 2006220.
- Schulz HL, Goetz T, Kaschkoetoe J, Weber BH (2004). "The Retinome – Defining a reference transcriptome of the adult mammalian retina/retinal pigment epithelium". BMC Genomics (Об транскриптом for eye colour). 5 (1): 50. Дои:10.1186/1471-2164-5-50. ЧВК 512282. PMID 15283859.
- Dowling, John (2007). "Сетчатка". Scholarpedia. 2 (12): 3487. Bibcode:2007SchpJ...2.3487D. Дои:10.4249/scholarpedia.3487.
- Khoshbin-e-Khoshnazar, M.R. (2014). "Quantum Superposition in the Retina:Evidences and Proposals". Нейроквантология. 12 (1): 97–101. Дои:10.14704/nq.2014.12.1.685.
внешняя ссылка
- Histology of the Eye, edited by William Krause, Dept. Pathology and Anatomical science, University of Missouri School of Medicine
- Eye, Brain, and Vision – online book – by David Hubel
- Kolb, H., Fernandez, E., & Nelson, R. (2003). Webvision: The neural organization of the vertebrate retina. Salt Lake City, Utah: John Moran Eye Center, Университет Юты. Проверено 22 июля 2014 года.
- Demo: Artificial Retina, MIT Technology Review, September 2004. Reports on implant research at Technology Review
- Successful photoreceptor transplantation, MIT Technology Review, November 2006. How stem cells might restore sight Technology Review
- Australian Vision Prosthesis Group, Graduate School of Biomedical Engineering, Университет Нового Южного Уэльса
- RetinaCentral, Genetics and Diseases of the Human Retina at Вюрцбургский университет
- Retinal layers image. NeuroScience 2nd Ed at Национальная медицинская библиотека США
- Jeremy Nathans's Seminars: "The Vertebrate Retina: Structure, Function, and Evolution"
- Retina – Cell Centered Database
- Histology image: 07901loa - Система обучения гистологии в Бостонском университете
- Энциклопедия MedlinePlus: 002291





