Кислотная сила - Acid strength
Кислотная сила это тенденция кислота, символизируемый химическая формула HA, чтобы диссоциировать на протон, H+, и анион, А−. В диссоциация сильной кислоты в растворе эффективно завершается, за исключением ее наиболее концентрированных растворов.
- HA → H+ + А−
Примеры сильные кислоты находятся соляная кислота (HCl), хлорная кислота (HClO4), азотная кислота (HNO3) и серная кислота (ЧАС2ТАК4).
Слабая кислота диссоциирует лишь частично, причем недиссоциированная кислота и продукты ее диссоциации присутствуют в растворе в равновесии друг с другом.
- HA ⇌ H+ + А−.
Уксусная кислота (CH3COOH) является примером слабой кислоты. Сила слабой кислоты количественно определяется ее константа диссоциации кислоты, пKа ценить.
Сила слабого органический кислота может зависеть от эффектов заместителей. Сила неорганический кислота зависит от степень окисления для атома, к которому может быть присоединен протон. Сила кислоты зависит от растворителя. Например, хлористый водород представляет собой сильную кислоту в водном растворе, но является слабой кислотой при растворении в ледяная уксусная кислота.
Меры силы кислоты
Обычной мерой силы кислоты является ее константа диссоциации кислоты (Kа), который может быть определяется экспериментально к титрование методы. Более сильные кислоты имеют больший Kа и меньшая логарифмическая константа (pKа = −log Kа) чем более слабые кислоты. Чем сильнее кислота, тем легче она теряет протон, H+. Два ключевых фактора, которые способствуют простоте депротонирование являются полярность связи H-A и размер атома A, которые определяют прочность связи H-A. Сила кислоты также зависит от стабильности конъюгированной основы.
Пока рKа значение измеряет тенденцию кислого растворенного вещества переносить протон в стандартный растворитель (чаще всего вода или ДМСО ), склонность кислотного растворителя переносить протон в эталонное растворенное вещество (чаще всего слабое анилин база) измеряется ее Функция кислотности Гаммета, то ЧАС0 ценить. Хотя эти два понятия силы кислоты часто сводятся к одной и той же общей тенденции вещества отдавать протон, pKа и ЧАС0 значения являются мерой различных свойств и иногда могут отличаться. Например, фтороводород, растворенный в воде (стр.Kа = 3,2) или ДМСО (pKа = 15), имеет pKа значения, указывающие на то, что он подвергается неполной диссоциации в этих растворителях, что делает его слабой кислотой. Однако, как тщательно высушенная чистая кислая среда, фтороводород имеет ЧАС0 значение –15,[1] что делает его более протонирующей средой, чем 100% серная кислота, и, таким образом, по определению суперкислотный.[2] (Во избежание двусмысленности в остальной части этой статьи термин «сильная кислота» будет, если не указано иное, относиться к кислоте, которая является сильной, если измерять ее pKа значение (pKа <–1,74). Такое использование согласуется с обычным языком большинства практикующих химиков.)
Когда рассматриваемая кислая среда представляет собой разбавленный водный раствор, ЧАС0 примерно равно pH значение, которое представляет собой отрицательный логарифм концентрации водного H+ в растворе. PH простого раствора кислоты в воде определяется как Kа и концентрация кислоты. Для слабых кислотных растворов это зависит от степень диссоциации, который может быть определен расчетом равновесия. Для концентрированных растворов кислот, особенно сильных кислот, для которых pH <0, ЧАС0 значение является лучшим показателем кислотности, чем pH.
Сильные кислоты

А сильная кислота это кислота, которая диссоциирует в соответствии с реакцией
- HA + S ⇌ SH+ + А−
где S представляет собой молекулу растворителя, такую как молекула воды или ДМСО до такой степени, что концентрация недиссоциированного вида НА слишком мала для измерения. Для практических целей можно сказать, что сильная кислота полностью диссоциирована. Пример сильной кислоты: соляная кислота
- HCl → H+ + Cl− (в водном растворе)
Любая кислота с п.Kа значение, которое меньше примерно -2, классифицируется как сильная кислота. Это результат очень высокого буферная емкость решений с значение pH 1 или меньше и известен как выравнивающий эффект.[3]
Ниже приведены сильные кислоты в водном растворе и растворе диметилсульфоксида. Значения pKа, не могут быть измерены экспериментально. Значения в следующей таблице являются средними значениями из 8 различных теоретических расчетов.
По оценкам пKа значения[4] Кислота Формула в воде в ДМСО Соляная кислота HCl -5.9 ± 0.4 −2.0 ± 0.6 Бромистоводородная кислота HBr -8.8 ± 0.8 −6.8 ± 0.8 Йодистоводородная кислота ЗДРАВСТВУЙ -9.5 ± 1 −10.9 ± 1 Трифликовая кислота H [CF3ТАК3] −14 ± 2 −14 ± 2 Хлорная кислота H [ClO4] −15 ± 2 −15 ± 2
Также в воде
- Азотная кислота HNO3 пKа = -1.6 [5]
- Серная кислота ЧАС2ТАК4 (только первая диссоциация, pKа1 ≈ −3)[6]:(стр.171)
В качестве протонаторов в органическая химия
- Фторантимоновая кислота H [SbF6]
- Волшебная кислота H [FSO3SbF5]
- Карборана суперкислота H [CHB11Cl11]
- Фтористоводородная кислота H [FSO3] (пKа = −6.4)[7]
Сульфоновые кислоты, Такие как п-толуолсульфоновая кислота (тозиловая кислота) - это класс сильных органических оксикислоты.[7] Некоторые сульфоновые кислоты можно выделить в виде твердых веществ. Полистирол функционализирован в сульфонат полистирола является примером вещества, представляющего собой твердую сильную кислоту.
Слабые кислоты

Слабая кислота - это вещество, которое частично диссоциирует при растворении в растворителе. В растворе существует равновесие между кислотой, ГК и продуктами диссоциации.
Растворитель (например, вода) в этом выражении опускается, если его концентрация практически не меняется в процессе диссоциации кислоты. Сила слабой кислоты может быть определена количественно через константа диссоциации, Kа, определяемый следующим образом, где [ИКС] обозначает концентрацию химического фрагмента, X.
Когда числовое значение Kа известно, что его можно использовать для определения степени диссоциации в растворе с данной концентрацией кислоты, ТЧАС, применяя закон сохранение массы.
куда ТЧАС стоимость аналитическая концентрация кислоты. Когда все величины в этом уравнении рассматриваются как числа, ионные заряды не отображаются, и это становится квадратное уровненеие в значении значения концентрации ионов водорода, [ЧАС].
Это уравнение показывает, что pH раствора слабой кислоты зависит как от ее Kа значение и его концентрация. Типичные примеры слабых кислот включают: уксусная кислота и фосфористая кислота. Кислота, такая как Щавелевая кислота (HOOC – COOH) называется двухосновный потому что он может потерять два протона и вступить в реакцию с двумя молекулами простого основания. Фосфорная кислота (ЧАС3PO4) является трехосновным.
Для более строгой обработки силы кислоты см. константа диссоциации кислоты. Это включает кислоты, такие как двухосновная кислота. Янтарная кислота, для которых нельзя использовать простой метод расчета pH раствора, показанный выше.
Экспериментальное определение
Экспериментальное определение pKа значение обычно выполняется с помощью титрование.[8] Типичная процедура будет следующей. Некоторое количество сильной кислоты добавляют к раствору, содержащему кислоту или соль кислоты, до точки, когда соединение полностью протонируется. Затем раствор титруют сильным основанием.
- HA + OH− → А− + H2О
пока только депротонированный вид A−, остается в растворе. В каждой точке титрования pH измеряется с помощью стеклянный электрод и pH метр. Константа равновесия находится путем подгонки рассчитанных значений pH к наблюдаемым значениям с использованием метода наименьших квадратов.
Конъюгат пара кислота / основание
Иногда говорят, что «конъюгат слабой кислоты является сильным основанием». Такое утверждение неверно. Например, уксусная кислота - это слабая кислота, которая имеет Kа = 1,75 х 10−5. Его сопряженная база - это ацетат ион с Kб = 10−14/Kа = 5,7 х 10−10 (из отношений Kа × Kб = 10−14), что, конечно, не соответствует сильной базе. Конъюгат слабой кислоты часто является слабым основанием и наоборот.
Кислоты в неводных растворителях
Сила кислоты варьируется от растворителя к растворителю. Кислота, сильная в воде, может быть слабой в менее основном растворителе, а кислота, которая слаба в воде, может быть сильной в более основном растворителе. В соответствии с Кислотно-основная теория Бренстеда – Лоури, растворитель S может принимать протон.
- HA + S ⇌ A− + HS+.
Например, соляная кислота - это слабая кислота в растворе в чистом виде. уксусная кислота, HO2CCH3, который более кислый, чем вода.
- HO2CCH3 + HCl ⇌ (HO)2CCH3+ + Cl−
Степень ионизации галогеноводородные кислоты убывает в порядке HI> HBr> HCl. Уксусная кислота считается дифференцирующий растворитель для трех кислот, а вода - нет.[6]:(стр.217)
Важным примером более основного растворителя, чем вода, является диметилсульфоксид, ДМСО, (CH3)2ТАК. Соединение, которое в воде является слабой кислотой, может стать сильной кислотой в ДМСО. Уксусная кислота является примером такого вещества. Обширная библиография с.Kа значения в растворе в ДМСО и других растворителях можно найти на Данные о кислотности и щелочности в неводных растворителях.
Суперкислоты являются сильными кислотами даже в растворителях с низкой диэлектрической проницаемостью. Примеры суперкислот: фторантимоновая кислота и волшебная кислота. Некоторые суперкислоты могут кристаллизоваться.[9] Они также могут количественно стабилизировать карбокатионы.[10]
Кислоты Льюиса реагирование с основаниями Льюиса в газовой фазе и неводные растворители классифицированы в Модель ECW и было показано, что не существует одного порядка концентраций кислоты.[11] Относительную акцепторную силу кислот Льюиса по отношению к ряду оснований по сравнению с другими кислотами Льюиса можно проиллюстрировать следующим образом: Графики C-B.[12][13] Было показано, что для определения порядка силы кислоты Льюиса необходимо учитывать по крайней мере два свойства. Для качественного Теория HSAB два свойства - твердость и прочность, а для количественного Модель ECW эти два свойства - электростатическое и ковалентное.
Факторы, определяющие силу кислоты
Индуктивный эффект
В органических карбоновых кислотах электроотрицательный заместитель может вытягивать электронную плотность из кислотной связи через индуктивный эффект, что приводит к меньшему pKа ценить. Эффект уменьшается, чем дальше электроотрицательный элемент находится от карбоксилатной группы, как показано в следующей серии галогенированный бутановые кислоты.
| Структура | Имя | пKа |
|---|---|---|
 | 2-хлорбутановая кислота | 2.86 |
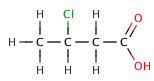 | 3-хлорбутановая кислота | 4.0 |
 | 4-хлорбутановая кислота | 4.5 |
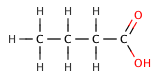 | бутановая кислота | 4.5 |
Влияние степени окисления
В комплекте оксокислоты элемента, pKа значения уменьшаются с увеличением степени окисления элемента. Оксокислоты хлора иллюстрируют эту тенденцию.[6]:(стр.171)
| Структура | Имя | Окисление государственный | пKа |
|---|---|---|---|
 | хлорная кислота | 7 | -8† |
 | хлорная кислота | 5 | -1 |
| хлористая кислота | 3 | 2.0 | |
 | хлорноватистая кислота | 1 | 7.53 |
† теоретический
Рекомендации
- ^ Лян, Джоан-Нан Джек (1976). Функция кислотности Гаммета для плавиковой кислоты и некоторых связанных суперкислотных систем (докторская диссертация) (PDF). Гамильтон, Онтарио: Университет Макмастера. п. 94.
- ^ Мисслер Г.Л., Тарр Д.А. Неорганическая химия (2-е изд., Prentice-Hall 1998, стр.170). ISBN 0-13-841891-8
- ^ Портерфилд, Уильям У. Неорганическая химия (Аддисон-Уэсли 1984) стр.260 ISBN 0-201-05660-7
- ^ Трумаль, Александр; Липпинг, Лаури; Кальюранд, Ивари; Koppel, Ilmar A .; Лейто, Иво (2016). «Кислотность сильных кислот в воде и диметилсульфоксиде». J. Phys. Chem. А. 120 (20): 3663–3669. Bibcode:2016JPCA..120.3663T. Дои:10.1021 / acs.jpca.6b02253. PMID 27115918.
- ^ Белл, Р. П. (1973), Протон в химии (2-е изд.), Итака, Нью-Йорк: Издательство Корнельского университета
- ^ а б c Housecroft, C.E .; Шарп, А. Г. (2004). Неорганическая химия (2-е изд.). Прентис Холл. ISBN 978-0-13-039913-7.
- ^ а б Гатри, Дж. П. (1978). «Гидролиз эфиров оксикислот: п.Kа значения для сильных кислот ». Может. J. Chem. 56 (17): 2342–2354. Дои:10.1139 / v78-385.
- ^ Martell, A.E .; Мотекайтис, Р.Дж. (1992). Определение и использование констант устойчивости. Вайли. ISBN 0-471-18817-4. Глава 4: Экспериментальная процедура для потенциометрии pH Измерение равновесия металлических комплексов
- ^ Чжан, Динлян; Реттиг, Стивен Дж .; Троттер, Джеймс; Обке, Фридхельм (1996). "Сверхкислотные анионы: кристаллические и молекулярные структуры ундекафтордиантимоната оксония (V), [H3O] [Sb2F11], Фторсульфат цезия, CsSO3F, бис (фторсульфат) водорода цезия, Cs [H (SO3F)2], Тетракис (фторсульфато) аурат цезия (III), Cs [Au (SO3F)4], Гексакис (фторсульфато) платинат цезия (IV), Cs2[Pt (SO3F)6] и антимонат цезия гексакис (фторсульфато) (V), Cs [Sb (SO3F)6]". Неорг. Chem. 35 (21): 6113–6130. Дои:10.1021 / ic960525l.
- ^ Джордж А. Олах, Шлосберг RH (1968). «Химия в суперкислотах. I. Водородный обмен и поликонденсация метана и алканов в FSO.3H – SbF5 («Волшебная кислота») Раствор. Протонирование алканов и промежуточность CH5+ и родственные ионы углеводородов. Высокая химическая активность «парафинов» в реакциях ионных растворов ». Журнал Американского химического общества. 90 (10): 2726–7. Дои:10.1021 / ja01012a066.
- ^ Vogel G.C .; Драго, Р. С. (1996). «Модель ECW». Журнал химического образования. 73: 701–707. Bibcode:1996JChEd..73..701V. Дои:10.1021 / ed073p701.
- ^ Лоуренс, К. и Гал, Дж.Ф. Шкалы основности и сродства Льюиса, данные и измерения, (Wiley 2010), стр. 50-51, IBSN 978-0-470-74957-9
- ^ Cramer, R.E .; Бопп, Т. Т. (1977). «Графическое отображение энтальпий образования аддуктов для кислот и оснований Льюиса». Журнал химического образования. 54: 612–613. Дои:10.1021 / ed054p612. На графиках, представленных в этом документе, используются более старые параметры. Улучшенные параметры E&C перечислены в Модель ECW.
внешняя ссылка
- Титрование кислот - бесплатное ПО для анализа данных и моделирование кривых потенциометрического титрования



![{ displaystyle K_ {a} = { frac {[H ^ {+}] [A ^ {-}]} {[HA]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/83ee86c6746a584bd7b209324db405b0563af917)
![{ displaystyle { begin {align} T_ {H} & = [H] + [HA] & = [H] + [A] [H] / K_ {a} & = [H] + [ H] ^ {2} / K_ {a} end {align}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2d1d8921a76226cabb40caf4153fb742226ac0b6)
![{ displaystyle [H] ^ {2} / K_ {a} + [H] -T_ {H} = 0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/20510aaf9a0ccaa6aa4bec6e7f9f6eb7222e8db9)