Свободно-радикальная теория старения - Free-radical theory of aging
Эта статья нужно больше медицинские справки за проверка или слишком сильно полагается на основные источники. (Май 2015 г.) |
В свободнорадикальная теория старения (FRTA) утверждает, что организмы возраст потому что клетки накапливаются свободный радикал повреждение с течением времени.[1] Свободный радикал - это любой атом или молекула, имеющая единственный неспаренный электрон во внешней оболочке.[2] Хотя некоторые свободные радикалы, такие как меланин не химически реактивный, большинство биологически значимых свободных радикалов обладают высокой реакционной способностью.[3] Для большинства биологических структур повреждение свободными радикалами тесно связано с окислительный повреждать. Антиоксиданты находятся восстановители, и ограничить окислительное повреждение биологических структур путем пассивирующий их от свободных радикалов.[4]
Строго говоря, теория свободных радикалов касается только свободных радикалов, таких как супероксид (O2− ), но с тех пор он был расширен, чтобы охватить окислительное повреждение от других активные формы кислорода Такие как пероксид водорода (ЧАС2О2), или же пероксинитрит (OONO−).[4]
Денхэм Харман впервые предложил свободнорадикальную теорию старения в 1950-х годах,[5] а в 1970-х расширили идею, чтобы вовлечь митохондриальный производство активных форм кислорода.[6]
В некоторых модельных организмах, таких как дрожжи и Дрозофила, есть доказательства того, что уменьшение окислительного повреждения может продлить жизнь.[7] Однако у мышей только 1 из 18 генетических изменений (делеция SOD-1), которые блокируют антиоксидантную защиту, сокращают продолжительность жизни.[8] Аналогичным образом в круглые черви (Caenorhabditis elegans ), блокируя выработку природного антиоксиданта супероксиддисмутаза недавно был показан увеличивать срок жизни.[9] Достаточно ли снижения окислительного повреждения ниже нормального для увеличения продолжительности жизни, остается открытым и спорным вопросом.
Фон
Свободнорадикальная теория старения была разработана Денхэм Харман в 1950-х годах, когда преобладающее научное мнение считало свободные радикалы слишком нестабильными, чтобы существовать в биологических системах.[10] Это было еще до того, как кто-то стал называть свободные радикалы причиной дегенеративных заболеваний.[11] Два источника вдохновили Хармана: 1) скорость теории жизни, который утверждает, что продолжительность жизни является обратной функцией скорости метаболизма, которая, в свою очередь, пропорциональна потреблению кислорода, и 2) наблюдение Реббеки Гершман о том, что гипербарическая кислородная токсичность и радиационная токсичность можно объяснить тем же основным феноменом: свободными радикалами кислорода.[10][12] Отмечая, что радиация вызывает «мутации, рак и старение», Харман утверждал, что свободные радикалы кислорода, образующиеся при нормальном дыхании, могут вызвать кумулятивный ущерб, который в конечном итоге приведет к потере функциональности организма и, в конечном итоге, к смерти.[10][12]
В последующие годы теория свободных радикалов была расширена и теперь включает не только старение. как таковой, но и возрастные заболевания.[11] Повреждение клеток свободными радикалами было связано с рядом заболеваний, включая: рак, артрит, атеросклероз, Болезнь Альцгеймера, и сахарный диабет.[13] Существуют некоторые свидетельства того, что свободные радикалы и некоторые химически активные формы азота запускают и усиливают механизмы гибели клеток в организме, такие как апоптоз и в крайних случаях некроз.[14]
В 1972 году Харман модифицировал свою первоначальную теорию.[11] В своей нынешней форме эта теория предполагает, что активные формы кислорода, которые образуются в митохондрии, наносит ущерб определенным макромолекулы включая липиды, белки и самое главное митохондриальная ДНК.[15] Это повреждение затем вызывает мутации, которые приводят к увеличению ROS производство и значительно увеличить накопление свободных радикалов в клетках.[15] Эта митохондриальная теория получила более широкое признание, что она может играть важную роль в процессе старения.[16]
С тех пор, как Харман впервые предложил свободнорадикальную теорию старения, в его первоначальную теорию постоянно вносились модификации и расширения.[16]
Процессы
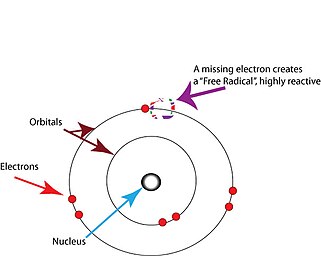
Свободные радикалы - это атомы или молекулы, содержащие неспаренные электроны.[2] Электроны обычно существуют парами в конкретных орбитали в атомах или молекулах.[17] Свободные радикалы, которые содержат только один электрон на любой орбитали, обычно нестабильны по отношению к потере или захвату лишнего электрона, поэтому все электроны в атоме или молекуле будут спаренными.[17]
Обратите внимание, что неспаренный электрон не подразумевает заряда - свободные радикалы могут быть положительно заряженными, отрицательно заряженными или нейтральными.
Повреждение происходит, когда свободный радикал сталкивается с другой молекулой и пытается найти другой электрон, чтобы спарить свой неспаренный электрон. Свободный радикал часто отталкивает электрон от соседней молекулы, в результате чего пораженная молекула сама становится свободным радикалом. Затем новый свободный радикал может оторвать электрон от следующей молекулы, и химическое вещество цепная реакция радикального производства.[18] Свободные радикалы, образующиеся в таких реакциях, часто заканчиваются удалением электрона из молекулы, которая изменяется или не может функционировать без него, особенно в биологии. Такое событие вызывает повреждение молекулы и, следовательно, клетки, которая ее содержит (поскольку молекула часто становится нефункциональной).
Цепная реакция, вызванная свободными радикалами, может приводить к сшиванию атомных структур. В случаях, когда цепная реакция, вызванная свободными радикалами, включает базовая пара молекулы в цепи ДНК, ДНК может стать поперечно связанной.[19]
Сшивание ДНК может, в свою очередь, привести к различным эффектам старения, особенно рак.[20] Другое сшивание может происходить между толстый и белок молекул, что приводит к появлению морщин.[21] Свободные радикалы могут окислять ЛПНП, и это ключевое событие в формировании бляшек в артериях, приводящих к сердечное заболевание и Инсульт.[22] Это примеры того, как свободнорадикальная теория старения использовалась для аккуратного «объяснения» происхождения многих хронические болезни.[23]
Считается, что свободные радикалы участвуют в процессе старения: супероксид и оксид азота.[24] В частности, увеличение количества супероксида влияет на старение, тогда как уменьшение образования оксида азота или его биодоступности делает то же самое.[24]
Антиоксиданты полезны для уменьшения и предотвращения повреждений от реакций свободных радикалов из-за их способности отдавать электроны, которые нейтрализуют радикал без образования другого. Аскорбиновая кислота например, может потерять электрон из-за свободного радикала и оставаться стабильным, передавая свой нестабильный электрон вокруг молекулы антиоксиданта.[25]
Это привело к гипотезе о том, что большое количество антиоксидантов,[26] с их способностью уменьшать количество свободных радикалов, могут уменьшить радикальные повреждения, вызывающие хронические заболевания, и даже радикальные повреждения, вызывающие старение.
Свидетельство
Многочисленные исследования продемонстрировали роль свободные радикалы в процессе старения и, таким образом, предположительно поддерживают теорию старения со свободными радикалами. Исследования показали значительное увеличение супероксидный радикал (SOR) формирование и перекисное окисление липидов у стареющих крыс.[27] Chung et al. предложить ROS продукция увеличивается с возрастом, и это указывает на то, что превращение XDH в XOD может быть важным фактором.[28] Это было подтверждено исследованием, которое показало производство супероксида ксантиноксидаза и БЕЗ синтазы в брыжеечные артерии был выше у старых крыс, чем у молодых.[29]
Гамильтон и др. изучили сходство в ослабленных эндотелиальный функционировать в гипертония и старение у людей, и было обнаружено значительное перепроизводство супероксида в обоих.[30] Этот вывод подтверждается исследованием 2007 года, в котором обнаружено, что эндотелиальный окислительный стресс развивается с возрастом у здоровых мужчин и связана с уменьшением эндотелий-зависимой дилатации.[31] Кроме того, исследование с использованием культивированных гладкомышечных клеток показало увеличение количества активных форм кислорода (АФК) в клетках, полученных от старых мышей.[32] Эти результаты были подтверждены вторым исследованием с использованием Клетки Лейдига выделен из семенников молодых и старых крыс.[33]
Choksi et al. Эксперимент с карликовыми мышами Эймса (DW) предполагает, что более низкие уровни выработки эндогенных АФК у мышей DW могут быть фактором их устойчивости к окислительному стрессу и долгой жизни.[34] Lener et al. предложить Nox4 активность увеличивает окислительное повреждение эндотелиальных клеток пупочной вены человека за счет сверхпродукции супероксида.[35] Кроме того, Rodriguez-Manas et al. обнаруженная дисфункция эндотелия в сосудах человека обусловлена коллективным действием сосудистого воспаления и окислительного стресса.[36]
Сасаки и др. сообщил о супероксид-зависимом хемилюминесценция обратно пропорционален максимальной продолжительности жизни у мышей, Крысы Вистар, и голуби.[37] Они предполагают, что передача сигналов АФК может быть определяющим фактором в процессе старения.[37] У людей Mendoza-Nunez et al. предположить, что возраст 60 лет и старше может быть связан с повышенным окислительным стрессом.[38] Миядзава нашел митохондриальный производство супероксид-аниона может привести к атрофия и дисфункция через митохондриально-опосредованные апоптоз.[39] Кроме того, они предполагают, что митохондриальный супероксид-анион играет важную роль в старении.[40] Lund et al. продемонстрировал роль эндогенный внеклеточный супероксиддисмутаза в защите от эндотелиальной дисфункции в процессе старения с использованием мышей.[41]
Модификации свободнорадикальной теории старения
Одна из основных критических замечаний по поводу свободнорадикальной теории старения направлена на предположение, что свободные радикалы ответственны за повреждение биомолекулы, что является основной причиной клеточное старение и старение организма.[42]:81 Было предложено несколько модификаций для интеграции текущих исследований в общую теорию.
Митохондриальная теория старения

Митохондриальная теория старения был впервые предложен в 1978 г.,[43][44] и вскоре после этого в 1980 году была представлена митохондриальная свободнорадикальная теория старения.[45] Теория считает митохондрии главной мишенью радикального повреждения, поскольку существует известный химический механизм, с помощью которого митохондрии могут производить Активные формы кислорода (ROS), митохондриальные компоненты, такие как мтДНК не так хорошо защищены, как ядерная ДНК, и исследованиями по сравнению повреждений ядер и мтДНК, которые демонстрируют более высокие уровни радикального повреждения митохондриальных молекул.[46] Электроны могут уйти из метаболический процессы в митохондриях, такие как Электронная транспортная цепь, и эти электроны могут, в свою очередь, реагировать с водой с образованием ROS, таких как супероксидный радикал, или косвенным путем гидроксильный радикал. Эти радикалы затем повреждают ДНК и белки митохондрий, и эти поврежденные компоненты, в свою очередь, более склонны производить побочные продукты АФК. Таким образом петля положительной обратной связи окислительного стресса, который со временем может привести к ухудшению состояния клеток, а затем и органов, и всего организма.[42]
Эта теория широко обсуждалась[47] и до сих пор неясно, как развиваются мутации мтДНК, индуцированные ROS.[42] Conte et al. предполагают, что замещенные железом цинковые пальцы могут генерировать свободные радикалы из-за близости цинкового пальца к ДНК и, таким образом, приводить к повреждению ДНК.[48]
Афанасьев предполагает, что супероксиддисмутационная активность CuZnSOD демонстрирует важную связь между продолжительностью жизни и свободными радикалами.[49] Связь между CuZnSOD и продолжительностью жизни была продемонстрирована Perez et al. которые указали, что на продолжительность жизни мышей повлияла делеция гена Sod1, который кодирует CuZnSOD.[50]
В отличие от обычно наблюдаемой связи между митохондриальными АФК (mtROS) и снижением продолжительности жизни, Yee et al. недавно наблюдали увеличение продолжительности жизни, опосредованное передачей сигналов mtROS в пути апоптоза. Это служит подтверждением возможности того, что наблюдаемые корреляции между повреждением ROS и старением не обязательно указывают на причинное участие ROS в процессе старения, но более вероятно из-за их модулирующих путей передачи сигнала, которые являются частью клеточных ответов на процесс старения.[51]
Эпигенетический окислительно-восстановительный сдвиг (EORS) теория старения
Брюэр предложил теорию, которая объединяет теорию свободных радикалов старения с инсулин сигнальные эффекты при старении.[52] Теория Брюера предполагает, что «сидячий образ жизни, связанный с возрастом, вызывает окислительные редокс сдвиг и нарушение функции митохондрий ».[52] Это митохондриальное нарушение ведет к малоподвижному поведению и ускоренному старению.[52]
Теория метаболической стабильности старения
Теория метаболической стабильности старения предполагает, что именно способность клеток поддерживать стабильную концентрацию АФК является основным фактором продолжительности жизни.[53] Эта теория критикует теорию свободных радикалов, потому что она игнорирует, что АФК являются специфическими сигнальными молекулами, которые необходимы для поддержания нормальных функций клетки.[53]
Митохормезис
Окислительный стресс может увеличить продолжительность жизни Caenorhabditis elegans вызывая вторичный ответ на первоначально повышенные уровни активных форм кислорода.[54] У млекопитающих вопрос о чистом влиянии активных форм кислорода на старение еще менее ясен.[55][56][57] Недавний эпидемиологический находки подтверждают процесс митогормезиса у людей и даже предполагают, что прием экзогенных антиоксидантов может усилить заболевание. распространенность у людей (согласно теории, потому что они предотвращают стимуляцию естественной реакции организма на соединения-окислители, которые не только нейтрализуют их, но и обеспечивают другие преимущества).[58]
Эффекты ограничения калорийности
Исследования показали, что ограничение калорий положительно влияет на продолжительность жизни организмов, даже если оно сопровождается увеличением окислительного стресса.[49] Многие исследования предполагают, что это может быть связано с антиоксидантным действием,[49] подавление окислительного стресса,[59] или устойчивость к окислительному стрессу[60] что происходит при ограничении калорий. Fontana et al. предполагают, что ограничение калорий повлияло на многочисленные сигнальные пути за счет уменьшения инсулиноподобный фактор роста I (ИФР-1).[61] Кроме того, они предполагают, что антиоксидантная СОД и каталаза участвуют в ингибировании этого пути передачи сигналов питательных веществ.[61]
Увеличение продолжительности жизни, наблюдаемое в ходе некоторых исследований ограничения калорийности, может происходить при отсутствии снижения или даже увеличения O2 потребление часто считается противоречащим митохондриальной теории старения со свободными радикалами.[49][62] Однако Барджа показал значительное снижение продукции митохондриальных радикалов кислорода (на единицу O2 потребляются) возникают при ограничении питания, упражнение аэробики, хронические упражнения и гипертиреоз.[62] Кроме того, генерация митохондриальных радикалов кислорода у долгоживущих птиц ниже, чем у короткоживущих млекопитающих сопоставимых размеров и размеров тела. скорость метаболизма. Таким образом, продукция митохондриальных АФК должна регулироваться независимо от O2 потребление в различных видах, тканях и физиологических состояниях.[62]
Вызовы теории старения со свободными радикалами
Голый крот-крыса
Голый землекоп - долгожитель (32 года) грызун. Согласно обзору Lewis et al.,[63] (2013), уровни активные формы кислорода (ROS) продукция у голого землекопа аналогична продуктивности другого грызуна, относительно недолговечного мышь (4 года). Они пришли к выводу, что не окислительный стресс влияет на продолжительность здоровья и продолжительность жизни этих грызунов, а скорее другие цитопротективные механизмы, которые позволяют животным справляться с высокими уровнями окислительного повреждения и стресса.[63] У голого землекопа важным механизмом цитопротекции, который может обеспечить гарантию долголетия, является повышенная экспрессия Ремонт ДНК гены, участвующие в нескольких ключевых путях репарации ДНК.[64] (Видеть Теория повреждений ДНК старения.) По сравнению с мышью, голый землекоп имел значительно более высокие уровни экспрессии генов, необходимых для путей репарации ДНК Ремонт несоответствия ДНК, негомологичное соединение концов и базовая эксцизионная пластика.[64]
Птицы
Среди птиц, попугаи живут примерно в 5 раз дольше, чем перепел. Активные формы кислорода (ROS) выработка в сердце, скелетных мышцах, печени и интактных эритроцитах оказалась сходной у попугаев и перепелов и не показала соответствия разнице в продолжительности жизни.[65] Эти выводы были сделаны, чтобы поставить под сомнение надежность теории старения, связанной с окислительным стрессом.[65]
Смотрите также
- Американская ассоциация старения
- Продление жизни
- Список тем, связанных с продлением жизни
- Старение
- Ограничение калорий
- Денхэм Харман
- Митохондриальная теория старения
Рекомендации
- ^ Hekimi S, Lapointe J, Wen Y. "Хороший" взгляд на свободные радикалы в процессе старения. Тенденции в клеточной биологии. 2011; 21 (10) 569-76.
- ^ а б Эрбас М., Секерчи Х. ЗНАЧЕНИЕ БЕСПЛАТНЫХ РАДИКАЛОВ И ВОЗНИКАЮЩИХ ПРИ ПРОИЗВОДСТВЕ ПРОДУКТОВ. SERBEST RADÏKALLERÏN ONEMÏ VE GIDA ÏSLEME SIRASINDA OLUSUMU. 2011; 36 (6) 349-56.
- ^ Херрлинг Т., Юнг К., Фукс Дж. (2008). «Роль меланина как защитника от свободных радикалов в коже и его роль в качестве индикатора свободных радикалов в волосах». Spectrochimica Acta Часть A: Молекулярная и биомолекулярная спектроскопия. 69 (5): 1429–35. Bibcode:2008AcSpA..69.1429H. Дои:10.1016 / j.saa.2007.09.030. PMID 17988942.
- ^ а б Холливелл Б. (2012). «Свободные радикалы и антиоксиданты: обновление личного взгляда». Отзывы о питании. 70 (5): 257–65. Дои:10.1111 / j.1753-4887.2012.00476.x. PMID 22537212.
- ^ Харман, Д. (1956). «Старение: теория, основанная на свободнорадикальной и радиационной химии». Журнал геронтологии. 11 (3): 298–300. Дои:10.1093 / geronj / 11.3.298. PMID 13332224.
- ^ Харман, Д. (1972). «Биологические часы: митохондрии?». Журнал Американского гериатрического общества. 20 (4): 145–147. Дои:10.1111 / j.1532-5415.1972.tb00787.x. PMID 5016631.
- ^ Фонтана, Луиджи; Куропатка, Линда; Лонго, Вальтер Д. (16 апреля 2010 г.). «Увеличение продолжительности здоровой жизни - от дрожжей до людей». Наука. 328 (5976): 321–326. Bibcode:2010Sci ... 328..321F. Дои:10.1126 / science.1172539. ЧВК 3607354. PMID 20395504.
- ^ Перес В.И., Боков А., Реммен Х.В., Меле Дж., Ран К., Икено Ю. и др. (2009). «Неужели теория старения с окислительным стрессом мертва?». Biochimica et Biophysica Acta (BBA) - Общие предметы. 1790 (10): 1005–14. Дои:10.1016 / j.bbagen.2009.06.003. ЧВК 2789432. PMID 19524016.
- ^ Ван Раммсдонк, Джереми М .; Хекими, Зигфрид (2009). Ким, Стюарт К. (ред.). «Удаление митохондриальной супероксиддисмутазы sod-2 продлевает продолжительность жизни у Caenorhabditis elegans». PLOS Genetics. 5 (2): e1000361. Дои:10.1371 / journal.pgen.1000361. ЧВК 2628729. PMID 19197346.
- ^ а б c Харман Д. (июль 1956 г.). «Старение: теория, основанная на свободнорадикальной и радиационной химии». J Gerontol. 11 (3): 298–300. Дои:10.1093 / geronj / 11.3.298. PMID 13332224.
- ^ а б c Харман Д. (2009). «Происхождение и эволюция теории старения свободных радикалов: краткая личная история, 1954–2009». Биогеронтология. 10 (6): 773–81. Дои:10.1007 / s10522-009-9234-2. PMID 19466577. S2CID 13512659.
- ^ а б Спикман Дж. Р., Селман С. (2011). «Теория повреждения свободных радикалов: накопление доказательств против простой связи окислительного стресса со старением и продолжительностью жизни». BioEssays. 33 (4): 255–9. Дои:10.1002 / bies.201000132. PMID 21290398. S2CID 13720843.
- ^ Клэнси Д., Бердсолл Дж. Мухи, черви и теория старения свободных радикалов. Обзоры исследований старения. (0).
- ^ Чаттерджи С., Лардинуа О., Бхаттачарджи С., Такер Дж., Корбетт Дж., Детердинг Л. и др. (2011). «Окислительный стресс индуцирует образование белков и радикалов ДНК в фолликулярных дендритных клетках зародышевого центра и модулирует характер гибели его клеток на позднем этапе сепсиса». Свободная радикальная биология и медицина. 50 (8): 988–99. Дои:10.1016 / j.freeradbiomed.2010.12.037. ЧВК 3051032. PMID 21215311.
- ^ а б Джанг YC, Реммен HV (2009). «Митохондриальная теория старения: взгляд на трансгенные и нокаутные модели мышей». Экспериментальная геронтология. 44 (4): 256–60. Дои:10.1016 / j.exger.2008.12.006. PMID 19171187. S2CID 19815246.
- ^ а б Грубер Дж, Шаффер С., Холливелл Б. (2008). «Митохондриальная свободнорадикальная теория старения - где мы находимся?». Границы биологических наук. 13 (13): 6554–79. Дои:10.2741/3174. PMID 18508680.
- ^ а б Орчин М., Макомбер Р.С., Пинхас А., Уилсон Р.М., редакторы. Словарь и понятия органической химии. 2-е изд: Джон Вили и сыновья; 2005 г.
- ^ Цуй Ханг; Конг Яхуи; Чжан Хун (2011). «Окислительный стресс, дисфункция митохондрий и старение». Журнал передачи сигналов. 2012: 646354. Дои:10.1155/2012/646354. ЧВК 3184498. PMID 21977319.
- ^ Crean C, Геацинтов Н.Е., Шафирович В. (2008). «Внутрицепочечные сшивки G-U, образованные окислением гуанина в 5'-d (GCU) и 5'-r (GCU)». Свободная радикальная биология и медицина. 45 (8): 1125–34. Дои:10.1016 / j.freeradbiomed.2008.07.008. ЧВК 2577587. PMID 18692567.
- ^ Диздароглу М., Яруга П. Механизмы повреждения ДНК свободными радикалами. Свободно-радикальные исследования. [Статья]. 2012; 46 (4) 382-419.
- ^ Пейджон Х., Асселинеу Д. Подход in vitro к хронологическому старению кожи за счет гликирования коллагена: биологический эффект гликирования на реконструированной модели кожи » Летопись Нью-Йоркской академии наук 2005;1043(1) 529-32.
- ^ Бамм В.В., Цемахович В.А., Шаклай Н.А. Окисление липопротеинов низкой плотности гемоглобином-гемихромом. Международный журнал биохимии и клеточной биологии. 2003; 35 (3) 349-58.
- ^ К. Рихтер, Дж. У. Парк, Б. Н. Эймс «Нормальное окислительное повреждение митохондриальной и ядерной ДНК обширно» «ПНАС», 1988 г.
- ^ а б Афанасьев И.Б. (2005). «Свободнорадикальные механизмы процессов старения в физиологических условиях». Биогеронтология. 6 (4): 283–90. Дои:10.1007 / s10522-005-2626-z. PMID 16333762. S2CID 7661778.
- ^ Багчи Д. и др. «Способность витаминов C и E поглощать свободные радикалы, а также экстракт проантоцианидина виноградных косточек in vitro» "Исследования в области молекулярной патологии и фармакологии" 1997 г.
- ^ Бьесальский Х. Свободнорадикальная теория старения. Текущее мнение о клиническом питании и метаболическом лечении. 2002 Январь 2002; 5 (1) 5-10.
- ^ Савада М, Карлсон Дж. С. (1987). «Изменения в образовании супероксидных радикалов и перекиси липидов в мозге, сердце и печени в течение жизни крысы». Механизмы старения и развития. 41 (1–2): 125–37. Дои:10.1016/0047-6374(87)90057-1. PMID 2828774. S2CID 22356132.
- ^ Чунг Х.Й., Сонг С.Х., Ким Х.Дж., Икено Й., Ю.П. «Модуляция почечной ксантин оксидоредуктазы при старении: экспрессия генов и генерация активных форм кислорода». Журнал питания, здоровья и старения. 3 (1): 19–23. PMID 10888479.
- ^ Якобсон А., Ян С., Гао К., Ринкон-Скиннер Т., Ривера А., Эдвардс Дж. И др. (2007). «Старение усиливает образование артериального супероксида, вызванное давлением». Американский журнал физиологии. Сердце и физиология кровообращения. 293 (3): H1344 – H50. Дои:10.1152 / ajpheart.00413.2007. ЧВК 4536921. PMID 17557915.
- ^ Гамильтон, Калифорния, Броснан М.Дж., Макинтайр М., Грэм Д., Доминичак А.Ф. (2001). «Избыток супероксида при гипертонии и старении: частая причина эндотелиальной дисфункции». Гипертония. 37 (2 Пет 2): 529–34. Дои:10.1161 / 01.hyp.37.2.529. PMID 11230330.
- ^ Донато А.Дж., Эскурза И., Сильвер А.Е., Леви А.С., Пирс Г.Л., Гейтс П.Е. и др. (2007). «Прямые доказательства эндотелиального окислительного стресса при старении у людей: связь с нарушением эндотелий-зависимой дилатации и активацией ядерного фактора-каппаВ». Циркуляционные исследования. 100 (11): 1659–66. Дои:10.1161 / 01.res.0000269183.13937.e8. PMID 17478731.
- ^ Мун С.К., Томпсон Л.Дж., Мадаманчи Н., Баллинджер С., Папаконстантину Дж., Хораист С. и др. (2001). «Старение, окислительные реакции и пролиферативная способность культивируемых клеток гладкой мускулатуры аорты мышей». Американский журнал физиологии. Сердце и физиология кровообращения. 280 (6): H779 – H88. Дои:10.1152 / ajpheart.2001.280.6.h2779. PMID 11356636.
- ^ Чен Х., Канжелло Д., Бенсон С., Фолмер Дж., Чжу Х., Труш М.А. и др. (2001). «Возрастное увеличение выработки митохондриального супероксида в тестостерон-продуцирующих клетках семенников коричневой норвежской крысы: связь со сниженной стероидогенной функцией?». Экспериментальная геронтология. 36 (8): 1361–73. Дои:10.1016 / s0531-5565 (01) 00118-8. PMID 11602210. S2CID 6034351.
- ^ Чокси КБ, Робертс Л.Дж., ДеФорд Дж. Х., Рабек Дж. П., Папаконстантину Дж. (2007). «Более низкие уровни F2-изопростанов в сыворотке и печени долгоживущих карликовых мышей Эймса». Сообщения о биохимических и биофизических исследованиях. 364 (4): 761–4. Дои:10.1016 / j.bbrc.2007.10.100. ЧВК 2238179. PMID 17964285.
- ^ Ленер Б., Козел Р., Пирхер Х., Хюттер Э., Грейссинг Р., Херндлер-Брандштеттер Д. и др. (2009). «НАДФН-оксидаза Nox4 ограничивает репликативную продолжительность жизни эндотелиальных клеток человека». Биохимический журнал. 423 (3): 363–74. Дои:10.1042 / bj20090666. ЧВК 2762686. PMID 19681754.
- ^ Родригес-Маньяс Л., Эль-Ассар М., Вальехо С., Лопес-Дорига П., Солис Дж., Петидье Р. и др. (2009). «Эндотелиальная дисфункция у пожилых людей связана с окислительным стрессом и сосудистым воспалением». Ячейка старения. 8 (3): 226–38. Дои:10.1111 / j.1474-9726.2009.00466.x. PMID 19245678. S2CID 24420773.
- ^ а б Сасаки Т., Унно К., Тахара С., Шимада А., Чиба И., Хосино М. и др. (2008). «Возрастное увеличение образования супероксида в головном мозге млекопитающих и птиц». Ячейка старения. 7 (4): 459–69. Дои:10.1111 / j.1474-9726.2008.00394.x. PMID 18419797. S2CID 12093820.
- ^ Мендоса-Нуньес В.М., Руис-Рамос М., Санчес-Родригес М.А., Ретана-Угальде Р., Муньос-Санчес Ю.Л. Окислительный стресс, связанный со старением, у здоровых людей. Журнал экспериментальной медицины Тохоку. 2007; 213 (3) 261-8.
- ^ Миядзава М., Исии Т., Ясуда К., Нода С., Онучи Х., Хартман П.С. и др. (2009). «Роль митохондриального супероксид-аниона (O2 (-)) на физиологическое старение мышей C57BL / 6J». Журнал радиационных исследований. 50 (1): 73–83. Bibcode:2009JRadR..50 ... 73M. Дои:10.1269 / jrr.08097. PMID 19218782.
- ^ Миядзава М., Исии Т., Ясуда К., Нода С., Онучи Х., Хартман П.С. и др.
- ^ Лунд Д.Д., Чу Й., Миллер Д.Д., Хейстад Д.Д. (2009). «Защитный эффект внеклеточной супероксиддисмутазы на функцию эндотелия при старении». Американский журнал физиологии. Сердце и физиология кровообращения. 296 (6): H1920 – H5. Дои:10.1152 / ajpheart.01342.2008. ЧВК 2716111. PMID 19376805.
- ^ а б c Афанасьев I (2010). «Сигнальные и повреждающие функции свободных радикалов в теории свободных радикалов, гормезисе и TOR». Старение и болезнь. 1 (2): 75–88. ЧВК 3295029. PMID 22396858.
- ^ Лобачев А.Н.Роль митохондриальных процессов в развитии и старении организма. Старение и рак (PDF), Химические рефераты. 1979 v. 91 N 25 91: 208561v. Deposited Doc., ВИНИТИ 2172-78, 1978, стр. 48
- ^ Лобачев А.Н.Биогенез митохондрий при дифференцировке клеток и старении (PDF), Депонированный док. ВИНИТИ 19.09.85, №6756-В85, 1985, с. 28
- ^ Микель Дж., Экономос А.С., Флеминг Дж. И др.Роль митохондрий в старении клеток, Exp Gerontol, 15, 1980, стр. 575–591.
- ^ Weindruch, Ричард (январь 1996 г.). «Ограничение калорийности и старение». Scientific American: 49–52.
- ^ Пооватингал С.К., Грубер Дж., Холливелл Б., Гунаван Р. (2009). «Стохастический дрейф точечных мутаций митохондриальной ДНК: новая перспектива ex silico». PLOS вычислительная биология. 5 (11): e1000572. Bibcode:2009PLSCB ... 5E0572P. Дои:10.1371 / journal.pcbi.1000572. ЧВК 2771766. PMID 19936024.
- ^ Conte D, Нариндрасорасак S, Саркар Б. (1996). "В естественных условиях и in vitro цинковый палец, замещенный железом, генерирует свободные радикалы и вызывает повреждение ДНК ». Журнал биологической химии. 271 (9): 5125–30. Дои:10.1074 / jbc.271.9.5125. PMID 8617792.
- ^ а б c d Афанасьев И. Сигнальные и повреждающие функции свободных радикалов в теории старения свободных радикалов, гормезисе и ТЗ. Старение и болезни. 2010; 1 (2) 75-88.
- ^ Перес В.И., Боков А., Ван Реммен Х., Меле Дж., Ран К., Икено Ю. и др. (2009). «Неужели теория старения с окислительным стрессом мертва?». Biochimica et Biophysica Acta (BBA) - Общие предметы. 1790 (10): 1005–14. Дои:10.1016 / j.bbagen.2009.06.003. ЧВК 2789432. PMID 19524016.
- ^ Йи К., Ян В., Хекими С. (2014). «Внутренний путь апоптоза опосредует ответную реакцию долголетия на митохондриальные АФК у C. elegans». Клетка. 157 (4): 897–909. Дои:10.1016 / j.cell.2014.02.055. ЧВК 4454526. PMID 24813612.
- ^ а б c Брюэр Дж. Дж. (2010). «Теория эпигенетического окислительно-восстановительного сдвига (EORS) старения объединяет теории сигналов свободных радикалов и инсулина». Экспериментальная геронтология. 45 (3): 173–9. Дои:10.1016 / j.exger.2009.11.007. ЧВК 2826600. PMID 19945522.
- ^ а б Бринк TC, Деметриус Л., Лехрах Х., Аджай Дж. (2009). «Связанные с возрастом транскрипционные изменения в экспрессии генов в различных органах мышей подтверждают теорию метаболической стабильности старения». Биогеронтология. 10 (5): 549–64. Дои:10.1007 / s10522-008-9197-8. ЧВК 2730443. PMID 19031007.
- ^ Schulz TJ, Zarse K, Voigt A, Urban N, Birringer M, Ristow M (2007). «Ограничение глюкозы увеличивает продолжительность жизни Caenorhabditis elegans, вызывая митохондриальное дыхание и увеличивая окислительный стресс». Клеточный метаболизм. 6 (4): 280–93. Дои:10.1016 / j.cmet.2007.08.011. PMID 17908557.
- ^ Сохал Р., Мокетт Р., Орр В. (2002). «Механизмы старения: оценка гипотезы окислительного стресса». Свободный Радик Биол Мед. 33 (5): 575–86. Дои:10.1016 / S0891-5849 (02) 00886-9. PMID 12208343.
- ^ Сохал Р. (2002). «Роль окислительного стресса и окисления белков в процессе старения». Свободный Радик Биол Мед. 33 (1): 37–44. Дои:10.1016 / S0891-5849 (02) 00856-0. PMID 12086680.
- ^ Ротанг S (2006). «Теории биологического старения: гены, белки и свободные радикалы». Free Radic Res. 40 (12): 1230–8. Дои:10.1080/10715760600911303. PMID 17090411. S2CID 11125090.
- ^ Бжелакович Г., Николова Д., Глууд Л.Л., Симонетти Р.Г., Глууд С. (2007). «Смертность в рандомизированных исследованиях антиоксидантных добавок для первичной и вторичной профилактики: систематический обзор и метаанализ». Журнал Американской медицинской ассоциации. 297 (8): 842–57. Дои:10.1001 / jama.297.8.842. PMID 17327526.. См. Также письмо к JAMA Филиппа Тейлора и Сэнфорд Доуси и Ответить авторами оригинальной статьи.
- ^ Castello L; Froio T; Cavallini G; Biasi F; Сапино А; Leonarduzzi G; и другие. (2005). «Ограничение калорий защищает от возрастного склероза аорты крысы». Журнал FASEB. 19 (13): 1863–5. Дои:10.1096 / fj.04-2864fje. PMID 16150801. S2CID 41825838.
- ^ Ungvari Z, Parrado-Fernandez C, Csiszar A, de Cabo R. Механизмы, лежащие в основе ограничения калорийности и регуляции продолжительности жизни: последствия для старения сосудов » Циркуляционные исследования 2008;102(5) 519-28.
- ^ а б Фонтана Л., Партридж Л., Лонго В.Д. Увеличение продолжительности здоровой жизни - от дрожжей до человека. Наука (Нью-Йорк, Нью-Йорк). 2010; 328 (5976) 321-6.
- ^ а б c Барха Г. Потребление кислорода митохондриями и производство активных форм кислорода модулируются независимо: значение для исследований старения. Исследования омоложения. 2007; 10 (2) 215-24.
- ^ а б Льюис К.Н., Анджяк Б., Ян Т., Буффенштейн Р. (2013). «Реакция голого землекопа на окислительный стресс: смирись с этим». Антиоксид. Редокс-сигнал. 19 (12): 1388–99. Дои:10.1089 / ars.2012.4911. ЧВК 3791056. PMID 23025341.
- ^ а б MacRae SL, Croken MM, Calder RB, Aliper A, Milholland B, White RR, Zhavoronkov A, Gladyshev VN, Seluanov A, Gorbunova V, Zhang ZD, Vijg J (2015). «Восстановление ДНК у видов с очень разной продолжительностью жизни». Старение. 7 (12): 1171–84. Дои:10.18632 / старение.100866. ЧВК 4712340. PMID 26729707.
- ^ а б Монтгомери МК, Халберт А.Дж., Баттемер В.А. (2012). «Объясняет ли теория окислительного стресса старения различия в продолжительности жизни птиц? I. Производство митохондриальных АФК». Exp. Геронтол. 47 (3): 203–10. Дои:10.1016 / j.exger.2011.11.006. PMID 22123429. S2CID 984298.
внешняя ссылка
Ограничение калорий
Биология старения
- Теории старения, основанные на повреждениях Включает обсуждение теории старения свободных радикалов.
