Имидоген - Imidogen - Wikipedia
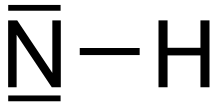 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК λ1-Азанилиден[1] | |||
| Другие имена Аминилен Азанилен водородный азот | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| 66 | |||
PubChem CID | |||
| |||
| |||
| Характеристики | |||
| ЧАСN | |||
| Молярная масса | 15.015 г · моль−1 | ||
| Конъюгированная кислота | Ион нитрения | ||
| Структура | |||
| линейный | |||
| Термохимия | |||
Теплоемкость (C) | 21,19 Дж К−1 моль−1 | ||
Стандартный моляр энтропия (S | 181,22 кДж · К−1 моль−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | 358,43 кДж моль−1 | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Имидоген является неорганическое соединение с химическая формула NH.[2] Как и другие простые радикалы, он обладает высокой реакционной способностью и, следовательно, недолговечен, за исключением разбавленного газа. Его поведение зависит от его кратность вращения, т.е. триплет по сравнению с синглетом основное состояние.
Продукция и свойства
Имидоген может быть произведен электрический разряд в атмосфере аммиак.[3]
Имидоген имеет большое вращательное расщепление и слабое спин-спиновое взаимодействие, поэтому вероятность его возникновения из-за столкновений будет ниже. Зеемановские переходы.[3] Имидоген в основном состоянии может быть захвачен магнитным путем, используя загрузка буферного газа от молекулярного пучка.[3]
Первое возбужденное состояние (a1Δ) имеет долгое время жизни, так как его релаксация в основное состояние (X3Σ−) запрещено спином.[4][5] Имидоген подвергается столкновению межсистемный переход.[6]
Реактивность
Без учета атомов водорода имидоген является изоэлектронный с карбен (CH2) и атомов кислорода (O), и он показывает сопоставимую реакционную способность.[4] Первое возбужденное состояние может быть обнаружено с помощью лазерно-индуцированная флуоресценция (LIF).[4] Методы LIF позволяют обнаруживать истощение, производство и химические продукты NH. Он реагирует с оксид азота (НЕТ):
- NH + NO → N2 + ОН
- NH + NO → N2O + H
Первая реакция более благоприятна с ΔЧАС0 из −408±2 кДж / моль по сравнению с ΔЧАС0 из −147±2 кДж / моль для последней реакции.[7]
Номенклатура
В банальное имя нитрен это предпочтительное название ИЮПАК. Систематические имена, λ1-азан и водородный азот, действительный ИЮПАК имена, построены согласно заместительной и аддитивной номенклатуре соответственно.
В соответствующих контекстах имидоген можно рассматривать как аммиак с удаленными двумя атомами водорода, и как таковой азилиден может использоваться как контекстно-зависимое систематическое название согласно заместительной номенклатуре. По умолчанию в этом названии не учитывается радикальность молекулы имидогена. Хотя, в еще более конкретном контексте, он также может называть нерадикальное состояние, тогда как бирадикальное состояние называется азандиил.
Астрохимия
Межзвездный NH был идентифицирован в диффузных облаках в направлении ζ Персей и HD 27778 с высоким разрешениемСигнал к шуму спектры NH A3Π → X3Полоса поглощения Σ (0,0) около 3358 Å.[8] Температура около 30 К (-243 ° C) способствует эффективному производству CN из NH в диффузном облаке.[9][10][8]
Реакции, относящиеся к астрохимии
Химические реакции[11][12] Реакция Константа скорости Скорость / [H2]2 N + H− → NH + e− 1×10−9 3.5×10−18 NH2 + O → NH + ОН 2.546×10−13 1.4×10−13 NH+
2 + е− → NH + H3.976×10−7 2.19×10−21 NH+
3 + е− → NH + H + H8.49×10−7 2.89×10−19 NH + N → N2 + H 4.98×10−11 4.36×10−16 NH + O → OH + N 1.16×10−11 1.54×10−14 NH + C+ → CN+ + H 7.8×10−10 4.9×10−19 NH + H3+ → NH+
2 + H21.3×10−9 3.18×10−19 NH + H+ → NH+ + H 2.1×10−9 4.05×10−20
Внутри диффузных облаков H− + N → NH + е− является основным механизмом формирования. Вблизи химического равновесия важными механизмами образования NH являются рекомбинации NH+
2 и NH+
3 ионы с электронами. В зависимости от поля излучения в диффузном облаке NH2 также может внести свой вклад.
NH разрушается в диффузных облаках фотодиссоциация и фотоионизация. В плотных облаках NH разрушается в результате реакции с атомарным кислородом и азотом. О+ и н+ образуют OH и NH в диффузных облаках. NH участвует в создании N2, ОН, Н, CN+, CH, N, NH+
2, NH+ для межзвездной среды.
О NH сообщалось в диффузной межзвездной среде, но не в плотных молекулярных облаках.[13] Цель обнаружения NH часто состоит в том, чтобы получить лучшую оценку постоянных вращения и колебательных уровней NH.[14] Это также необходимо для подтверждения теоретических данных, которые предсказывают содержания N и NH в звездах, которые производят N и NH, и другие звезды с оставшимися следовыми количествами N и NH.[15] Используя текущие значения вращательных постоянных и колебаний NH, а также ОЙ и CH позволяют изучать содержание углерода, азота и кислорода, не прибегая к полному синтезу спектра с трехмерной моделью атмосферы.[16]
Смотрите также
- Диимид (димер)
Рекомендации
- ^ Красная книга ИЮПАК 2005
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ а б c Campbell, W. C .; Циката, Э .; van Buuren, L .; Lu, H .; Дойл, Дж. М. (2007). «Магнитный захват и зеемановская релаксация NH (X3Σ−)". Письма с физическими проверками. 98 (21): 213001. arXiv:физика / 0702071. Дои:10.1103 / PhysRevLett.98.213001.
- ^ а б c Hack, W .; Ратманн, К. (1990). «Элементарная реакция имидогена (а1Δ) с оксидом углерода ». Журнал физической химии. 94 (9): 3636–3639. Дои:10.1021 / j100372a050.
- ^ Национальный институт стандартов и технологий[требуется полная цитата ]
- ^ Adams, J. S .; Пастернак, Л. (1991). «Индуцированное столкновением межсистемное пересечение в имидогене (a1Δ) → имидоген (X3Σ−)". Журнал физической химии. 95 (8): 2975–2982. Дои:10.1021 / j100161a009.
- ^ Patel-Misra, D .; Дагдигян, П. Дж. (1992). «Динамика имидогена (X3Σ−) + оксид азота (X2Π) реакция: внутреннее состояние распределения гидроксила (X2Π) товар ». Журнал физической химии. 96 (8): 3232–3236. Дои:10.1021 / j100187a011.
- ^ а б Мейер, Дэвид М .; Рот, Кэтрин С. (1 августа 1991 г.). «Открытие межзвездного NH». Астрофизический журнал. 376: L49 – L52. Bibcode:1991ApJ ... 376L..49M. Дои:10.1086/186100.
- ^ Wagenblast, R .; Уильямс, Д. А .; Миллар, Т. Дж .; Неджад, Л. А. М. (1993). «О происхождении NH в диффузных межзвездных облаках». Ежемесячные уведомления Королевского астрономического общества. 260 (2): 420–424. Bibcode:1993МНРАС.260..420Вт. Дои:10.1093 / минрас / 260.2.420.
- ^ Crutcher, R.M .; Уотсон, В. Д. (1976). «Верхний предел и значение молекулы NH в диффузных межзвездных облаках». Астрофизический журнал. 209 (1): 778–781. Bibcode:1976ApJ ... 209..778C. Дои:10.1086/154775.
- ^ Prasad, S. S .; Охотница, В. Т. (1980). «Модель химии газовой фазы в межзвездных облаках. I. Базовая модель, библиотека химических реакций и химии соединений C, N и O». Серия дополнений к астрофизическому журналу. 43: 1. Bibcode:1980ApJS ... 43 .... 1П. Дои:10.1086/190665.
- ^ "База данных UMIST по астрохимии 2012 / astrochemistry.net".
- ^ Чернихаро, Хосе; Goicoechea, Javier R .; Ко, Эммануэль (2000). "Обнаружение C в дальнем инфракрасном диапазоне3 в Стрельце B2 и IRC +10216 ". Письма в астрофизический журнал. 534 (2): L199 – L202. Bibcode:2000ApJ ... 534L.199C. Дои:10.1086/312668. HDL:10261/192089. ISSN 1538-4357.
- ^ Ram, R. S .; Bernath, P. F .; Хинкль, К. Х. (1999). «Инфракрасная эмиссионная спектроскопия NH: Сравнение криогенного эшелле-спектрографа со спектрометром с преобразованием Фурье». Журнал химической физики. 110 (12): 5557. Bibcode:1999ЖЧФ.110.5557Р. Дои:10.1063/1.478453.
- ^ Grevesse, N .; Lambert, D. L .; Sauval, A.J .; Van Dishoeck, E. F .; Farmer, C. B .; Нортон, Р. Х. (1990). «Идентификация солнечных колебательно-вращательных линий NH и содержания солнечного азота». Астрономия и астрофизика. 232 (1): 225. Bibcode:1990 А и А ... 232..225 г. ISSN 0004-6361.
- ^ Фребель, Анна; Цанга, Ремо; Эрикссон, Кьелл; Кристлиб, Норберт; Аоки, Вако (2008). "HE 1327–2326, неразвитая звезда с [Fe / H] <–5.0. II. Новое скорректированное содержание 3D – 1D из спектра UVES очень большого телескопа". Астрофизический журнал. 684 (1): 588–602. arXiv:0805.3341. Bibcode:2008ApJ ... 684..588F. Дои:10.1086/590327. ISSN 0004-637X.