Температура плавления - Melting point - Wikipedia

В температура плавления (или, редко, точка разжижения) вещества является температура при котором он меняется государственный из твердый к жидкость. В точке плавления твердая и жидкая фазы существуют в равновесие. Температура плавления вещества зависит от давление и обычно указывается в стандартное давление например, 1 атмосфера или 100 кПа.
Когда рассматривается как температура обратного перехода от жидкости к твердому телу, ее называют температурой. Точка замерзания или же точка кристаллизации. Из-за способности веществ к очень круто, точка замерзания может оказаться ниже фактического значения. Когда определяется «характерная точка замерзания» вещества, фактически фактическая методология почти всегда «принцип наблюдения исчезновения, а не образования льда, то есть температура плавления.[1]
Примеры

Для большинства веществ таяние и замораживание баллы примерно равны. Например, точка плавления и точка замерзания Меркурий составляет 234,32 Кельвин (−38.83 ° C или −37,89° F ).[2] Однако некоторые вещества обладают разными температурами перехода твердое тело-жидкость. Например, агар плавится при 85 ° C (185 ° F) и затвердевает при 31 ° C (88 ° F; 304 K); такая зависимость от направления известна как гистерезис. Температура плавления льда при давлении в 1 атмосферу очень близка. [3] до 0 ° С (32 ° F, 273 К); это также известно как ледяная точка. В присутствии зародышеобразователи, точка замерзания воды не всегда совпадает с точкой плавления. В отсутствие нуклеаторов вода может существовать как переохлажденный жидкость до -48,3 ° C (-55 ° F, 224,8 K) перед замерзанием.
В химический элемент с самой высокой температурой плавления вольфрам при 3414 ° С (6177 ° F, 3687 К);[4] это свойство делает вольфрам идеальным для использования в качестве нити в лампочках. Часто цитируемый углерод не плавится при атмосферном давлении, но возвышенный примерно при 3726,85 ° С (6740,33 ° F; 4000,00 К); жидкая фаза существует только при давлении выше 10 МПа (99 атм) и, по оценкам, 4 030–4 430 ° C (7 290–8 010 ° F; 4 300–4 700 K) (см. фазовая диаграмма углерода ). Карбид тантала гафния (Та4HfC5) это огнеупорный соединение с очень высокой температурой плавления 4215 К (3942 ° C, 7128 ° F).[5] Квантово-механическое компьютерное моделирование предсказало, что сплав HfN0.38C0.51 будет иметь еще более высокую температуру плавления (около 4400 К),[6] что сделало бы его веществом с наивысшей температурой плавления при атмосферном давлении. Это предсказание позже было подтверждено экспериментом.[7] На другом конце шкалы гелий не замерзает при нормальном давлении даже при температурах, сколь угодно близких к абсолютный ноль; давление более чем в двадцать раз выше нормы атмосферное давление необходимо.
| Список общих химических веществ | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Химическая[Я] | Плотность (грамм/см3) | Таять (K) [8] | Кипятить (K) | |||||||||
| Вода @STP | 1 | 273 | 373 | |||||||||
| Припой (Pb60Sn40) | 456 | |||||||||||
| Кокосовое масло | 307.2 | - | ||||||||||
| Парафиновая свеча | 0.9 | 310 | 643 | |||||||||
| Водород | 0.00008988 | 14.01 | 20.28 | |||||||||
| Гелий | 0.0001785 | —[II] | 4.22 | |||||||||
| Бериллий | 1.85 | 1560 | 2742 | |||||||||
| Углерод | 2.267 | —[III][9] | 4000[III][9] | |||||||||
| Азот | 0.0012506 | 63.15 | 77.36 | |||||||||
| Кислород | 0.001429 | 54.36 | 90.20 | |||||||||
| Натрий | 0.971 | 370.87 | 1156 | |||||||||
| Магний | 1.738 | 923 | 1363 | |||||||||
| Алюминий | 2.698 | 933.47 | 2792 | |||||||||
| Сера | 2.067 | 388.36 | 717.87 | |||||||||
| Хлор | 0.003214 | 171.6 | 239.11 | |||||||||
| Калий | 0.862 | 336.53 | 1032 | |||||||||
| Титана | 4.54 | 1941 | 3560 | |||||||||
| Утюг | 7.874 | 1811 | 3134 | |||||||||
| Никель | 8.912 | 1728 | 3186 | |||||||||
| Медь | 8.96 | 1357.77 | 2835 | |||||||||
| Цинк | 7.134 | 692.88 | 1180 | |||||||||
| Галлий | 5.907 | 302.9146 | 2673 | |||||||||
| Серебро | 10.501 | 1234.93 | 2435 | |||||||||
| Кадмий | 8.69 | 594.22 | 1040 | |||||||||
| Индий | 7.31 | 429.75 | 2345 | |||||||||
| Йод | 4.93 | 386.85 | 457.4 | |||||||||
| Тантал | 16.654 | 3290 | 5731 | |||||||||
| Вольфрам | 19.25 | 3695 | 5828 | |||||||||
| Платина | 21.46 | 2041.4 | 4098 | |||||||||
| Золото | 19.282 | 1337.33 | 3129 | |||||||||
| Меркурий | 13.5336 | 234.43 | 629.88 | |||||||||
| Свинец | 11.342 | 600.61 | 2022 | |||||||||
| Висмут | 9.807 | 544.7 | 1837 | |||||||||
Примечания
| ||||||||||||
Измерения точки плавления

Много лабораторные методы существуют для определения точек плавления. Скамейка Кофлера представляет собой металлическую полосу с температурным градиентом (диапазон от комнатной температуры до 300 ° C). Любое вещество может быть помещено на участок полосы, чтобы выявить его термическое поведение при температуре в этой точке. Дифференциальная сканирующая калориметрия дает информацию о температуре плавления вместе с ее энтальпия плавления.

Базовый прибор для определения температуры плавления для анализа кристаллических твердых веществ состоит из масляная ванна с прозрачным окном (самая простая конструкция: Трубка Тиле ) и простую лупу. Несколько зерен твердого вещества помещают в тонкую стеклянную трубку и частично погружают в масляную ванну. Масляную баню нагревают (и перемешивают), и с помощью лупы (и внешнего источника света) можно наблюдать плавление отдельных кристаллов при определенной температуре. Вместо масляной ванны можно использовать металлический блок. Некоторые современные инструменты имеют автоматическое оптическое обнаружение.
Измерение также может производиться непрерывно во время рабочего процесса. Например, нефтеперерабатывающие заводы измеряют точку замерзания дизельного топлива «в режиме онлайн», что означает, что проба берется из технологического процесса и измеряется автоматически. Это позволяет проводить более частые измерения, так как пробу не нужно собирать вручную и отправлять в удаленную лабораторию.
Технологии изготовления огнеупорных материалов
Для тугоплавких материалов (например, платины, вольфрама, тантала, некоторых карбидов и нитридов и т. Д.) Чрезвычайно высокая температура плавления (обычно считается выше, скажем, 1800 ° C) может быть определена путем нагревания материала в печи черного тела и измерение температуры черного тела с помощью оптического пирометр. Для материалов с самой высокой температурой плавления это может потребовать экстраполяции на несколько сотен градусов. Известно, что спектральная яркость раскаленного тела зависит от его температуры. Оптический пирометр сравнивает яркость исследуемого тела с яркостью источника, который ранее был откалиброван в зависимости от температуры. Таким образом, измерение абсолютной величины интенсивности излучения не требуется. Однако для определения калибровки пирометра необходимо использовать известные температуры. Для температур выше диапазона калибровки источника необходимо использовать метод экстраполяции. Эта экстраполяция осуществляется с помощью Закон планка излучения. Константы в этом уравнении неизвестны с достаточной точностью, что приводит к увеличению ошибок экстраполяции при более высоких температурах. Однако для этой экстраполяции были разработаны стандартные методы.
Рассмотрим случай использования золота в качестве источника (т.пл. = 1063 ° C). В этом методе ток через нить накала пирометра регулируется до тех пор, пока интенсивность света нити не будет соответствовать интенсивности света черного тела при температуре плавления золота. Это устанавливает температуру первичной калибровки и может быть выражено через ток через лампу пирометра. При той же настройке тока пирометр наводится на другое черное тело с более высокой температурой. Между пирометром и этим черным телом вставлена поглощающая среда с известной пропускной способностью. Затем температура черного тела регулируется до тех пор, пока не будет совпадать его интенсивность и интенсивность нити накала пирометра. Истинная более высокая температура черного тела затем определяется по закону Планка. Затем поглощающая среда удаляется, и ток через нить накаливания регулируется так, чтобы интенсивность нити накала соответствовала силе черного тела. Таким образом устанавливается вторая точка калибровки пирометра. Этот шаг повторяется для переноса калибровки на более высокие температуры. Теперь температуры и соответствующие им токи накала пирометра известны, и можно построить кривую зависимости температуры от тока. Затем эту кривую можно экстраполировать на очень высокие температуры.
При определении температуры плавления тугоплавкого вещества этим методом необходимо либо иметь условия черного тела, либо знать излучательная способность измеряемого материала. Сохранение тугоплавкого материала в жидком состоянии может вызвать экспериментальные трудности. Таким образом, температуры плавления некоторых тугоплавких металлов были измерены путем наблюдения излучения из полости черного тела в твердых металлических образцах, которые были намного длиннее, чем их ширина. Для образования такой полости просверливается отверстие перпендикулярно длинной оси в центре стержня из материала. Затем эти стержни нагревают, пропуская через них очень большой ток, и излучение, выходящее из отверстия, наблюдается с помощью оптического пирометра. На точку плавления указывает потемнение отверстия при появлении жидкой фазы, разрушающей условия черного тела. Сегодня методы бесконтейнерного лазерного нагрева в сочетании с быстрыми пирометрами и спектропирометрами используются для точного контроля времени, в течение которого образец находится при экстремальных температурах. Такие эксперименты продолжительностью менее секунды решают несколько проблем, связанных с более традиционными измерениями точки плавления, проводимыми при очень высоких температурах, такими как испарение образца и реакция с контейнером.
Термодинамика
Чтобы твердое вещество расплавилось, требуется тепло, чтобы поднять его температуру до точки плавления. Однако для плавления требуется дополнительное тепло: это называется теплота плавления, и является примером скрытая теплота.
С точки зрения термодинамики, при температуре плавления изменение Свободная энергия Гиббса (ΔG) материала равна нулю, но энтальпия (ЧАС) и энтропия (S) материала увеличиваются (ΔH, ΔS> 0). Явление плавления происходит, когда свободная энергия Гиббса жидкости становится ниже, чем у твердого вещества для этого материала. При разных давлениях это происходит при определенной температуре. Также можно показать, что:
Здесь Т, ΔS и ΔH соответственно температура при температуре плавления изменение энтропии плавления и изменение энтальпии плавления.
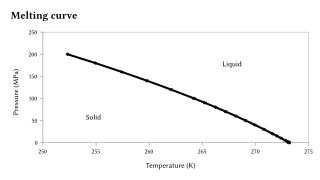
Температура плавления чувствительна к очень большим изменениям давление, но обычно эта чувствительность на порядки меньше, чем у точка кипения, поскольку переход твердое тело-жидкость представляет собой лишь небольшое изменение объема.[10][11] Если, как это наблюдается в большинстве случаев, вещество более плотное в твердом состоянии, чем в жидком состоянии, температура плавления будет повышаться с увеличением давления. В противном случае происходит обратное поведение. Примечательно, что это относится к воде, как показано графически справа, а также к Si, Ge, Ga, Bi. При чрезвычайно больших перепадах давления наблюдаются существенные изменения температуры плавления. Например, температура плавления кремния при атмосферном давлении (0,1 МПа) составляет 1415 ° C, но при давлениях выше 10 ГПа она снижается до 1000 ° C.[12]
Температуры плавления часто используются для характеристики органических и неорганических соединений и определения их чистота. Точка плавления чистого вещества всегда выше и имеет меньший диапазон, чем точка плавления нечистого вещества или, в более общем смысле, смесей. Чем выше количество других компонентов, тем ниже температура плавления и тем шире будет диапазон температур плавления, часто называемый «пастообразным диапазоном». Температура, при которой начинается плавление смеси, известна как «солидус», а температура, при которой плавление завершается, называется «ликвидусом». Эвтектики - это особые типы смесей, которые ведут себя как однофазные. Они резко плавятся при постоянной температуре с образованием жидкости такого же состава. В качестве альтернативы, при охлаждении жидкость с эвтектическим составом затвердеет в виде однородно диспергированных мелких (мелкозернистых) смешанных кристаллов того же состава.
В отличие от кристаллических твердых тел, очки не обладают температурой плавления, при нагревании плавно переходят в стеклование в вязкая жидкость.При дальнейшем нагревании они постепенно размягчаются, что может характеризоваться определенным точки размягчения.
Депрессия точки замерзания
Точка замерзания растворитель подавляется, когда добавляется другое соединение, что означает, что решение имеет более низкую температуру замерзания, чем чистый растворитель. Это явление используется в технических приложениях, чтобы избежать замерзания, например, при добавлении соли или этиленгликоля в воду.
Правило Карнелли
В органическая химия, Правило Карнелли, основанная в 1882 г. Томас Карнелли, утверждает, что высоко молекулярная симметрия связана с высокой температурой плавления.[13] Карнелли основал свое правило на исследовании 15 000 химических соединений. Например, для трех структурные изомеры с молекулярная формула C5ЧАС12 температура плавления увеличивается в серии изопентан -160 ° С (113 К) н-пентан −129,8 ° С (143 К) и неопентан -16,4 ° С (256,8 К).[14] Точно так же в ксилолы а также дихлорбензолы температура плавления увеличивается на порядок мета, орто и затем пара. Пиридин имеет более низкую симметрию, чем бензол следовательно, его температура ниже, но температура плавления снова увеличивается с диазин и триазины. Многие клеточные соединения, такие как адамантан и кубан с высокой симметрией имеют относительно высокие температуры плавления.
Высокая температура плавления является следствием высокого теплота плавления, низкий энтропия плавления или их комбинацию. В высокосимметричных молекулах кристаллическая фаза плотно упакована с множеством эффективных межмолекулярных взаимодействий, приводящих к более высокому изменению энтальпии при плавлении.

Прогнозирование температуры плавления веществ (критерий Линдеманна)
Попытка предсказать объемную точку плавления кристаллических материалов была впервые сделана в 1910 г. Фредерик Линдеманн.[16] Идея теории заключалась в наблюдении того, что средняя амплитуда тепловых колебаний увеличивается с увеличением температуры. Плавление начинается, когда амплитуда колебаний становится достаточно большой, чтобы соседние атомы частично занимали одно и то же пространство. В Критерий Линдеманна заявляет, что таяние ожидается, когда вибрация среднеквадратичная амплитуда превышает пороговое значение.
Предполагая, что все атомы в кристалле колеблются с одинаковой частотой ν, среднюю тепловую энергию можно оценить с помощью теорема о равнораспределении в качестве[17]
куда м это атомная масса, ν это частота, ты - средняя амплитуда колебаний, kB это Постоянная Больцмана, и Т это абсолютная температура. Если пороговое значение ты2 является c2а2 куда c это Постоянная Линдеманна и а это атомный интервал, то температура плавления оценивается как
В зависимости от оценки средней тепловой энергии можно получить несколько других выражений для расчетной температуры плавления. Еще одно часто используемое выражение для критерия Линдеманна:[18]
Из выражения для Частота Дебая за ν, у нас есть
куда θD это Температура Дебая и час это Постоянная Планка. Ценности c диапазон от 0,15 до 0,3 для большинства материалов.[19]
Прогноз температуры плавления
В феврале 2011 г. Альфа Эзар выпустили более 10000 точек плавления соединений из своего каталога как открытые данные. Этот набор данных был использован для создания случайный лес модель для предсказания точки плавления, которая сейчас находится в свободном доступе.[20] Данные по открытой температуре плавления также доступны на сайте Природа предшествует.[21] Высококачественные данные, полученные из патентов, а также моделей[22] разработанные с этими данными были опубликованы Tetko и другие.[23]
Смотрите также
Рекомендации
Цитаты
- ^ Рамзи, Дж. А. (1 мая 1949 г.). «Новый метод определения точки замерзания малых количеств». Журнал экспериментальной биологии. 26 (1): 57–64. PMID 15406812.
- ^ Haynes, п. 4.122.
- ^ Температура плавления очищенной воды составляет 0,002519 ± 0,000002 ° C, см. Фейстель, Р. и Вагнер, В. (2006). "Новое уравнение состояния для H2O Ice Ih ". J. Phys. Chem. Ref. Данные. 35 (2): 1021–1047. Bibcode:2006JPCRD..35.1021F. Дои:10.1063/1.2183324.
- ^ Haynes, п. 4.123.
- ^ Agte, C. и Alterthum, H. (1930). «Исследования систем с карбидами при высокой температуре плавления и вклад в проблему плавления углерода». Z. Tech. Phys. 11: 182–191.
- ^ Hong, Q.-J .; ван де Валле, А. (2015). «Прогноз материала с наивысшей известной температурой плавления на основе расчетов молекулярной динамики ab initio». Phys. Ред. B. 92 (2): 020104 (R). Bibcode:2015PhRvB..92b0104H. Дои:10.1103 / PhysRevB.92.020104.
- ^ Буйневич, В.С .; Непапушев, А.А .; Московских, Д.О .; Трусов, Г.В .; Кусков, К.В .; Вадченко, С.Г .; Рогачев, А.С .; Мукасян, А. (Март 2020 г.). «Производство сверхвысокотемпературного нестехиометрического карбонитрида гафния методами синтеза горением и искрового плазменного спекания». Керамика Интернэшнл. 46 (10): 16068–16073. Дои:10.1016 / j.ceramint.2020.03.158.
- ^ Holman, S.W .; Lawrence, R. R .; Барр, Л. (1 января 1895 г.). «Точки плавления алюминия, серебра, золота, меди и платины». Труды Американской академии искусств и наук. 31: 218–233. Дои:10.2307/20020628. JSTOR 20020628.
- ^ а б «Карбон». rsc.org.
- ^ Точное соотношение выражается в Соотношение Клаузиуса – Клапейрона.
- ^ «J10 Heat: изменение агрегатного состояния веществ через изменение теплосодержания: изменение агрегатного состояния веществ и уравнение Клапейрона-Клаузиуса». Получено 19 февраля 2008.
- ^ Тонков, Е.Ю. и Понятовский, Э. Г. (2005) Фазовые превращения элементов под высоким давлением., CRC Press, Бока Ратон, стр. 98 ISBN 0-8493-3367-9
- ^ Браун, Р. Дж. С. и Р. Ф. С. (2000). «Точка плавления и молекулярная симметрия». Журнал химического образования. 77 (6): 724. Bibcode:2000JChEd..77..724B. Дои:10.1021 / ed077p724.
- ^ Haynes, С. 6.153–155.
- ^ Gilman, H .; Смит, К. Л. (1967). «Тетракис (триметилсилил) силан». Журнал металлоорганической химии. 8 (2): 245–253. Дои:10.1016 / S0022-328X (00) 91037-4.
- ^ Линдеманн Ф.А. (1910). «Расчет частот колебаний молекул». Phys. Z. 11: 609–612.
- ^ Соркин, С., (2003), Точечные дефекты, структура решетки и плавление, Диссертация, Технион, Израиль.
- ^ Филип Хофманн (2008). Физика твердого тела: введение. Wiley-VCH. п. 67. ISBN 978-3-527-40861-0. Получено 13 марта 2011.
- ^ Нельсон Д. Р. (2002), Дефекты и геометрия в физике конденсированного состояния, Издательство Кембриджского университета, ISBN 0-521-00400-4
- ^ Прогноз температуры плавления с помощью SMILES. Qsardb.org. Проверено 13 сентября 2013 г.
- ^ Брэдли, Жан-Клод; Ланг, Эндрю; Уильямс, Энтони; Кертин, Эван (11 августа 2011 г.). «Открытый сборник точек плавления ONS». Природа предшествует. Дои:10.1038 / npre.2011.6229.1.
- ^ Модели точки плавления OCHEM. ochem.eu. Проверено 18 июня, 2016.
- ^ Тетько, Игорь В; м. Лоу, Дэниел; Уильямс, Энтони Дж (2016). «Разработка моделей для прогнозирования данных о температуре плавления и пиролиза, связанных с несколькими сотнями тысяч соединений, добытых из ПАТЕНТОВ». Журнал химинформатики. 8: 2. Дои:10.1186 / s13321-016-0113-у. ЧВК 4724158. PMID 26807157.
Источники
- Процитированные работы
- Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). CRC Press. ISBN 978-1439855119.
внешняя ссылка
- Таблицы температур плавления и кипения, т. 1 Томас Карнелли (Харрисон, Лондон, 1885–1887)
- Таблицы температур плавления и кипения, т. 2 Томас Карнелли (Харрисон, Лондон, 1885–1887)
- Патентно добытые данные Более 250 000 бесплатно загружаемых данных о температуре плавления. Также можно скачать на фигшер






