Мембранный потенциал - Membrane potential

Мембранный потенциал (также трансмембранный потенциал или же мембранное напряжение) разница в электрический потенциал между интерьером и экстерьером биологического клетка. Для внешней части ячейки типичные значения мембранного потенциала, обычно выражаемые в единицах Милливольт и обозначается как мВ, диапазон от –40 мВ до –80 мВ.
Все клетки животных окружены мембрана состоит из липидный бислой с белки встроен в него. Мембрана служит как изолятором, так и диффузионным барьером для движения ионы. Трансмембранные белки, также известный как ионный транспортер или же ионный насос белки, активно проталкивают ионы через мембрану и создают градиенты концентрации через мембрану, и ионные каналы позволяют ионам перемещаться через мембрану вниз по этим градиентам концентрации. Ионные насосы и ионные каналы электрически эквивалентны набору батареи и резисторы, вставленные в мембрану, и поэтому создают напряжение между двумя сторонами мембраны.
Почти все плазматические мембраны имеют электрический потенциал на себе, причем внутренняя часть обычно отрицательна по отношению к внешней стороне.[1] Мембранный потенциал выполняет две основные функции. Во-первых, он позволяет ячейке функционировать как батарея, обеспечивая питание для работы множества «молекулярных устройств», встроенных в мембрану. Во-вторых, электрически возбудимые клетки Такие как нейроны и мышечные клетки, он используется для передачи сигналов между разными частями соты. Сигналы генерируются путем открытия или закрытия ионных каналов в одной точке мембраны, вызывая локальное изменение мембранного потенциала. На это изменение электрического поля могут быстро влиять как соседние, так и более удаленные ионные каналы в мембране. Эти ионные каналы затем могут открываться или закрываться в результате изменения потенциала, воспроизводя сигнал.
В невозбудимых клетках и в возбудимых клетках в их исходном состоянии мембранный потенциал поддерживается на относительно стабильном уровне, называемом потенциал покоя. Для нейронов типичные значения потенциала покоя составляют от –70 до –80 милливольт; то есть внутренняя часть ячейки имеет отрицательное базовое напряжение немного меньше одной десятой вольта. Открытие и закрытие ионных каналов может вызвать отклонение от потенциала покоя. Это называется деполяризация если внутреннее напряжение становится менее отрицательным (скажем, от –70 мВ до –60 мВ), или гиперполяризация если внутреннее напряжение становится более отрицательным (скажем, от –70 мВ до –80 мВ). В возбудимых клетках достаточно большая деполяризация может вызвать потенциал действия, при котором мембранный потенциал изменяется быстро и значительно в течение короткого времени (порядка от 1 до 100 миллисекунд), часто меняя полярность. Потенциалы действия генерируются при активации определенных потенциалзависимые ионные каналы.
В нейронах факторы, влияющие на мембранный потенциал, разнообразны. Они включают в себя множество типов ионных каналов, некоторые из которых являются химически закрытыми, а некоторые - регулируемыми по напряжению. Поскольку потенциалзависимые ионные каналы контролируются мембранным потенциалом, в то время как сам мембранный потенциал находится под влиянием тех же самых ионных каналов, возникают петли обратной связи, которые допускают сложную временную динамику, включая колебания и регенеративные события, такие как потенциалы действия.
Физическая основа
Мембранный потенциал клетки определяется двумя факторами: электрической силой и диффузией. Электрическая сила возникает из-за взаимного притяжения между частицами с противоположными электрическими зарядами (положительным и отрицательным) и взаимного отталкивания между частицами с одинаковым типом заряда (как положительными, так и отрицательными). Диффузия возникает из-за статистической тенденции частиц перераспределяться из регионов с высокой концентрацией в регионы с низкой концентрацией.
Напряжение
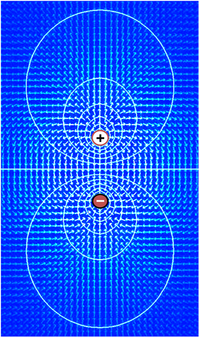
Напряжение, что является синонимом разность электрических потенциалов, это способность пропускать электрический ток через сопротивление. В самом деле, простейшее определение напряжения дает Закон Ома: V = IR, где V - напряжение, I - ток, а R - сопротивление. Если источник напряжения, такой как батарея, помещен в электрическую цепь, чем выше напряжение источника, тем больше ток, который он будет проводить через доступное сопротивление. Функциональное значение напряжения заключается только в потенциале различия между двумя точками в цепи. Идея наличия напряжения в одной точке бессмысленна. В электронике принято назначать нулевое напряжение какому-либо произвольно выбранному элементу схемы, а затем назначать напряжения для других элементов, измеряемых относительно этой нулевой точки. Не имеет значения, какой элемент выбран в качестве нулевой точки - функция схемы зависит только от разницы, а не от напряжений. как таковой. Однако в большинстве случаев и по соглашению нулевой уровень чаще всего назначается той части схемы, которая находится в контакте с земля.
Тот же принцип применим к напряжению в клеточной биологии. В электрически активной ткани разность потенциалов между любыми двумя точками можно измерить, вставив электрод в каждую точку, например, один внутри и один снаружи клетки, и подключив оба электрода к выводам того, что по сути является специализированным вольтметром. По соглашению, нулевое значение потенциала присваивается внешней стороне ячейки, а знак разности потенциалов между внешней и внутренней стороной определяется потенциалом внутренней части относительно внешнего нуля.
В математических терминах определение напряжения начинается с концепции электрическое поле E, векторное поле, задающее величину и направление каждой точке пространства. Во многих ситуациях электрическое поле представляет собой консервативное поле, что означает, что его можно выразить как градиент скалярной функции V, то есть, E = –∇V. Это скалярное поле V называется распределением напряжения. Обратите внимание, что определение допускает произвольную постоянную интегрирования, поэтому абсолютные значения напряжения не имеют смысла. В общем, электрические поля можно рассматривать как консервативные, только если магнитные поля не оказывают на них значительного влияния, но это условие обычно хорошо применимо к биологической ткани.
Поскольку электрическое поле представляет собой градиент распределения напряжения, быстрые изменения напряжения в небольшой области подразумевают сильное электрическое поле; и наоборот, если напряжение остается примерно одинаковым в большой области, электрические поля в этой области должны быть слабыми. Сильное электрическое поле, эквивалентное сильному градиенту напряжения, подразумевает, что сильная сила действует на любые заряженные частицы, находящиеся внутри области.
Ионы и силы, управляющие их движением
Электрические сигналы в биологических организмах, как правило, управляются ионы.[3] Наиболее важными катионами для потенциала действия являются: натрий (Na+) и калий (K+).[4] Оба они одновалентный катионы, несущие один положительный заряд. Потенциалы действия также могут включать: кальций (Ca2+),[5] который является двухвалентный катион, несущий двойной положительный заряд. В хлористый анион (Cl−) играет важную роль в потенциалах действия некоторых водоросли,[6] но играет незначительную роль в потенциалах действия большинства животных.[7]
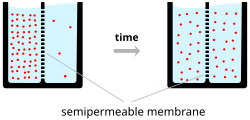
Ионы проникают через клеточную мембрану под двумя воздействиями: распространение и электрические поля. Простой пример, в котором два раствора - A и B - разделены пористым барьером, показывает, что диффузия гарантирует, что они в конечном итоге смешаются с равными растворами. Это смешивание происходит из-за разницы в их концентрациях. Область с высокой концентрацией будет распространяться в сторону области с низкой концентрацией. Чтобы расширить пример, пусть раствор A содержит 30 ионов натрия и 30 ионов хлора. Кроме того, пусть раствор B содержит только 20 ионов натрия и 20 ионов хлора. Если предположить, что барьер позволяет обоим типам ионов проходить через него, тогда будет достигнуто устойчивое состояние, при котором оба раствора содержат 25 ионов натрия и 25 ионов хлора. Если, однако, пористый барьер является селективным по отношению к пропусканию ионов, то сама по себе диффузия не будет определять полученный раствор. Возвращаясь к предыдущему примеру, давайте теперь построим барьер, проницаемый только для ионов натрия. Теперь только натрий может диффундировать через барьер от его более высокой концентрации в растворе A до более низкой концентрации в растворе B. Это приведет к большему накоплению ионов натрия, чем ионы хлорида в растворе B, и меньшему количеству ионов натрия, чем ионы хлорида в растворе А.
Это означает, что чистый положительный заряд в растворе B обусловлен более высокой концентрацией положительно заряженных ионов натрия, чем отрицательно заряженных ионов хлорида. Точно так же в растворе А имеется отрицательный заряд из-за большей концентрации отрицательных ионов хлора, чем положительных ионов натрия. Поскольку противоположные заряды притягиваются, а одинаковые заряды отталкиваются, на ионы теперь также влияют электрические поля, а также силы диффузии. Следовательно, положительные ионы натрия с меньшей вероятностью попадут в теперь более положительный раствор B и останутся в растворе, который стал более отрицательным. Точка, в которой силы электрических полей полностью противодействуют силе, обусловленной диффузией, называется равновесным потенциалом. В этот момент чистый поток конкретного иона (в данном случае натрия) равен нулю.
Плазменные мембраны

Каждая животная клетка заключена в плазматическая мембрана, который имеет структуру липидный бислой со многими типами крупных молекул, встроенных в него. Поскольку она состоит из молекул липидов, плазматическая мембрана по своей природе имеет высокое электрическое сопротивление, другими словами, низкую внутреннюю проницаемость для ионов. Однако некоторые молекулы, встроенные в мембрану, способны либо активно переносить ионы с одной стороны мембраны на другую, либо обеспечивать каналы, по которым они могут перемещаться.[8]
В электрической терминологии плазматическая мембрана функционирует как комбинированный резистор и конденсатор. Сопротивление возникает из-за того, что мембрана препятствует перемещению зарядов через нее. Емкость возникает из-за того, что липидный бислой настолько тонкий, что скопление заряженных частиц на одной стороне вызывает электрическую силу, которая тянет противоположно заряженные частицы к другой стороне. Емкость мембраны относительно не зависит от молекул, которые в нее встроены, поэтому ее более или менее инвариантное значение оценивается примерно в 2 мкФ / см.2 (общая емкость участка мембраны пропорциональна его площади). С другой стороны, проводимость чистого липидного бислоя настолько низка, что в биологических ситуациях она всегда определяется проводимостью альтернативных путей, обеспечиваемых встроенными молекулами. Таким образом, емкость мембраны более или менее фиксирована, но сопротивление сильно варьируется.
Толщина плазматической мембраны оценивается примерно в 7-8 нанометров. Поскольку мембрана такая тонкая, для создания внутри нее сильного электрического поля не требуется очень большого трансмембранного напряжения. Типичные мембранные потенциалы в клетках животных составляют порядка 100 милливольт (то есть одна десятая вольт), но расчеты показывают, что это создает электрическое поле, близкое к максимальному, которое может выдержать мембрана - было подсчитано, что напряжение разница намного больше 200 милливольт может вызвать пробой диэлектрика, то есть дуга через мембрану.
Облегченное распространение и транспортировка
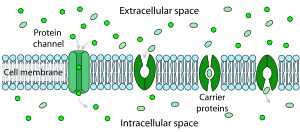
Устойчивость чистого липидного бислоя к прохождению через него ионов очень высока, но структуры, встроенные в мембрану, могут значительно усилить движение ионов либо активно или же пассивно, через механизмы, называемые облегченный транспорт и облегченное распространение. Двумя типами структур, которые играют наибольшую роль, являются ионные каналы и ионные насосы, оба обычно образуются из скоплений белковых молекул. Ионные каналы обеспечивают проходы, по которым ионы могут перемещаться. В большинстве случаев ионный канал проницаем только для определенных типов ионов (например, натрия и калия, но не хлорида или кальция), а иногда проницаемость варьируется в зависимости от направления движения ионов. Ионные насосы, также известные как переносчики ионов или белки-переносчики, активно транспортируют определенные типы ионов с одной стороны мембраны на другую, иногда используя для этого энергию, полученную в результате метаболических процессов.
Ионные насосы
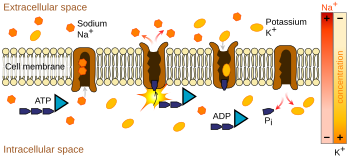
Ионные насосы находятся интегральные мембранные белки которые выполняют активный транспорт т. е. использовать клеточную энергию (АТФ), чтобы «накачать» ионы против градиента их концентрации.[9] Такие ионные насосы забирают ионы с одной стороны мембраны (уменьшая их концентрацию там) и выпускают их с другой стороны (увеличивая их концентрацию там).
Ионный насос, наиболее соответствующий потенциалу действия, - это натриево-калиевый насос, который переносит три иона натрия из клетки и два иона калия внутрь.[10] Как следствие, концентрация калий ионы K+ внутри нейрона примерно в 20 раз больше, чем внешняя концентрация, тогда как концентрация натрия снаружи примерно в девять раз больше, чем внутри.[11][12] Аналогичным образом другие ионы имеют разные концентрации внутри и вне нейрона, например кальций, хлористый и магний.[12]
Если бы количество ионов каждого типа было равным, натрий-калиевый насос был бы электрически нейтральным, но из-за обмена три к двум он дает чистое перемещение одного положительного заряда от внутриклеточного к внеклеточному для каждого цикла. тем самым способствуя положительной разнице напряжений. Насос имеет три эффекта: (1) он делает концентрацию натрия высокой во внеклеточном пространстве и низкой во внутриклеточном пространстве; (2) он делает концентрацию калия высокой во внутриклеточном пространстве и низкой во внеклеточном пространстве; (3) он придает внутриклеточному пространству отрицательное напряжение по отношению к внеклеточному пространству.
Натрий-калиевый насос работает относительно медленно. Если бы ячейка была инициализирована повсюду равными концентрациями натрия и калия, насосу потребовалось бы несколько часов, чтобы установить равновесие. Насос работает постоянно, но становится все менее эффективным, поскольку концентрации натрия и калия, доступные для перекачивания, уменьшаются.
Ионные насосы влияют на потенциал действия только путем установления относительного соотношения внутриклеточных и внеклеточных концентраций ионов. Потенциал действия в основном включает открытие и закрытие ионных каналов, а не ионных насосов. Если ионные насосы отключены путем удаления их источника энергии или добавления ингибитора, такого как уабаин аксон все еще может запускать сотни тысяч потенциалов действия, прежде чем их амплитуда начнет значительно уменьшаться.[9] В частности, ионные насосы не играют значительной роли в реполяризации мембраны после потенциала действия.[4]
Другой функционально важный ионный насос - это натрий-кальциевый обменник. Этот насос работает концептуально аналогично натрий-калиевому насосу, за исключением того, что в каждом цикле он заменяет три Na+ из внеклеточного пространства на один Ca++ из внутриклеточного пространства. Поскольку чистый поток заряда направлен внутрь, этот насос, по сути, работает «под гору» и, следовательно, не требует никаких источников энергии, кроме мембранного напряжения. Его наиболее важным эффектом является выкачивание кальция наружу - он также позволяет поступать внутрь натрию, тем самым противодействуя натрий-калиевому насосу, но, поскольку общие концентрации натрия и калия намного выше, чем концентрации кальция, этот эффект относительно не важен. Конечным результатом натрий-кальциевого обменника является то, что в состоянии покоя внутриклеточные концентрации кальция становятся очень низкими.
Ионные каналы

Ионные каналы находятся интегральные мембранные белки с порами, через которые ионы могут перемещаться между внеклеточным пространством и внутренним пространством клетки. Большинство каналов специфичны (селективны) для одного иона; например, большинство калиевых каналов характеризуются соотношением селективности 1000: 1 для калия по сравнению с натрием, хотя ионы калия и натрия имеют одинаковый заряд и лишь незначительно различаются по радиусу. Пора канала обычно настолько мала, что ионы должны проходить через нее в одиночном порядке.[14] Поры каналов могут быть открытыми или закрытыми для прохождения ионов, хотя ряд каналов демонстрирует различные уровни субпроводимости. Когда канал открыт, ионы проникают через канал, снижая трансмембранный градиент концентрации этого конкретного иона. Скорость ионного потока через канал, то есть амплитуда одноканального тока, определяется максимальной проводимостью канала и электрохимической движущей силой для этого иона, которая представляет собой разницу между мгновенным значением мембранного потенциала и значением обратный потенциал.[15]
Канал может иметь несколько разных состояний (соответствующих разным конформации белка), но каждое такое состояние бывает либо открытым, либо закрытым. В общем, закрытые состояния соответствуют либо сокращению поры, что делает ее непроходимой для иона, либо отдельной части белка, закрывающей пору. Например, зависимый от напряжения натриевый канал подвергается инактивация, в котором часть белка качается в пору, запечатывая ее.[16] Эта инактивация отключает ток натрия и играет важную роль в потенциале действия.
Ионные каналы можно классифицировать по тому, как они реагируют на окружающую среду.[17] Например, ионные каналы, участвующие в потенциале действия: каналы, чувствительные к напряжению; они открываются и закрываются в ответ на напряжение на мембране. Лиганд-закрытые каналы образуют другой важный класс; эти ионные каналы открываются и закрываются в ответ на связывание молекула лиганда, например нейротрансмиттер. Другие ионные каналы открываются и закрываются под действием механических сил. Еще другие ионные каналы, такие как сенсорные нейроны - открываться и закрываться в ответ на другие раздражители, такие как свет, температура или давление.
Каналы утечки
Каналы утечки представляют собой простейший тип ионных каналов, поскольку их проницаемость более или менее постоянна. Типы каналов утечки, которые имеют наибольшее значение в нейронах, - это калиевые и хлоридные каналы. Даже они не являются совершенно постоянными по своим свойствам: во-первых, большинство из них зависят от напряжения в том смысле, что они проводят лучше в одном направлении, чем в другом (другими словами, они выпрямители ); во-вторых, некоторые из них могут быть отключены химическими лигандами, даже если для работы им не требуются лиганды.
Лиганд-закрытые каналы
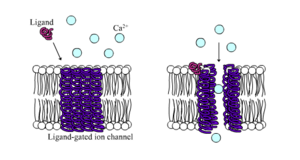
Ионные каналы, управляемые лигандами представляют собой каналы, проницаемость которых значительно увеличивается, когда какой-либо тип химического лиганда связывается со структурой белка. Клетки животных содержат сотни, если не тысячи, их типов. Большое подмножество функционирует как рецепторы нейротрансмиттеров - они происходят в постсинаптический сайтов, а химический лиганд, который их закрывает, высвобождается пресинаптическим аксонный терминал. Одним из примеров этого типа является Рецептор AMPA, рецептор нейротрансмиттера глутамат что при активации пропускает ионы натрия и калия. Другой пример - ГАМКА рецептор, рецептор нейротрансмиттера ГАМК при активации пропускает ионы хлора.
Рецепторы нейротрансмиттеров активируются лигандами, которые появляются во внеклеточной области, но есть и другие типы каналов, управляемых лигандами, которые контролируются взаимодействиями на внутриклеточной стороне.
Каналы, зависимые от напряжения
Управляемые по напряжению ионные каналы, также известный как потенциалзависимые ионные каналы, - каналы, на проницаемость которых влияет мембранный потенциал. Они образуют еще одну очень большую группу, каждый член которой имеет определенную ионную селективность и определенную зависимость от напряжения. Многие из них также зависят от времени - другими словами, они не сразу реагируют на изменение напряжения, а только после задержки.
Одним из наиболее важных представителей этой группы является тип потенциалзависимого натриевого канала, который лежит в основе потенциалов действия - их иногда называют Натриевые каналы Ходжкина-Хаксли потому что изначально они характеризовались Алан Ллойд Ходжкин и Эндрю Хаксли в своих исследованиях физиологии потенциала действия, получивших Нобелевскую премию. Канал закрывается при уровне напряжения покоя, но внезапно открывается, когда напряжение превышает определенный порог, обеспечивая большой приток ионов натрия, который вызывает очень быстрое изменение мембранного потенциала. Восстановление от потенциала действия частично зависит от типа регулируемого по напряжению калиевого канала, который закрывается на уровне напряжения покоя, но открывается вследствие большого изменения напряжения, возникающего во время действия потенциала действия.
Потенциал разворота
В обратный потенциал (или же равновесный потенциал) иона представляет собой значение трансмембранного напряжения, при котором диффузионные и электрические силы уравновешиваются, так что нет чистого потока ионов через мембрану. Это означает, что трансмембранное напряжение точно противодействует силе диффузии иона, так что суммарный ток иона через мембрану равен нулю и не изменяется. Обратный потенциал важен, потому что он дает напряжение, которое действует на каналы, проницаемые для этого иона, другими словами, он дает напряжение, которое генерирует градиент концентрации ионов, когда он действует как аккумулятор.
Равновесный потенциал того или иного иона обычно обозначают обозначениями Eион.Равновесный потенциал для любого иона можно рассчитать с помощью Уравнение Нернста.[18] Например, обратный потенциал для ионов калия будет следующим:
куда
- Eэкв, К+ - равновесный потенциал калия, измеряемый в вольт
- р универсальный газовая постоянная, равно 8,314 джоули · K−1· Моль−1
- Т это абсолютная температура, измеряется в кельвины (= K = градусы Цельсия + 273,15)
- z это количество элементарные сборы рассматриваемого иона, участвующего в реакции
- F это Постоянная Фарадея, что равно 96 485 кулоны · Моль−1 или J · V−1· Моль−1
- [K+]о внеклеточная концентрация калия, измеренная в моль · М−3 или ммоль · л−1
- [K+]я это внутриклеточная концентрация калия
Даже если два разных иона имеют одинаковый заряд (т. Е. K+ и Na+), они все еще могут иметь очень разные равновесные потенциалы при условии, что их внешняя и / или внутренняя концентрации различаются. Возьмем, к примеру, равновесные потенциалы калия и натрия в нейронах. Равновесный потенциал калия EK составляет -84 мВ с 5 мМ калия снаружи и 140 мМ внутри. С другой стороны, равновесный потенциал натрия, ENa, составляет приблизительно +66 мВ с приблизительно 12 мМ натрия внутри и 140 мМ снаружи.[примечание 1]
Изменения мембранного потенциала в процессе развития
А нейрон мембранный потенциал покоя фактически изменяется во время разработка организма. Для того, чтобы нейрон в конечном итоге принял свою полноценную взрослую функцию, его потенциал должен строго регулироваться во время развития. По мере развития организма мембранный потенциал покоя становится все более отрицательным.[19] Глиальные клетки также дифференцируются и размножаются по мере развития в мозг.[20] Добавление этих глиальных клеток увеличивает способность организма регулировать внеклеточные калий. Падение внеклеточного калия может привести к снижению мембранного потенциала на 35 мВ.[21]
Возбудимость клеток
Возбудимость клетки - это изменение мембранного потенциала, которое необходимо для клеточных реакций в различных тканях. Возбудимость клеток - это свойство, которое индуцируется во время раннего эмбриогенеза.[22] Возбудимость клетки также определяется как легкость, с которой может быть вызвана реакция.[23] Отдыхающие и пороговые потенциалы формирует основу возбудимости клетки, и эти процессы являются фундаментальными для генерации градиентных потенциалов и потенциалов действия.
Самое важное регуляторы возбудимости клеток внеклеточные электролит концентрации (т.е. Na+, К+, Ca2+, Cl−, Mg2+ ) и ассоциированные белки. Важными белками, регулирующими возбудимость клеток, являются: потенциалзависимые ионные каналы, ионные транспортеры (например. Na + / K + -АТФаза, транспортеры магния, кислотно-основные переносчики ), мембранные рецепторы и активируемые гиперполяризацией каналы с циклическими нуклеотидами.[24] Например, калиевые каналы и рецепторы, чувствительные к кальцию являются важными регуляторами возбудимости в нейроны, сердечные миоциты и многие другие возбудимые клетки, такие как астроциты.[25] Ион кальция также самый важный второй посланник в возбужденном клеточная сигнализация. Инициируется активация синаптических рецепторов длительные изменения в возбудимости нейронов.[26] Щитовидная железа, надпочечник и другие гормоны также регулируют возбудимость клеток.
Считается, что многие типы клеток имеют возбудимую мембрану. Возбудимые клетки - нейроны, миоциты (сердечные, скелетные, гладкий ), сосудистый эндотелиальные клетки, юкстагломерулярные клетки, интерстициальные клетки Кахаля, многие виды эпителиальные клетки (например. бета-клетки, альфа-клетки, дельта-клетки, энтероэндокринные клетки ), глиальный клетки (например, астроциты), механорецептор ячейки (например, волосковые клетки и Ячейки Меркель ), хеморецептор ячейки (например, клетки клубочка, вкусовые рецепторы ), немного клетки растений и возможно иммунные клетки.[27] Астроциты демонстрируют форму неэлектрической возбудимости, основанную на внутриклеточных изменениях кальция, связанных с экспрессией нескольких рецепторов, через которые они могут обнаруживать синаптический сигнал. В нейронах существуют различные мембранные свойства в некоторых частях клетки, например, дендритная возбудимость наделяет нейроны способностью обнаруживать совпадения пространственно разделенных входов.[28]
Эквивалентная схема
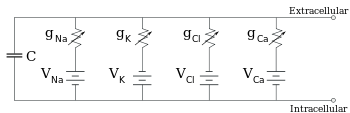
Электрофизиологи моделируют эффекты разницы концентраций ионов, ионных каналов и емкости мембраны в терминах эквивалентная схема, который предназначен для отображения электрических свойств небольшого участка мембраны. Эквивалентная схема состоит из конденсатора, включенного параллельно с четырьмя дорожками, каждая из которых состоит из последовательно включенной батареи с переменной проводимостью. Емкость определяется свойствами липидного бислоя и считается фиксированной. Каждый из четырех параллельных путей исходит от одного из основных ионов: натрия, калия, хлорида и кальция. Напряжение каждого ионного пути определяется концентрацией иона на каждой стороне мембраны; увидеть Потенциал разворота раздел выше. Проводимость каждого ионного пути в любой момент времени определяется состояниями всех ионных каналов, которые потенциально проницаемы для этого иона, включая каналы утечки, лиганд-зависимые каналы и потенциал-управляемые ионные каналы.
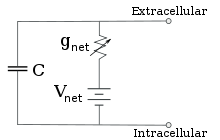
Для фиксированных концентраций ионов и фиксированных значений проводимости ионного канала эквивалентную схему можно дополнительно уменьшить, используя Уравнение гольдмана как описано ниже, к схеме, содержащей емкость, параллельную батарее, и проводимость. В электрическом смысле это разновидность RC схема (резистивно-емкостная цепь), а ее электрические свойства очень просты. Начиная с любого начального состояния, ток, протекающий либо по проводимости, либо по емкости, затухает с экспоненциальным изменением во времени с постоянной времени τ = RC, куда C - емкость мембранного участка, а R = 1 / гсеть это чистое сопротивление. В реальных ситуациях постоянная времени обычно находится в диапазоне 1–100 миллисекунд. В большинстве случаев изменения в проводимости ионных каналов происходят в более быстром масштабе времени, поэтому RC-цепь не является хорошим приближением; однако дифференциальное уравнение, используемое для моделирования мембранного участка, обычно является модифицированной версией уравнения RC-цепи.
Потенциал отдыха
Когда мембранный потенциал клетки остается в течение длительного периода времени без значительных изменений, это называется потенциал покоя или напряжение покоя. Этот термин используется для мембранного потенциала невозбудимых клеток, а также для мембранного потенциала возбудимых клеток в отсутствие возбуждения. В возбудимых клетках другими возможными состояниями являются градиентные мембранные потенциалы (переменной амплитуды) и потенциалы действия, которые являются большими, полное или нулевое возрастание мембранного потенциала, которое обычно следует за фиксированным течением времени. Возбудимые клетки включают нейроны, мышечные клетки и некоторые секреторные клетки в железы. Однако даже в других типах клеток напряжение на мембране может изменяться в ответ на внешние или внутриклеточные стимулы. Например, деполяризация плазматической мембраны, по-видимому, является важным шагом в запрограммированная гибель клеток.[29]
Взаимодействия, которые создают потенциал покоя, моделируются Уравнение гольдмана.[30] По форме это похоже на уравнение Нернста, показанное выше, в том смысле, что оно основано на зарядах рассматриваемых ионов, а также на разнице между их внутренней и внешней концентрацией. Однако при этом также учитывается относительная проницаемость плазматической мембраны для каждого рассматриваемого иона.
Три иона, которые появляются в этом уравнении, - это калий (K+), натрий (Na+) и хлорид (Cl−). Кальций не включен, но может быть добавлен в ситуациях, в которых он играет важную роль.[31] Будучи анионом, хлоридные термины трактуются иначе, чем катионные термины; внутриклеточная концентрация указана в числителе, а внеклеточная концентрация - в знаменателе, который является обратным по отношению к терминам катионов. пя обозначает относительную проницаемость иона типа i.
По сути, формула Гольдмана выражает мембранный потенциал как средневзвешенное значение реверсивных потенциалов для отдельных типов ионов, взвешенных по проницаемости. (Хотя мембранный потенциал изменяется примерно на 100 мВ во время действия потенциала действия, концентрации ионов внутри и снаружи клетки существенно не меняются. Они остаются близкими к их соответствующим концентрациям, когда мембрана находится в состоянии покоя.) В большинстве клеток животных проницаемость для калия намного выше в состоянии покоя, чем проницаемость для натрия. Как следствие, потенциал покоя обычно близок к потенциалу обращения калия.[32][33] Проницаемость для хлоридов может быть достаточно высокой, чтобы быть значительной, но, в отличие от других ионов, хлорид не перекачивается активно и, следовательно, уравновешивается при обратном потенциале, очень близком к потенциалу покоя, определяемому другими ионами.
Значения мембранного потенциала покоя в большинстве клеток животных обычно варьируются от потенциала обратного калия (обычно около -80 мВ) до около -40 мВ. Потенциал покоя в возбудимых клетках (способных производить потенциалы действия) обычно составляет около -60 мВ - более деполяризованные напряжения могут привести к спонтанной генерации потенциалов действия. Незрелые или недифференцированные клетки демонстрируют сильно изменчивые значения напряжения покоя, обычно значительно более положительные, чем в дифференцированных клетках.[34] В таких клетках значение потенциала покоя коррелирует со степенью дифференцировки: недифференцированные клетки в некоторых случаях могут вообще не показывать трансмембранную разницу напряжений.
Поддержание потенциала покоя может быть метаболически затратным для клетки из-за необходимости активной перекачки ионов для противодействия потерям из-за каналов утечки. Стоимость наиболее высока, когда функция ячейки требует особенно деполяризованного значения мембранного напряжения. Например, потенциал отдыха при дневном свете мясная муха (Каллифора вицина) фоторецепторы может достигать -30 мВ.[35] Этот повышенный мембранный потенциал позволяет клеткам очень быстро реагировать на визуальные сигналы; стоимость состоит в том, что поддержание потенциала покоя может потреблять более 20% от общего количества сотовых АТФ.[36]
С другой стороны, высокий потенциал покоя недифференцированных клеток может быть метаболическим преимуществом. Этот очевидный парадокс разрешается путем исследования происхождения этого потенциала покоя. Мало-дифференцированные клетки характеризуются чрезвычайно высоким входным сопротивлением,[34] что означает, что на этом этапе жизни клетки присутствует мало каналов утечки. Как очевидный результат, проницаемость для калия становится аналогичной проницаемости для ионов натрия, что помещает потенциал покоя между потенциалами реверсирования для натрия и калия, как обсуждалось выше. Сниженные токи утечки также означают, что нет необходимости в активной перекачке, чтобы компенсировать, поэтому низкие метаболические затраты.
Градуированные потенциалы
Как объяснялось выше, потенциал в любой точке клеточной мембраны определяется разницей концентрации ионов между внутриклеточными и внеклеточными областями, а также проницаемостью мембраны для каждого типа ионов. Концентрации ионов обычно не меняются очень быстро (за исключением Ca2+, где базовая внутриклеточная концентрация настолько низка, что даже небольшой приток может увеличить ее на порядки), но проницаемость ионов может измениться за доли миллисекунды в результате активации лиганд-зависимых ионных каналов. Изменение мембранного потенциала может быть большим или маленьким, в зависимости от того, сколько ионных каналов активировано и какого они типа, и может быть длинным или коротким, в зависимости от продолжительности времени, в течение которого каналы остаются открытыми. Изменения этого типа называются градуированные потенциалы, в отличие от потенциалов действия, которые имеют фиксированную амплитуду и время действия.
Как можно вывести из Уравнение гольдмана Как показано выше, эффект увеличения проницаемости мембраны для определенного типа иона смещает мембранный потенциал в сторону обратного потенциала для этого иона. Таким образом, открывая Na+ каналов сдвигает мембранный потенциал в сторону Na+ обратный потенциал, который обычно составляет около +100 мВ. Аналогичным образом, открывая K+ каналов сдвигает мембранный потенциал примерно к –90 мВ и открывает Cl− каналов смещает его примерно в сторону –70 мВ (потенциал покоя большинства мембран). Таким образом, Na+ каналы сдвигают мембранный потенциал в положительную сторону, К+ каналы сдвигают его в отрицательном направлении (кроме случаев, когда мембрана гиперполяризована до значения более отрицательного, чем K+ обратный потенциал), а Cl− каналы имеют тенденцию сдвигать его в сторону потенциала покоя.
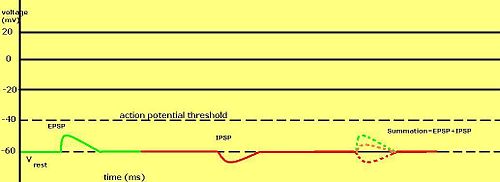
Градуированные мембранные потенциалы особенно важны в нейроны, где они производятся синапсы - временное изменение мембранного потенциала, вызванное активацией синапса единичным градуированным потенциалом действия, называется постсинаптический потенциал. Нейротрансмиттеры что действовать, чтобы открыть Na+ каналы обычно вызывают более положительный мембранный потенциал, в то время как нейротрансмиттеры, активирующие K+ каналы обычно делают его более негативным; те, которые блокируют эти каналы, имеют противоположный эффект.
Считается ли постсинаптический потенциал возбуждающим или тормозящим, зависит от обратного потенциала для ионов этого тока и порога, с которого клетка запускает потенциал действия (около –50 мВ). Постсинаптический ток с реверсивным потенциалом выше порога, такой как типичный Na+ ток, считается возбуждающим. Ток с обратным потенциалом ниже порога, например, типичный K+ ток, считается тормозящим. Ток с реверсивным потенциалом выше потенциала покоя, но ниже порога сам по себе не будет вызывать потенциалы действия, но будет производить подпороговые колебания мембранного потенциала. Таким образом, нейротрансмиттеры, открывающие Na+ каналы производят возбуждающие постсинаптические потенциалы, или ВПСП, тогда как нейротрансмиттеры, которые открывают K+ или Cl− каналы обычно производят тормозящие постсинаптические потенциалы, или IPSP. Когда несколько типов каналов открыты в один и тот же период времени, их постсинаптические потенциалы суммируются (складываются).
Прочие ценности
С точки зрения биофизики отдыхающий мембранный потенциал - это просто мембранный потенциал, который является результатом проницаемости мембраны, которая преобладает, когда клетка находится в состоянии покоя. Вышеупомянутое уравнение средневзвешенных значений всегда применимо, но следующий подход может быть более легко визуализирован: в любой данный момент для иона существует два фактора, которые определяют, какое влияние этот ион будет иметь на мембранный потенциал клетки:
- Движущая сила этого иона
- Проницаемость этого иона
Если движущая сила высока, то ион «проталкивается» через мембрану. Если проницаемость высока, иону будет легче диффундировать через мембрану.
- Движущая сила это чистая электрическая сила, доступная для перемещения этого иона через мембрану. Он рассчитывается как разница между напряжением, при котором ион «хочет» находиться (его равновесный потенциал), и фактическим мембранным потенциалом (Eм). Итак, формально движущая сила для иона = Eм - Eион
- Например, при нашем ранее рассчитанном потенциале покоя -73 мВ движущая сила на калий составляет 7 мВ: (-73 мВ) - (-80 мВ) = 7 мВ. Движущая сила натрия будет (-73 мВ) - (60 мВ) = -133 мВ.
- Проницаемость это мера того, насколько легко ион может пересечь мембрану. Обычно он измеряется как (электрическая) проводимость и единица измерения, Сименс, соответствует 1 Кл · с−1· V−1, это один кулон в секунду на вольт потенциала.
Итак, в покоящейся мембране, хотя движущая сила для калия мала, ее проницаемость очень высока. Натрий имеет огромную движущую силу, но почти не проницаемость в состоянии покоя. В этом случае калий проводит ток примерно в 20 раз больше, чем натрий, и, таким образом, имеет в 20 раз большее влияние на Eм чем натрий.
Однако рассмотрим другой случай - пик потенциала действия. Здесь проницаемость для Na высокая, а проницаемость для K относительно низкая. Таким образом, мембрана приближается к ENa и далеко от EK.
Чем больше ионов проницаемо, тем сложнее предсказать мембранный потенциал. Однако это можно сделать с помощью Уравнение Гольдмана-Ходжкина-Каца или уравнение взвешенных средних. Подставляя градиенты концентрации и проницаемости ионов в любой момент времени, можно определить мембранный потенциал в этот момент. Уравнения GHK означают, что в любой момент значение мембранного потенциала будет средневзвешенным значением равновесных потенциалов всех проникающих ионов. «Вес» - это относительная проницаемость ионов через мембрану.
Эффекты и последствия
В то время как клетки расходуют энергию для транспортировки ионов и создания трансмембранного потенциала, они, в свою очередь, используют этот потенциал для транспортировки других ионов и метаболитов, таких как сахар. Трансмембранный потенциал митохондрии стимулирует производство АТФ, которая является общей валютой биологической энергии.
Клетки могут использовать энергию, которую они хранят в потенциале покоя, для управления потенциалами действия или другими формами возбуждения. Эти изменения мембранного потенциала позволяют общаться с другими клетками (как с потенциалами действия) или инициировать изменения внутри клетки, что происходит в яйцо когда он является удобренный по сперма.
В нейрональных клетках потенциал действия начинается с выброса ионов натрия в клетку через натриевые каналы, что приводит к деполяризации, в то время как восстановление включает выброс калия наружу через калиевые каналы. Оба эти потока происходят пассивная диффузия.
Смотрите также
- Биоэлектрохимия
- Электрохимический потенциал
- Уравнение гольдмана
- Мембранная биофизика
- Матрица микроэлектродов
- Соляная проводимость
- Поверхностный потенциал
- Эффект Гиббса – Доннана
- Синаптический потенциал
Примечания
- ^ Обратите внимание, что признаки ENa и EK противоположны. Это связано с тем, что градиент концентрации калия направлен из ячейки, а градиент концентрации натрия направлен внутрь ячейки. Мембранные потенциалы определяются относительно внешней части клетки; таким образом, потенциал -70 мВ означает, что внутренняя часть ячейки отрицательна по сравнению с внешней.
Рекомендации
- ^ Брюс, Альбертс (18 ноября 2014 г.). Молекулярная биология клетки (Шестое изд.). Нью-Йорк, штат Нью-Йорк. ISBN 9780815344322. OCLC 887605755.
- ^ Кэмпбелл Биология, 6-е издание
- ^ Джонстон и Ву, стр. 9.
- ^ а б Bullock, Orkand, and Grinnell, стр. 140–41.
- ^ Bullock, Orkand, and Grinnell, стр. 153–54.
- ^ Маммерт Х., Градманн Д. (1991). «Потенциалы действия в Acetabularia: измерение и моделирование потоков, управляемых напряжением». Журнал мембранной биологии. 124 (3): 265–73. Дои:10.1007 / BF01994359. PMID 1664861. S2CID 22063907.
- ^ Шмидт-Нильсен, п. 483.
- ^ Либ WR, Штейн WD (1986). «Глава 2. Простая диффузия через мембранный барьер». Транспорт и диффузия через клеточные мембраны. Сан-Диего: Academic Press. С. 69–112. ISBN 978-0-12-664661-0.
- ^ а б Ходжкин А.Л., Кейнс Р.Д. (1955). "Активный транспорт катионов в гигантских аксонах от Сепия и Лолиго". J. Physiol. 128 (1): 28–60. Дои:10.1113 / jphysiol.1955.sp005290. ЧВК 1365754. PMID 14368574.
- ^ Caldwell PC, Ходжкин А.Л., Кейнс Р.Д., Шоу Т.И. (1960). "Влияние инъекции богатых энергией фосфатных соединений на активный транспорт ионов в гигантских аксонах Лолиго". J. Physiol. 152 (3): 561–90. Дои:10.1113 / jphysiol.1960.sp006509. ЧВК 1363339. PMID 13806926.
- ^ Штейнбах HB, Шпигельман S (1943). «Баланс натрия и калия в аксоплазме нервов кальмаров». J. Cell. Комп. Физиол. 22 (2): 187–96. Дои:10.1002 / jcp.1030220209.
- ^ а б Ходжкин А.Л. (1951). «Ионная основа электрической активности нервов и мышц». Биол. Rev. 26 (4): 339–409. Дои:10.1111 / j.1469-185X.1951.tb01204.x. S2CID 86282580.
- ^ CRC Справочник по химии и физике, 83-е издание, ISBN 0-8493-0483-0, стр. 12–14–12–16.
- ^ Эйзенман Г (1961). «Об элементарном атомарном происхождении равновесной ионной специфичности». У Кляйнцеллера; Котык (ред.). Симпозиум по мембранному транспорту и метаболизму. Нью-Йорк: Academic Press. С. 163–79.Эйзенман Г (1965). «Некоторые элементарные факторы, участвующие в специфической ионной проницаемости». Proc. 23-е Междунар. Congr. Physiol. Наук, Токио. Амстердам: Excerta Med. Найденный. С. 489–506.
* Даймонд Дж. М., Райт Э. М. (1969). «Биологические мембраны: физические основы ионной и некектролитной селективности». Ежегодный обзор физиологии. 31: 581–646. Дои:10.1146 / annurev.ph.31.030169.003053. PMID 4885777. - ^ Юнге, стр. 33–37.
- ^ Цай С.К., Ли В., Сести Ф. (2007). «Множественные режимы регулирования тока калия а-типа». Curr. Pharm. Des. 13 (31): 3178–84. Дои:10.2174/138161207782341286. PMID 18045167.
- ^ Гольдин А.Л. (2007). «Нейрональные каналы и рецепторы». В Waxman SG (ред.). Молекулярная неврология. Берлингтон, Массачусетс: Elsevier Academic Press. С. 43–58. ISBN 978-0-12-369509-3.
- ^ Purves и другие., стр. 28–32; Bullock, Orkand, and Grinnell, стр. 133–134; Schmidt-Nielsen, стр. 478–480, 596–597; Юнге, стр. 33–35.
- ^ Sanes, Dan H .; Такач, Екатерина (1 июня 1993 г.). «Активно-зависимое уточнение тормозных связей». Европейский журнал нейробиологии. 5 (6): 570–574. Дои:10.1111 / j.1460-9568.1993.tb00522.x. ISSN 1460-9568. PMID 8261131. S2CID 30714579.
- ^ KOFUJI, P .; НЬЮМАН, Э.А. (2004-01-01). «Буферизация калия в центральной нервной системе». Неврология. 129 (4): 1045–1056. Дои:10.1016 / j.neuroscience.2004.06.008. ISSN 0306-4522. ЧВК 2322935. PMID 15561419.
- ^ Sanes, Dan H .; Рех, Томас А. (01.01.2012). Развитие нервной системы (Третье изд.). Elsevier Academic Press. С. 211–214. ISBN 9780080923208. OCLC 762720374.
- ^ Тости, Элизабетта (28.06.2010). «Динамические роли ионных токов в раннем развитии». Молекулярное воспроизводство и развитие. 77 (10): 856–867. Дои:10.1002 / мрд.21215. ISSN 1040-452X. PMID 20586098. S2CID 38314187.
- ^ Boyet, M.R .; Джуэлл, Б. (1981). «Анализ влияния изменения скорости и ритма на электрическую активность сердца». Прогресс в биофизике и молекулярной биологии. 36 (1): 1–52. Дои:10.1016/0079-6107(81)90003-1. ISSN 0079-6107. PMID 7001542.
- ^ Спинелли, Валентина; Сартиани, Лаура; Муджелли, Алессандро; Романелли, Мария Новелла; Цербай, Элизабетта (2018). «Активированные гиперполяризацией каналы с циклическими нуклеотидами: патофизиологические, онтогенетические и фармакологические сведения об их функции в клеточной возбудимости». Канадский журнал физиологии и фармакологии. 96 (10): 977–984. Дои:10.1139 / cjpp-2018-0115. HDL:1807/90084. ISSN 0008-4212. PMID 29969572.
- ^ Джонс, Брайан Л .; Смит, Стивен М. (30 марта 2016 г.). «Кальций-чувствительный рецептор: ключевая мишень для внеклеточной передачи сигналов кальция в нейронах». Границы физиологии. 7: 116. Дои:10.3389 / fphys.2016.00116. ISSN 1664-042X. ЧВК 4811949. PMID 27065884.
- ^ Дебанн, Доминик; Инглеберт, Янис; Руссье, Микаэль (2019). «Пластичность собственной нейрональной возбудимости» (PDF). Текущее мнение в нейробиологии. 54: 73–82. Дои:10.1016 / j.conb.2018.09.001. PMID 30243042. S2CID 52812190.
- ^ Давенпорт, Беннетт; Ли, Юань; Хайзер, Джастин В .; Шмитц, Карстен; Перро, Анн-Лор (23.07.2015). "Сигнатурные каналы возбудимости, больше нет: каналы L-типа в иммунных клетках". Границы иммунологии. 6: 375. Дои:10.3389 / fimmu.2015.00375. ISSN 1664-3224. ЧВК 4512153. PMID 26257741.
- ^ Сакманн, Берт (21 апреля 2017 г.). «От отдельных клеток и отдельных столбцов к кортикальным сетям: дендритная возбудимость, обнаружение совпадений и синаптическая передача в срезах головного мозга и головном мозге». Экспериментальная физиология. 102 (5): 489–521. Дои:10.1113 / ep085776. ISSN 0958-0670. ЧВК 5435930. PMID 28139019.
- ^ Франко Р., Бортнер С.Д., Сидловски Я.А. (январь 2006 г.). «Возможная роль электрогенного транспорта ионов и деполяризации плазматической мембраны в апоптозе». J. Membr. Биол. 209 (1): 43–58. Дои:10.1007 / s00232-005-0837-5. PMID 16685600. S2CID 849895.
- ^ Purves и другие., стр. 32–33; Bullock, Orkand, and Grinnell, стр. 138–140; Шмидт-Нильсен, стр. 480; Юнге, стр. 35–37
- ^ Спенглер С.Г. (1972). «Расширение уравнения постоянного поля для включения двухвалентных и одновалентных ионов». Алабамский журнал медицинских наук. 9 (2): 218–23. PMID 5045041.
- ^ Purves и другие., п. 34; Bullock, Orkand и Grinnell, стр. 134; Шмидт-Нильсен С. 478–480.
- ^ Purves и другие., стр. 33–36; Bullock, Orkand и Grinnell, стр. 131.
- ^ а б Магнусон Д.С., Морассутти Д.С., Стейнс В.А., Макберни М.В., Маршалл К.С. (14 января 1995 г.). «Электрофизиологическое созревание in vivo нейронов, полученных из линии мультипотентных клеток-предшественников (эмбриональной карциномы)». Развитие мозга. 84 (1): 130–41. Дои:10.1016 / 0165-3806 (94) 00166-В. PMID 7720212.
- ^ Juusola M, Kouvalainen E, Järvilehto M, Weckström M (сентябрь 1994 г.). «Контрастное усиление, отношение сигнал / шум и линейность в адаптированных к свету фоторецепторах мясных мух». J Gen Physiol. 104 (3): 593–621. Дои:10.1085 / jgp.104.3.593. ЧВК 2229225. PMID 7807062.
- ^ Лафлин С.Б., де Руйтер ван Стивенинк Р.Р., Андерсон Дж.С. (май 1998 г.). «Метаболическая стоимость нейронной информации». Nat. Неврологи. 1 (1): 36–41. Дои:10.1038/236. PMID 10195106. S2CID 204995437.
дальнейшее чтение
- Альбертс и др. Молекулярная биология клетки. Издательство Garland; 4-е издание Bk & Cdr (март 2002 г.). ISBN 0-8153-3218-1. Бакалавриат.
- Гайтон, Артур С., Джон Э. Холл. Учебник медицинской физиологии. W.B. Компания Сондерс; 10-е издание (15 августа 2000 г.). ISBN 0-7216-8677-X. Бакалавриат.
- Хилле, Б. Ионный канал возбудимых мембран Sinauer Associates, Сандерленд, Массачусетс, США; 1-е издание, 1984 г. ISBN 0-87893-322-0
- Николлс, Дж. Г., Мартин, А. Р. и Уоллес, Б. От нейрона к мозгу Sinauer Associates, Inc. Сандерленд, Массачусетс, США, 3-е издание, 1992 г. ISBN 0-87893-580-0
- Ове-Стен Кнудсен. Биологические мембраны: теория транспорта, потенциалов и электрических импульсов. Cambridge University Press (26 сентября 2002 г.). ISBN 0-521-81018-3. Выпускной уровень.
- Национальная медицинская серия для независимого исследования. Физиология. Липпинкотт Уильямс и Уилкинс. Филадельфия, Пенсильвания, США, 4-е издание, 2001 г. ISBN 0-683-30603-0

![E_ {eq, K ^ +} = frac {RT} {zF} ln frac {[K ^ +] _ {o}} {[K ^ +] _ {i}},](https://wikimedia.org/api/rest_v1/media/math/render/svg/b7eb1afcc5d7a5032ff24be5c403b43b1307b01e)
![E_ {m} = frac {RT} {F} ln { left ( frac {P _ { mathrm {K}} [ mathrm {K} ^ {+}] _ mathrm {out} + P_ { mathrm {Na}} [ mathrm {Na} ^ {+}] _ mathrm {out} + P _ { mathrm {Cl}} [ mathrm {Cl} ^ {-}] _ mathrm {in}} {P _ { mathrm {K}} [ mathrm {K} ^ {+}] _ mathrm {in} + P _ { mathrm {Na}} [ mathrm {Na} ^ {+}] _ mathrm { in} + P _ { mathrm {Cl}} [ mathrm {Cl} ^ {-}] _ mathrm {out}} right)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4b29151571b6fb807674bf342d01f178908a1a98)