Саркоцистис - Sarcocystis
| Саркоцистис | |
|---|---|
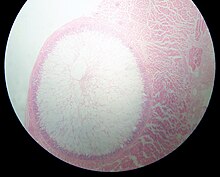 | |
| Саркоцистис киста в овца пищевод. Киста примерно 4 мм в поперечнике. | |
| Научная классификация | |
| Clade: | SAR |
| Infrakingdom: | Альвеолаты |
| Тип: | Apicomplexa |
| Учебный класс: | Conoidasida |
| Заказ: | Eucoccidiorida |
| Семья: | Sarcocystidae |
| Род: | Саркоцистис Ланкестер, 1882 г. |
| Разновидность | |
Видеть Разновидность раздел. | |
Саркоцистис это род из паразиты, большинство видов заражают млекопитающие, и некоторые заразные рептилии и птицы.
Жизненный цикл типичного представителя этого рода включает два вида хозяев: окончательный хозяин и промежуточный хозяин. Часто окончательный хозяин - хищник, а промежуточный хозяин - его жертва. Паразит размножается половым путем в кишечнике окончательного хозяина, передается с фекалиями и проглатывается промежуточным хозяином. Там он в конечном итоге попадает в мышечную ткань. Когда промежуточный хозяин съедается окончательным хозяином, цикл завершается. Окончательный хозяин обычно не проявляет никаких симптомов инфекции, в отличие от промежуточного хозяина.
Около 130 признанных разновидность принадлежат к этому роду. Пересмотр таксономии рода продолжается, и все признанные в настоящее время виды могут относиться к гораздо меньшему числу видов, которые могут инфицировать несколько хозяев.
Название Саркоцистис происходит от Греческий: саркс = плоть и Кистис = мочевой пузырь.
История
Организм был впервые обнаружен в мышь Мишера в 1843 году.[1] Его открытия изначально не интерпретировались как связанные с протистом, и в литературе упоминались структуры, которые он описал как «канальцы Мишера». Между прочим, сын Мишера, Иоганн Фридрих Мишер, обнаруженный ДНК. Подобные структуры были обнаружены в свинья мышцы в 1865 году, но они оставались безымянными до 1899 года, когда название Sarcocystis miescheriana был предложен им.
Первоначально, были ли эти организмы грибы или простейшие было неясно. Эта неопределенность была разрешена в 1967 году, когда электронно-микроскопические исследования показали, что они были простейшими, относящимися к Токсоплазма и Эймерия. Жизненный цикл оставался неизвестным до 1970 года, когда брадизоиты из саркоцист в мышцах птиц были инокулированы в культивируемые клетки млекопитающих, и было обнаружено, что они претерпевают развитие в половую стадию и ооцисты. Исследования передачи с Саркоцистис крупного рогатого скота (считавшегося тогда единственным видом, Sarcocystis fusiformis) у собак, кошек и человека выявили три морфологически различных вида, которые были названы С. bovicanis, С. бовифелис, и С. bovihominis. Это и пост-1972 г. Саркоцистис был пересмотрен в течение того же десятилетия.[2]
Жизненный цикл
В гетероксенный (более одного обязательного хоста) жизненный цикл этих апикомплекс паразиты оставалось неясным до 1972 года, когда были признаны отношения «жертва-хищник» между его окончательными и промежуточными хозяевами.[3] Сейчас известны жизненные циклы примерно 60 из этих видов.
В общих чертах гаметогония и спорогония происходят в кишечник окончательного хоста, в то время как оба шизогония, который происходит в различных тканях, и образование саркоцисты (содержащий брадизоиты и метроциты ) происходит главным образом в мышцы промежуточного хоста. В некоторых случаях один вид может выступать как окончательным, так и промежуточным хозяином.
Ооцисты проходят в кал зараженного окончательного хозяина. Ооциста подвергается спорогонии, образуя две спороцисты. Как только это будет завершено, сама ооциста подвергнется лизис, высвобождая спороцисты в окружающую среду. Спороцисты обычно содержат четыре спорозоиты и измерьте 15–19 на 8–10 мкм.
Промежуточные хосты, такие как крупный рогатый скот или свиньи глотают спороцисты. Затем спорозоиты высвобождаются в организме и мигрируют в сосуды, где проходят первые два поколения бесполого размножения. Эти раунды приводят к развитию меронты. Эта стадия длится от 15 до 16 дней после приема спороцист. Мерозоиты выходят из меронтов второго поколения и входят в одноядерные клетки, где они развиваются путем эндодиогенез. Последующие поколения мерозоитов развиваются вниз по течению в направлении кровотока к артериолам, капиллярам, венулам и венам по всему телу, впоследствии развиваясь в последнее бесполое поколение в мышцах.
Мерозоиты, попадая в мышечные клетки, округляются с образованием метроциты и инициировать саркоциста формирование. Саркоцисты начинаются как одноклеточные тельца, содержащие один метроцит, и в результате бесполого размножения накапливаются многочисленные метроциты, и саркоциста увеличивается в размерах. По мере созревания саркоцисты из небольших округлых неинфекционных метроцитов образуются тела в форме полумесяца, называемые брадизоиты (также известные как «брадизойские мерозоиты»[4]), которые заразны для окончательного хозяина. Время, необходимое для созревания, зависит от вида и может занять 2 месяца и более.
У видов, у которых развиваются симптомы, они обычно возникают через 20-40 дней после проглатывания спороцист и во время последующей миграции спорозоитов по сосудам тела. В пораженных тканях развиваются острые поражения (отеки, кровоизлияния и некрозы). Паразит имеет пристрастие к скелетным мышцам (миозит), сердечной мышце (петехиальные кровоизлияния в сердечную мышцу и серозные оболочки) и лимфатическим узлам (отек, некроз и кровотечение). Эти поражения связаны с созреванием меронтов второго поколения в эндотелиальных и субэндотелиальных клетках. Иногда наблюдается мононуклеарная инфильтрация или гиперемия в собственной пластинке тонкой кишки. После острой фазы кисты могут обнаруживаться в различных мышечных тканях, как правило, без патологии.
После того, как промежуточный хозяин съеден окончательным хозяином, таким как собака или человек, паразит подвергается половому размножению в кишечнике, чтобы создать макрогамты и микрогамонты. Большинство окончательных хозяев не проявляют никаких клинических признаков или симптомов. Слияние макрогамонта и микрогамонта создает зигота, которая перерастает в ооцисту. Ооциста проходит через фекалии, завершая жизненный цикл.
Совсем недавно был описан второй жизненный цикл, посредством которого плотоядные животные и всеядные проходят инфекционные стадии с фекалиями. Проглатывание этого материала может привести к успешному заражению проглотившего животного.
Птицы
Хотя саркоцисты были впервые обнаружены в мышцах птиц Куном в 1865 году, первый жизненный цикл с участием птицы (Gallus gallus ) и плотоядное животное (Собаки фамильярные ) не был описан до 1977 года Munday et al.[5] В 1986 году был проведен первый жизненный цикл с участием птиц как определяющих (ястреб-тетеревятник - Accipiter gentilis ) и среднего (атлантическая канарейка - Серин канария ) Хосты были описаны Церном и Квасновском.[6]
Таксономия
Таксономия этого рода и его связь с другими родами простейших в настоящее время изучаются.
Родственные роды включают: Беснойя, Кариоспора, Цистоизоспора, Френкелия, Изоспора, Hammondia, Гиалоклоссия, Ланкестерелла, Neospora, и Токсоплазма.
Саркоцистис - самый крупный род в семействе Sarcocystidae, состоящий из видов, заражающих целый ряд животных, включая млекопитающих, птиц и рептилий. ФренкелияДругой род этого семейства состоит из паразитов, которые используют грызунов в качестве промежуточных хозяев, а хищных птиц - в качестве окончательных хозяев.
Беснойя, Hammondia, Neospora, и Токсоплазма видимо образуют единый клады. Внутри этой клады Токсоплазма и Neospora кажутся сестры-клады. Изоспора также, кажется, принадлежит к этому кладу, и эта клада является сестрой Саркоцистис. Френкелия кажется очень тесно связанным с Саркоцистис.
Несколько молекулярных исследований показали, что Френкелия на самом деле разновидность Саркоцистис. Этот род отличался от Саркоцистис на основе его склонности к проникновению в мозг а не внутри мышцы. Это различие может быть недействительным с таксономической точки зрения.
Внутри рода идентифицировано несколько клад. К ним относятся тот, который содержит С. дисперса, С. Lacertae, Слизистая оболочка, S. muris, С. нейрона, и S. rodentifelis.[7] Френкелия также группы с этой кладой.
Разновидность
- Sarcocystis accipitris
- Sarcocystis alces
- Sarcocystis alceslatrans
- Sarcocystis ameivamastigodryasi
- Sarcocystis americana
- Sarcocystis arieticanis
- Sarcocystis asinus
- Sarcocystis atheridis
- Sarcocystis aucheniae
- Sarcocystis bertrami
- Sarcocystis bigemina
- Sarcocystis booliati
- Sarcocystis bovicanis
- Sarcocystis bovifelis
- Sarcocystis bovihominis
- Sarcocystis buffalonis
- Sarcocystis calchasi
- Sarcocystis cameli
- Sarcocystis camelopardalis
- Sarcocystis campestris
- Sarcocystis chamaleonis
- Sarcocystis cernae
- Sarcocystis cervi
- Sarcocystis cervicanis
- Sarcocystis canis
- Sarcocystis capracanis
- Sarcocystis cornixi
- Sarcocystis crotali
- Sarcocystis cruzi
- Sarcocystis cuniculi
- Sarcocystis cymruensis
- Sarcocystis danzani
- Sarcocystis dasypi
- Sarcocystis debonei
- Sarcocystis diminuta
- Sarcocystis dirumpens
- Саркоцистис дисперса
- Sarcocystis dubeyella
- Sarcocystis dubeyi
- Sarcocystis equicanis
- Sarcocystis falcatula
- Sarcocystis fayeri
- Sarcocystis felis
- Sarcocystis fulicae
- Sarcocystis fusiformis
- Sarcocystis gallotiae
- Sarcocystis garnhami
- Sarcocystis gracilis
- Sarcocystis grueneri
- Sarcocystis halieti
- Sarcocystis hoarensis
- Sarcocystis fusiformis
- Sarcocystis gallotiae
- Sarcocystis gerbilliechis
- Sarcocystis gigantea
- Sarcocystis giraffae
- Sarcocystis gongyli
- Sarcocystis gracilis
- Sarcocystis greineri
- Sarcocystis grueneri
- Sarcocystis hardangeri
- Sarcocystis hemioni
- Sarcocystis hemionilatrantis
- Sarcocystis hericanis
- Sarcocystis hircicanis
- Sarcocystis hirsuta
- Sarcocystis hjorti
- Sarcocystis hofmanni
- Sarcocystis hominis
- Sarcocystis horvathi
- Sarcocystis iberica
- Sarcocystis idahoensis
- Sarcocystis inghami
- Sarcocystis jamaicensis
- Sarcocystis jorrini
- Sarcocystis kinosterni
- Sarcocystis kirkpatricki
- Sarcocystis kirmsei [8]
- Sarcocystis klaseriensis
- Sarcocystis kortei
- Sarcocystis lacertae
- Sarcocystis lamacanis
- Sarcocystis leporum
- Sarcocystis levinei
- Sarcocystis lindemanni
- Sarcocystis lindsayi
- Sarcocystis linearis
- Sarcocystis medusiformis
- Sarcocystis melis
- Sarcocystis mephitisi
- Sarcocystis miescheriana
- Sarcocystis mihoensis
- Sarcocystis mitrani
- Sarcocystis mongolica
- Sarcocystis montanaensis
- Sarcocystis morae
- Слизистая оболочка саркоцистоза
- Sarcocystis moulei
- Sarcocystis murinotechis
- Sarcocystis muris
- Sarcocystis muriviperae
- Sarcocystis neotomafelis
- Sarcocystis nesbitti
- Sarcocystis neuroona
- Sarcocystis odoi
- Sarcocystis odocoileocanis
- Sarcocystis ovicanis
- Sarcocystis ovifelis
- Sarcocystis oviformis
- Sarcocystis ovalis
- Sarcocystis phacochoeri
- Sarcocystis phoeniconaii
- Sarcocystis podarcicolubris
- Sarcocystis poephagi
- Sarcocystis poephagicanis
- Sarcocystis porcifelis
- Sarcocystis porcihominis
- Sarcocystis rangi
- Sarcocystis rangiferi
- Sarcocystis rauschorum
- Sarcocystis rileyi
- Sarcocystis rodentifelis
- Sarcocystis roudabushi
- Sarcocystis scandinavica
- Sarcocystis sebeki
- Sarcocystis sibirica
- Sarcocystis sigmodontis
- Sarcocystis silva
- Саркоцистис сингапурский
- Sarcocystis speeri
- Sarcocystis stehlinii
- Sarcocystis stenodactylicolubris
- Sarcocystis strixi
- Sarcocystis suicanis
- Sarcocystis suihominis
- Sarcocystis sulawesiensis
- Sarcocystis sybillensis
- Sarcocystis tarandi
- Sarcocystis tarandivulpes
- Sarcocystis tenella
- Sarcocystis tilopodi
- Sarcocystis turcicii
- Sarcocystis turdi
- Sarcocystis ursusi
- Sarcocystis venatoria
- Sarcocystis villivilliso
- Sarcocystis wapiti
- Sarcocystis zamani
Эволюция
Эти простейшие в основном встречаются у млекопитающих. Похоже, что они не заражают млекопитающих надотряда. Афротерия и заразить только два вида Ксенартра. Из-за этой закономерности род, возможно, произошел в Северном полушарии от ранее существовавших видов простейших, инфицировавших млекопитающих. сумчатые также инфицированы этим родом, сумчатые могли быть первоначальными хозяевами этого рода, а паразиты были распространились в Северное полушарие птицами. Третья возможность заключается в том, что этот род первоначально инфицировал птиц и распространился через этих хозяев по всему миру. Последняя возможность из-за существования жизненных циклов, в которых и промежуточными, и конечными хозяевами являются рептилии, род, возможно, произошел от рептилий и распространился оттуда на другие роды. Решение этого вопроса требует результатов дальнейших молекулярных исследований.
Клинический: Человек
Заражение этим паразитом известно как саркоспоридиоз. Из-за первоначальной путаницы в систематике этого паразита он первоначально назывался Isospora hominis. Более старая литература может относиться к этому организму.
Эпидемиология
Инфекция человека считается редкой, и было опубликовано менее 100 случаев инвазивного заболевания (к 1990 г. было зарегистрировано около 46 случаев). Эти цифры сильно недооценивают бремя болезней, которое несет человечество.
На сегодняшний день зарегистрированы крайние возрастные категории: 26-дневный младенец и 75-летний мужчина. Сообщалось об инфекциях из Африка, Европа (Германия, Испания и Польша ), Соединенные Штаты (Калифорния ), Центральная и Южная Америка, Китай, Индия, Тибет, Малайзия, и Юго-Восточная Азия.
Исследования стула у тайских рабочих показали, что саркоцистная инфекция имеет распространенность около 23%. Практически все случаи оказались бессимптомными, что, вероятно, объясняет отсутствие распознавания. Получено исследование 100 человеческих языков вскрытие в Малая выявили уровень заражения 21%. Разницы по полу обнаружено не было, возрастной диапазон составлял от 16 до 57 лет (иметь в виду 37,7 года).[9]
В 2012 году в Малайзии была зарегистрирована вспышка заболевания, затронувшая 93 человека.[10] Sarcocystis nesbitti подтвердилось в нескольких случаях.
История
Первое сообщение о заражении человека было сделано Линдеманном в 1868 году. Хотя впоследствии было опубликовано несколько дополнительных отчетов, эти ранние описания не считались окончательными. Первое общепризнанное окончательное описание этой болезни было опубликовано в 1894 году Барабаном и Сен-Реми.[11] Этот вид был назван Риволтой в честь Линдеманля в 1898 году.
Считалось, что инвазивные формы принадлежат к одному виду, С. Линдеманни, а кишечная форма - к S. hominis (из недоваренной говядины) или S. suihominis (из недоваренной свинины). В описание из С. Линдеманни с тех пор был признан неудовлетворительным и признан nomen nudum (имя без описания). В настоящее время считается, что два вида могут вызывать заражение человека: С. bovihominis (S. hominis) и S. suihominis. Другие виды, включая С. Несбитти иногда сообщалось о заражении людей.[нужна цитата ]
Путь заражения
Заражение происходит при недоварке мясо проглочен. Инкубационный период 9–39 дней. Вспышки среди людей произошли в Европе. Крысы - известный носитель. Загрязненная вода может вызвать инфекцию, но это остается теоретической возможностью.
Патология
Патология бывает двух видов: редкая инвазивная форма с васкулит и миозит и кишечная форма, которая представлена тошнота, боль в животе и понос. Кишечная форма обычно протекает в легкой форме и длится менее 48 часов, но иногда может быть тяжелой или даже опасной для жизни. Инвазивная форма может поражать самые разные ткани, включая лимфатические узлы, мышцы и гортань.
Клинические признаки
В исследованиях на добровольцах с инфицированной говядиной симптомы проявлялись через 3–6 часов после еды. К ним относятся анорексия, тошнота, боль в животе, вздутие живота, диарея, рвота, одышка и тахикардия. Все симптомы были временными и длились около 36 часов. Во второй серии симптомы - боль в животе, вздутие живота, водянистая диарея и эозинофилия - появились через 1 неделю и исчезли через 3 недели.
Клинические случаи были связаны с острой лихорадкой, миалгиями, бронхоспазмом, зудящими высыпаниями, лимфаденопатией, подкожными узелками, связанными с эозинофилией, повышенной скоростью оседания эритроцитов и повышенным уровнем креатининкиназы. Симптомы могут длиться до пяти лет. Сообщалось об одном случае сегментарного некротического энтерита.
Диагностика
Окончательный диагноз биопсия инфицированной мышцы. Саркоцисты идентифицируются с гематоксилин и эозин. Окрашивание PAS может быть полезным, но его поглощение бывает разным. Наряду с саркоцистами могут быть обнаружены воспалительные клетки. Другие находки включают миозит, мионекроз, периваскулярное и интерстициальное воспаление, васкулит и эозинофильный миозит.
Уход
Поскольку инфекция редко бывает симптоматической, лечение требуется редко. Исследования не опубликованы, поэтому лечение остается эмпирическим. Агенты, которые были использованы, включают: альбендазол, метронидазол, и котримоксазол при миозите. Кортикостероиды также использовались для облегчения симптомов.
Ампролиум и салиномицин были эффективны в предотвращении тяжелых заболеваний и смерти экспериментально инфицированных телят и ягнят. Эти агенты до сих пор не испытывались на людях.
Профилактика
Заражение можно предотвратить, приготовив мясо перед едой. В качестве альтернативы, замораживание мяса при -5 ° C в течение нескольких дней перед приемом пищи убивает спороцисты.
Клинический: нечеловеческий

Четыре признанных вида заражают крупный рогатый скот: С. бовифелис, С. bovihominis (S. hominis), S. cruzi (С. bovicanis), и С. хирсута. S. cruzi это единственный вид, который, как известно, является патогенным для крупного рогатого скота. Сообщалось о нескольких клинических синдромах, связанных с этим паразитом: эозинофильный миозит; аборты, мертворождения и смерти беременных коров; два случая некротических энцефалит у телок также не сообщалось. Типичными клиническими признаками острого саркоцистоза крупного рогатого скота являются: анорексия, гипертермия (42 ° C и более), анемия, кахексия, увеличенный пальпируемый лимфатический узел, чрезмерное слюноотделение и выпадение волос на кончике хвоста.[12]
Овцы могут быть инфицированы четырьмя признанными видами Саркоцистис: S. arieticanis и S. tenella (С. ovicanis) являются патогенными; S. gigantea (С. ovifelis) и С. medusiformis непатогены. Заражение этими паразитами распространено в США: более 80% обследованных овец обнаруживают признаки инфекции.[13] С. arieticanis и S. tenella оба вызывают внекишечные заболевания. Анемия, анорексия, атаксия и аборты - главные клинические признаки. Миозит с вялым паралич было зарегистрировано как следствие инфекции. Протозойный миелоэнцефалит овец это признанный синдром, который может возникать во время вспышек. Обычные патологические находки в таких случаях многоочаговые. спинной мозг отек и некроз белого вещества, глиальные узелки и легкие или умеренные негнойные энцефаломиелит. Диагноз может быть установлен по тельцам простейших (12,7–23,0 мкм), которые иммуноцитохимически окрашивают Саркоцистис эпитопы.
Четыре признанных вида заражают свиней: С. medusiformis, S. meischeriana (S. suicanis), S. porcifelis, и S. suihominis. S. porcifelis патогенен для свиней, вызывая диарею, миозит и хромоту.
Пять видов заражают лошадей: S. asinus, С. Бертрами, С. equicanis, С. Файери, и С. нейрона (S. falcatula). Все используют псовых в качестве окончательных хозяев; также сообщалось о трансплацентарной инфекции. С. нейрона причины протозойный миелоэнцефалит лошадей. Воздействие этого паразита, по-видимому, обычное явление в Соединенных Штатах, причем серологические исследования это указывает на то, что 50–60% всех лошадей на Среднем Западе США подвергались этому воздействию. Клинические признаки включают нарушения походки, в том числе атаксию, костяшки пальцев и перекрестный переход. Может возникнуть атрофия мышц, обычно односторонняя. Поражения обычно очаговые. Поражение ствола мозга - обычное явление. Также наблюдаются депрессия, слабость, наклон головы и дисфагия.С. Файери может вызвать миозит у лошадей.
Смертельное заражение альпаки (Лама пакос ) с безымянным видом. Результаты включали диссеминированный эозинофильный миозит, аборт и гемоабдомен. Миозит был связан с кровотечением, некрозом и дегенерацией.[14] Заражение S. tilopodi мышечной ткани в гуанако было сообщено.[15]
S. hemionilatrantis заражает оленей-мулов. Сообщалось о смерти от экспериментальной инокуляции.
Эти паразиты также могут инфицировать птиц, вызывая три различные клинические формы: острое заболевание легких, мышечное заболевание и неврологическое заболевание. Симптомы включают летаргию, одышку, покачивание хвостом, желтоватый помет и внезапную смерть. Наличие кист в мышцах диких птиц известно как «рисовая грудка».
Заболеваемость у животных

Заражение Саркоцистис обычное дело. Показатели у свиней варьируются: 18% в Айова,[16] 27% в Филиппины,[17] 43% в Испании,[18] 57% в Уругвай,[19] и 68% в Индии [20] Уровень инфицирования овец обычно превышает 90%.[18][21][22][23] У верблюдов такой же высокий уровень заражения.[21][23] Уровни выше 80% известны у крупного рогатого скота и коз.[21][22] Заболеваемость буйволами, яками и хайнаг превышает 80%[21][23] в то время как заболеваемость среди лошадей, ослов и кур ниже.[22][23]
Диагностика
Диагноз обычно ставится вскрытие путем обследования скелетных мышц. У некоторых видов кисты могут быть видны невооруженным глазом (утки, мышей, кролики и овца ), но в большинстве случаев требуется микроскопическое исследование.
Ante mortem диагноз может быть поставлен с использованием тестирования кожной чувствительности или тесты фиксации комплемента. Биопсия мышц также является диагностической, но используется гораздо реже.
Микроскопия
Ооцисты с двумя спороцистами или отдельные спороцисты в кале человека являются диагностическим признаком кишечной инфекции. Они впервые появляются через 14-18 дней после употребления в пищу говядины (S. hominis) и через 11-13 дней после употребления в пищу свинины (S. suihominis). Флотация на основе растворов высокой плотности, включающих хлорид натрия, хлорид цезия, сульфат цинка, сахарозу, перколл, фиколл-гипак или другие подобные среды с градиентом плотности, предпочтительнее формалин-этилацетат или другие методы осаждения. Спороцисты S. hominis в среднем 9,3 на 14,7 мкм и S. suihominis в среднем 10,5 на 13,5 мкм. Из-за совпадения размеров сам по себе размер не является надежным диагностическим критерием вида. Подтверждающее окрашивание периодической кислотой Шиффа (PAS) может быть выполнено, поскольку стены окрашиваются положительно. Горячий сафранин + метиленовый синий также использовался для окрашивания.[24] ПЦР усиление рРНК также могут быть использованы.
Стенки клеток
Стенки саркоцисты могут быть полезны в диагностике видов: 24 типа стенок идентифицированы у 62 видов. S. hominis и S. suihominis у обоих стены типа 10. Стена S. hominis имеет толщину до 6 мкм и выглядит радиально исчерченной от выступов ворсинок до 7 мкм длиной. Его брадизоиты имеют длину от 7 до 9 мкм. Стена S. suihominis толщина от 4 до 9 мкм, длина ворсинок достигает 13 мкм. Его брадизоиты имеют длину 15 мкм.
Дифференциальная диагностика
Известно несколько других родов гетероксенных и цистообразующих кокцидий,[25] включая Беснойя, Цистоизоспора, Френкелия, Hammondia, Neospora и Токсоплазма.[26] Связанные, но моноксенный спорообразующие роды включают Изоспора. Отличая эти роды от Саркоцистис в диагностическом материале может быть затруднено без иммунохимических пятен.
Уход
Текущие методы лечения не совсем удовлетворительны. Ампролиум (100 мг / кг, ежедневно в течение 30 дней) при профилактическом кормлении, снижает заболеваемость крупного рогатого скота, зараженного S. cruzi. Профилактическое введение ампролиума или салиномицина также защищало экспериментально инфицированных овец.
У лошадей лечение ограничивалось ингибиторами дигидрофолатредуктазы, такими как сульфаниламиды и пириметамин. Обычно используется сульфадиазин (20 мг / кг перорально) один или два раза в день. Инфицированным лошадям также следует назначать пириметамин в дозе 1,0 мг / кг один раз в день перорально в течение 120 дней или дольше. Диклазурил и толтразурил и другие кокцидиостатики оцениваются для лечения EPM.
Вакцинация
Вакцины в настоящее время неизвестны. У свиней, привитых экспериментально, развивается стойкий иммунитет, поэтому вакцина вполне возможна.
Отношения хозяин-паразит
Жизненный цикл паразита обычно включает хищника и животное-жертву. Один вид может заразить несколько животных-жертв или хищников. По крайней мере, у 56 видов известны окончательные и промежуточные хозяева. Многие виды названы в честь признанных хозяев.
Список известных отношений паразит-хозяин можно найти на странице Sarcocystis: отношения хозяин-паразит.
Геном
С. нейрона является предметом текущего (по состоянию на сентябрь 2011 г.) геномного проекта.
Примечания
Хореоспоридиум теперь считается синонимом Саркоцистис. Исходный типовой вид был Sarcocystis miescheriana. С тех пор его описание было сочтено менее чем удовлетворительным и S. muris был предложен как типовой вид. С. турди не может быть допустимым видом.
Isospora bigemina был реклассифицирован как Sarcocystis bigemina. Isospora hominis был реклассифицирован как Sarcocystis hominis. С. bovihominis является синонимом S. hominis. S. cruzi является синонимом С. bovicanis. S. gigantea является синонимом С. ovifelis. С. хирсута является синонимом С. бовифелис. С. idahoensis и S. roudabushi может быть одного вида. S. miescheriana является синонимом S. suicanis. С. нейрона младший синоним S. falcatula. С. неврома - наиболее часто используемое название этого вида. S. poephagi может быть того же вида, что и С. хирсута. С. poephagicanis может быть того же вида, что и S. cruzi. S. tenella является синонимом С. ovicanis.
Смотрите также
Рекомендации
- ^ Мишер, Ф. (1843). "Ueber eigenthiimliche Schlauche in den Muskeln einer Hausmaus. Ber. U.d". Verhandl. Натурф. Ges. Базель. 5: 198–202.
- ^ Маркус, МБ (1978). «Саркоцистоз и саркоцистоз у домашних животных и человека». Достижения в области ветеринарии и сравнительной медицины. 22: 159–193. PMID 104559.
- ^ Маркус, МБ; Киллик-Кендрик, Р. Гарнем, PCC (1974). «Кокцидиальная природа и жизненный цикл Sarcocystis». Журнал тропической медицины и гигиены. 77 (11): 248–259. PMID 4219030.
- ^ Маркус, МБ (1987). «Термины для кокцидиевых мерозоитов». Анналы тропической медицины и паразитологии. 81 (4): 463. Дои:10.1080/00034983.1987.11812147. PMID 3446034.
- ^ Munday BL, Хамфри JD, Кила V (1977). "Патология, вызванная распространенностью и вероятным жизненным циклом вида Саркоцистис у домашней птицы ». Птичий Дис. 21 (4): 697–703. Дои:10.2307/1589428. JSTOR 1589428. PMID 415727.
- ^ Cerná Ž, Kvašňovská Z (1986). "Жизненный цикл, связанный с отношениями птица-птица у sarcocystis coccidia с описанием Sarcocystis accipitris sp.n " (PDF). Folia Parasitologica. 33 (4): 305–9.
- ^ Эльшейха HM, Lacher DW, Mansfield LS (2005). «Филогенетические отношения Sarcocystis neuroona лошадей и опоссумов к другим цистообразующим кокцидиям, выведенным из последовательностей гена рРНК SSU ». Паразитол. Res. 97 (5): 345–57. Дои:10.1007 / s00436-005-1396-5. PMID 16133298. S2CID 36507563.
- ^ Garnham, P. C. C .; Дагган, А. Дж .; Синден Р. Э. (1979). "Новый вид Саркоцистис в мозгу двух экзотических птиц ». Анналы человеческих и сравнительных паразитологий. 54 (4): 393–400. Дои:10.1051 / паразит / 1979544393. PMID 119465.

- ^ Вонг К.Т., Патманатан Р. (1992). «Высокая распространенность саркоцистоза скелетных мышц человека в Юго-Восточной Азии». Пер. R. Soc. Троп. Med. Hyg. 86 (6): 631–2. Дои:10.1016/0035-9203(92)90161-5. PMID 1287922.
- ^ Абубакар С., Теох Б.Т., Сэм С.С., Чанг Л.Й., Джохари Дж., Хой П.С., Лакбир-Сингх Г.К., Итальяно С.М., Омар С.Ф., Вонг К.Т., Рамли Н., Тан СТ (2013). "Вспышка заражения человека Sarcocystis nesbitti, Малайзия, 2012 г. ". Возникающий зараз. Дис. 19 (12): 1989–91. Дои:10.3201 / eid1912.120530. ЧВК 3840867. PMID 24274071.
- ^ Барабан М. Ле и Сен-Реми М. Г. (1894) Sur un cas de tub psorospermiques observés chez l'homme. Компт. Ренд. Soc. Биол. 46: 231–203
- ^ Маркус, МБ; Ван Дер Лугт, Дж. Дж.; Дубей, JP (2004). Саркоцистоз. Глава 20 в: Инфекционные болезни домашнего скота (ред. Я. Кутцер и Р. К. Тастин), Том 1 (2-е изд.). Издательство Оксфордского университета. С. 360–375. ISBN 978-0195782028.
- ^ Дубей Дж. П., Линдси Д. С., Спир Калифорния, Файер Р., Ливингстон С. В. (1988). "Sarcocystis arieticanis и другие Саркоцистис виды овец в Соединенных Штатах ". J. Parasitol. 74 (6): 1033–8. Дои:10.2307/3282228. JSTOR 3282228. PMID 3142990.
- ^ La Perle KM, Silveria F, Андерсон DE, Blomme EA (1999). «Болезнь Дальмени у альпаки (Лама пакос): саркоцистоз, эозинофильный миозит и прерывание беременности ». J. Comp. Патол. 121 (3): 287–93. Дои:10.1053 / jcpa.1999.0321. PMID 10486166.
- ^ С. Майкл Хоган. 2008 г. Гуанако: лама гуанико, GlobalTwitcher.com, изд. Н. Стрёмберг В архиве 2011-03-04 на Wayback Machine
- ^ Дубей Дж. П., Пауэлл EC (1994). "Распространенность Саркоцистис у свиноматок из Айовы ". Вет. Паразитол. 52 (1–2): 151–5. Дои:10.1016/0304-4017(94)90045-0. PMID 8030181.
- ^ Клаверия Ф.Г., Де Ла Пенья С., Крус-Флорес MJ (2001). "Sarcocystis miescherianm epma инфекция у домашних свиней (Sus scrofa) на Филиппинах". J. Parasitol. 87 (4): 938–9. Дои:10.1645 / 0022-3395 (2001) 087 [0938: СМИИДП] 2.0.CO; 2. PMID 11534668.
- ^ а б Перейра А., Бермеджо М. (1988). "Распространенность Саркоцистис кисты у свиней и овец в Испании ». Вет. Паразитол. 27 (3–4): 353–5. Дои:10.1016/0304-4017(88)90049-0. PMID 3130717.
- ^ Фрейр А., Шиффлет Л., Мендес Дж. (1992). «Саркоспоридиозная инфекция свиней в Уругвае». Вет. Паразитол. 41 (1–2): 167–71. Дои:10.1016 / 0304-4017 (92) 90020-а. PMID 1561758.
- ^ Салеке А., Бхатия ВВ (1991). "Распространенность Саркоцистис у домашних свиней в Индии ». Вет. Паразитол. 40 (1–2): 151–3. Дои:10.1016 / 0304-4017 (91) 90092-а. PMID 1763484.
- ^ а б c d Латиф Б.М., Аль-Делеми Дж. К., Мохаммед Б. С., Аль-Баяти С. М., Аль-Амири А. М. (1999). "Распространенность Саркоцистис виды у мясных животных в Ираке ". Вет. Паразитол. 84 (1–2): 85–90. Дои:10.1016 / s0304-4017 (99) 00046-1. PMID 10435793.
- ^ а б c Вольдемескель М, Гебреаб Ф (1996). «Распространенность саркоцист в домашнем скоте северо-запада Эфиопии». Журнал ветеринарной медицины, серия B. 43 (1): 55–8. Дои:10.1111 / j.1439-0450.1996.tb00287.x. PMID 8919969.
- ^ а б c d Фукуйо М, Батцэцэг Г, Бьямбаа Б (2002). "Распространенность Саркоцистис инфекция у мясных животных в Монголии ». Юго-Восточная Азия J. Trop. Med. Здравоохранение. 33 (3): 490–5. PMID 12693581.
- ^ Маркус, МБ; Буш, Дж. Б. (1987). «Окрашивание кокцидиальных ооцист». Ветеринарная запись. 121 (14): 329. Дои:10.1136 / vr.121.14.329-а. PMID 2447695. S2CID 32442162.
- ^ «Жизненный цикл паразитов кокцидий». Получено 12 мая 2014.
- ^ Грегарины, гемогрегарины, кокцидии, плазмодии и гемопротеиды. 216: Эльзевир. 1977. с. 580. ISBN 978-0323163255.CS1 maint: location (связь)
внешняя ссылка
- Саркоцистис в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Саркоцистис геномный проект
- Рассмотрение: Файер Р. (2004). «Sarcocystis spp. При инфекциях человека». Clin. Microbiol. Rev. 17 (4): 894–902, содержание. Дои:10.1128 / CMR.17.4.894-902.2004. ЧВК 523554. PMID 15489353.
