Перекись натрия - Sodium peroxide
 | |
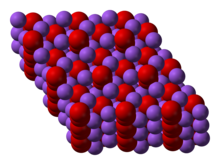 | |
 | |
| Имена | |
|---|---|
| Другие имена Двуокись натрия Flocool Solozone Перекись динатрия | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.828 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1504 |
| |
| |
| Характеристики | |
| Na2О2 | |
| Молярная масса | 77,98 г / моль |
| Внешность | порошок от желтого до белого |
| Плотность | 2,805 г / см3 |
| Температура плавления | 460 ° С (860 ° F, 733 К) (разлагается) |
| Точка кипения | 657 ° С (1215 ° F, 930 К) (разлагается) |
| бурно реагирует | |
| Растворимость | растворим в кислоте не растворим в основании реагирует с этиловый спирт |
| −28.10·10−6 см3/ моль | |
| Структура | |
| шестиугольник | |
| Термохимия | |
Теплоемкость (C) | 89,37 Дж / (моль · К) |
Стандартный моляр энтропия (S | 95 Дж / (моль · К)[1] |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −515 кДж · моль−1[1] |
Свободная энергия Гиббса (Δжграмм˚) | -446,9 кДж / моль |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материалов |
Классификация ЕС (DSD) (устарело) | |
| R-фразы (устарело) | R8, R35 |
| S-фразы (устарело) | (S1 / 2), S8, S27, S39, S45 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Родственные соединения | |
Другой катионы | Перекись лития Перекись калия Перекись рубидия Перекись цезия |
| Оксид натрия Супероксид натрия | |
Родственные соединения | Едкий натр Пероксид водорода |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Перекись натрия это неорганическое соединение с формулой Na2О2. Это желтоватое твердое вещество является продуктом воспламенения натрия в избытке кислорода.[3] Это прочная база. Этот перекись металла существует в нескольких гидраты и пероксигидраты, включая Na2О2· 2H2О2· 4H2На2О2· 2H2На2О2· 2H2О2, а Na2О2· 8H2О.[4] Октагидрат, который легко приготовить, имеет белый цвет в отличие от безводного материала.[5]
Характеристики
Пероксид натрия кристаллизуется с гексагональной симметрией.[6] При нагревании гексагональный форма претерпевает переход в фазу неизвестной симметрии при 512 ° C.[7] При дальнейшем нагревании выше температуры кипения 657 ° C соединение разлагается до Na2O, отпуская O2.[8]
- 2 Na2О2 → 2 Na2О + О2
Подготовка
Октагидрат получают путем обработки гидроксида натрия перекисью водорода.[5]
Пероксид натрия можно получить в больших масштабах реакцией металлического натрия с кислородом при 130–200 ° C, в процессе, который приводит к оксид натрия, который в отдельной стадии поглощает кислород:[7][9]
- 4 Na + O2 → 2 Na2О
- 2 Na2О + О2 → 2 Na2О2
Его также можно получить путем пропускания газообразного озона над твердым йодид натрия внутри платина или же палладий трубка. Озон окисляет натрий с образованием пероксида натрия. В йод можно сублимировать мягким нагреванием. Платина или палладий катализируют реакцию и не подвергаются воздействию пероксида натрия.
Использует
Перекись натрия гидролизует давать едкий натр и пероксид водорода согласно реакции[9]
- Na2О2 + 2 часа2О → 2 NaOH + Н2О2
Перекись натрия использовалась для отбеливания древесной массы при производстве бумаги и текстиля. В настоящее время он в основном используется для специализированных лабораторных операций, например, для добычи полезных ископаемых из различных руд. Перекись натрия может продаваться под торговыми названиями Solozone[7] и Flocool.[8] В химических препаратах в качестве окислителя используется перекись натрия. Он также используется в качестве источника кислорода, реагируя с углекислым газом с образованием кислорода и карбоната натрия:
- 2 Na2О2 + 2 СО2 → 2 Na2CO3 + O2
Таким образом, он особенно полезен для акваланга, подводных лодок и т. Д. Перекись лития имеет аналогичное использование.
Рекомендации
- ^ а б Зумдал, Стивен С. (2009). Химические принципы 6-е изд.. Компания Houghton Mifflin. п. A23. ISBN 978-0-618-94690-7.
- ^ http://www.nmsu.edu/safety/programs/chem_safety/NFPA-ratingS-Z.htm
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1984). Химия элементов. Оксфорд: Pergamon Press. п. 98. ISBN 978-0-08-022057-4.
- ^ Харальд Якоб, Стефан Лейнингер, Томас Леманн, Сильвия Якоби, Свен Гутворт «Пероксосоединения, неорганические» Энциклопедия промышленной химии Ульмана, 2007, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a19_177.pub2.
- ^ а б Р. А. Пеннеман (1950). «Калий-натрий 8-гидрат пероксида». Неорг. Синтезатор. 3: 1–4. Дои:10.1002 / 9780470132340.ch1.CS1 maint: использует параметр авторов (связь)
- ^ Tallman, R. L .; Margrave, J. L .; Бейли, С. В. (1957). «Кристаллическая структура пероксида натрия». Варенье. Chem. Soc. 79 (11): 2979–80. Дои:10.1021 / ja01568a087.
- ^ а б c Макинтайр, Дж. Э., изд. Словарь неорганических соединений, Чепмен и Холл: 1992.
- ^ а б Льюис, Р. Дж. Опасные свойства промышленных материалов Сакса, 10-е изд., John Wiley & Sons, Inc .: 2000.
- ^ а б Э. Дёнгес «Литий и пероксиды натрия» в Справочнике по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 1. п. 979.

