Оксид церия (IV) - Cerium(IV) oxide
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Оксид церия (IV) | |
| Другие имена Оксид церия, Церия, Диоксид церия | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.013.774 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| Исполнительный директор2 | |
| Молярная масса | 172,115 г / моль |
| Внешность | белое или бледно-желтое твердое вещество, немного гигроскопичный |
| Плотность | 7,215 г / см3 |
| Температура плавления | 2400 ° С (4350 ° F, 2670 К) |
| Точка кипения | 3500 ° С (6330 ° F, 3770 К) |
| нерастворимый | |
| +26.0·10−6 см3/ моль | |
| Структура | |
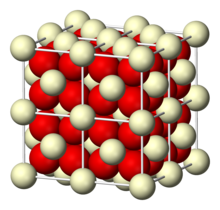
| кубический (флюорит )[1] | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Родственные соединения | Оксид церия (III) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Оксид церия (IV), также известный как оксид церия, диоксид церия, церия, оксид церия или же диоксид церия, является окись из редкоземельный металл церий. Это бледно-желто-белый порошок с химической формулой CeO.2. Это важный коммерческий продукт и промежуточное звено в очистке элемента от руд. Отличительным свойством этого материала является его обратимое превращение в нестехиометрический оксид.[2]
Производство
Церий встречается в природе в виде смеси с другими редкоземельными элементами в основных рудах. бастнезит и монацит. После экстракции ионов металла водным основанием Ce отделяют от этой смеси добавлением окислителя с последующим регулированием pH. На этом этапе используется низкая растворимость CeO.2 и тот факт, что другие редкоземельные элементы сопротивляются окислению.[2]
Оксид церия (IV) образуется прокаливание из оксалат церия или же гидроксид церия.
Церий также образует оксид церия (III), Ce
2О
3, который нестабилен и окисляется до оксида церия (IV).[3]
Структура и дефектное поведение
Оксид церия принимает структура флюорита, пространственная группа Fm3м, # 225, содержащий 8-координатный Ce4+ и 4-координатный O2−. При высоких температурах он выделяет кислород, чтобы нестехиометрическая, анионодефицитная форма сохраняющий решетку флюорита.[4] Этот материал имеет формулу CeO(2−Икс), где 0 < Икс < 0.28.[5] Значение Икс зависит как от температуры, поверхностного окончания, так и от парциального давления кислорода. Уравнение
было показано, что предсказывает равновесную нестехиометрию Икс в широком диапазоне парциальных давлений кислорода (103–10−4 Па) и температуры (1000–1900 ° С).[6]
Нестехиометрическая форма имеет цвет от синего до черного и демонстрирует как ионную, так и электронную проводимость, причем ионная является наиболее значительной при температурах> 500 ° C.[7]
Число кислородных вакансий часто измеряют с помощью Рентгеновская фотоэлектронная спектроскопия сравнить соотношение Ce3+
к Ce4+
.
Дефект химии
В самом стабильном флюорит В фазе церия он обнаруживает несколько дефектов в зависимости от парциального давления кислорода или напряженного состояния материала.[8][9][10][11]
Основными дефектами, вызывающими озабоченность, являются кислородные вакансии и небольшие размеры. поляроны (электроны, локализованные на катионах церия). Увеличение концентрации кислородных дефектов увеличивает скорость диффузии оксидных анионов в решетке, что отражается в увеличении ионная проводимость. Эти факторы обеспечивают благоприятные характеристики оксида церия в качестве твердого электролита в твердооксидные топливные элементы. Нелегированный и легированный диоксид церия также демонстрируют высокую электронную проводимость при низких парциальных давлениях кислорода из-за восстановления иона церия, приводящего к образованию небольших частиц. поляроны. Поскольку атомы кислорода в кристалле церия расположены в плоскостях, диффузия этих анионов легка. Скорость диффузии увеличивается с увеличением концентрации дефектов.
Наличие кислородных вакансий на замыкающих плоскостях церия определяет энергетику взаимодействия церия с молекулами адсорбата и его смачиваемость. Контроль таких поверхностных взаимодействий является ключом к использованию церия в каталитических приложениях.[12]
Естественное явление
Оксид церия (IV) встречается в природе в виде минерала. церианит- (Ce).[13][14] Это редкий пример минерала четырехвалентного церия, другими примерами являются стетиндит- (Ce) и дирнезит- (La). Суффикс «- (Ce)» известен как модификатор Левинсона и используется, чтобы показать, какой элемент доминирует в определенном месте в структуре.[15] Часто встречается в названиях минералов, содержащих редкоземельные элементы (РЗЭ). Появление церианита- (Ce) связано с некоторыми примерами цериевая аномалия, где Ce, который легко окисляется, отделяется от других РЗЭ, которые остаются трехвалентными и, таким образом, соответствуют структурам других минералов, кроме церианита (Ce).[16][13][14]
Катализ и поверхностная активность
Основное появляющееся применение прикладного CeO2 материалы в области катализа. На поверхности церия в его наиболее стабильной флюоритовой фазе преобладают плоскости (111) с более низкой энергией, которые имеют тенденцию проявлять более низкую поверхностную энергию. Церием (IV) чаще всего катализируется реакция сдвиг водяного газа реакция, включающая окисление монооксид углерода. Церий был исследован для катализа различных реакций конверсии углеводородов, включая CO.2 метанирование и каталитическое окисление углеводородов, таких как толуол.[17][18]
Поверхностная функциональность CeO2 во многом проистекает из присущих ему гидрофобность, характерная для оксидов редкоземельных элементов. Гидрофобность имеет тенденцию придавать устойчивость к дезактивации воды на поверхности катализаторов и, таким образом, усиливает адсорбцию органических соединений. Гидрофобность, которую, наоборот, можно рассматривать как органофильность, обычно связана с более высокими каталитическими характеристиками и желательна в приложениях, включающих органические соединения и селективный синтез.[19]
Взаимопревращаемость CeOИкс материалы являются основой использования оксида церия в качестве катализатора окисления. Одно небольшое, но показательное использование - его использование в стенах самоочищающиеся печи в качестве катализатора окисления углеводородов в процессе высокотемпературной очистки. Другой небольшой, но известный пример - его роль в окислении природного газа в газовые мантии.[20]
Основываясь на четком взаимодействии с поверхностью, церий находит дальнейшее применение в качестве сенсора в каталитические преобразователи в автомобильной промышленности, регулирование соотношения воздух-выхлоп для уменьшения НЕТИкс и монооксид углерода выбросы.[21]
Дальнейшие приложения
Полировка
Основное промышленное применение оксида церия - полировка, особенно химико-механическое выравнивание (CMP).[2] Для этой цели он вытеснил многие другие оксиды, которые использовались ранее, такие как оксид железа и цирконий. Для любителей это также известно как «румяна для оптиков».[22][23]
Оптика
Исполнительный директор2 используется для обесцвечивания стекла путем превращения примесей железа с зеленоватым оттенком в почти бесцветные оксиды железа.[2]
Оксид церия нашел применение в инфракрасные фильтры, как окислитель в каталитические преобразователи и как замена диоксид тория в раскаленные мантии[24]
Смешанная проводимость
Из-за значительного ионный и электронный проводимость оксида церия, он хорошо подходит для использования в качестве смешанный дирижер,[25] со значительной ценностью в топливная ячейка исследования и разработки.
Биомедицинские приложения
Наночастицы оксида церия (nanoceria) были исследованы на предмет их антибактериальной и антиоксидантной активности.[26]
Исследование
Эта статья слишком полагается на Рекомендации к основные источники. (Июнь 2020 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
Фотокатализ
Хотя он прозрачен для видимого света, он поглощает ультрафиолетовый радиации сильно, так что это перспективная замена оксид цинка и оксид титана в солнцезащитные кремы, так как он имеет более низкий фотокаталитический Мероприятия.[27] Однако его термокаталитические свойства должны быть уменьшены путем покрытия частиц аморфный кремнезем или же нитрид бора.[нужна цитата ]
Топливные элементы
Церия представляет интерес как материал для твердооксидные топливные элементы (ТОТЭ) из-за относительно высокого содержания кислорода ионная проводимость (т.е. атомы кислорода легко проходят через него) при промежуточных температурах (500-650 ° C) и более низкой энтальпии ассоциации по сравнению с системой диоксида циркония.[28]
Расщепление воды
В оксид церия (IV) – оксид церия (III) цикл или генеральный директор2/ Ce2О3 цикл состоит из двух шагов термохимический расщепление воды процесс на основе оксида церия (IV) и оксид церия (III) за производство водорода.[29]
Антиоксидант
Nanoceria привлекла внимание как биологический антиоксидант.[30][31]
Рекомендации
- ^ Прадёт Патнаик. Справочник неорганических химикатов. Макгроу-Хилл, 2002 г., ISBN 0-07-049439-8
- ^ а б c d Клаус Рейнхардт и Хервиг Винклер (2000). «Церий мишметалл, сплавы церия и соединения церия». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a06_139.CS1 maint: использует параметр авторов (связь).
- ^ «Стандартные термодинамические свойства химических веществ» (PDF). Архивировано из оригинал (PDF) 29 октября 2013 г.
- ^ Исследование поверхностей оксида церия методом DFT Прикладная наука о поверхности 2019 том 478
- ^ Дефекты и дефектные процессы в неметаллических твердых телах Уильям Хейс, A. M. Stoneham Courier Dover Publications, 2004.
- ^ Булфин, Б .; Lowe, A. J .; Keogh, K. A .; Murphy, B.E .; Lübben, O .; Красников, С. А .; Швец, И. В. (2013). «Аналитическая модель CeO2 Окисление и восстановление ». Журнал физической химии C. 117 (46): 24129–24137. Дои:10.1021 / jp406578z. HDL:2262/76279.
- ^ Гилланёва, К .; Галусек, Д. (2011). «Глава 1: Керамические оксиды». В Риделе, Ральф; Чен, Ай-Ви (ред.). Керамика и технологии, материалы и свойства, том 2. Джон Уайли и сыновья. ISBN 978-3-527-31156-9.
- ^ Munnings, C .; Badwal, S.P.S .; Фини, Д. (2014). «Спонтанное стресс-индуцированное окисление ионов Ce в оксиде церия, легированном Gd, при комнатной температуре». Ионика. 20 (8): 1117–1126. Дои:10.1007 / s11581-014-1079-2. S2CID 95469920.
- ^ Badwal, S.P.S .; Даниэль Фини; Фабио Чакки; Кристофер Маннингс; Джастин Кимптон; Джон Дреннан (2013). «Структурная и микроструктурная стабильность электролита церия - гадолиния при воздействии восстанавливающих сред высокотемпературных топливных элементов». J. Mater. Chem. А. 1 (36): 10768–10782. Дои:10.1039 / C3TA11752A.
- ^ Анандкумар, Мариаппан; Бхаттачарья, Шасвата; Дешпанде, Атул Суреш (23.08.2019). «Низкотемпературный синтез и исследование однофазных многокомпонентных золей наночастиц оксида флюорита». RSC Advances. 9 (46): 26825–26830. Дои:10.1039 / C9RA04636D. ISSN 2046-2069.
- ^ Пинто, Фелипе М (2019). «Кислородные дефекты и химия поверхности восстанавливаемых оксидов». Границы в материалах. 6: 260. Bibcode:2019FrMat ... 6..260P. Дои:10.3389 / фматс.2019.00260. S2CID 204754299. Получено 19 октября 2020.
- ^ Фронзи, Марко; Ассади, М. Хусейн Н .; Ханаор, Дориан А.Х. (2019). «Теоретическое понимание гидрофобности поверхностей с низким индексом CeO2». Прикладная наука о поверхности. 478: 68–74. arXiv:1902.02662. Bibcode:2019ApSS..478 ... 68F. Дои:10.1016 / j.apsusc.2019.01.208. S2CID 118895100.
- ^ а б "Церианит- (Ce)". www.mindat.org. Получено 2020-11-12.
- ^ а б «Список минералов». www.ima-mineralogy.org. 2011-03-21. Получено 2020-11-12.
- ^ Берк, Эрнст (2008). «Использование суффиксов в названиях минералов» (PDF). Элементы. 4 (2): 96.
- ^ Пан, Юаньминь; Стауффер, Мел Р. (2000). «Аномалия церия и фракционирование Th / U в палеопочвах Flin Flon 1,85 млрд лет: ключ к изучению сопутствующих минералов, богатых РЗЭ и ураном, и их значение для реконструкции палеоатмосферы». Американский минералог. 85 (7): 898–911.
- ^ Руози Пэн; и др. (2018). «Влияние размера наночастиц Pt на каталитическое окисление толуола над катализаторами Pt / CeO2». Прикладной катализ B: Окружающая среда. 220.
- ^ Монтини, Тициано; Мельчионна, Микеле; Монай, Маттео; Форнасьеро, Паоло (2016). «Основы и каталитические применения CeO2-Основанные материалы ». Химические обзоры. 116 (10): 5987–6041. Дои:10.1021 / acs.chemrev.5b00603. PMID 27120134.CS1 maint: использует параметр авторов (связь)
- ^ Пайер, Иоахим; Пеншке, Кристофер; Зауэр, Иоахим (2013). «Кислородные дефекты и химия поверхности церия: квантово-химические исследования по сравнению с экспериментом». Химические обзоры. 113 (6): 3949–3985. Дои:10.1021 / cr3004949. PMID 23651311.CS1 maint: использует параметр авторов (связь)
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Твигг, Мартин В. (2011). «Каталитический контроль выбросов от автомобилей». Катализ сегодня. 163: 33–41. Дои:10.1016 / j.cattod.2010.12.044.
- ^ Свойства обычных абразивов (Бостонский музей изящных искусств)
- ^ База данных материалов МИД.
- ^ «Диоксид церия». ДаНа. Архивировано из оригинал на 2013-03-02.
- ^ «Смешанные проводники». Институт Макса Планка твердотельных исследований. Получено 16 сентября 2016.
- ^ Rajeshkumar, S .; Наик, Пунам (2018). «Синтез и биомедицинские применения наночастиц оксида церия - обзор». Отчеты по биотехнологии. 17: 1–5. Дои:10.1016 / j.btre.2017.11.008. ISSN 2215-017X. ЧВК 5723353. PMID 29234605.
- ^ Жолобак, Н.М .; Иванов, В.К .; Щербаков, А.Б .; Шапорев, А.С .; Полежаева, О.С .; Баранчиков, А.Е .; Спивак, Н.Я .; Третьяков, Ю.Д. (2011). «УФ-защита, фотокаталитическая активность и фотоцитотоксичность растворов коллоида церия». Журнал фотохимии и фотобиологии B: Биология. 102 (1): 32–38. Дои:10.1016 / j.jphotobiol.2010.09.002. PMID 20926307.
- ^ Арачи, Ю. (июнь 1999 г.). «Электропроводность системы ZrO2 – Ln2O3 (Ln = лантаноиды)». Ионика твердого тела. 121 (1–4): 133–139. Дои:10.1016 / S0167-2738 (98) 00540-2.
- ^ «Производство водорода из циклов солнечного термохимического разделения воды». SolarPACES. Архивировано из оригинал 30 августа 2009 г.
- ^ Каракоти, А. С .; Монтейро-Ривьер, Н. А .; Aggarwal, R .; Davis, J. P .; Narayan, R.J .; Self, W. T .; McGinnis, J .; Сил, С. (2008). «Наноцерия как антиоксидант: синтез и биомедицинские применения». JOM. 60 (3): 33–37. Bibcode:2008JOM .... 60c..33K. Дои:10.1007 / s11837-008-0029-8. ЧВК 2898180. PMID 20617106.CS1 maint: использует параметр авторов (связь)
- ^ Хуссейн С., Аль-Нсур Ф., Райс А.Б., Маршберн Дж., Инлинг Б., Джи З., Зинк Дж. И., Уокер Н.Дж., Гаранциотис С. (2012). «Наночастицы диоксида церия вызывают апоптоз и аутофагию в моноцитах периферической крови человека». САУ Нано. 6 (7): 5820–9. Дои:10.1021 / nn302235u. ЧВК 4582414. PMID 22717232.



