Диссоциация с переносом электрона - Electron-transfer dissociation


Диссоциация с переносом электрона (ETD) является методом фрагментация многозарядный газообразный макромолекулы в масс-спектрометр между этапами тандемная масс-спектрометрия (МС / МС).[1] Похожий на диссоциация с захватом электронов, ETD вызывает фрагментацию больших многозарядных катионы путем передачи электроны им.[2] ETD широко используется с полимерами и биологическими молекулами, такими как белки и пептиды за анализ последовательности.[3] Перенос электрона вызывает пептидный каркас раскол в c- и z-ионы при выходе лабильный пост-трансляционные модификации (ПТМ) цела.[4] Этот метод хорошо работает только для ионов пептида или полимера с более высоким зарядом (z> 2).[2] Однако относительно диссоциация, вызванная столкновением (CID), ETD полезен для фрагментации более длинных пептидов или даже целых белков.[5] Это делает технику важной для нисходящая протеомика. Метод был разработан Охота и коллеги в Университет Вирджинии.[6]
История
Диссоциация с захватом электронов (ECD) была разработана в 1998 году для фрагментации больших белков для масс-спектрометрического анализа.[7] Поскольку для ECD требуется большое количество электронов, близких к тепловым (<0,2 эВ), первоначально он использовался исключительно с Масс-спектрометрия с ионным циклотронным резонансом с преобразованием Фурье (FTICR), самый дорогой вид приборов МС.[8] Менее дорогие варианты, такие как квадрупольное время пролета (Q-TOF), квадрупольная ионная ловушка (QIT) и линейная квадрупольная ионная ловушка (QLT) инструменты использовали более энергоемкие диссоциация, вызванная столкновением метод (CID), приводящий к случайной фрагментации пептидов и белков.[9] В 2004 году Syka et al. объявила о создании ETD, метода диссоциации, подобного ECD, но с использованием недорогого, широко доступного коммерческого спектрометра. Первые эксперименты по ETD были проведены на масс-спектрометре QLT с ионизация электрораспылением (ESI) источник.[10]
Принцип действия
Диссоциация с переносом электрона включает несколько этапов. Обычно белковая смесь сначала разделяется с помощью высокоэффективная жидкостная хроматография (ВЭЖХ). Следующий многократно протонированный молекулы-предшественники генерируются ионизацией электрораспылением и вводятся в масс-спектрометр. (В ETD можно использовать только молекулы с зарядом 2+ или больше.) Для того, чтобы электрон был передан положительным молекулам-предшественникам, генерируются анионы-радикалы и помещаются вместе с ними в ионную ловушку. Во время ионно-ионной реакции электрон передается положительно заряженному белку или пептиду, вызывая фрагментацию по основной цепи пептида. Наконец, полученные фрагменты подвергаются массовому анализу.[11]
Радикальный анионный препарат
В оригинальных экспериментах с ETD антрацен (C14ЧАС10) был использован для генерации реактивных анион-радикалов через отрицательные химическая ионизация.[10] Несколько полициклический ароматический углеводород молекулы были использованы в последующих экспериментах, с флуорантен в настоящее время предпочтительный реагент.[12] Однако флуорантен имеет лишь около 40% эффективности в переносе электронов, поэтому ведется поиск других молекул с низким сродством к электрону.[11]
Инъекция и фрагментация

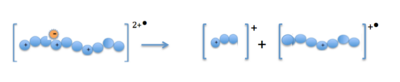
Когда катионы-предшественники (белки или пептиды) и анион-радикалы объединяются в ионной ловушке, электрон передается многозарядному катиону. Это образует нестабильный положительный катион-радикал с одним положительным зарядом меньше и с нечетным электроном.[13] Фрагментация происходит вдоль основной цепи пептида по связи N- Cα, что приводит к образованию ионов фрагментов c- и z-типа.[14]
Массовый анализ
Фрагментация, вызванная ETD, позволяет получить более полную информацию о последовательности белка из спектров ETD, чем из тандемной масс-спектрометрии CID. Поскольку многие ионы c- и z-типа обнаруживаются в основной цепи пептидов, по спектрам фрагментации ETD можно различить почти полное покрытие последовательности многих пептидов.[15] Последовательности из 15-40 аминокислот как на N-конце, так и на C-конце белка могут быть прочитаны с использованием масса к заряду значения для одно- и двухзарядных ионов. Эти последовательности вместе с измеренной массой интактного белка можно сравнить с записями в базе данных для известных белков и выявить посттрансляционные модификации.[16]
Приборы


Диссоциация с переносом электрона происходит в ионная ловушка масс-спектрометр с источником ионизации электрораспылением. В первых экспериментах по ETD в Университете Вирджинии использовалась радиочастотная квадрупольная линейная ионная ловушка (LQT), модифицированная источником химической ионизации (CI) на задней стороне прибора (см. Диаграмму справа).[10] Поскольку спектр может быть получен примерно за 300 миллисекунд, жидкостная хроматография часто сочетается с ETD MS / MS.[11] Недостатком использования LQT является то, что массовая разрешающая способность меньше, чем у других масс-спектрометров.[14]
В последующих исследованиях были опробованы другие инструменты для улучшения массового разрешения. Наличие отрицательного источника ХИ на задней панели прибора мешает работе анализатора высокого разрешения в LQT-Orbitrap и квадрупольном времяпролетном (QTOF), поэтому были введены альтернативные методы ионизации для анион-радикалов.[11]
В 2006 году группа в Университете Пердью во главе с Скотт Маклаки использовали тандемный масс-спектрометр квадруполь / время пролета (QqTOF) с импульсным источником двойной ионизации нано-ESI / химической ионизацией при атмосферном давлении (APCI) с использованием анион-радикалов 1,3-динитробензола в качестве донора электронов.[17] Позже лаборатория Университета Висконсина адаптировала гибридный квадрупольный масс-спектрометр с линейной ионной ловушкой и орбитальной ловушкой для использования ETD. В этом методе также используется метод начальной ионизации анион-радикалов 9-антраценкарбоновой кислоты с помощью импульсных двойных источников ESI.[18]
Поскольку ETD становится все более популярным для анализа структуры белков и пептидов, реализация на легко доступных масс-спектрометрах с ионной ловушкой в сочетании с масс-анализаторами высокого разрешения продолжает развиваться.[19]
Приложения
Протеомика
ETD широко используется при анализе белков и больших пептидов. Важные посттрансляционные модификации, включая фосфорилирование гликозилирование и дисульфидные связи все анализируют с помощью ETD.[20]
Полимерная химия
Хотя анализ полимеров на основе МС в основном проводился с использованием одностадийной МС, тандемная МС также использовалась для характеристики компонентов полимера. CID - наиболее распространенный используемый метод диссоциации, но ETD использовался как дополнительный метод. Уникальные разрывы связи в результате ETD предоставляют ценную диагностическую информацию.[2]
Смотрите также
Рекомендации
- ^ Дасс, Чхабил (2007). Основы современной масс-спектрометрии. Хобокен, Нью-Джерси: John Wiley & Sons. п. 128. ISBN 978-0-470-11848-1.
- ^ а б c Харт-Смит, Джин (15 января 2014 г.). «Обзор тандемной масс-спектрометрии диссоциации с захватом и переносом электронов в химии полимеров». Analytica Chimica Acta. Полимерная масс-спектрометрия. 808: 44–55. Дои:10.1016 / j.aca.2013.09.033. PMID 24370092.
- ^ Бродбелт, Дженнифер С. (11 декабря 2015 г.). «Методы ионной активации пептидов и белков». Аналитическая химия. 88 (1): 30–51. Дои:10.1021 / acs.analchem.5b04563. ЧВК 5553572. PMID 26630359.
- ^ Кун, Джошуа Дж .; Syka, John E.P .; Шабановиц, Джеффри; Хант, Дональд Ф. (апрель 2005 г.). «Тандемная масс-спектрометрия для анализа последовательности пептидов и белков». Биотехнологии. 38 (4): 519, 521, 523. Дои:10.2144 / 05384te01. PMID 15884666. Получено 15 апреля, 2016.
- ^ Хорошо, Дэвид М .; Виртала, Мэтью; McAlister, Graeme C .; Кун, Джошуа Дж. (2007-11-01). «Рабочие характеристики масс-спектрометрии с диссоциацией с переносом электронов». Молекулярная и клеточная протеомика. 6 (11): 1942–1951. Дои:10.1074 / mcp.M700073-MCP200. ISSN 1535-9476. PMID 17673454.
- ^ Патент США 7534622, Дональд Ф. Хант, Джошуа Дж. Кун, Джон Э.П. Syka, Jarrod A. Marto, "Диссоциация с переносом электрона для масс-спектрометрического анализа биополимерных последовательностей", выпущено 19 мая 2009 г.
- ^ Зубарев, Роман А .; Kelleher, Neil L .; Маклафферти, Фред В. (1998-04-01). «Диссоциация с захватом электроном многозарядных белковых катионов. Неэргодический процесс». Журнал Американского химического общества. 120 (13): 3265–3266. Дои:10.1021 / ja973478k. ISSN 0002-7863.
- ^ McLafferty, Fred W .; Хорн, Дэвид М .; Брейкер, Катрин; Ге, Инь; Льюис, Марк А .; Серда, Блас; Зубарев, Роман А .; Карпентер, Барри К. (2001-03-01). «Электронно-захватная диссоциация газообразных многозарядных ионов с помощью ионного циклотронного резонанса с преобразованием Фурье». Журнал Американского общества масс-спектрометрии. 12 (3): 245–249. Дои:10.1016 / S1044-0305 (00) 00223-3. ISSN 1044-0305. PMID 11281599.
- ^ Митчелл Уэллс, Дж .; Маклаки, Скотт А. (01.01.2005). Энзимология, БТ - Методы в (ред.). Индуцированная столкновением диссоциация (CID) пептидов и белков. Методы в энзимологии. Биологическая масс-спектрометрия. 402. С. 148–185. Дои:10.1016 / с0076-6879 (05) 02005-7. ISBN 9780121828073. PMID 16401509.
- ^ а б c Syka JE, Coon JJ, Schroeder MJ, Shabanowitz J, Hunt DF (2004). «Анализ последовательности пептидов и белков с помощью масс-спектрометрии с диссоциацией с переносом электрона». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 101 (26): 9528–33. Bibcode:2004ПНАС..101.9528С. Дои:10.1073 / pnas.0402700101. ЧВК 470779. PMID 15210983.
- ^ а б c d Ким, Мин-Сик; Пандей, Ахилеш (01.02.2012). «Масс-спектрометрия диссоциации с переносом электронов в протеомике». Протеомика. 12 (4–5): 530–542. Дои:10.1002 / pmic.201100517. ISSN 1615-9861. ЧВК 3664229. PMID 22246976.
- ^ Chi, An; Хаттенхауэр, Кертис; Geer, Lewis Y .; Кун, Джошуа Дж .; Syka, John E.P .; Бай, Дина Л .; Шабановиц, Джеффри; Берк, Дэниел Дж .; Троянская, Ольга Григорьевна (13.02.2007). «Анализ сайтов фосфорилирования белков из Saccharomyces cerevisiae с помощью масс-спектрометрии с диссоциацией с переносом электрона (ETD)». Труды Национальной академии наук. 104 (7): 2193–2198. Bibcode:2007PNAS..104.2193C. Дои:10.1073 / pnas.0607084104. ISSN 0027-8424. ЧВК 1892997. PMID 17287358.
- ^ «Диссоциация электронного переноса». Национальная лаборатория сильного магнитного поля. 28 августа 2015 г.. Получено 1 марта, 2016.
- ^ а б Ци, Юйлинь; Фольмер, Дитрих А. (2015-10-01). «Электронные методы фрагментации в масс-спектрометрии: обзор». Обзоры масс-спектрометрии. 36 (1): 4–15. Bibcode:2017MSRv ... 36 .... 4 кв.. Дои:10.1002 / mas.21482. ISSN 1098-2787. PMID 26445267.
- ^ Чжан, Цибинь; Фролов, Андрей; Тан, Нин; Хоффманн, Ральф; ван де Гур, Том; Metz, Thomas O .; Смит, Ричард Д. (15 марта 2007 г.). «Применение масс-спектрометрии диссоциации с переносом электрона в анализах неферментативно гликированных пептидов». Быстрые коммуникации в масс-спектрометрии. 21 (5): 661–666. Bibcode:2007RCMS ... 21..661Z. Дои:10.1002 / rcm.2884. ISSN 1097-0231. ЧВК 2731431. PMID 17279487.
- ^ Chi, An; Бай, Дина Л .; Geer, Lewis Y .; Шабановиц, Джеффри; Хант, Дональд Ф. (01.01.2007). «Анализ интактных белков в хроматографической временной шкале с помощью тандемной масс-спектрометрии диссоциации с переносом электрона». Международный журнал масс-спектрометрии. Проблема чести Дональда Ф. Ханта. 259 (1–3): 197–203. Bibcode:2007IJMSp.259..197C. Дои:10.1016 / j.ijms.2006.09.030. ЧВК 1826913. PMID 17364019.
- ^ Ся, Ю; Chrisman, Paul A .; Эриксон, Дэвид Э .; Лю, Цзянь; Лян, Сяожун; Лондри, Фрэнк А.; Ян, Мин Дж .; Маклакки, Скотт А. (01.06.2006). «Реализация ионно-ионных реакций в квадрупольном / времяпролетном тандемном масс-спектрометре». Аналитическая химия. 78 (12): 4146–4154. Дои:10.1021 / ac0606296. ISSN 0003-2700. ЧВК 2575740. PMID 16771545.
- ^ McAlister, Graeme C .; Фанстиэль, Дуг; Хорошо, Дэвид М .; Берггрен, В. Трэвис; Енот, Джошуа Дж. (2007-05-01). «Реализация диссоциации с переносом электрона на масс-спектрометре с гибридной линейной ионной ловушкой и орбитальной ловушкой». Аналитическая химия. 79 (10): 3525–3534. Дои:10.1021 / ac070020k. ISSN 0003-2700. ЧВК 2662514. PMID 17441688.
- ^ Журов, Константин О .; Форнелли, Лука; Wodrich, Matthew D .; Laskay, Ünige A .; Цыбин Юрий О. (28.05.2013). «Принципы масс-спектрометрии диссоциации с захватом и переносом электронов применительно к анализу структуры пептидов и белков». Обзоры химического общества. 42 (12): 5014–30. Дои:10.1039 / c3cs35477f. ISSN 1460-4744. PMID 23450212.
- ^ Визнер, Юлия; Премслер, Томас; Зикманн, Альберт (2008-11-01). «Применение диссоциации с переносом электрона (ETD) для анализа посттрансляционных модификаций». Протеомика. 8 (21): 4466–4483. Дои:10.1002 / pmic.200800329. ISSN 1615-9861. PMID 18972526.
