Ни- - Nor-
В химическая номенклатура, ни- это префикс назвать структурный аналог это может быть полученный от исходного соединения путем удаления одного атома углерода вместе с соответствующими атомами водорода. Нор-соединение может быть получено удалением CH
3, CH
2, или группу CH, или атом C. Префикс «нор-» также включает исключение метиленовый мостик в циклический исходное соединение, за которым следует сжатие кольца. (Префикс "гомо-"что указывает на следующего более высокого члена в гомологическая серия, обычно ограничивается нециклическими атомами углерода).[1][2][3] Условия десметил- или же деметил- являются синонимами слова «нор-».
«Нор» - это сокращение от нормального. Первоначально этот термин использовался для обозначения полностью деметилированной формы исходного соединения.[4]Позже смысл ограничился удалением одной группы. Также не пишется непосредственно перед названием основы без дефиса между ними, если после или не стоит другой префикс (например, α-). Если несколько групп удаляются, используется префикс dinor, trinor, tetranor и т. Д. Префиксу предшествует номер позиции (местоположение) исчезающих атомов углерода. Например 2,3-динор. Первоначальная нумерация исходного соединения сохраняется. Согласно номенклатуре IUPAC, этот префикс нет написано курсивными буквами[5] и, в отличие от Nor, когда это ди или больше, в конце чисел, разделенных запятыми, используется дефис. Например, 2,3-динор-6-кето-простагландин F1α образуется путем бета-окисления исходного соединения 6-кето-простагландина F1α.[6] Здесь, хотя на самом деле углерод 1 и 2 теряются в результате окисления. Новый углерод 1 теперь стал CCOH, похожим на исходное соединение, выглядя так, как если бы только углерод 2 и 3 были удалены из исходного соединения. «Динор» не обязательно должен быть восстановлением соседних атомов углерода, например 5-Ацетил-4,18-диноретиноевая кислота, где 4 относится к атому углерода кольца и 18 относится к метильной группе на 5-м атоме углерода кольца.[3]
Альтернативное использование «ни» для обозначения неразветвленной формы соединения в ряду изомеров (также называемое «нормальным») устарело и не допускается в названиях IUPAC.
История

Возможно, самое раннее известное использование префикс «ни» - это не слова А. Маттиссена и Г.К. Фостер в 1867 г. в публикации о реакции между сильной кислотой и опиановая кислота (см. картинку).
Опиановая кислота (C10ЧАС10О5) представляет собой соединение с двумя метильными группами, и они назвали его «диметилноропиановая кислота». После реакции с сильной кислотой соединение было получено только с одним метилом (C9ЧАС8О5). Эту частично деметилированную опиановую кислоту они назвали «метилнормальная опиановая кислота». Полностью деметилированное соединение (C8ЧАС6О5) обозначали термином «нормальная опиановая кислота», сокращенно «норопиановая кислота».

Точно так же Маттиссен и Фостер назвали наркотик, который имеет три метокси группы, «триметилнор-наркотин». Единственный деметилированный наркотин назывался «диметилнор-наркотин», более деметилированный наркотин - «метилнор-наркотин», а полностью деметилированная форма «нормальным наркотином» или «нор-наркотином».[7]
"С того времени значение приставки было обобщено, чтобы обозначать замену одной или нескольких метильных групп на H или исчезновение CH2 из углеродной цепи ".[4]
В настоящее время значение ограничено для обозначения удаления только одной группы из исходной структуры, а не полностью деметилированной формы исходного соединения.[1]
В литературе «нор» иногда называют «следующим более низким гомологом», хотя в этом контексте "гомолог" это неточный термин. «Ни» относится только к удалению одного атома углерода с сопутствующим водородом, но не к удалению других единиц. «Nor» сравнивает два родственных соединения; он не описывает отношения к гомологическая серия.
Ложная этимология
Предполагается, что "ни" не является акроним немецкого "N оhne радикал "("азот без радикальный "). Сначала британский фармаколог Джон Х. Гэддум следовал этой теории,[8] но в ответ на отзыв А. Вулман,[9] Гаддум отказался от этой этимологии.[4]Вулман считал, что "N ohne Radikal" был немцем. мнемонический и вероятно backronym, а не реальное значение приставки «ни». Это можно поспорить с фактом "что приставка ни используется для многих соединений, которые вообще не содержат азота".[9]
Устаревшее использование термина
Первоначально «ни» не имело двусмысленного значения, так как термин «нормальный» мог также относиться к неразветвленной форме в ряду изомеров, например, как с алканы, алканолы и некоторые аминокислоты.[10][11][12]
Названия неразветвленных алканов и алканолов, например "нормальный бутан " и "нормальный пропиловый спирт ", которые сейчас устарели,[13] стали префиксом н-однако не «ни».[14]Остальные «нормальные» соединения получили приставку «ни». Старшая банальные имена, подобно норлейцин и норвалин следует отказаться;[11] использование префикса для изомерных соединений не поощрялось еще в 1955 году или ранее.[10]

Примеры
 | 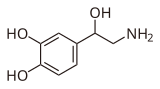 | |
| адреналин | норэпинефрин | |
 | 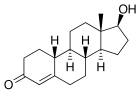 | |
| тестостерон | нортестостерон |
Смотрите также
Рекомендации
- ^ а б ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "ни ". Дои:10.1351 / goldbook.N04210
- ^ Предпочтительные названия IUPAC, предварительная рекомендация сентябрь 2004 г. Глава 1 13.4.4.3 Приставкой "ни", стр.18-19
- ^ а б Совместная комиссия IUPAC-IUB по биохимической номенклатуре (JCBN): Ни ретиноидов Номенклатура ретиноидов, Рекомендации 1981; 4.6.
- ^ а б c Гаддум Дж. Х. (июнь 1956 г.). «Приставка« Нор »в химической номенклатуре». Природа. 177 (1046): 1046. Bibcode:1956Натура.177.1046G. Дои:10.1038 / 1771046b0.
- ^ Предварительная рекомендация IUPAC по именам, сентябрь 2004 г .; Глава 1, 16.5.3 Термины, выделенные курсивом, стр.89-90
- ^ «2,3-динор-6-кето Простагландин F1α (натриевая соль) | Cayman Chemical».
- ^ А. Маттиссен, Г.К. Взращивать: «Исследования химического состава наркотина и продуктов его разложения»; J. Chem. Soc., 358 (1868). Аннотация опубликована в: "Труды Лондонского королевского общества, том 16" С. 39-41. PDF: [1]
- ^ Гаддум Дж. Х. (февраль 1953 г.). «Книжное обозрение: Дополнительная фармакопея». Природа. 171 (350): 350. Bibcode:1956Натура.177..350Г. Дои:10.1038 / 177350a0.(несвободный доступ)
- ^ а б Вулман AM (июнь 1956 г.). «Приставка« Нор »в химической номенклатуре». Природа. 177 (1046): 1046. Bibcode:1956Натура.177.1046W. Дои:10.1038 / 1771046a0.
- ^ а б Система номенклатуры ТЕРПЕНОВЫХ УГЛЕВОДОРОДОВ-Том 14 Американское химическое общество (1955); Приложение D Префикс Nor-; Дои:10.1021 / ba-1955-0014.ch008
- ^ а б Совместная комиссия IUPAC-IUB по биохимической номенклатуре (JCBN): 'Нор' аминокислоты, Номенклатура и символика аминокислот и пептидов; 15.2.3.
- ^ Комиссия IUPAC-IUB по биохимической номенклатуре (JCBN): Сокращенное обозначение производных аминокислот и пептидов - Предварительные правила Журнал биологической химии, Vol. 241, № 11, выпуск от 10 июня 1966 г., с. 2492
- ^ Р. Кобер и У. Бюнцли-Трепп: IUPAC, Систематическая номенклатура документации CIPAC - анализ С. 12-13. Седьмое СОВМЕСТНОЕ совещание CIPAC / ФАО / ВОЗ - Симпозиум (54-е совещание CIPAC и 9-е совещание JMPS); Любляна, 8 июня 2010 г.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "алкильные группы ". Дои:10.1351 / goldbook.A00228
