Пептидилпролилизомераза А - Peptidylprolyl isomerase A
Пептидилпролилизомераза А (PPIA), также известный как циклофилин А (CypA) или ротамаза А является фермент что у людей кодируется PPIA ген на хромосоме 7.[4][5][6] Как член семейства пептидилпролилцис-транс-изомераз (PPIase), этот белок катализирует цис-транс изомеризация имидного пролина пептидные связи, что позволяет ему регулировать многие биологические процессы, в том числе внутриклеточная передача сигналов, транскрипция, воспаление, и апоптоз.[4][7][8][9][10] Благодаря своим различным функциям PPIA участвует в широком спектре воспалительные заболевания, включая атеросклероз и артрит, и вирусные инфекции.[8][9][10]
Структура
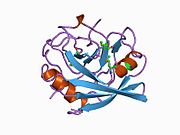
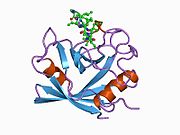
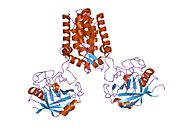
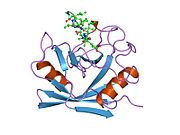
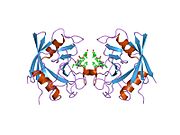
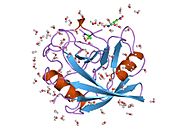
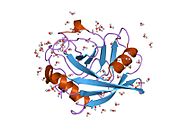
PPIA - это 18 кДа, 165-аминокислота длинный цитозольный белок.[11] Как и другие циклофилины PPIA образует β-цилиндрическую структуру с гидрофобным ядром. Этот β-бочонок состоит из восьми антипараллельных β-нитей и ограничен двумя α-спиралями вверху и внизу.[7][11][12] Кроме того, β-витки и петли в прядях способствуют гибкости ствола.[12] Его активный центр представляет собой гидрофобный карман, который связывает пептиды, содержащие пролин. Циклоспорин может связывать этот карман, чтобы ингибировать ферментативную активность белка.[7]
Функция
Этот ген кодирует член пептидил-пролил цис-транс-изомеразы (PPIase ) семья. PPIases катализируют цис-транс-изомеризацию имидных пептидных связей пролина в олигопептиды и ускорить сворачивание белка.[4][11] Как правило, PPIases встречаются во всех эубактерии и эукариоты, а также в нескольких архебактерии, и, следовательно, очень консервативны.[7][10] Из 18 известных циклофилинов человека PPIA является наиболее экспрессируемым изоферментом.[10] В частности, PPIA преимущественно выражается в ядро и цитоплазма клетки, где он участвует во внутриклеточной передаче сигналов, транспорте белков и регуляции транскрипции.[7][8][9][10][11] В гемопоэтических клетках субклеточная локализация PPIA из ядра в цитоплазму наблюдали во время c-Jun N-терминальная киназа - и сериновая протеаза -зависимое нарушение микротрубочек. Эта локализация коррелирует с задержкой G2 / M, указывая на то, что функция белка PPIase может регулироваться динамикой микротрубочек во время клеточного цикла.[11] PPIA также был связан с митохондрии.[13]
Более того, фермент участвует в воспалительных и апоптотических процессах во внеклеточной среде. В присутствии активные формы кислорода (ROS), гладкомышечные клетки сосудов (VSMC), моноциты / макрофаги и эндотелиальные клетки (ЭК) секретируют PPIA, чтобы вызвать воспалительный ответ и смягчить повреждение тканей.[8][9][11][14] PPIA также может активировать Акт и NF-κB сигнализация, что приводит к усилению регуляции Bcl-2, антиапоптотический белок, и, таким образом, предотвращает апоптоз ЭК в ответ на окислительный стресс.[9] PPIA может также регулировать ERK1 / 2, JNK, p38 киназа, Akt и IκB сигнальные пути через активацию CD147 рецептор.[11] PPIA-опосредованная активация киназных путей ERK, JNK и p38 также способствует ангиогенез.[11] Кроме того, PPIA индуцирует миграцию и пролиферацию клеток в гладких мышцах.[8] В случае Т-клеток PPIA регулирует Т-клеточно-специфическую тирозинкиназу ITK при стимуляции Т-клеточного рецептора.[10]
Клиническое значение
Белок PPIA является важным компонентом апоптоза. Во время нормального эмбриологический процессов или во время повреждения клеток (например, ишемия-реперфузия во время сердечные приступы и удары ) или во время разработки и процессов в рак, апоптотическая клетка претерпевает структурные изменения, включая сжатие клеток, образование пузырей плазматической мембраны, ядерную конденсацию и фрагментацию ДНК и ядро. Далее следует фрагментация на апоптотические тельца, которые быстро удаляются фагоциты, тем самым предотвращая воспалительный отклик.[15] Это способ гибели клеток, определяемый характерными морфологическими, биохимическими и молекулярными изменениями. Сначала он был описан как «усадочный некроз», а затем этот термин был заменен на апоптоз, чтобы подчеркнуть его противоположную роль. митоз в кинетике тканей. На более поздних стадиях апоптоза вся клетка становится фрагментированной, образуя ряд апоптотических телец, связанных с плазматической мембраной, которые содержат ядерные и / или цитоплазматические элементы. Ультраструктурный вид некроз Совершенно иначе, основными признаками которого являются набухание митохондрий, разрушение плазматической мембраны и распад клеток. Апоптоз встречается во многих физиологический и патологический процессы. Он играет важную роль во время эмбриональный развитие как запрограммированная гибель клеток и сопровождает множество нормальных инволюционных процессов, в которых оно служит механизмом для удаления «нежелательных» клеток.
Как провоспалительный цитокин, PPIA активно участвует в острых и хронических воспалительных заболеваниях, включая сепсис, атеросклероз и ревматоидный артрит.[8][9][10] Таким образом, терапевтическое воздействие на PPIA с помощью селективных ингибиторов может оказаться эффективным в борьбе с такими воспалительными заболеваниями и симптомами.[9][10] Корреляция между уровнями PPIA в плазме и симптомами гипергликемии также способствует использованию PPIA в качестве биомаркера диабета и сосудистых заболеваний.[8]
Кроме того, PPIA участвует в мозговой гипоксия -ишемия путем внесения вклада в ядерную транспортировку AIF, проапоптотический фактор в нейронах.[10] Для поддержания целостности гематоэнцефалического барьера и смягчения травм головного мозга PPIA помогает рекрутировать циркулирующие моноциты и стимулирует пути выживания и роста.[8] В сердечных миогенных клетках циклофилины активируются тепловым шоком и гипоксией-реоксигенацией, а также сложный с белки теплового шока. Таким образом, циклофилины могут выполнять функцию кардиозащиты во время ишемии -реперфузионная травма.
В настоящее время экспрессия PPIA сильно коррелирует с патогенезом рака, но конкретные механизмы еще предстоит выяснить.[11][14] Сверхэкспрессия PPIA была связана с гепатоцеллюлярная карцинома, рак легких, аденокарцинома поджелудочной железы, карцинома эндометрия, плоскоклеточный рак пищевода, и меланома.[11][13]
Белок также может взаимодействовать с несколькими ВИЧ белки, включая p55 gag, Vpr и капсид белок, и было показано, что он необходим для образования инфекционного ВИЧ вирионы.[4][16] В результате PPIA способствует возникновению вирусных заболеваний, таких как: СПИД, гепатит С, корь, и грипп А.[10]
Взаимодействия
Было показано, что пептидилпролилизомераза А взаимодействовать с:
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000196262 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c d «Ген Entrez: пептидилпролилизомераза А PPIA (циклофилин А)».
- ^ Haendler B, Hofer E (июль 1990 г.). «Характеристика гена циклофилина человека и родственных процессированных псевдогенов». Европейский журнал биохимии / FEBS. 190 (3): 477–82. Дои:10.1111 / j.1432-1033.1990.tb15598.x. PMID 2197089.
- ^ Хольцман Т.Ф., Иган Д.А., Идалджи Р., Симмер Р.Л., Хелфрих Р., Тейлор А., Беррес Н.С. (февраль 1991 г.). «Предварительная характеристика клонированной нейтральной изоэлектрической формы пептидилпролилизомеразы циклофилина человека». Журнал биологической химии. 266 (4): 2474–9. PMID 1989998.
- ^ а б c d е Казуи Т., Иноуэ Н., Ямада О., Комацу С. (январь 1992 г.). «Избирательная церебральная перфузия при операции по поводу аневризмы дуги аорты: переоценка». Летопись торакальной хирургии. 53 (1): 109–14. Дои:10.1016 / 0003-4975 (92) 90767-х. PMID 1530810.
- ^ а б c d е ж грамм час я Рамачандран С., Венугопал А., Кутти В.Р., А.В., Г.Д., Читрасри В., Муллассари А., Пратапчандран Н.С., Сантош К.Р., Пиллай М.Р., Карта СС (7 февраля 2014 г.). «Уровень циклофилина А в плазме повышен у пациентов с сахарным диабетом 2 типа и предполагает наличие сосудистого заболевания». Сердечно-сосудистая диабетология. 13: 38. Дои:10.1186/1475-2840-13-38. ЧВК 3922405. PMID 24502618.
- ^ а б c d е ж грамм Вэй Ю., Цзиньчуань Ю., Йи Л., Цзюнь В., Чжунцюнь В., Цуйпин В. (июнь 2013 г.). «Антиапоптотическая и проапоптотическая передача сигналов циклофилина А в эндотелиальных клетках». Воспаление. 36 (3): 567–72. Дои:10.1007 / s10753-012-9578-7. PMID 23180369. S2CID 24968009.
- ^ а б c d е ж грамм час я j k л Hoffmann H, Schiene-Fischer C (июль 2014 г.). «Функциональные аспекты внеклеточных циклофилинов». Биологическая химия. 395 (7–8): 721–35. Дои:10.1515 / hsz-2014-0125. PMID 24713575. S2CID 32395688.
- ^ а б c d е ж грамм час я j k Obchoei S, Wongkhan S, Wongkham C, Li M, Yao Q, Chen C (ноябрь 2009 г.). «Циклофилин А: потенциальные функции и терапевтическая мишень для рака человека». Монитор медицинских наук. 15 (11): RA221–32. PMID 19865066.
- ^ а б Ван Т., Юнь Ч., Гу Си, Чанг В. Р., Лян округ Колумбия (август 2005 г.). «1.88 Кристаллическая структура домена C hCyP33: новый домен пептидил-пролил цис-транс-изомеразы». Сообщения о биохимических и биофизических исследованиях. 333 (3): 845–9. Дои:10.1016 / j.bbrc.2005.06.006. PMID 15963461.
- ^ а б Йе Й, Хуанг А, Хуан С, Лю Дж, Ван Б, Лин К., Чен Кью, Цзэн И, Чен Х, Тао Х, Вэй Дж, Ву И (2013). «Сравнительный митохондриальный протеомный анализ гепатоцеллюлярной карциномы больных». Приложение Proteomics Clin Appl. 7 (5–6): 403–15. Дои:10.1002 / prca.201100103. PMID 23589362. S2CID 5906425.
- ^ а б Яо Ц., Ли М., Ян Х, Чай Х, Фишер В., Чен С. (март 2005 г.). «Роль циклофилинов в раке и других системах органов». Всемирный журнал хирургии. 29 (3): 276–80. Дои:10.1007 / s00268-004-7812-7. PMID 15706440. S2CID 11678319.
- ^ Керр Дж. Ф., Уилли А. Х., Карри А. Р. (август 1972 г.). «Апоптоз: основной биологический феномен с широким спектром влияния на кинетику тканей». Британский журнал рака. 26 (4): 239–57. Дои:10.1038 / bjc.1972.33. ЧВК 2008650. PMID 4561027.
- ^ Агарвал, ПК (август 2004 г.). «Цис / транс-изомеризация в капсидном белке ВИЧ-1, катализируемая циклофилином А: выводы из вычислительных и теоретических исследований». Белки. 56 (3): 449–63. Дои:10.1002 / prot.20135. PMID 15229879. S2CID 19907859.
- ^ Бразин К.Н., Маллис Р.Дж., Фултон Д.Б., Андреотти А.Х. (февраль 2002 г.). «Регулирование тирозинкиназы Itk пептидил-пролилизомеразой циклофилин А». Труды Национальной академии наук Соединенных Штатов Америки. 99 (4): 1899–904. Дои:10.1073 / pnas.042529199. ЧВК 122291. PMID 11830645.
дальнейшее чтение
- Franke EK, Luban J (1995). «Циклофилин и gag в репликации и патогенезе ВИЧ-1». Активация клеток и апоптоз при ВИЧ-инфекции. Успехи экспериментальной медицины и биологии. 374. стр.217–28. Дои:10.1007/978-1-4615-1995-9_19. ISBN 978-0-306-45063-1. PMID 7572395.
- Сокольская E, Любань J (август 2006 г.). «Циклофилин, TRIM5 и врожденный иммунитет к ВИЧ-1». Текущее мнение в микробиологии. 9 (4): 404–8. Дои:10.1016 / j.mib.2006.06.011. PMID 16815734.