Фосфид кальция - Calcium phosphide
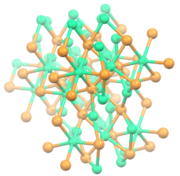 | |
| Имена | |
|---|---|
| Название ИЮПАК Фосфид кальция | |
| Другие имена Фотофор, CP, политанол | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.766 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| Ca3п2 | |
| Молярная масса | 182,18 г / моль |
| Внешность | красно-коричневый кристаллический порошок или серые комки |
| Плотность | 2,51 г / см3 |
| Температура плавления | ~ 1600 ° С |
| разлагается | |
| Опасности | |
| Главный опасности | Источник токсичных фосфин, опасная реакция с водой |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасность |
| H260, H300, H311, H318, H330, H400 | |
| P231 + 232, P233, P280, P301 + 310, P405, P501 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Фосфид кальция (CP) это неорганическое соединение с формулой Ca3п2. Это один из нескольких фосфиды кальция, описываемого как солеподобный материал, состоящий из Ca2+ и P3−. Другие, более экзотические фосфиды кальция имеют формулу CaP, CaP.3, Ca2п2, а Са5п8.
Ca3п2 имеет вид красно-коричневого кристаллического порошка или серых комков. Его торговое название Фотофор для зажигательного использования или Политанол для использования в качестве родентицид.[1]
Подготовка и состав
Он может быть образован реакцией элементов,[2] но чаще его получают карботермическим восстановлением фосфата кальция:[3]
- Ca3(PO4)2 + 8 С → Са3п2 + 8 СО
Структура комнатной температуры формы Ca3п2 не подтверждено рентгеновской кристаллографией. Высокотемпературная фаза характеризуется Утонченность Ритвельда. Ca2+ центры восьмигранные.[2]
Использует
Фосфиды металлов используются в качестве родентицид. Смесь пищи и фосфида кальция оставляют там, где ее могут съесть грызуны. Кислота в пищеварительной системе грызунов реагирует с фосфидом с образованием токсичного газа. фосфин. Этот метод борьбы с паразитами можно использовать в местах, где грызуны невосприимчивы ко многим из них. варфарин -тип (антикоагулянт ) яды появились. Другие пестициды, похожие на фосфид кальция: фосфид цинка и фосфид алюминия.
Фосфид кальция также используется в фейерверк, торпеды самовоспламеняющийся военно-морской пиротехнические ракеты, и различные водоактивируемые боеприпасы. В 1920-е и 1930-е годы Чарльз Кингсфорд Смит использовались отдельные плавучие канистры карбид кальция и фосфид кальция в виде морских факелов продолжительностью до десяти минут. Предполагается, что фосфид кальция, полученный путем кипячения костей в моче в закрытом сосуде, был ингредиентом какого-то древнего Греческий огонь формулы.[4]
Фосфид кальция - обычная примесь в карбид кальция, что может привести к самовозгоранию образовавшегося ацетилена, загрязненного фосфином.[5]
Соображения безопасности
При контакте с кислотами или водой материал выделяет фосфин, который токсичен и легко воспламеняется.
Смотрите также
Рекомендации
- ^ Ричард К. Ропп (31 декабря 2012 г.). Энциклопедия соединений щелочноземельных металлов. Newnes. стр. 231–. ISBN 978-0-444-59553-9.
- ^ а б Лилия С. Се, Лесли М. Шуп, Элизабет М. Сейбель, Куинн Д. Гибсон, Вэйвэй Се, Кава, Роберт Дж. (2015). «Новая форма Ca3P2 с кольцом узлов Дирака». Материалы APL. 3: 083602. arXiv:1504.01731. Дои:10.1063/1.4926545.CS1 maint: использует параметр авторов (связь)
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Колин МакЭведи (1992),Новый атлас пингвинов средневековой истории, Нью-Йорк: Пингвин.
- ^ GOV, Управление реагирования и восстановления NOAA, США. "ФОСФИД КАЛЬЦИЯ | CAMEO Chemicals | NOAA". cameochemicals.noaa.gov. Получено 2016-08-26.

